1 . 下列事实不能 用元素周期律知识解释的是
| A.氧化性:Cl2>S | B.稳定性:HBr>HI | C.酸性:H2SO4>HClO | D.碱性:NaOH>Mg(OH)2 |
您最近一年使用:0次
2018-11-12更新
|
147次组卷
|
3卷引用:北京市2017年春季普通高中会考化学试题
2018高三上·浙江·专题练习
2 . 下列说法错误的是
| A.硅胶可防止食物受潮是由于其具有吸水性 |
| B.镁、铝都能与氢氧化钠溶液反应 |
| C.Na2CO3可用作食用碱,Na2CO3溶液显碱性 |
| D.酸性重铬酸钾用于检查酒驾是利用其强氧化性 |
您最近一年使用:0次
3 . 为探究浓硫酸的性质,某兴趣小组进行如下实验:取2g蔗糖(C12H22O11)放入大试管中,加入2~3滴水,再加入约3mL浓硫酸,迅速搅拌。实验中可以观察到试管内的固体由白色变为黑色,后体积迅速膨胀,同时闻到刺激性气味,试管壁摸起来发烫。
⑴试管内的黑色物质是:______ 。该物质的生成表现了浓硫酸的______ 性。
⑵滴加浓硫酸之前加入2~3滴水的目的是______ 。写出黑色物质与浓硫酸反应的化学方程式:______ 。
⑶兴趣小组设计用如图所示的装置检验反应中生成的气体。

①X、Y分别是______ 和______ 。
②已知酸性KMnO4溶液具有强氧化性,图中所示装置中酸性KMnO4溶液的作用是______ 。
⑴试管内的黑色物质是:
⑵滴加浓硫酸之前加入2~3滴水的目的是
⑶兴趣小组设计用如图所示的装置检验反应中生成的气体。

①X、Y分别是
②已知酸性KMnO4溶液具有强氧化性,图中所示装置中酸性KMnO4溶液的作用是
您最近一年使用:0次
解题方法
4 . 高铁酸钾(K2FeO4)是一种新型净水剂,制备流程如下。
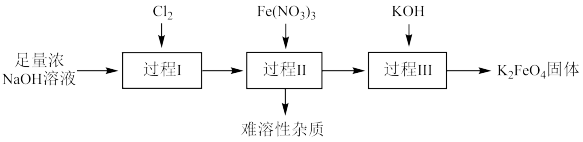
资料:在碱性溶液中的溶解度K2FeO4<Na2FeO4
(1)K2FeO4具有强氧化性,其中铁元素的化合价为______ 价。
(2)过程Ⅰ中制备NaClO的离子方程式为______ 。
(3)除Na2FeO4外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为______ 。
(4)下列说法正确的是______ (填字母)。
a.过程Ⅱ中生成了Na2FeO4
b.过程Ⅰ~Ⅲ中,需要进行过滤操作的是过程Ⅲ

资料:在碱性溶液中的溶解度K2FeO4<Na2FeO4
(1)K2FeO4具有强氧化性,其中铁元素的化合价为
(2)过程Ⅰ中制备NaClO的离子方程式为
(3)除Na2FeO4外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为
(4)下列说法正确的是
a.过程Ⅱ中生成了Na2FeO4
b.过程Ⅰ~Ⅲ中,需要进行过滤操作的是过程Ⅲ
您最近一年使用:0次
5 . 某学习小组设计实验,探究二氧化硫的漂白性和还原性。
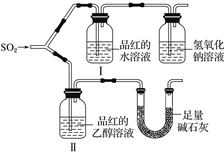
(1)漂白性
甲同学用如图所示装置(气密性良好)进行实验,观察到如下现象:Ⅰ中红色褪去,Ⅱ中无变化。
①甲同学作对照实验的目的是_________________________________________ 。
②足量碱石灰的作用是_____________________________________________ 。
甲同学由此得出的实验结论是_________________________________________ 。
(2)还原性
乙同学将SO2通入FeCl3溶液中,使其充分反应。
①SO2与FeCl3反应的离子方程式是____________________ ,检验该反应所得含氧酸根离子的方法是___________________________________________________________ 。
②实验中观察到溶液由黄色变为红棕色,静置一段时间,变为浅绿色。资料显示:红棕色为FeSO3 (墨绿色难溶物)与FeCl3 溶液形成的混合色。 则②中红棕色变为浅绿色的原因是_________________________________________________________ 。
乙同学得出的实验结论是二氧化硫可还原三氯化铁。

(1)漂白性
甲同学用如图所示装置(气密性良好)进行实验,观察到如下现象:Ⅰ中红色褪去,Ⅱ中无变化。
①甲同学作对照实验的目的是
②足量碱石灰的作用是
甲同学由此得出的实验结论是
(2)还原性
乙同学将SO2通入FeCl3溶液中,使其充分反应。
①SO2与FeCl3反应的离子方程式是
②实验中观察到溶液由黄色变为红棕色,静置一段时间,变为浅绿色。资料显示:红棕色为FeSO3 (墨绿色难溶物)与FeCl3 溶液形成的混合色。 则②中红棕色变为浅绿色的原因是
乙同学得出的实验结论是二氧化硫可还原三氯化铁。
您最近一年使用:0次
6 . 某同学通过查阅资料发现氨气可在纯氧中安静燃烧,遂设计如下装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验。回答下列问题:
I: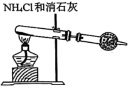
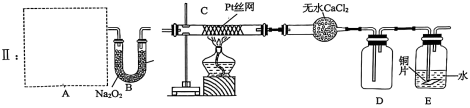
(1)若用装置Ⅰ制取纯净、干燥的氨气,大试管中发生反应的化学方程式为___________ ,干燥管中盛装的物质是 ___________ ;
(2)若按装置Ⅱ进行实验,A处是气体发生装置,若要求进入装置C中的气体是氨气与纯净的氧气,则A中应加入的一种药品是___________ (填标号);
A. NaHCO3 B.NH4HCO3 C.NH4Cl D.浓氨水
Ⅱ中B装置的作用为___________ ;写出C中发生反应的化学方程式 ___________ ;
I:


(1)若用装置Ⅰ制取纯净、干燥的氨气,大试管中发生反应的化学方程式为
(2)若按装置Ⅱ进行实验,A处是气体发生装置,若要求进入装置C中的气体是氨气与纯净的氧气,则A中应加入的一种药品是
A. NaHCO3 B.NH4HCO3 C.NH4Cl D.浓氨水
Ⅱ中B装置的作用为
您最近一年使用:0次
名校
7 . 实验小组探究某补铁口服液中铁元素的价态。
【查阅资料】
KSCN中的硫元素为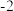 价,易被氧化为
价,易被氧化为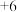 价。
价。
【实验过程】
【分析与解释】
(1)由实验Ⅰ可得出的结论是___________ 。
(2)根据实验Ⅱ中的现象,可以断定该补铁口服液中铁元素的价态为 价,滴加
价,滴加 溶液后
溶液后 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(3)一段时间后,发现实验Ⅱ中溶液红色褪去,可能的原因是___________ ;小组同学为证实自己的猜想,设计如下对照实验:向1mL 0.1 KSCN溶液中加入足量5%
KSCN溶液中加入足量5%  溶液,再加入
溶液,再加入 溶液,观察到
溶液,观察到___________ ,证实了小组同学的猜想是正确的。
【查阅资料】
KSCN中的硫元素为
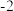 价,易被氧化为
价,易被氧化为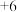 价。
价。【实验过程】
| 编号 | 实验操作 | 实验现象 |
| 实验Ⅰ |  | 无明显变化 |
| 实验Ⅱ |  | 溶液变红 |
(1)由实验Ⅰ可得出的结论是
(2)根据实验Ⅱ中的现象,可以断定该补铁口服液中铁元素的价态为
 价,滴加
价,滴加 溶液后
溶液后 发生反应的离子方程式为
发生反应的离子方程式为(3)一段时间后,发现实验Ⅱ中溶液红色褪去,可能的原因是
 KSCN溶液中加入足量5%
KSCN溶液中加入足量5%  溶液,再加入
溶液,再加入 溶液,观察到
溶液,观察到
您最近一年使用:0次
2021-06-20更新
|
612次组卷
|
5卷引用:北京市海淀区2020-2021学年高一下学期学业水平合格性考试适应练习化学试题
北京市海淀区2020-2021学年高一下学期学业水平合格性考试适应练习化学试题(已下线)周末培优4 金属及其化合物的实验题和工艺流程题-2021-2022学年高一化学课后培优练(人教版2019必修第一册)(已下线)易错专题23 Fe2+和Fe3+的检验与转化-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)北京市第十一中学2021-2022学年高一下学期6月月考化学试题(已下线)第三章 铁 金属材料(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)
名校
8 . 某小组同学以不同方案探究Cu粉与FeCl3溶液的反应。
(1)甲同学向FeCl3溶液中加入Cu粉,观察到溶液的颜色变为浅蓝色,由此证明发生了反应,其离子方程式是__ 。
(2)乙同学通过反应物的消耗证明了上述反应的发生:将Cu粉加入到滴有少量KSCN的FeCl3溶液中,观察到溶液红色褪色,有白色沉淀A产生。
针对白色沉淀A,查阅资料:A可能为CuCl和CuSCN(其中硫元素的化合价为-2价)中的一种或两种。实验过程如下:
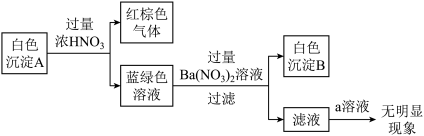
请回答:
①根据白色沉淀B是__ (填化学式),判断沉淀A中一定存在CuSCN。
②仅根据白色沉淀A与过量浓HNO3反应产生的实验现象,不能判断白色沉淀A中一定存在CuSCN,从氧化还原角度说明理由:__ 。
③向滤液中加入a溶液后无明显现象,说明A不含CuCl,则a是__ (填化学式)。
根据以上实验,证明A仅为CuSCN。
④进一步查阅资料并实验验证了CuSCN的成因,将该反应的方程式补充完整:
_ Cu2++_ SCN-=_ CuSCN↓+_ (SCN)2
⑤结合上述过程以及Fe(SCN)3 Fe3++3SCN-的平衡,分析(2)中溶液红色褪去的原因:
Fe3++3SCN-的平衡,分析(2)中溶液红色褪去的原因:__ 。
(3)已知(SCN)2称为拟卤素,其氧化性与Br2相近。将KSCN溶液滴入(1)所得的溶液中,观察到溶液变红色,则溶液变红的可能原因是__ 或__ 。
(1)甲同学向FeCl3溶液中加入Cu粉,观察到溶液的颜色变为浅蓝色,由此证明发生了反应,其离子方程式是
(2)乙同学通过反应物的消耗证明了上述反应的发生:将Cu粉加入到滴有少量KSCN的FeCl3溶液中,观察到溶液红色褪色,有白色沉淀A产生。
针对白色沉淀A,查阅资料:A可能为CuCl和CuSCN(其中硫元素的化合价为-2价)中的一种或两种。实验过程如下:

请回答:
①根据白色沉淀B是
②仅根据白色沉淀A与过量浓HNO3反应产生的实验现象,不能判断白色沉淀A中一定存在CuSCN,从氧化还原角度说明理由:
③向滤液中加入a溶液后无明显现象,说明A不含CuCl,则a是
根据以上实验,证明A仅为CuSCN。
④进一步查阅资料并实验验证了CuSCN的成因,将该反应的方程式补充完整:
⑤结合上述过程以及Fe(SCN)3
 Fe3++3SCN-的平衡,分析(2)中溶液红色褪去的原因:
Fe3++3SCN-的平衡,分析(2)中溶液红色褪去的原因:(3)已知(SCN)2称为拟卤素,其氧化性与Br2相近。将KSCN溶液滴入(1)所得的溶液中,观察到溶液变红色,则溶液变红的可能原因是
您最近一年使用:0次
2020-04-27更新
|
322次组卷
|
5卷引用:北京市2020普通高中学业水平考试等级性抽样测试化学试题
9 . 某实验室设计实验比较碳酸氢钠片与铝碳酸镁片两种抗酸药的效果。
【资料1】人体胃液的主要成分有盐酸、胃蛋白酶原、黏液。在盐酸作用下胃蛋白酶原转化为胃蛋白酶,起到消化食物的作用。当pH超过5.0时,胃蛋白酶完全失活,会导致消化不良。当盐酸过多,会产生大量的胃蛋白酶,分解胃壁蛋白,引起疼痛。抗酸药的主要作用机理是对过多的胃酸进行适量中和,控制胃液pH值处于3~5之间缓解疼痛。
【资料2】pH越低,c(H+)越大,酸性越强
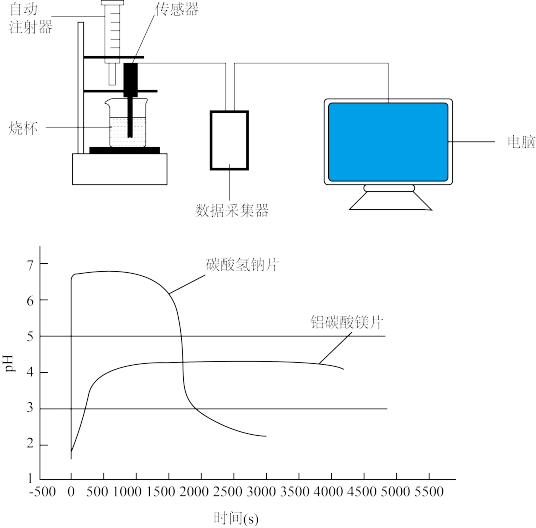
实验准备:
①在烧杯中放入100mLpH为1.5盐酸,模拟胃环境。
②用自动注射器可向烧杯中以1mL/min的速度滴入盐酸,模拟人体胃酸的分泌过程。
实验操作:
按照抗酸药说明书上的使用剂量,将药片研磨成粉末,向烧杯中加入抗酸药粉末,打开自动注射器,向烧杯中滴入盐酸。同时通过传感器采集烧杯中溶液pH随时间变化的数据。
请回答下列问题:
(1)碳酸氢钠片与盐酸反应的离子方程式是__________ 。
(2)铝碳酸镁片(有效成分为Al2Mg6(OH)16CO3·4H2O)能消耗盐酸的原因是其组成中含有_________ 。
(3)0~500秒内与盐酸反应的平均速率更快的是_______ (填抗酸药名称),理由是_________ 。
(4)该实验表明铝碳酸镁片的抗酸效果比碳酸氢钠片更佳,理由是___________ 。
【资料1】人体胃液的主要成分有盐酸、胃蛋白酶原、黏液。在盐酸作用下胃蛋白酶原转化为胃蛋白酶,起到消化食物的作用。当pH超过5.0时,胃蛋白酶完全失活,会导致消化不良。当盐酸过多,会产生大量的胃蛋白酶,分解胃壁蛋白,引起疼痛。抗酸药的主要作用机理是对过多的胃酸进行适量中和,控制胃液pH值处于3~5之间缓解疼痛。
【资料2】pH越低,c(H+)越大,酸性越强

实验准备:
①在烧杯中放入100mLpH为1.5盐酸,模拟胃环境。
②用自动注射器可向烧杯中以1mL/min的速度滴入盐酸,模拟人体胃酸的分泌过程。
实验操作:
按照抗酸药说明书上的使用剂量,将药片研磨成粉末,向烧杯中加入抗酸药粉末,打开自动注射器,向烧杯中滴入盐酸。同时通过传感器采集烧杯中溶液pH随时间变化的数据。
请回答下列问题:
(1)碳酸氢钠片与盐酸反应的离子方程式是
(2)铝碳酸镁片(有效成分为Al2Mg6(OH)16CO3·4H2O)能消耗盐酸的原因是其组成中含有
(3)0~500秒内与盐酸反应的平均速率更快的是
(4)该实验表明铝碳酸镁片的抗酸效果比碳酸氢钠片更佳,理由是
您最近一年使用:0次
10 . 铁是重要的常见金属材料,也是人类较早使用的金属之一。完成下列问题:
(1)铁路大提速后,为将短铁轨焊接成长铁轨,可在铁轨接口处加入氧化铁和铝粉的混合物,用镁条引燃发生反应,配平其化学方程式: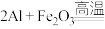
______ 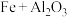 。
。
(2)向20 mL的沸水中逐滴滴加5~6滴FeCl3饱和溶液,继续煮沸至观察到透明的红褐色。此分散系分散质中粒子直径的范围是______ (填“<1”或“1~100”)nm。
(3)电子工业上常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。上述事实利用了FeCl3溶液的______ (填“氧化性”或“还原性”)。
(1)铁路大提速后,为将短铁轨焊接成长铁轨,可在铁轨接口处加入氧化铁和铝粉的混合物,用镁条引燃发生反应,配平其化学方程式:
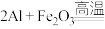
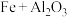 。
。(2)向20 mL的沸水中逐滴滴加5~6滴FeCl3饱和溶液,继续煮沸至观察到透明的红褐色。此分散系分散质中粒子直径的范围是
(3)电子工业上常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。上述事实利用了FeCl3溶液的
您最近一年使用:0次



