解题方法
1 . 全球空气污染日趋严重,消除氮氧化物污染对建设宜居环境具有重要意义。
Ⅰ.已知: ①
①
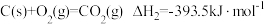 ②
②
 ③
③
(1)某反应的平衡常数表达式为 ,写出该反应的热化学方程式:
,写出该反应的热化学方程式:______ 。
Ⅱ.在 的密闭容器中,通入一定量的N2O4,发生反应
的密闭容器中,通入一定量的N2O4,发生反应 。
。
(2)图甲为该反应过程中有关物理量Y随温度X(其他条件不变)变化的关系图。Y可表示___________ (填字母)。
A.逆反应速率 B.气体的密度 C.平衡常数 D. 的转化率 E.气体的平均摩尔质量
的转化率 E.气体的平均摩尔质量

(3)图乙为 时,体系中各物质的物质的量浓度随时间变化关系。
时,体系中各物质的物质的量浓度随时间变化关系。
①在 时段,反应速率
时段,反应速率 为
为___________  。
。
②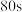 后,改变反应温度为
后,改变反应温度为 ,
,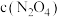 以
以 的平均速率降低,经
的平均速率降低,经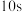 后又达到平衡。则T
后又达到平衡。则T___________ (填“>”或“<”)100,判断理由是___________ 。在 时反应达平衡后,将反应容器的容积缩小一半,平衡向
时反应达平衡后,将反应容器的容积缩小一半,平衡向___________ (填“正反应”或“逆反应”)方向移动,判断的理由是___________ 。
Ⅰ.已知:
 ①
①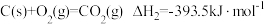 ②
② ③
③(1)某反应的平衡常数表达式为
 ,写出该反应的热化学方程式:
,写出该反应的热化学方程式:Ⅱ.在
 的密闭容器中,通入一定量的N2O4,发生反应
的密闭容器中,通入一定量的N2O4,发生反应 。
。(2)图甲为该反应过程中有关物理量Y随温度X(其他条件不变)变化的关系图。Y可表示
A.逆反应速率 B.气体的密度 C.平衡常数 D.
 的转化率 E.气体的平均摩尔质量
的转化率 E.气体的平均摩尔质量
(3)图乙为
 时,体系中各物质的物质的量浓度随时间变化关系。
时,体系中各物质的物质的量浓度随时间变化关系。①在
 时段,反应速率
时段,反应速率 为
为 。
。②
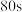 后,改变反应温度为
后,改变反应温度为 ,
,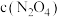 以
以 的平均速率降低,经
的平均速率降低,经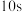 后又达到平衡。则T
后又达到平衡。则T 时反应达平衡后,将反应容器的容积缩小一半,平衡向
时反应达平衡后,将反应容器的容积缩小一半,平衡向
您最近一年使用:0次
2 . 下列有关化学图象表现的内容错误的是
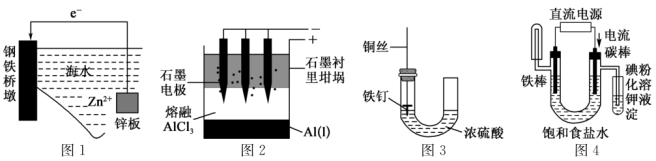

| A.图1表示牺牲阳极法 |
B.图2表示电解熔融 制备 制备 |
| C.图3所示装置中的铁钉几乎没被腐蚀 |
D.图4能验证 溶液(含酚酞)的电解产物 溶液(含酚酞)的电解产物 |
您最近一年使用:0次
2021-12-30更新
|
508次组卷
|
3卷引用:山西省运城市教育发展联盟2021-2022学年高二上学期12月月考化学试题
3 .  和
和 的混合气体俗称合成气。利用
的混合气体俗称合成气。利用 制备合成气反应历程分两步,步骤Ⅰ:
制备合成气反应历程分两步,步骤Ⅰ: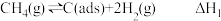 (慢反应);步骤Ⅱ:
(慢反应);步骤Ⅱ: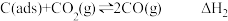 (快反应)。上述反应中
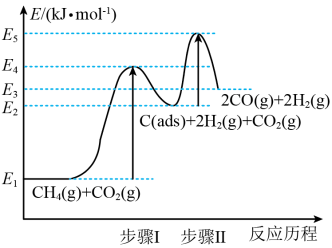
(快反应)。上述反应中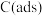 为吸附性活性炭,反应历程的能量变化如图所示,下列说法错误的是
为吸附性活性炭,反应历程的能量变化如图所示,下列说法错误的是
 和
和 的混合气体俗称合成气。利用
的混合气体俗称合成气。利用 制备合成气反应历程分两步,步骤Ⅰ:
制备合成气反应历程分两步,步骤Ⅰ: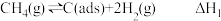 (慢反应);步骤Ⅱ:
(慢反应);步骤Ⅱ: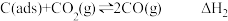 (快反应)。上述反应中
(快反应)。上述反应中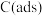 为吸附性活性炭,反应历程的能量变化如图所示,下列说法错误的是
为吸附性活性炭,反应历程的能量变化如图所示,下列说法错误的是
A.制备合成气总反应的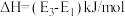 |
B.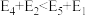 |
| C.该反应在高温下能自发进行 |
D.使用催化剂后, 和 和 平衡产率不改变 平衡产率不改变 |
您最近一年使用:0次
2021-12-30更新
|
350次组卷
|
4卷引用:山西省运城市教育发展联盟2021-2022学年高二上学期12月月考化学试题
山西省运城市教育发展联盟2021-2022学年高二上学期12月月考化学试题(已下线)专题25 关于化学平衡的计算-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)辽宁省凌源市2021-2022学年高三下学期高三开学考试化学试题河南省商丘市2021-2022学年高二下学期4月月考化学试题
名校
4 . 下列有关化学反应与能量变化的叙述正确的是
| A.相同条件下,等物质的量的硫蒸气和硫固体分别完全燃烧,前者放出热量更多 |
B.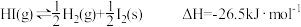 ,则 ,则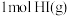 充分分解后放出 充分分解后放出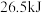 的热量 的热量 |
C.由“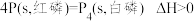 ”可知,白磷比红磷稳定 ”可知,白磷比红磷稳定 |
D.同温同压下,反应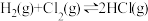 在光照和点燃条件的 在光照和点燃条件的 不同 不同 |
您最近一年使用:0次
2021-12-30更新
|
337次组卷
|
3卷引用:山西省运城市教育发展联盟2021-2022学年高二上学期12月月考化学试题
名校
5 . CO2/HCOOH循环在氢能的贮存/释放、燃料电池等方面具有重要应用。
Ⅰ.CO2催化加氢:向含有催化剂的KHCO3溶液中通入H2生成HCOO-。
(1)该反应过程中的离子反应方程式为___ 。
(2)为测定HCO 转化为HCOO-的转化率,取10.00mL反应后的溶液,用0.1000mol/L的酸性高锰酸钾溶液滴定,将HCOO-氧化为CO2。滴定至终点时,实验现象为
转化为HCOO-的转化率,取10.00mL反应后的溶液,用0.1000mol/L的酸性高锰酸钾溶液滴定,将HCOO-氧化为CO2。滴定至终点时,实验现象为___ 。实验中平均消耗酸性高锰酸钾溶液10.00mL,则HCOO-的浓度为___ 。
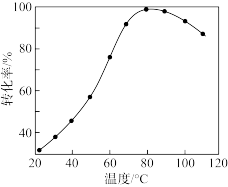
(3)其他条件不变,在相同时间内,HCO 转化为HCOO-的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内,HCO
转化为HCOO-的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内,HCO 催化加氢的转化率迅速上升,其原因可能是
催化加氢的转化率迅速上升,其原因可能是___ 。(写出一条即可)在温度超过80℃以后,转化率下降,其原因可能是___ 。(写出一条即可)
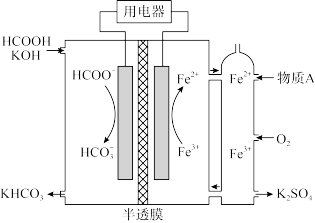
Ⅱ.HCOOH燃料电池:研究HCOOH燃料电池性能的装置如图所示,两电极区间用允许K+、H+通过的半透膜隔开。
(4)电池负极电极反应式为:___ 。
(5)放电过程中需补充的物质A___ 。(填化学式)
Ⅰ.CO2催化加氢:向含有催化剂的KHCO3溶液中通入H2生成HCOO-。
(1)该反应过程中的离子反应方程式为
(2)为测定HCO
 转化为HCOO-的转化率,取10.00mL反应后的溶液,用0.1000mol/L的酸性高锰酸钾溶液滴定,将HCOO-氧化为CO2。滴定至终点时,实验现象为
转化为HCOO-的转化率,取10.00mL反应后的溶液,用0.1000mol/L的酸性高锰酸钾溶液滴定,将HCOO-氧化为CO2。滴定至终点时,实验现象为(3)其他条件不变,在相同时间内,HCO
 转化为HCOO-的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内,HCO
转化为HCOO-的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内,HCO 催化加氢的转化率迅速上升,其原因可能是
催化加氢的转化率迅速上升,其原因可能是
Ⅱ.HCOOH燃料电池:研究HCOOH燃料电池性能的装置如图所示,两电极区间用允许K+、H+通过的半透膜隔开。
(4)电池负极电极反应式为:
(5)放电过程中需补充的物质A

您最近一年使用:0次
名校
6 . 常温下,用0.1mol/LKOH溶液滴定10.00mL某浓度的H2B溶液,溶液的pH随着KOH溶液体积变化的曲线如图(⑤是酸恰好消耗完的点。混合溶液的体积可看成混合前溶液的体积之和,滴定过程中温度变化忽略不计,lg3=0.47),回答下列问题:

(1)滴定过程中
__ 。(填“变大”或“变小”)
(2)已知:Ka1=1.0×10-5、Ka2=3.0×10-9、pH1=3;则H2B溶液的浓度为__ ,pH2=__ 。
(3)②溶液中的物料守恒为c(K+)=___ 。
(4)③溶液呈___ (填“酸性”或“碱性”)。
(5)图中5个点中,水的电离程度从大到小的顺序为:___ 。

(1)滴定过程中

(2)已知:Ka1=1.0×10-5、Ka2=3.0×10-9、pH1=3;则H2B溶液的浓度为
(3)②溶液中的物料守恒为c(K+)=
(4)③溶液呈
(5)图中5个点中,水的电离程度从大到小的顺序为:
您最近一年使用:0次
名校
7 . 如图是利用氯碱工业的原理图。回答下列问题:
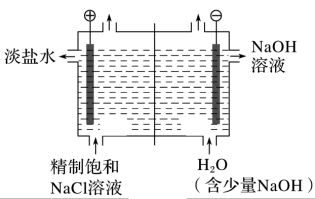
(1)请写出氯碱工业的电极反应方程式:__ ,__ 。(注明电极)
(2)图中的离子交换膜是__ (填“阳离子”或“阴离子”)交换膜,采用该离子交换膜的作用有__ (写出一点)。
(3)请写出检验左室气体产物的方法__ 。
(4)请写出NaOH在工业上的一种用途__ 。

(1)请写出氯碱工业的电极反应方程式:
(2)图中的离子交换膜是
(3)请写出检验左室气体产物的方法
(4)请写出NaOH在工业上的一种用途
您最近一年使用:0次
名校
8 . 下列说法错误的是
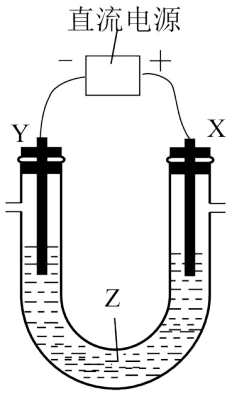

| A.电解精炼铜时候,X极为粗铜 |
| B.电解冶炼K单质,在Y极得到钾 |
| C.电镀时,镀件挂在Y极 |
| D.在镀件上镀铜时,为使镀层光亮,可在硫酸铜溶液中加入一些氨水 |
您最近一年使用:0次
名校
9 . 室温下,将0.3molBaSO4加入5L1mol/LNa2CO3溶液中,不考虑体积变化,达到平衡时,c(SO )=0.02mol/L,下列说法错误的是
)=0.02mol/L,下列说法错误的是
 )=0.02mol/L,下列说法错误的是
)=0.02mol/L,下列说法错误的是| A.有BaCO3沉淀生成 |
| B.依据题干信息可推出:Ksp[BaSO4]<Ksp[BaCO3] |
| C.向溶液中继续加入少量Na2CO3固体,BaCO3沉淀增多 |
| D.向溶液中继续加入少量蒸馏水,BaCO3沉淀减少 |
您最近一年使用:0次
名校
10 . 如图为水的电离平衡平衡图象,下列说法正确的是


| A.T1>T2 |
B.Q点能大量共存的离子:Na+、Fe3+、SO 、Cl- 、Cl- |
| C.T1温度下,向Q点加入NaOH溶液,其组成可移动到N点 |
| D.水的电离程度:M=N<Q(M、N两点与Q距离相等) |
您最近一年使用:0次



