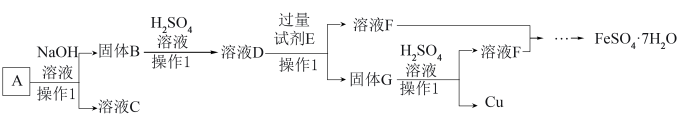
(1)操作1的名称是
(2)溶液C的溶质主要是
(3)检验溶液D中含Fe3+的方法是
(4)FeSO4·7H2O可处理工业废水中有毒的
 ,反应的离子方程式为Fe2++
,反应的离子方程式为Fe2++ +H+→Fe3++Cr3++H2O(未配平),该反应中,氧化剂与还原剂的物质的量之比为
+H+→Fe3++Cr3++H2O(未配平),该反应中,氧化剂与还原剂的物质的量之比为(5)FeSO4·7H2O由于保存不当容易被空气中氧气氧化而变质,可用酸性KMnO4溶液测定其纯度,测定原理为5Fe2++
 +8H+=5Fe3++Mn2++4H2O。现有一瓶绿矾样品,取出ag于试管中,往其中加入Vmlcmol/L酸性KMnO4溶液恰好完全反应,则绿矾样品的纯度为
+8H+=5Fe3++Mn2++4H2O。现有一瓶绿矾样品,取出ag于试管中,往其中加入Vmlcmol/L酸性KMnO4溶液恰好完全反应,则绿矾样品的纯度为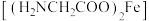 是一种补血剂,工业上用赤铁矿(含少量铝、铜、锰的氧化物)制备甘氨酸亚铁的流程图如下:
是一种补血剂,工业上用赤铁矿(含少量铝、铜、锰的氧化物)制备甘氨酸亚铁的流程图如下:
已知:甘氨酸
 易溶于水,微溶于乙醇,具有两性,例如甘氨酸可与碳酸钠反应生成
易溶于水,微溶于乙醇,具有两性,例如甘氨酸可与碳酸钠反应生成 (
( )
)回答下列问题:
(1)“碱浸”去除的元素是
(2)“还原”时的离子方程式是
(3)“沉淀”的离子方程式是
(4)柠檬酸的作用是防止
 氧化,则“反应”的化学方程式为
氧化,则“反应”的化学方程式为(5)
 也是一种常用的补血剂,在空气中易变质,检验其是否变质的试剂是
也是一种常用的补血剂,在空气中易变质,检验其是否变质的试剂是 的含量。
的含量。①配制:用分析天平称取
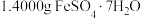 样品,再用煮沸并冷却的蒸馏水配制
样品,再用煮沸并冷却的蒸馏水配制 溶液。配制时除量筒外还需要的定量仪器是
溶液。配制时除量筒外还需要的定量仪器是②以下操作,会导致所配溶液浓度偏大的是
A.配溶液所用
 晶体已部分失去结晶水
晶体已部分失去结晶水B.转移前,容量瓶内有少量蒸馏水
C.定容时俯视刻度线
D.定容时液面超过刻度线,立即用胶头滴管吸出
E.摇匀后液面低于刻度线
③滴定:用酸化的
 溶液滴定
溶液滴定取
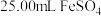 溶液于锥形瓶中,用
溶液于锥形瓶中,用 的
的 溶液滴定至
溶液滴定至 溶液恰好完全反应,消耗
溶液恰好完全反应,消耗 溶液
溶液 ,则样品中
,则样品中 的含量为
的含量为(1)将Na、
 、
、 、NaOH长时间露置在空气中,最终都会变为
、NaOH长时间露置在空气中,最终都会变为(2)探究某
 样品是否已经变质:取少量
样品是否已经变质:取少量 样品,将其溶于水,加入
样品,将其溶于水,加入 溶液,充分振荡后,观察到
溶液,充分振荡后,观察到 样品已经与空气中的
样品已经与空气中的 发生反应变质。
发生反应变质。(3)“神舟号”载人航天器的返回舱内,为防止
 浓度过大引起宇航员困乏,可用
浓度过大引起宇航员困乏,可用 降低
降低 的浓度,有关反应的化学方程式为
的浓度,有关反应的化学方程式为 (超氧化钾)代替
(超氧化钾)代替 也能达到同样的目的,反应产物也很相似,试计算用
也能达到同样的目的,反应产物也很相似,试计算用 和
和 分别与
分别与 反应,产生等质量的
反应,产生等质量的 ,所需
,所需 和
和 的质量比为
的质量比为(4)食品工业经常把
 和
和 用作膨松剂,室温下向含某膨松剂试样(
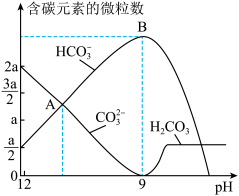
用作膨松剂,室温下向含某膨松剂试样(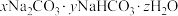 )的溶液中逐滴加入稀盐酸,反应过程中含碳元素的微粒数随pH变化的图像如图所示。(已知:
)的溶液中逐滴加入稀盐酸,反应过程中含碳元素的微粒数随pH变化的图像如图所示。(已知: 因有逸出未画出;
因有逸出未画出; 与少量盐酸发生下列反应:
与少量盐酸发生下列反应: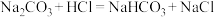 )。
)。①x:y=
②图中B点溶液溶质的主要成分为
【资料】常用的酸碱指示剂及其变色范围如下:
酚酞:pH<8.2无色 8.2<pH<10浅红色 pH>10红色
甲基橙:pH<3.1红色 3.1<pH<4.4橙色 pH>4.4黄色
【实验步骤】
I、迅速地称取烧碱样品0.50g,溶解后配制成100mL溶液,备用。
Ⅱ、将0.1000mol/LHCl标准溶液装入酸式滴定管,调0,记录起始读数V0;用碱式滴定管取20.00mL样品溶液于锥形瓶中,滴加2滴酚酞;以HCl标准溶液滴定至第一终点(此时溶质为NaCl和NaHCO3),记录酸式滴定管的读数V1;然后再向锥形瓶内滴加2滴甲基橙,继续用HCl标准溶液滴定至第二终点,记录酸式滴定管的读数。重复上述操作两次,记录数据如下:
| 实验序号 | 1 | 2 | 3 |
| V0/mL | 0.00 | 0.00 | 0.00 |
| V1/mL | 21.72 | 21.68 | 21.70 |
| V2/mL | 23.72 | 23.68 | 23.70 |
(1)烧碱样品变质的原因(用化学方程式表示)
(2)步骤I中所需的玻璃仪器有烧杯、玻璃棒、胶头滴管和
(3)酸式滴定管用蒸馏水洗净后、装入标准溶液前,应进行的操作是
(4)滴定至第一终点的过程中,发生反应的离子方程式为
(5)判断滴定至第二终点的现象是溶液由
(6)样品中NaOH的质量分数w(NaOH)=
(7)下列操作会导致测得的NaOH质量分数偏高的是
a.达到第一终点前,锥形瓶中有气泡产生
b.记录酸式滴定管读数时,俯视标准液液面
c.第一终点后继续滴定时,锥形瓶中有少许液体溅出
【实验I】用
 的
的 溶液测定某食用白醋中醋酸的物质的量浓度,某同学列出实验步骤:
溶液测定某食用白醋中醋酸的物质的量浓度,某同学列出实验步骤:A.分别向碱式滴定管、酸式滴定管注入
 标准溶液和待测醋酸至0刻度以上2~3cm
标准溶液和待测醋酸至0刻度以上2~3cmB.调节滴定管液面至0或0刻度以下,记下读数
C.用
 标准溶液滴定至终点,记下滴定管液面的刻度
标准溶液滴定至终点,记下滴定管液面的刻度D.用标准溶液清洗碱式滴定管2~3次;待测醋酸清洗酸式滴定管2~3次
E.用待测醋酸清洗锥形瓶2~3次
F.排气泡使滴定管尖嘴充满溶液,把滴定管固定好
G.滴定管检漏,用水清洗所有仪器,备用
H.通过酸式滴定管向锥形瓶注入20.00mL待测醋酸,并加入2滴指示剂
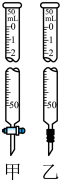
(1)①从上述实验步骤中选出正确的并按操作先后排序:
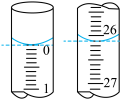
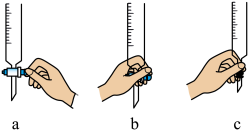
②滴定开始和结束时读数若如图所示,
 标准溶液的体积为
标准溶液的体积为(2)有学生在实验过程中实验数据记录如下:
滴定序号 | 待测液体积(mL) | 所消耗 | |
滴定前 | 滴定后 | ||
1 | 25.00 | 0.50 | 20.60 |
2 | 25.00 | 1.10 | 21.00 |
3 | 25.00 | 2.20 | 22.20 |
根据实验数据计算,c(待测液)
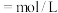 ,若滴定时标准液和待测液的浓度变大,滴定突跃范围变
,若滴定时标准液和待测液的浓度变大,滴定突跃范围变(3)常温下,若用
 溶液分别滴定20.00mL等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如图所示:达到B、D状态时,反应消耗的
溶液分别滴定20.00mL等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如图所示:达到B、D状态时,反应消耗的 溶液的体积a
溶液的体积a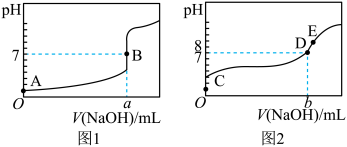
(4)测定
 的纯度。
的纯度。称取ag样品,先用硫酸溶解,配成
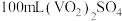 溶液,取20mL溶液置于锥形瓶中,再加入
溶液,取20mL溶液置于锥形瓶中,再加入 溶液
溶液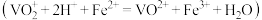 ,最后用
,最后用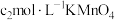 溶液滴定过量的
溶液滴定过量的 至
至 溶液的体积为
溶液的体积为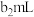 ,已知
,已知 被还原为
被还原为 ,
, 的质量分数是
的质量分数是 的摩尔质量:
的摩尔质量: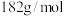 ),下列情况会导致产品纯度偏大的是
),下列情况会导致产品纯度偏大的是A.
 溶液部分变质(含
溶液部分变质(含 ) B.滴定达终点时,仰视刻度线读数
) B.滴定达终点时,仰视刻度线读数C.滴定前,在锥形瓶中加水稀释待测液 D.滴定终点时,滴定管尖嘴内有气泡生成
E.
 溶液因露空放置太久而变质F.酸式滴定管未用标准液润洗
溶液因露空放置太久而变质F.酸式滴定管未用标准液润洗
 (
(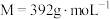 )。摩尔盐是浅蓝绿色晶体,溶于水,但在水中溶解度比硫酸亚铁和硫酸铵都要小,几乎不溶于乙醇,在空气中比硫酸亚铁稳定。以下是摩尔盐的制备步骤。
)。摩尔盐是浅蓝绿色晶体,溶于水,但在水中溶解度比硫酸亚铁和硫酸铵都要小,几乎不溶于乙醇,在空气中比硫酸亚铁稳定。以下是摩尔盐的制备步骤。Ⅰ.把30%
 溶液和废铁屑混合、煮沸、冷却,将洗涤铁屑后的
溶液和废铁屑混合、煮沸、冷却,将洗涤铁屑后的 溶液装入右边广口瓶中。
溶液装入右边广口瓶中。Ⅱ.在锥形瓶中用处理过的铁屑和稀
 反应制取
反应制取 。
。Ⅲ.将硫酸亚铁溶液与硫酸铵溶液混合,结晶,过滤,用乙醇洗涤后再低温烘干,得到摩尔盐。

(1)装硫酸的仪器的名称是
(2)用
 溶液洗涤废铁屑的目的是
溶液洗涤废铁屑的目的是(3)Fe屑和稀
 反应产生的氢气可赶走装置中的氧气及
反应产生的氢气可赶走装置中的氧气及 溶液中的溶解氧,操作时应先关闭活塞
溶液中的溶解氧,操作时应先关闭活塞(4)摩尔盐中铵离子检验方法是
(5)步骤Ⅲ过滤后用乙醇洗涤后再低温烘干。用乙醇洗涤的原因是
(6)取10.00g所制得的固体于小烧杯中,加入适量稀硫酸,溶解后在
 容量瓶中定容。取定容后溶液
容量瓶中定容。取定容后溶液 于锥形瓶中,用
于锥形瓶中,用 的
的 溶液滴定至终点。平行操作三次,消耗
溶液滴定至终点。平行操作三次,消耗 溶液的体积分别为
溶液的体积分别为 、
、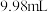 、
、 。此样品中
。此样品中 含量最接近
含量最接近A.11% B.12% C.13% D.14%
导致该测定结果比理论值偏低的可能原因是
A.配摩尔盐溶液定容时俯视刻度线 B.取摩尔盐溶液的滴定管没有润洗
C.滴定用的锥形瓶洗净后未干燥 D.高锰酸钾部分变质
(7)将摩尔盐隔绝空气加热到773K时会分解,分解产物有氧化铁、硫的氧化物、氨气和水。写出该反应的化学方程式
7 . (1)实验室有一瓶久置的亚硫酸钠溶液,同学分成甲、乙两小组对该瓶亚硫酸钠溶液成分进行实验探究。
【提出问题】该溶液中溶质成分是什么?该溶液中亚硫酸钠的物质的量浓度是多少?
【查阅资料】 有较强还原性,在空气中易被氧气氧化
有较强还原性,在空气中易被氧气氧化
【作出猜想】猜想 :没有变质,成分是
:没有变质,成分是
猜想 :完全变质,成分是
:完全变质,成分是
猜想 :部分变质,成分是
:部分变质,成分是 和
和
【实验探究Ⅰ】
(1)甲组设计实验探究溶液是否变质
甲组 | 实验操作 | 现象 | 结论 |
步骤 | 取少量样品于试管中加入过量稀盐酸 | 产生气泡 | 溶液中含有 |
步骤 | 另取样品于试管中,滴加足量氯化钡溶液,再滴加足量稀盐酸 | 溶液中含有 |
实验结论:样品部分变质。样品在空气中变质的化学方程式:
【实验探究Ⅱ】
(2)乙组设计如下实验测定
 溶液物质的量浓度。
溶液物质的量浓度。①连好装置并检查装置气密性,在锥形瓶中放入 该样品,通入
该样品,通入 。
。
②称量C装置的质量为 。
。
③关闭活塞 ,用注射器推入浓硫酸至不再产生气泡,注射器可以换为
,用注射器推入浓硫酸至不再产生气泡,注射器可以换为
④打开活塞 ,再缓缓鼓入一定量的
,再缓缓鼓入一定量的 ,继续通入
,继续通入 的作用是
的作用是
⑤再次称量C装置的质量为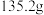 。
。

⑥计算出原溶液中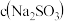 =
= 装置,实验结果将
装置,实验结果将 填“偏大”“不变”或“偏小”
填“偏大”“不变”或“偏小” 。
。
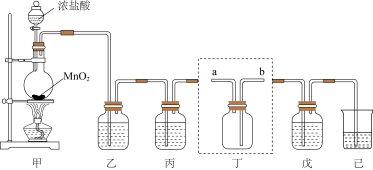
回答下列问题:
(1)装置甲中发生反应的离子方程式为
(2)装置乙、丙中盛装的试剂分别为是
(3)装置丁用来收集纯净且干燥的氯气,进气口为
(4)装置戊中盛装石灰乳用来制备漂白粉,则装置戊中发生反应的化学方程式为
(5)漂白粉长时间暴露在空气中容易发生变质,为了判断一份久置的漂白粉是否变质及变质程度,甲、乙两位同学分别设计实验进行验证:甲同学取适量漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊:他又取少量漂白粉样品配成溶液,滴在pH试纸上,最终试纸变白。
已知:
 溶液呈碱性:
溶液呈碱性: ;
;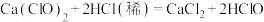
①漂白粉中的
 能与空气中的
能与空气中的 和水蒸气反应,从而发生变质,写出该反应的化学方程
和水蒸气反应,从而发生变质,写出该反应的化学方程②乙同学认为甲同学的实验无法证明漂白粉是否变质,原因是
③由乙同学的实验可以证明漂白粉
(6)装置己的作用是吸收多余的氯气,可选用试剂______。(填标号)。
| A.稀硫酸 | B. | C. | D. |
(1)探究一包Na2O2样品是否已经变质:取少量样品,加水将其溶解,加入
(2)该实验小组为了粗略测定过氧化钠的质量分数,称取了mg样品,并设计用下图装置来测定过氧化钠的质量分数。
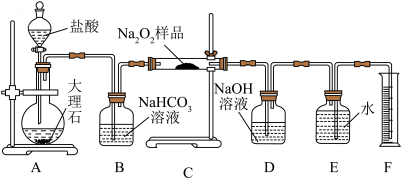
②将仪器连接好以后,必须进行的第一步操作是
③写出装置C中发生的主要反应的化学方程式:
④装置D的作用是
⑤实验结束后,装置F中水的体积为VmL,已知氧气的密度为ρg·mL-1,样品中Na2O2质量分数为
 而变质。为了测定过氧化钠的纯度,称取ag样品并设计如图装置来测定过氧化钠的质量分数。
而变质。为了测定过氧化钠的纯度,称取ag样品并设计如图装置来测定过氧化钠的质量分数。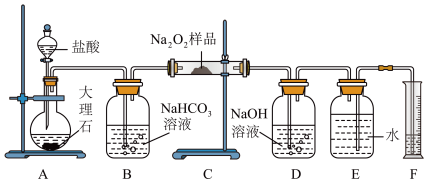
(1)将仪器连接好以后,必须进行的第一步操作是
(2)装置C中发生反应的化学方程式为
(3)D中NaOH溶液的作用为
(4)实验结束时,读取实验中生成气体的体积时,不合理的是
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.读取量筒中水的体积时,应使视线与凹液面的最低点相平
(5)读出量筒内水的体积后,折算成标准状况下氧气的体积为
 ,则样品中过氧化钠的质量分数为
,则样品中过氧化钠的质量分数为


