解题方法
1 . 走进“化学村”。“化学村”的布局如下:
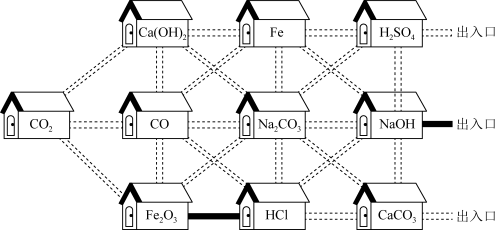
(1)10户“居民”中,俗称熟石灰的是___________ ,属于氧化物的有___________ 。
(2)“居民”CO与Fe2O3反应的化学方程式为___________ ,该反应是为___________ 。(填氧化还原反应或非氧化还原反应)

(1)10户“居民”中,俗称熟石灰的是
(2)“居民”CO与Fe2O3反应的化学方程式为
您最近一年使用:0次
2 . 已知,有一质量分数为40%的NaOH溶液,密度为1.42g/mL,求:
(1)该NaOH溶液的物质的量浓度为___________ ;
(2)取上述NaOH溶液50mL,加水稀释至355mL,稀释后的NaOH溶液的物质的量浓度为___________ ;
(3)将一定量的Na、Fe混合物投入足量水中,充分反应,共收集到气体44.8L(标准状况下),若将同质量、同组分的Na、Fe混合物投入足量盐酸中,充分反应,共收集到气体56.0L(标准状况下)。问:Na和Fe分别多少克___________ ?(该题请写出相应的计算过程,没过程不得分。)
(1)该NaOH溶液的物质的量浓度为
(2)取上述NaOH溶液50mL,加水稀释至355mL,稀释后的NaOH溶液的物质的量浓度为
(3)将一定量的Na、Fe混合物投入足量水中,充分反应,共收集到气体44.8L(标准状况下),若将同质量、同组分的Na、Fe混合物投入足量盐酸中,充分反应,共收集到气体56.0L(标准状况下)。问:Na和Fe分别多少克
您最近一年使用:0次
3 . 我们世界的生产、生活都离不开化学。下列有关说法中错误的是
A.用 漂白纸浆和用活性炭为糖浆脱色的原理相同 漂白纸浆和用活性炭为糖浆脱色的原理相同 |
B. 的医用酒精可用于杀菌消毒 的医用酒精可用于杀菌消毒 |
C.维生素 可用作食品抗氧剂 可用作食品抗氧剂 |
| D.卤水点豆腐的本质是蛋白质的聚沉 |
您最近一年使用:0次
解题方法
4 . 某研究性学习小组拟用如下装置设计实验,来探究纯净、干燥的氯气与氨气的反应。按要求回答下列问题:

(1)装置A中盛装浓盐酸的仪器名称是_______ ;装置D的作用是_______ ;装置E中饱和食盐水的作用是_______ ;
(2)导气管的正确连接顺序中,a与_______ 连接(填小写字母);
(3)装置F中发生8NH3+3Cl2=6NH4Cl+N2,该反应中氧化剂与还原剂的物质的量之比是_______ ,为使两种气体充分接触,明显地看到_______ 现象,则装置F中j与_______ 连接(填小写字母);
(4)装置B中所发生反应的化学方程式是_______ ;
(5)该学习小组研究发现,整套实验方案的主要缺陷是缺少_______ 装置。

(1)装置A中盛装浓盐酸的仪器名称是
(2)导气管的正确连接顺序中,a与
(3)装置F中发生8NH3+3Cl2=6NH4Cl+N2,该反应中氧化剂与还原剂的物质的量之比是
(4)装置B中所发生反应的化学方程式是
(5)该学习小组研究发现,整套实验方案的主要缺陷是缺少
您最近一年使用:0次
解题方法
5 . 回答下列问题:
(1)在分析化学中,可以采用酸性高锰酸钾与Fe2+反应来检测Fe2+的含量:Fe2+与酸性高锰酸钾发生如下反应:Fe2++MnO +H+=Mn2++Fe3++H2O。
+H+=Mn2++Fe3++H2O。
①配平上述离子方程式并用单线桥法描述电子转移的方向及数目:_____ 。
____Fe2++____MnO +_____H+=_____Mn2++_____Fe3++_____H2O
+_____H+=_____Mn2++_____Fe3++_____H2O
②若有0.5molKMnO4参与反应,则有____ 个电子发生转移。
③其中,_____ 是氧化剂,____ 元素被氧化。
(2)以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3•6H2O)的工艺流程如图:
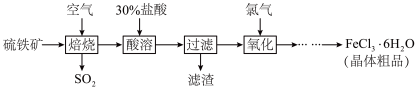
完成下列填空:
①硫铁矿焙烧后的烧渣中含有Fe2O3、Fe3O4等。酸溶后溶液中主要存在的阳离子有____ ,不能用硫酸代替盐酸的原因是____ 。
②通入氯气时,主要反应的离子方程式为____ 。从氧化后的溶液中得到氯化铁晶体的实验步骤为____ 、____ 、过滤洗涤。
(1)在分析化学中,可以采用酸性高锰酸钾与Fe2+反应来检测Fe2+的含量:Fe2+与酸性高锰酸钾发生如下反应:Fe2++MnO
 +H+=Mn2++Fe3++H2O。
+H+=Mn2++Fe3++H2O。①配平上述离子方程式并用单线桥法描述电子转移的方向及数目:
____Fe2++____MnO
 +_____H+=_____Mn2++_____Fe3++_____H2O
+_____H+=_____Mn2++_____Fe3++_____H2O②若有0.5molKMnO4参与反应,则有
③其中,
(2)以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3•6H2O)的工艺流程如图:

完成下列填空:
①硫铁矿焙烧后的烧渣中含有Fe2O3、Fe3O4等。酸溶后溶液中主要存在的阳离子有
②通入氯气时,主要反应的离子方程式为
您最近一年使用:0次
解题方法
6 . 饮用水消毒剂有多种,其中既能对水进行杀菌消毒,又能起到聚沉水中的悬浮物和杂质的是
| A.明矾 | B.氯水 | C.三氯化铝 | D.高铁酸钠(Na2FeO4) |
您最近一年使用:0次
7 . 下图是CO还原CuO的装置图:
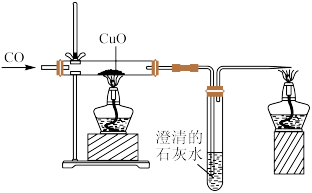
(1)需要先通一会一氧化碳,为了先_______ ,防止一氧化碳纯度不够而爆炸,通一会一氧化碳之后再加热。结束时,先撤掉_______ ,继续通一会一氧化碳,直到玻璃管冷却,防止生成的铜又被氧化,一氧化碳_______ (填“有”或“没有”)毒,加强通风换气,这里通入的气体必须处理掉,用点燃或者小气球收集;
(2)如果用点燃的方法处理多余的CO,化学方程式是_______ ,产物_______ (填“是”或“不是”)温室效应的气体之一,其固体俗称_______ ;
(3)生活中冶炼金属(还原金属氧化物)除常用CO外,还有H2和C等,从经济型和实用型考虑:
①首饰加工店你建议用_______ ,(选填“CO”、“H2或” 或“C”);
②农村打铁铺你建议用_______ ,(选填“CO”、“H2或” 或“C”);
(4)CO还原CuO反应的化学方程式CO+CuO Cu+CO2中,氧化剂是:
Cu+CO2中,氧化剂是:_______ ,还原剂是:_______ ,氧化产物是:_______ ,还原产物是:_______ 。

(1)需要先通一会一氧化碳,为了先
(2)如果用点燃的方法处理多余的CO,化学方程式是
(3)生活中冶炼金属(还原金属氧化物)除常用CO外,还有H2和C等,从经济型和实用型考虑:
①首饰加工店你建议用
②农村打铁铺你建议用
(4)CO还原CuO反应的化学方程式CO+CuO
 Cu+CO2中,氧化剂是:
Cu+CO2中,氧化剂是:
您最近一年使用:0次
解题方法
8 . 工业上采用电解的方法来制备活泼金属铝。纯净的氧化铝熔点很高(约为2045℃),在实际生产中,通过加入助熔剂冰晶石( )在1000℃左右就可得到熔融体。
)在1000℃左右就可得到熔融体。

主要的电极反应为:
阴极: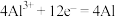
阳极:
总反应为:
在阳极生成的氧气全部与石墨电极反应生成一氧化碳气体和二氧化碳气体,因此在电解过程中,需要不断补充石墨电极,则:
(1)生产1t金属铝,转移电子的物质的量是___________ 。
(2)工业生产中,生产1t铝阳极损失0.6t石墨。石墨被氧化的产物是____ ,质量为______ 。
 )在1000℃左右就可得到熔融体。
)在1000℃左右就可得到熔融体。
主要的电极反应为:
阴极:
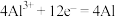
阳极:

总反应为:

在阳极生成的氧气全部与石墨电极反应生成一氧化碳气体和二氧化碳气体,因此在电解过程中,需要不断补充石墨电极,则:
(1)生产1t金属铝,转移电子的物质的量是
(2)工业生产中,生产1t铝阳极损失0.6t石墨。石墨被氧化的产物是
您最近一年使用:0次
9 . 请根据元素周期律、元素周期表的知识解决下列问题。
(1)写出以下元素的元素符号。其单质氧化性最强的元素:______ ,短周期中其单质还原性最强的元素:________ 。
(2)从原子结构的角度说明Cl的得电子能力比S强的原因:___________ 。
(3)已知33As、35Br位于同一周期,请完成下列排序。
①As3-、Br-的还原性:_______ >_______ 。
②H3AsO4、H2SO4、H3PO4的酸性:_______ >_______ >________ 。
(1)写出以下元素的元素符号。其单质氧化性最强的元素:
(2)从原子结构的角度说明Cl的得电子能力比S强的原因:
(3)已知33As、35Br位于同一周期,请完成下列排序。
①As3-、Br-的还原性:
②H3AsO4、H2SO4、H3PO4的酸性:
您最近一年使用:0次
10 . 动手实践:在食盐中加碘是预防碘缺乏症的有效方法。通常,在食盐中加碘有两种方法:一种是加入碘化钾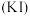 ,另一种是加入碘酸钾
,另一种是加入碘酸钾 。请设计实验方案检测某种含碘盐中加入的是碘化钾还是碘酸钾,并检测自己家中的含碘盐
。请设计实验方案检测某种含碘盐中加入的是碘化钾还是碘酸钾,并检测自己家中的含碘盐_________ 。[提示:①碘单质 遇淀粉变蓝;②维生素C是生活中可利用的还原剂;③“84”消毒液是生活中可利用的氧化剂]
遇淀粉变蓝;②维生素C是生活中可利用的还原剂;③“84”消毒液是生活中可利用的氧化剂]
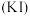 ,另一种是加入碘酸钾
,另一种是加入碘酸钾 。请设计实验方案检测某种含碘盐中加入的是碘化钾还是碘酸钾,并检测自己家中的含碘盐
。请设计实验方案检测某种含碘盐中加入的是碘化钾还是碘酸钾,并检测自己家中的含碘盐 遇淀粉变蓝;②维生素C是生活中可利用的还原剂;③“84”消毒液是生活中可利用的氧化剂]
遇淀粉变蓝;②维生素C是生活中可利用的还原剂;③“84”消毒液是生活中可利用的氧化剂]
您最近一年使用:0次



