解题方法
1 . 电解熔融氯化钙可以得到金属钙和氯气,钙在氯气中燃烧又能生成氯化钙。请根据已有知识,按下图箭头符号所表示的物质间发生的转化,写出相应反应的化学方程式,并指出哪些是氧化还原反应。
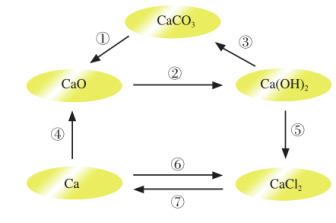
①_______ ;②_______ ;③_______ ;④_______ ;⑤_______ ;⑥_______ ;⑦_______ ;哪些反应是氧化还原反应_______ 。

①
您最近一年使用:0次
名校
解题方法
2 . CO和CO2是碳的两种重要氧化物。
(1)在标准状况下,5.6L CO2的物质的量是_______ mol,质量是_______ g;
(2)14g CO的体积是_______ L(标准状况);
(3)标准状况下11.2L CO与_______ g CO2中所含的氧原子数相同;
(4)标准状况下11.2L CO2与足量的Na2O2反应时转移电子数为_______ 。
(1)在标准状况下,5.6L CO2的物质的量是
(2)14g CO的体积是
(3)标准状况下11.2L CO与
(4)标准状况下11.2L CO2与足量的Na2O2反应时转移电子数为
您最近一年使用:0次
名校
3 . 工业上可用以下方案使饮用水中 含量达标。
含量达标。
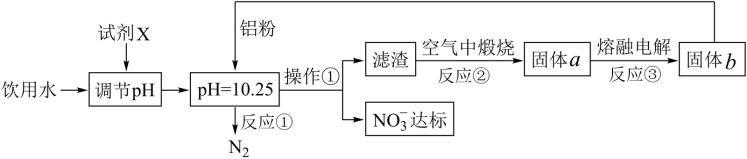
已知:滤渣的成分为 ,固体a是
,固体a是 ,固体b是
,固体b是 。
。
(1)流程中操作①的名称为_________ 。
(2)写出反应①中铝粉和 反应的离子方程式:
反应的离子方程式:_________ 。
(3)已知反应②为非氧化还原的分解反应,写出该反应的化学方程式:_________ 。
(4)已知反应③也是分解反应,写出该反应的化学方程式:_________ 。
(5)关于 ,下列说法不正确的是
,下列说法不正确的是_________ 。
A、是两性氧化物 B、是碱性氧化物 C、能与 溶液反应 D、能与稀硫酸反应 E、是电解质 F、固体状态可以导电
溶液反应 D、能与稀硫酸反应 E、是电解质 F、固体状态可以导电
(6)还可用以下化学反应使饮用水中 含量达标,完成下列离子方程式:
含量达标,完成下列离子方程式:_________ 。

 含量达标。
含量达标。
已知:滤渣的成分为
 ,固体a是
,固体a是 ,固体b是
,固体b是 。
。(1)流程中操作①的名称为
(2)写出反应①中铝粉和
 反应的离子方程式:
反应的离子方程式:(3)已知反应②为非氧化还原的分解反应,写出该反应的化学方程式:
(4)已知反应③也是分解反应,写出该反应的化学方程式:
(5)关于
 ,下列说法不正确的是
,下列说法不正确的是A、是两性氧化物 B、是碱性氧化物 C、能与
 溶液反应 D、能与稀硫酸反应 E、是电解质 F、固体状态可以导电
溶液反应 D、能与稀硫酸反应 E、是电解质 F、固体状态可以导电(6)还可用以下化学反应使饮用水中
 含量达标,完成下列离子方程式:
含量达标,完成下列离子方程式:
您最近一年使用:0次
4 . 填空
(1)用双线桥法表示氧化还原反应2KMnO4 K2MnO4+MnO2+O2↑电子转移的方向和数目
K2MnO4+MnO2+O2↑电子转移的方向和数目_____ 。
(2)在这个反应6Fe2++ +14H+=6Fe3++2Cr3++7H2O中氧化剂为
+14H+=6Fe3++2Cr3++7H2O中氧化剂为_______ ,还原剂为_______ ,_______ 元素被还原,氧化产物是_______ ;氧化性强弱为:_______ >_______ 。
(3)写出下列反应的离子方程式。
①铜与硝酸银溶液的反应:_______ 。
②Na和H2O的反应:_______ 。
(1)用双线桥法表示氧化还原反应2KMnO4
 K2MnO4+MnO2+O2↑电子转移的方向和数目
K2MnO4+MnO2+O2↑电子转移的方向和数目(2)在这个反应6Fe2++
 +14H+=6Fe3++2Cr3++7H2O中氧化剂为
+14H+=6Fe3++2Cr3++7H2O中氧化剂为(3)写出下列反应的离子方程式。
①铜与硝酸银溶液的反应:
②Na和H2O的反应:
您最近一年使用:0次
名校
解题方法
5 . 回答下列问题
(1)在下列各反应均涉及HCl:
①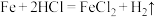 ②
②
③ ④
④
其中HCl做还原剂的是_______ (填序号),HCl做氧化剂的是_______ (填序号);试比较Cl2、Br2、KClO3的氧化性,其由强到弱的顺序为_______ ;试用“单线桥法”标明④中电子转移的方向和数目_______ 。
(2)黑火药着火时主要发生化学反应: 。该反应中被还原的元素为
。该反应中被还原的元素为_______ ,氧化产物为_______ ,若生成14gN2,则转移电子数目为_______ 。
(3)CuCl常用作催化剂,可以在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液加热生成CuCl沉淀,请写出该反应的离子方程式_______ 。
(1)在下列各反应均涉及HCl:
①
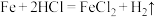 ②
②
③
 ④
④
其中HCl做还原剂的是
(2)黑火药着火时主要发生化学反应:
 。该反应中被还原的元素为
。该反应中被还原的元素为(3)CuCl常用作催化剂,可以在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液加热生成CuCl沉淀,请写出该反应的离子方程式
您最近一年使用:0次
解题方法
6 . 氟及化合物
(1)德国人斯瓦恩哈德是从事玻璃加工的一名工人。1670年,他无意中将萤石与浓硫酸1∶1混合在一起,结果产生了一种具有刺激性气味的烟雾,他发现这种气体能腐蚀玻璃,从而研究出一种不用金刚石或其他磨料也可以在玻璃上刻蚀图案的方法。利用这种方法,斯瓦恩哈德制成了许多玻璃艺术品,成为有名的玻璃雕刻艺术家。写出上述化学反应方程式_______ 。
(2)单质氟的制备是化学史上一段悲壮的历史,有多位化学家中毒,甚至付出生命,但是化学家们不畏艰难、前仆后继。终于,1886年法国化学家莫瓦桑在总结前人经验与教训的基础上,在低温下电解熔融的氟化氢钾制得单质氟,这距离氢氟酸的发现已经过去一百多年之久。写出电解制备单质氟的反应方程式_______ 。
(3)又过了整整一百年,化学方法制取F2获得成功。其步骤如下:在 存在下,用
存在下,用 氧化
氧化 ;
; 和HF反应;
和HF反应;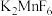 和
和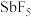 反应。写出各步的化学反应方程式
反应。写出各步的化学反应方程式_______ 、_______ 、_______ 。
(4)氟单质的反应性非常强,可与稀有气体氙发生反应。已知:
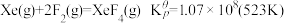 ,
,
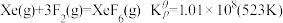 ,
,
XeF6的立方晶型中有四聚体单元, 与其中5个F的键长为
与其中5个F的键长为 ,与第6个F的键长为
,与第6个F的键长为 。
。
①在满足反应速率的前题下,应如何控制温度才有利于 的生成
的生成_______ 。
②若在523K下以Xe和F2制取XeF6,并使产物中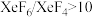 ,计算说明F2的平衡分压至少应保持在标准压力的
,计算说明F2的平衡分压至少应保持在标准压力的_______ 倍(精确到小数点后第一位)?
③指出XeF6气体的分子构型_______ 。
④说明XeF6晶体中存在着什么样的离子_______ ?画出正离子的构型简图_______ 。
⑤按照电子理论,将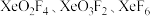 酸性从大到小的顺序排列
酸性从大到小的顺序排列_______ 。
(5)法国科学家盖·吕萨克也曾试图制备氢氟酸。1809年,他把氟化钙与硼酸混和加热,但是却意外地制成了一种所谓的“氟酸气”A。气体A可与 发生反应,生成多卤阳离子B和一四面体阴离子C,写出离子反应方程式
发生反应,生成多卤阳离子B和一四面体阴离子C,写出离子反应方程式_______ ,画B的结构简图_______ ;将A通入碳酸钠溶液也可发生反应,写出离子反应方程式_______ 。
(6)氟与硼可形成一系列硼的低卤化物,如,具有平面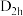 结构的
结构的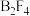 、类似乙硼烷结构的
、类似乙硼烷结构的 ,画出
,画出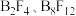 的结构简图
的结构简图_______ 、_______ 。
(7)在 溶液中加入
溶液中加入 ,然后再加入
,然后再加入 ,通过计算说明能否发生氧化还原反应
,通过计算说明能否发生氧化还原反应_______ 。(已知 ,
, ,
, ,设有关物质的浓度都为
,设有关物质的浓度都为 )。
)。
(1)德国人斯瓦恩哈德是从事玻璃加工的一名工人。1670年,他无意中将萤石与浓硫酸1∶1混合在一起,结果产生了一种具有刺激性气味的烟雾,他发现这种气体能腐蚀玻璃,从而研究出一种不用金刚石或其他磨料也可以在玻璃上刻蚀图案的方法。利用这种方法,斯瓦恩哈德制成了许多玻璃艺术品,成为有名的玻璃雕刻艺术家。写出上述化学反应方程式
(2)单质氟的制备是化学史上一段悲壮的历史,有多位化学家中毒,甚至付出生命,但是化学家们不畏艰难、前仆后继。终于,1886年法国化学家莫瓦桑在总结前人经验与教训的基础上,在低温下电解熔融的氟化氢钾制得单质氟,这距离氢氟酸的发现已经过去一百多年之久。写出电解制备单质氟的反应方程式
(3)又过了整整一百年,化学方法制取F2获得成功。其步骤如下:在
 存在下,用
存在下,用 氧化
氧化 ;
; 和HF反应;
和HF反应;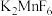 和
和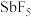 反应。写出各步的化学反应方程式
反应。写出各步的化学反应方程式(4)氟单质的反应性非常强,可与稀有气体氙发生反应。已知:
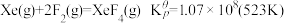 ,
,
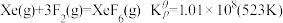 ,
,
XeF6的立方晶型中有四聚体单元,
 与其中5个F的键长为
与其中5个F的键长为 ,与第6个F的键长为
,与第6个F的键长为 。
。①在满足反应速率的前题下,应如何控制温度才有利于
 的生成
的生成②若在523K下以Xe和F2制取XeF6,并使产物中
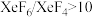 ,计算说明F2的平衡分压至少应保持在标准压力的
,计算说明F2的平衡分压至少应保持在标准压力的③指出XeF6气体的分子构型
④说明XeF6晶体中存在着什么样的离子
⑤按照电子理论,将
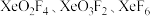 酸性从大到小的顺序排列
酸性从大到小的顺序排列(5)法国科学家盖·吕萨克也曾试图制备氢氟酸。1809年,他把氟化钙与硼酸混和加热,但是却意外地制成了一种所谓的“氟酸气”A。气体A可与
 发生反应,生成多卤阳离子B和一四面体阴离子C,写出离子反应方程式
发生反应,生成多卤阳离子B和一四面体阴离子C,写出离子反应方程式(6)氟与硼可形成一系列硼的低卤化物,如,具有平面
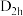 结构的
结构的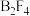 、类似乙硼烷结构的
、类似乙硼烷结构的 ,画出
,画出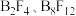 的结构简图
的结构简图(7)在
 溶液中加入
溶液中加入 ,然后再加入
,然后再加入 ,通过计算说明能否发生氧化还原反应
,通过计算说明能否发生氧化还原反应 ,
, ,
, ,设有关物质的浓度都为
,设有关物质的浓度都为 )。
)。
您最近一年使用:0次
解题方法
7 . 工业废水中的砷(As)(以+3和+5价的形式存在)会对环境造成严重污染。某化学兴趣小组分别以H3AsO3和H3AsO4以及Na3AsO3和Na3AsO4溶液模拟该类废水进行研究后,发现沉淀法和吸附法能使废水中的砷含量显著降低,达到排放标准。
(1)沉淀法:
①在H3AsO3水溶液中加入适量石灰乳,能够产生Ca3(AsO3)2沉淀。该反应的化学方程式为_______ 。
②在Na3AsO4溶液中加入磷酸铋(BiPO4),室温下达到平衡:BiPO4 (s)+ AsO (aq)
(aq)  BiAsO4 (s)+ PO
BiAsO4 (s)+ PO (aq),则溶液中c(AsO
(aq),则溶液中c(AsO )/c(PO
)/c(PO )=
)=_______ 。已知:Ksp(BiPO4)= a,Ksp(BiAsO4)=b
(2)氧化吸附法:
①已知AsO 比AsO
比AsO 的毒性更强,Bi5+具有强氧化性。写出碱性溶液中,Bi5+氧化AsO
的毒性更强,Bi5+具有强氧化性。写出碱性溶液中,Bi5+氧化AsO 得到BiAsO4沉淀的离子方程式
得到BiAsO4沉淀的离子方程式_______ 。
②Fe(OH)3胶体对五价砷有着良好的吸附性,溶液的pH对吸附剂表面所带电荷有影响。采用Bi5+和Fe2+联合处理含砷废水,在AsO 溶液中分别加入Bi5+和Fe2+,两种试剂先后顺序是
溶液中分别加入Bi5+和Fe2+,两种试剂先后顺序是_______ ,原因是_______ 。
③研究发现;pH越高,Fe(OH)3胶体对五价砷的吸附能力越弱,原因是_______ 。
(1)沉淀法:
①在H3AsO3水溶液中加入适量石灰乳,能够产生Ca3(AsO3)2沉淀。该反应的化学方程式为
②在Na3AsO4溶液中加入磷酸铋(BiPO4),室温下达到平衡:BiPO4 (s)+ AsO
 (aq)
(aq)  BiAsO4 (s)+ PO
BiAsO4 (s)+ PO (aq),则溶液中c(AsO
(aq),则溶液中c(AsO )/c(PO
)/c(PO )=
)=(2)氧化吸附法:
①已知AsO
 比AsO
比AsO 的毒性更强,Bi5+具有强氧化性。写出碱性溶液中,Bi5+氧化AsO
的毒性更强,Bi5+具有强氧化性。写出碱性溶液中,Bi5+氧化AsO 得到BiAsO4沉淀的离子方程式
得到BiAsO4沉淀的离子方程式②Fe(OH)3胶体对五价砷有着良好的吸附性,溶液的pH对吸附剂表面所带电荷有影响。采用Bi5+和Fe2+联合处理含砷废水,在AsO
 溶液中分别加入Bi5+和Fe2+,两种试剂先后顺序是
溶液中分别加入Bi5+和Fe2+,两种试剂先后顺序是③研究发现;pH越高,Fe(OH)3胶体对五价砷的吸附能力越弱,原因是
您最近一年使用:0次
名校
解题方法
8 . 氮是一种地球上含量丰富的元素。如图表示氮及其化合物在一定条件下的转化关系:
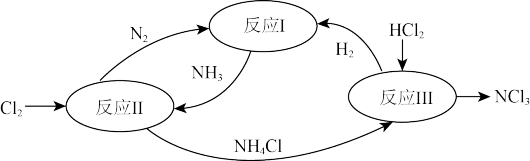
(1)氮元素在不同的物质中存在循环,体现了化学反应前后_______ (填“分子种类”、“原子种类”或“离子种类”)不变
(2)反应Ⅰ所属的基本反应类型是_______
(3)反应Ⅱ的化学方程式为_______
(4)氨是氮肥工业的重要原料;某化肥厂生产铵态氮肥 的工艺流程如图:
的工艺流程如图:
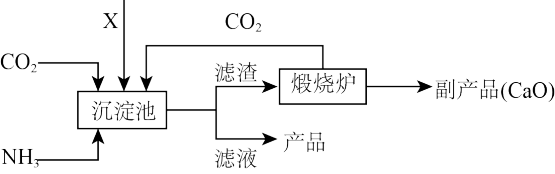
①加入的X应为_______ (填字母序号)
A. B.
B. C.
C.
②生产流程中能被循环利用的物质是_______

(1)氮元素在不同的物质中存在循环,体现了化学反应前后
(2)反应Ⅰ所属的基本反应类型是
(3)反应Ⅱ的化学方程式为
(4)氨是氮肥工业的重要原料;某化肥厂生产铵态氮肥
 的工艺流程如图:
的工艺流程如图:
①加入的X应为
A.
 B.
B. C.
C.
②生产流程中能被循环利用的物质是
您最近一年使用:0次
名校
9 . 唐代李白《秋浦歌(第十四)》“炉火照天地,红星乱紫烟,赥郎明月夜,歌声动寒川”,展现了一幅瑰玮壮观的秋夜冶炼图。秋浦(今安徽省贵池县西)是唐代铜的产地,其铜矿含 ,在冶炼过程中存在主要反应:①
,在冶炼过程中存在主要反应:①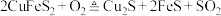 ②
②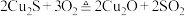
③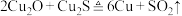 。下列有关叙述正确的是
。下列有关叙述正确的是
 ,在冶炼过程中存在主要反应:①
,在冶炼过程中存在主要反应:①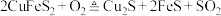 ②
②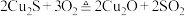
③
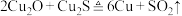 。下列有关叙述正确的是
。下列有关叙述正确的是A.上述冶炼方法属于热还原法,还原剂为 |
| B.反应①中铜元素化合价不变,铁元素的化合价降低 |
C.反应②中有2mol 发生反应时,共转移6mol 发生反应时,共转移6mol |
D.反应③中 是氧化剂, 是氧化剂, 既是氧化剂又是还原剂 既是氧化剂又是还原剂 |
您最近一年使用:0次
2022-10-01更新
|
273次组卷
|
2卷引用:湖南省株洲市第一中学2021届高三第一次模拟检测化学试题
10 . 下列选项中所描述的关系中物质的量比为2:1的是
| A.NO2与水反应中的氧化剂与还原剂之比 |
| B.H2S与SO2反应中氧化产物与还原产物之比 |
C.CH4(g)+CO2(g) 2CO(g)+2H2(g)平衡时速率υ(正、CH4),υ(逆、CO)之比 2CO(g)+2H2(g)平衡时速率υ(正、CH4),υ(逆、CO)之比 |
| D.氢氧燃料电池工作时,同一时间内正负极消耗的两种气体(同温同压条件下) |
您最近一年使用:0次
2022-09-26更新
|
76次组卷
|
2卷引用:辽宁省沈阳市新民市第一高级中学2020-2021学年高一下学期期中考试化学试题



