1 . 已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
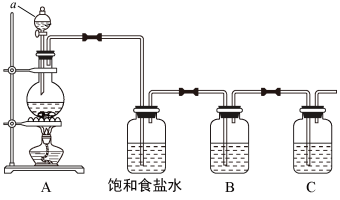
(1)仪器a的名称为___________
(2)请写出A装置中发生反应的化学方程式___________ 。
(3)饱和食盐水的作用是___________ 。
(4)装置B中盛放的试剂是___________ (选填下列所给试剂的编号),反应离子方程式是___________ 。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液
(5)还有哪些事实能够说明氯元素的非金属性比疏元素的非金属性强___________ (填编号)
① 比
比 稳定
稳定
② 氧化性比
氧化性比 强
强
③ 酸性比
酸性比 强
强
④ 酸性比
酸性比 强 ⑤氯原子最外层有7个电子,硫原子最外层有6个电子
强 ⑤氯原子最外层有7个电子,硫原子最外层有6个电子
⑥ 与铁反应生成
与铁反应生成 ,而S与铁反应生成
,而S与铁反应生成

(1)仪器a的名称为
(2)请写出A装置中发生反应的化学方程式
(3)饱和食盐水的作用是
(4)装置B中盛放的试剂是
A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液(5)还有哪些事实能够说明氯元素的非金属性比疏元素的非金属性强
①
 比
比 稳定
稳定 ②
 氧化性比
氧化性比 强
强 ③
 酸性比
酸性比 强
强④
 酸性比
酸性比 强 ⑤氯原子最外层有7个电子,硫原子最外层有6个电子
强 ⑤氯原子最外层有7个电子,硫原子最外层有6个电子⑥
 与铁反应生成
与铁反应生成 ,而S与铁反应生成
,而S与铁反应生成
您最近一年使用:0次
解题方法
2 . 面对新冠病毒,VB空气防护卡也成了“网红”,成为人们讨论的话题。商品介绍卡片中含有的主要活性成分——亚氯酸钠,在接触空气时可以释放安全可靠的低浓度二氧化氯( ),从而达到消除病毒、细菌活性的防护效果。
),从而达到消除病毒、细菌活性的防护效果。 的一种生产工艺如下:
的一种生产工艺如下:
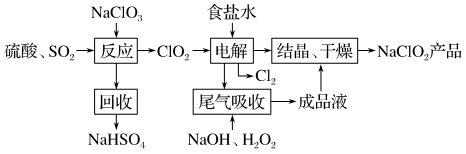
回答下列问题:
(1)写出“反应”步骤中生成 的化学反应方程式:
的化学反应方程式:_______ 。
(2)“电解”所用食盐水由粗盐水精制而成,精制时,为除去 、
、 、
、 ,要加入的试剂分别为
,要加入的试剂分别为_______ 、_______ 、_______ ,为得到纯净的NaCl溶液还需加入_______ (以上填写相应物质的化学式)。
(3)“电解”产生的 可用于工业制漂白液,写出离子反应方程式:
可用于工业制漂白液,写出离子反应方程式:_______ 。
(4)“尾气吸收”是吸收“电解”过程排出的少量 ,此吸收反应中,氧化剂与还原剂的物质的量之比为
,此吸收反应中,氧化剂与还原剂的物质的量之比为_______ ,该反应中还原产物是_______ 。
(5)有同学推测VB空气防护卡原理是因为 与空气中的
与空气中的 发生反应得到
发生反应得到 ,同时得到钠的两种正盐,试写出相应的化学反应方程式:
,同时得到钠的两种正盐,试写出相应的化学反应方程式:_______ 。
 ),从而达到消除病毒、细菌活性的防护效果。
),从而达到消除病毒、细菌活性的防护效果。 的一种生产工艺如下:
的一种生产工艺如下:
回答下列问题:
(1)写出“反应”步骤中生成
 的化学反应方程式:
的化学反应方程式:(2)“电解”所用食盐水由粗盐水精制而成,精制时,为除去
 、
、 、
、 ,要加入的试剂分别为
,要加入的试剂分别为(3)“电解”产生的
 可用于工业制漂白液,写出离子反应方程式:
可用于工业制漂白液,写出离子反应方程式:(4)“尾气吸收”是吸收“电解”过程排出的少量
 ,此吸收反应中,氧化剂与还原剂的物质的量之比为
,此吸收反应中,氧化剂与还原剂的物质的量之比为(5)有同学推测VB空气防护卡原理是因为
 与空气中的
与空气中的 发生反应得到
发生反应得到 ,同时得到钠的两种正盐,试写出相应的化学反应方程式:
,同时得到钠的两种正盐,试写出相应的化学反应方程式:
您最近一年使用:0次
2022-01-19更新
|
504次组卷
|
2卷引用:辽宁省五校2021-2022学年高一上学期期末联考化学试题
解题方法
3 . 采用 双催化剂,可实现用
双催化剂,可实现用 消除酸性废水中的致癌阴离子
消除酸性废水中的致癌阴离子 、
、 ,
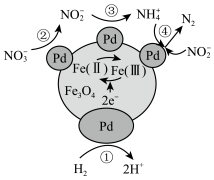
, 中Fe元素的两种价态分别表示为Fe(Ⅱ)、Fe(Ⅲ),其反应历程如图所示。下列说法错误的是
中Fe元素的两种价态分别表示为Fe(Ⅱ)、Fe(Ⅲ),其反应历程如图所示。下列说法错误的是
 双催化剂,可实现用
双催化剂,可实现用 消除酸性废水中的致癌阴离子
消除酸性废水中的致癌阴离子 、
、 ,
, 中Fe元素的两种价态分别表示为Fe(Ⅱ)、Fe(Ⅲ),其反应历程如图所示。下列说法错误的是
中Fe元素的两种价态分别表示为Fe(Ⅱ)、Fe(Ⅲ),其反应历程如图所示。下列说法错误的是
| A.反应历程中Fe(Ⅱ)与Fe(Ⅲ)总物质的量不变 |
B.过程②发生的反应为: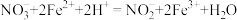 |
C.过程①中产生0.5mol 则消除46g 则消除46g |
| D.用该法处理后废水的酸性也会变弱 |
您最近一年使用:0次
名校
4 . 磁性纳米四氧化三铁在催化剂、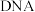 检测、疾病的诊断和治疗等领域应用广泛,其制备方法有多种,“共沉淀法”制备纳米
检测、疾病的诊断和治疗等领域应用广泛,其制备方法有多种,“共沉淀法”制备纳米 的流程如下:
的流程如下:
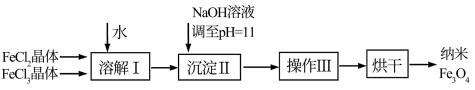
(1)Ⅱ中的反应温度需控制在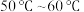 之间,生成
之间,生成 的离子方程式是
的离子方程式是_______ 。
(2)操作Ⅲ分离 的方法为过滤,所需的玻璃仪器为烧杯、
的方法为过滤,所需的玻璃仪器为烧杯、_______ 、_______ 。
(3)某同学依据上述“共沉淀法”的思路在实验室模拟制备纳米 ;为得到较纯净的纳米
;为得到较纯净的纳米 ,
, 与
与 的物质的量之比最好为
的物质的量之比最好为_______ 。但实际操作时,却很难控制这一比例,原因是_______ 。
(4)经过多次实验发现,当混合溶液中 时,容易得到理想的纳米
时,容易得到理想的纳米 。在此条件下,如何检验
。在此条件下,如何检验 是否沉淀完全
是否沉淀完全_______ 。
(5)以太阳能为热源分解 ,铁氧化合物循环分解水制
,铁氧化合物循环分解水制 的过程如图所示。
的过程如图所示。
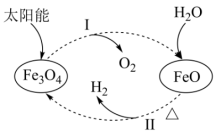
①下列叙述正确的是_______ (填字母)。
A.过程Ⅰ的能量转化为太阳能→化学能
B.过程Ⅰ中 为氧化剂
为氧化剂
C.过程中的 为碱性氧化物
为碱性氧化物
D.铁氧化合物循环制 与电解水制
与电解水制 相比,具有节约能源的优点
相比,具有节约能源的优点
②请写出反应Ⅱ对应的化学方程式_______ 。
(6)为了防止枪支生锈,常采用化学处理使钢铁零件表面生成 的致密保护层——“发蓝”。化学处理过程中其中一步的反应为:
的致密保护层——“发蓝”。化学处理过程中其中一步的反应为: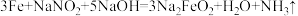 。下列有关的叙述不正确的是_______(填字母)。
。下列有关的叙述不正确的是_______(填字母)。
 检测、疾病的诊断和治疗等领域应用广泛,其制备方法有多种,“共沉淀法”制备纳米
检测、疾病的诊断和治疗等领域应用广泛,其制备方法有多种,“共沉淀法”制备纳米 的流程如下:
的流程如下:
(1)Ⅱ中的反应温度需控制在
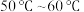 之间,生成
之间,生成 的离子方程式是
的离子方程式是(2)操作Ⅲ分离
 的方法为过滤,所需的玻璃仪器为烧杯、
的方法为过滤,所需的玻璃仪器为烧杯、(3)某同学依据上述“共沉淀法”的思路在实验室模拟制备纳米
 ;为得到较纯净的纳米
;为得到较纯净的纳米 ,
, 与
与 的物质的量之比最好为
的物质的量之比最好为(4)经过多次实验发现,当混合溶液中
 时,容易得到理想的纳米
时,容易得到理想的纳米 。在此条件下,如何检验
。在此条件下,如何检验 是否沉淀完全
是否沉淀完全(5)以太阳能为热源分解
 ,铁氧化合物循环分解水制
,铁氧化合物循环分解水制 的过程如图所示。
的过程如图所示。
①下列叙述正确的是
A.过程Ⅰ的能量转化为太阳能→化学能
B.过程Ⅰ中
 为氧化剂
为氧化剂C.过程中的
 为碱性氧化物
为碱性氧化物D.铁氧化合物循环制
 与电解水制
与电解水制 相比,具有节约能源的优点
相比,具有节约能源的优点②请写出反应Ⅱ对应的化学方程式
(6)为了防止枪支生锈,常采用化学处理使钢铁零件表面生成
 的致密保护层——“发蓝”。化学处理过程中其中一步的反应为:
的致密保护层——“发蓝”。化学处理过程中其中一步的反应为: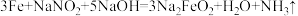 。下列有关的叙述不正确的是_______(填字母)。
。下列有关的叙述不正确的是_______(填字母)。A. 的氧化性大于 的氧化性大于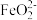 的氧化性 的氧化性 |
B.反应中转移电子 ,则生成还原产物 ,则生成还原产物 |
| C.枪支“发蓝”实质上是使铁表面钝化生成致密保护层导致难以生锈 |
D.上述反应中,若有 单质铁被氧化,生成的氨气在标准状况下的体积为1.12升(假设氨气完全逸出) 单质铁被氧化,生成的氨气在标准状况下的体积为1.12升(假设氨气完全逸出) |
您最近一年使用:0次
2022-01-19更新
|
287次组卷
|
2卷引用:辽宁省抚顺市六校协作体2021-2022学年高一上学期期末考试化学试题
解题方法
5 . 已知氢碘酸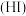 是一种具有强还原性的强酸,
是一种具有强还原性的强酸, 可以与多种物质【如:
可以与多种物质【如: 、
、 、
、 、
、 、
、 、
、 等】发生不同类型的化学反应.请回答下列问题:
等】发生不同类型的化学反应.请回答下列问题:
(1)下图可表示离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是_________ (填标号).
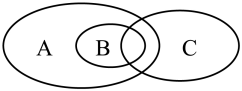
(2) 在水溶液中的电离方程式为
在水溶液中的电离方程式为_________________ .
(3)常温下 溶液与
溶液与 反应的化学方程式为
反应的化学方程式为 ,说明还原性
,说明还原性
______  (填“>”、“<”或“=).
(填“>”、“<”或“=).
(4)在反应 ,氧化剂与还原剂的物质的量之比为
,氧化剂与还原剂的物质的量之比为________ .
(5)下列三种氧化剂均可以将 氧化生成
氧化生成 ,自身对应的还原产物情况如下:
,自身对应的还原产物情况如下:
请判断等物质的量的三种氧化剂分别与足量HI作用,得到I2质量最多的是________ (填选项标号).
(6)向 胶体中逐滴加入HI稀溶液,会出现如下一系列变化:先出现红褐色沉淀;随后沉淀溶解,溶液呈黄色:最后溶液颜色加深.
胶体中逐滴加入HI稀溶液,会出现如下一系列变化:先出现红褐色沉淀;随后沉淀溶解,溶液呈黄色:最后溶液颜色加深.
①红褐色沉淀溶解,反应的离子方程式为___________________________ .
②最后溶液颜色加深,反应的离子方程式为______________________________ .
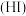 是一种具有强还原性的强酸,
是一种具有强还原性的强酸, 可以与多种物质【如:
可以与多种物质【如: 、
、 、
、 、
、 、
、 、
、 等】发生不同类型的化学反应.请回答下列问题:
等】发生不同类型的化学反应.请回答下列问题:(1)下图可表示离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(2)
 在水溶液中的电离方程式为
在水溶液中的电离方程式为(3)常温下
 溶液与
溶液与 反应的化学方程式为
反应的化学方程式为 ,说明还原性
,说明还原性
 (填“>”、“<”或“=).
(填“>”、“<”或“=).(4)在反应
 ,氧化剂与还原剂的物质的量之比为
,氧化剂与还原剂的物质的量之比为(5)下列三种氧化剂均可以将
 氧化生成
氧化生成 ,自身对应的还原产物情况如下:
,自身对应的还原产物情况如下:选项 | A | B | C |
氧化剂 |
|
|
|
还原产物 |
|
|
|
(6)向
 胶体中逐滴加入HI稀溶液,会出现如下一系列变化:先出现红褐色沉淀;随后沉淀溶解,溶液呈黄色:最后溶液颜色加深.
胶体中逐滴加入HI稀溶液,会出现如下一系列变化:先出现红褐色沉淀;随后沉淀溶解,溶液呈黄色:最后溶液颜色加深.①红褐色沉淀溶解,反应的离子方程式为
②最后溶液颜色加深,反应的离子方程式为
您最近一年使用:0次
6 . 某离子反应中涉及 、
、 、
、 、H+、N2、Cl-六种粒子,其中
、H+、N2、Cl-六种粒子,其中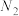 的物质的量随时间变化的曲线如图所示.下列判断正确的是
的物质的量随时间变化的曲线如图所示.下列判断正确的是

 、
、 、
、 、H+、N2、Cl-六种粒子,其中
、H+、N2、Cl-六种粒子,其中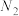 的物质的量随时间变化的曲线如图所示.下列判断正确的是
的物质的量随时间变化的曲线如图所示.下列判断正确的是
| A.反应后溶液的酸性增强 | B.标准状况下,生成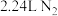 时,反应中转移 时,反应中转移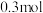 电子 电子 |
| C.氧化产物与还原产物的物质的量之比为2∶1 | D. 被还原,是还原剂 被还原,是还原剂 |
您最近一年使用:0次
2022-01-18更新
|
317次组卷
|
2卷引用:辽宁省锦州市2021-2022学年高一上学期期末考试化学试题
解题方法
7 . 下列反应对应的离子方程式正确的是
A.将 溶液与酸性 溶液与酸性 溶液混合: 溶液混合: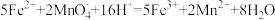 |
B.向稀硫酸中加入少量氧化亚铁: |
C.向稀盐酸中加入少量铁粉: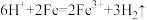 |
D.向氢氧化钠稀溶液中加入适量的铝片: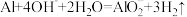 |
您最近一年使用:0次
名校
8 . 某工厂的工业废水中含有大量FeSO4和较多的Cu2+。为了减小污染并变废为宝,工厂计划从该废水中回收FeSO4和金属铜。现根据以下流程图,在实验室模拟该过程,回答下列问题。
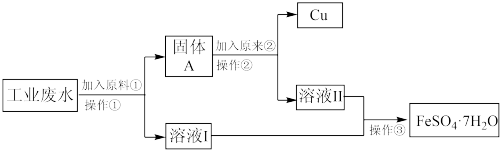
(1)原料①代表的物质为_______ ,原料②代表的物质为_______ 。
(2)实验室模拟操作①和②用到的玻璃仪器有_______ 。
(3)向盛有2mL溶液Ⅱ的试管中,滴入少量过氧化氢溶液,试写出发生反应的离子方程式,并用双线桥标出电子转移的方向和数目_______ ,再向所得溶液中滴加适量的淀粉KI溶液,现象为_______ ,发生反应的离子方程式为_______ ;向另一支盛有2mLKMnO4溶液的试管中,滴入适量溶液Ⅱ,发生反应的离子方程式为_______ 。

(1)原料①代表的物质为
(2)实验室模拟操作①和②用到的玻璃仪器有
(3)向盛有2mL溶液Ⅱ的试管中,滴入少量过氧化氢溶液,试写出发生反应的离子方程式,并用双线桥标出电子转移的方向和数目
您最近一年使用:0次
名校
9 . 随着新型冠状病毒感染的肺炎确诊病例越来越多,消毒已成了人们关注的话题。前不久李兰娟院士说过新冠病毒的几个弱点,比如含氯的消毒剂就可以有效的灭活病毒。某校化学兴趣小组为制备并收集氯气,设计下图装置,装置中的夹持装置和加热装置均已略去。
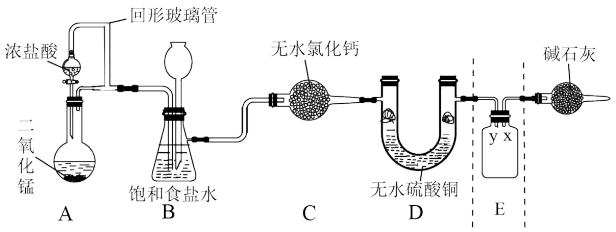
回答下列问题:
(1)写出盛放浓盐酸的仪器名称_______ ,回形玻璃管的作用是_______ 。
(2)写出装置A中发生反应的化学方程式_______ 。
(3)装置C的作用是_______ 。
(4)E装置中导管_______ (填“x”或“y”)应伸至靠近集气瓶底部。
(5)ClO2是目前国际上公认的新一代高效、广谱、安全的杀菌、保鲜剂,在水处理等方面具有广泛的应用。与Cl2相比,ClO2不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
①我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示:
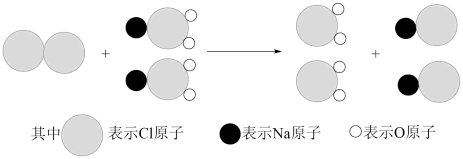
该反应的化学方程式_______ 。
②将ClO2通入酸性淀性粉碘化钾溶液,溶液变成蓝色,ClO2被还原为氯离子,该反应的离子方程式为:_______ 。

回答下列问题:
(1)写出盛放浓盐酸的仪器名称
(2)写出装置A中发生反应的化学方程式
(3)装置C的作用是
(4)E装置中导管
(5)ClO2是目前国际上公认的新一代高效、广谱、安全的杀菌、保鲜剂,在水处理等方面具有广泛的应用。与Cl2相比,ClO2不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
①我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示:

该反应的化学方程式
②将ClO2通入酸性淀性粉碘化钾溶液,溶液变成蓝色,ClO2被还原为氯离子,该反应的离子方程式为:
您最近一年使用:0次
名校
解题方法
10 . NaNO2是一种食品添加剂,但它也能致癌。酸性KMnO4溶液与NaNO2反应的离子方程式为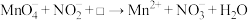 。下列叙述中正确的是
。下列叙述中正确的是
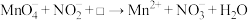 。下列叙述中正确的是
。下列叙述中正确的是A.该反应中 被还原 被还原 | B.Mn2+的还原性强于 |
| C.生成1molNaNO3需消耗0.4molKMnO4 | D.□中的粒子是OH- |
您最近一年使用:0次




