名校
解题方法
1 . 室温下,通过下列实验探究0.01000 mo/L  溶液的性质:
溶液的性质:
实验1:实验测得0.01000 mol/L 溶液pH为8.6
溶液pH为8.6
实验2:向溶液中滴加等体积0.01000 mol/L HCl溶液,pH由8.6降为4.8
实验3:向溶液中加入等体积0.0200 mo/L 溶液,出现白色沉淀
溶液,出现白色沉淀
实验4:向稀硫酸酸化的 溶液中滴加
溶液中滴加 溶液至溶液褪色
溶液至溶液褪色
下列说法不正确的是
 溶液的性质:
溶液的性质:实验1:实验测得0.01000 mol/L
 溶液pH为8.6
溶液pH为8.6实验2:向溶液中滴加等体积0.01000 mol/L HCl溶液,pH由8.6降为4.8
实验3:向溶液中加入等体积0.0200 mo/L
 溶液,出现白色沉淀
溶液,出现白色沉淀实验4:向稀硫酸酸化的
 溶液中滴加
溶液中滴加 溶液至溶液褪色
溶液至溶液褪色下列说法不正确的是
A.0.0100   溶液中满足: 溶液中满足: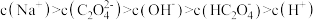 |
B.实验2滴加盐酸过程中存在某一点满足: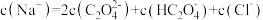 |
C.实验3所得上层清液中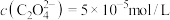 [已知室温时 [已知室温时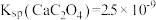 ] ] |
D.实验4发生反应的离子方程式为: |
您最近一年使用:0次
2022-09-02更新
|
601次组卷
|
5卷引用:辽宁省沈阳市五校协作体2021-2022学年高二上学期期末联考化学试题
2 . 氮、磷都是第ⅤA族元素,一些含氮、磷的化合物在生产生活中均有重要应用。
(1)磷化铝、磷化锌、磷化钙是我国目前最常见的熏蒸杀虫剂,都能与水或酸反应产生有毒气体膦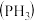 ,写出磷化铝与水反应的化学方程式:
,写出磷化铝与水反应的化学方程式:___________ 。
(2)羟基磷灰石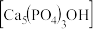 是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
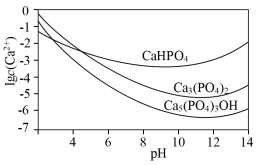
①图中所示3种钙盐,其中在人体中最稳定的存在形式是___________ (填化学式)。
②实验室制备羟基磷灰石时,应将___________ (填“磷酸”或“氢氧化钙悬浊液”,下同)滴加到___________ 中。
(3)氮的氧化物对大气污染比较严重,一定条件下可用 消除污染,请写出
消除污染,请写出 与
与 反应的化学方程式:
反应的化学方程式:___________ ,该反应中,被氧化的氮原子和被还原的氮原子的物质的量之比为___________ ,每消耗1mol ,同时转移
,同时转移___________ mol电子。
(1)磷化铝、磷化锌、磷化钙是我国目前最常见的熏蒸杀虫剂,都能与水或酸反应产生有毒气体膦
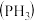 ,写出磷化铝与水反应的化学方程式:
,写出磷化铝与水反应的化学方程式:(2)羟基磷灰石
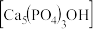 是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
①图中所示3种钙盐,其中在人体中最稳定的存在形式是
②实验室制备羟基磷灰石时,应将
(3)氮的氧化物对大气污染比较严重,一定条件下可用
 消除污染,请写出
消除污染,请写出 与
与 反应的化学方程式:
反应的化学方程式: ,同时转移
,同时转移
您最近一年使用:0次
12-13高三上·浙江宁波·期中
名校
3 . NaNO2是一种食品添加剂,它能致癌。酸性KMnO4溶液与NaNO2反应的化学方程式是:  +
+ +____→Mn2++
+____→Mn2++ +H2O。下列叙述中正确的是
+H2O。下列叙述中正确的是
 +
+ +____→Mn2++
+____→Mn2++ +H2O。下列叙述中正确的是
+H2O。下列叙述中正确的是A.该反应中 被还原 被还原 |
| B.反应过程中溶液的pH减小 |
| C.生成1molNaNO3需消耗0.4molKMnO4 |
| D.横线中的粒子是OH- |
您最近一年使用:0次
2022-07-26更新
|
558次组卷
|
45卷引用:辽宁省盘锦市高级中学2017-2018学年高二下学期期末考试化学试题
辽宁省盘锦市高级中学2017-2018学年高二下学期期末考试化学试题(已下线)2014届福建省南侨中学等五校高中毕业班期末摸底考试化学试卷河南省安阳市第三十六中学2018-2019学年高二6月月考化学试题黑龙江省牡丹江市第一高级中学2019-2020学年高二上学期开学检测化学试题(已下线)2013届浙江省宁波市效实中学高三上学期期中考试化学试卷(已下线)2014高考化学名师知识点精编 专题4氧化还原反应练习卷2016届湖南省益阳市箴言中学高三上学期第二次模拟测试化学试卷2017届新疆兵团农二师华山中学高三上学前考试化学试卷2016-2017学年河南省南阳一中高一上月考二化学卷2016-2017学年河南省南阳一中高一月考二化学卷天津市和平区2017-2018学年高一上学期期中质量调查化学试题2018-2019学年人教版高中化学必修一模块综合测评题(A)2018-2019学年苏教版高中化学必修一 模块综合测评(A)(已下线)专题2.3 氧化还原反应(练)-《2020年高考一轮复习讲练测》云南省漾濞二中2020届高三上学期开学考试化学试题江西省赣州市寻乌中学2020届高三上学期第一阶段考试化学试题(已下线)专题四 氧化还原反应(提分特训)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训(已下线)衔接点09 氧化还原反应的表示-2020年【衔接教材·暑假作业】初高中衔接化学(已下线)第09讲 氧化还原反应的计算及方程式的配平(精练)——2021年高考化学一轮复习讲练测高一必修第一册(鲁科2019)考试帮 模块综合测评B卷人教版(2019)高一必修第一册 模块综合测评-B卷贵州省铜仁市思南中学2021届高三上学期第二次月考化学试题江西省上饶市万年中学2020-2021学年高一上学期期中考试化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练湖南省武冈市第二中学2020-2021学年高一上学期第一次月考化学试题(已下线)衔接点09 氧化还原反应的表示-2021年初升高化学无忧衔接西藏拉萨市拉萨中学2022届高三上学期第一次月考理综化学试题黑龙江省哈尔滨市第六中学2021-2022学年高三上学期期中考试化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)4.2.2 氧化还原反应方程式的配平(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)黑龙江省哈尔滨市第九中学2021-2022学年高一上学期期中学业阶段性评价考试化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)考点05 氧化还原反应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题01 物质及其变化-2023年高考化学一轮复习小题多维练(全国通用)黑龙江省佳木斯市第八中学2022-2023学年高三上学期第一次调研(开学考试)化学试题黑龙江省哈尔滨市香坊区第九中学校2021-2022学年高一上学期期中考试化学试题西藏林芝市第二高级中学2022-2023学年高三上学期第二次月考化学试题(已下线)第一章 化学物质及其变化 第5练 氧化还原反应的计算与方程式的配平(已下线)考点05 氧化还原反应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)山东省枣庄市第三中学2022-2023学年高一上学期12月期中考试化学试题宁夏银川市第二中学2023-2024学年高三上学期统练二化学试题黑龙江省龙西北名校联合体2023-2024学年高三上学期期中考试化学试题黑龙江省齐齐哈尔市龙西北高中名校联盟2023-2024学年高三上学期10月联考化学试题江西省南昌市第十九中学2022-2023学年高一上学期12月第二次月考化学试卷
解题方法
4 . 氧化锌又称锌白,作为添加剂在多种材料和产品中有广泛应用,一种以锌精矿(主要成分是ZnS,还有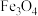 、CuO、
、CuO、 等杂质)为原料制备锌白的工艺流程如下:
等杂质)为原料制备锌白的工艺流程如下:
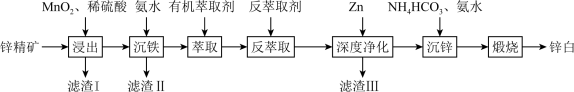
已知:25℃时相关物质的 如下表:
如下表:
回答下列问题:
(1)滤渣Ⅰ的主要成分除过量 外,还有S和
外,还有S和_______ (填化学式)。“浸出”时, 氧化ZnS的离子方程式为
氧化ZnS的离子方程式为_______ 。
(2)“沉铁”时,滴加氨水需要调节pH最低为_______ (通常认为残留在溶液中离子浓度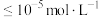 时,沉淀完全)。
时,沉淀完全)。
(3)“萃取,反萃取”时发生的反应是 。有机萃取剂能分离
。有机萃取剂能分离 和
和 ,为了提高反萃取效率,反萃取剂应该呈
,为了提高反萃取效率,反萃取剂应该呈_______ (填“酸”“碱”或“中”)性。
(4)“深度净化”中加Zn的目的是_______ 。
(5)“沉锌”时,恰好完全反应,过滤、洗涤得到碱式碳酸锌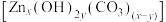 ,反应的离子方程式为
,反应的离子方程式为_______ 。检验沉淀洗涤干净的方法是_______ 。
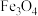 、CuO、
、CuO、 等杂质)为原料制备锌白的工艺流程如下:
等杂质)为原料制备锌白的工艺流程如下:
已知:25℃时相关物质的
 如下表:
如下表:| 物质 |  |  |  |  |  |
 | 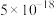 | 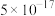 | 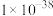 | 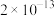 |  |
(1)滤渣Ⅰ的主要成分除过量
 外,还有S和
外,还有S和 氧化ZnS的离子方程式为
氧化ZnS的离子方程式为(2)“沉铁”时,滴加氨水需要调节pH最低为
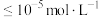 时,沉淀完全)。
时,沉淀完全)。(3)“萃取,反萃取”时发生的反应是
 。有机萃取剂能分离
。有机萃取剂能分离 和
和 ,为了提高反萃取效率,反萃取剂应该呈
,为了提高反萃取效率,反萃取剂应该呈(4)“深度净化”中加Zn的目的是
(5)“沉锌”时,恰好完全反应,过滤、洗涤得到碱式碳酸锌
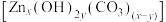 ,反应的离子方程式为
,反应的离子方程式为
您最近一年使用:0次
解题方法
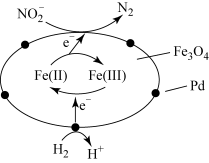
5 . 在催化剂作用下,H2可处理废水中的NO ,反应原理如图所示。下列说法错误的是
,反应原理如图所示。下列说法错误的是
 ,反应原理如图所示。下列说法错误的是
,反应原理如图所示。下列说法错误的是
| A.Fe3O4具有传递电子的作用 |
| B.Pd和Fe3O4均是该过程的催化剂 |
| C.处理后的废水中酸性增强 |
D.每消耗67.2L(标准状况下)H2,可还原2molNO |
您最近一年使用:0次
解题方法
6 . 硫酸是重要的化工原料,可用于生产化肥、农药、炸药等。工业上以黄铁矿(主要成分为FeS2,含有少量SiO2杂质)为主要原料制备硫酸的工艺流程如下图所示:
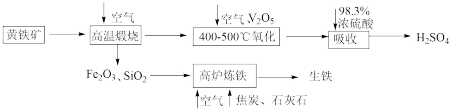
回答下列问题:
(1)“高温煅烧”前,将黄铁矿粉碎的目的是_______ ;煅烧时发生反应的化学方程式为_______ 。
(2)“氧化”时,发生反应的化学方程式为_______ 。
(3)“吸收”时,从SO3的性质角度分析,选用98.3%浓硫酸而不用水的主要原因是_______ 。
(4)研究证明,高炉中Fe2O3与CO反应不能完全转化为CO2和Fe,据此写出高炉炼铁时Fe2O3与CO反应的化学方程式:_______ ;若投入Fe2O3的质量为160t,经过5h后,产出含碳量为2%的生铁100t,则该反应中Fe2O3的转化率为_______ 。

回答下列问题:
(1)“高温煅烧”前,将黄铁矿粉碎的目的是
(2)“氧化”时,发生反应的化学方程式为
(3)“吸收”时,从SO3的性质角度分析,选用98.3%浓硫酸而不用水的主要原因是
(4)研究证明,高炉中Fe2O3与CO反应不能完全转化为CO2和Fe,据此写出高炉炼铁时Fe2O3与CO反应的化学方程式:
您最近一年使用:0次
2022-07-12更新
|
316次组卷
|
2卷引用:辽宁省凌源市高中2022-2023学年高二下学期3月联考化学试题
7 . 某废镍催化剂主要含金属 、
、 、
、 及
及 、
、 和
和 等。以该废镍催化剂为原料制备草酸镍晶体
等。以该废镍催化剂为原料制备草酸镍晶体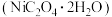 的工艺流程如下:
的工艺流程如下:
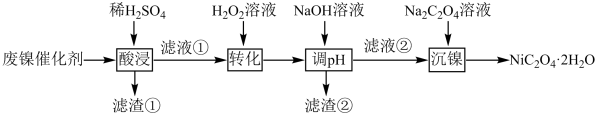
已知常温下几种金属离子开始沉淀和完全沉淀时的 如下表:
如下表:
回答下列问题:
(1)滤渣①的化学式为_______ ;“转化”时发生反应的离子方程式为_______ 。
(2)利用上述表格数据,计算 的
的
_______ ,如果“转化”后的溶液中 浓度为
浓度为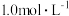 ,则“调
,则“调 ”应控制的
”应控制的 范围是
范围是_______ 。
(3)“沉镍”时, 溶液滴加过快会导致产品不纯,其原因是
溶液滴加过快会导致产品不纯,其原因是_______ 。
(4)产品草酸镍晶体纯度的测定.称取产品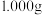 ,经过量稀硫酸处理后,用高锰酸钾标准溶液滴定,滴定终点时消耗
,经过量稀硫酸处理后,用高锰酸钾标准溶液滴定,滴定终点时消耗 的高锰酸钾溶液
的高锰酸钾溶液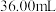 ,则产品中
,则产品中 的质量分数是
的质量分数是_______ ,若某同学测出产品的纯度超过100%,若滴定过程操作无错误,则可能原因是_______ 。
 、
、 、
、 及
及 、
、 和
和 等。以该废镍催化剂为原料制备草酸镍晶体
等。以该废镍催化剂为原料制备草酸镍晶体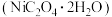 的工艺流程如下:
的工艺流程如下:
已知常温下几种金属离子开始沉淀和完全沉淀时的
 如下表:
如下表:| 金属离子 |  |  |  |  |
开始沉淀时(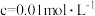 )的 )的 | 7.2 | 3.7 | 2.2 | 7.5 |
完全沉淀时(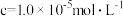 )的 )的 | 8.7 | 4.7 | 3.2 | 9.0 |
(1)滤渣①的化学式为
(2)利用上述表格数据,计算
 的
的
 浓度为
浓度为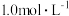 ,则“调
,则“调 ”应控制的
”应控制的 范围是
范围是(3)“沉镍”时,
 溶液滴加过快会导致产品不纯,其原因是
溶液滴加过快会导致产品不纯,其原因是(4)产品草酸镍晶体纯度的测定.称取产品
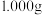 ,经过量稀硫酸处理后,用高锰酸钾标准溶液滴定,滴定终点时消耗
,经过量稀硫酸处理后,用高锰酸钾标准溶液滴定,滴定终点时消耗 的高锰酸钾溶液
的高锰酸钾溶液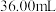 ,则产品中
,则产品中 的质量分数是
的质量分数是
您最近一年使用:0次
2022-01-20更新
|
166次组卷
|
4卷引用:辽宁省凌源市高中2022-2023学年高二下学期3月联考化学试题
8 . 已知还原性:SO >I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是
>I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是
 >I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是
>I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是A.当a≥b时,发生的离子反应为SO +Cl2+H2O=SO +Cl2+H2O=SO +2H++2Cl- +2H++2Cl- |
B.当5a=4b时,发生的离子反应为4SO +2I-+5Cl2+4H2O=4SO +2I-+5Cl2+4H2O=4SO +I2+8H++10Cl- +I2+8H++10Cl- |
C.当a≤b≤ a时,反应中转移电子的物质的量n(e-)为a mol≤n(e-)≤3a mol a时,反应中转移电子的物质的量n(e-)为a mol≤n(e-)≤3a mol |
D.当a<b< a时,溶液中SO a时,溶液中SO 、I-与Cl-的物质的量之比为a∶(3a-2b)∶2b 、I-与Cl-的物质的量之比为a∶(3a-2b)∶2b |
您最近一年使用:0次
2021-12-24更新
|
637次组卷
|
8卷引用:辽宁省抚顺市2016-2017学年高二下学期期末考试化学试题
辽宁省抚顺市2016-2017学年高二下学期期末考试化学试题浙江省2018版考前特训(2017年10月)学考70快练:9 定量离子方程式的书写判断与计算2016年10月浙江省普通高校招生选考科目考试化学试题(已下线)考点05 氧化还原反应——备战2019年浙江新高考化学考点(已下线)解密04 离子反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密04 离子反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)【2023】【高一下】【其他】【杭二中-期中复习卷】【高中化学】【邵威宏收集】浙江省湖州市吴兴高级中学2023-2024学年高一上学期12月月考化学试题
2010·江西·二模
名校
解题方法
9 . 已知NH4CuSO3与足量的10mol·L-1硫酸混合微热,产生下列现象:①有红色金属生成②产生刺激性气味的气体③溶液呈现蓝色。据此判断下列说法正确的是
| A.反应中硫酸作氧化剂 |
| B.NH4CuSO3中硫元素被氧化 |
| C.刺激性气味的气体是氨气 |
| D.1molNH4CuSO3完全反应转移0.5mol电子 |
您最近一年使用:0次
2021-09-14更新
|
413次组卷
|
93卷引用:辽宁省瓦房店市高级中学2016-2017学年高二下学期期末考试化学试题
辽宁省瓦房店市高级中学2016-2017学年高二下学期期末考试化学试题【全国百强校】山东师范大学附属中学2017-2018学年高二下学期第八次学分认定(期末)考试化学试题2015届辽宁省抚顺市二中高三上学期期中考试化学试卷2016-2017学年河北正定中学高二上开学考试化学卷2017届辽宁省沈阳东北育才学校高三上期中模拟化学卷黑龙江省大庆实验中学2017-2018学年高二上学期开学考试化学试题山东省济宁市汶上圣泽中学2019-2020学年高二下学期第二次检测化学试题安徽省安庆市2019-2020学年高一下学期期末测试化学试卷四川省射洪中学2019-2020学年高一上期期末英才班能力素质监测化学试题吉林省大安市第一中学校2021-2022学年高二上学期期初考试化学试题 山东省济南市章丘区第四中2022-2023学年高一上学期1月期末线上测试化学试题(已下线)江西省重点中学协作体2010届高三第二次联考(化学)(已下线)2011届河南省豫南九校高三上学期第二次联考化学试卷(已下线)2012届黑龙江省牡丹江一中高三上学期期中考试化学试卷(已下线)2012届山东省济宁市邹城二中高三第二次质量检测化学试卷2014届河北衡水中学高三上学期期中考试化学试卷(已下线)2014届黑龙江省佳木斯市第一中学高三第三次调研化学试卷(已下线)2014届河北冀州中学高三上学期期中考试往届化学试卷(已下线)2014高考名师推荐化学氧化还原反应的概念2016届河北省衡水中学高三上学期二调化学试卷2016届重庆市万州二中高三上学期9月月考化学试卷2016届山东省潍坊第一中学高三上学期10月月考化学试卷2016届甘肃省天水市第一中学高三上学期期中测试化学试卷2016届山东省青岛市高三上学期期中测试化学试卷2016届江苏省淮安市四星级高中高三上学期10月阶段测化学试卷2016届黑龙江省双鸭山一中高三上学期12月月考化学试卷2015-2016学年湖北省枣阳市第七中学高一上学期期中考试化学试卷2015-2016学年浙江省杭州市五校联盟高三12月月考化学试卷2016届吉林省东北师大附属中学高三上四次模拟化学卷2015-2016学年河南省信阳高级中学高一下开学测化学试卷2016届内蒙古赤峰市宁城县高三下学期第三次统一模拟考试化学试卷2016届内蒙古赤峰二中高三第四次模拟理综化学试卷2017届吉林省松原油田高中高三上第一次阶段测化学卷2017届福建省仙游一中高三上第一次月考化学试卷2017届江西省南昌二中高三上第二次考试化学试卷2017届河北省石家庄辛集中学高三上期中化学试卷2017届河南省周口市淮阳中学高三上10月月考化学试卷2017届内蒙古赤峰市宁城县高三上统一考试化学试卷2017届江西省兴国中学、兴国三中等四校高三上第一次联考化学卷2016-2017学年河北省冀州中学高一上11月月考化学卷2017届江西省兴国中学等四校高三上联考一化学试卷2017届吉林省长春实验中学高三第五次模拟化学卷2016-2017学年湖北省鄂东南省级示范高中高一下学期期中联考化学试卷陕西省西藏民族学院附属中学2017届高三考前冲刺(一)理科综合化学试题2018届高三一轮复习化学:微考点11-氧化还原反应的概念江西省临川区第二中学2018届高三上学期第三次月考化学试题湖南省永州市祁阳县第一中学2018届高三10月月考化学试题陕西省西安市长安区第一中学2017-2018学年高一下学期第一次教学质量检测化学试题广西陆川县中学2017-2018学年高一下学期3月月考化学试题【全国百强校】黑龙江省哈尔滨市第六中学2019届高三上学期开学阶段性考试(8月)化学试题湖南省湖南师范大学附属中学2019届高三上学期月考(一)化学试题【全国百强校】陕西省陕西师大附属中学2019届高三上学期月考化学试题【全国百强校】湖南省师范大学附属中学2019届高三上学期月考化学试题江西省赣州市会昌中学2019届高三上学期第一次月考(10月)化学试题河北省承德市第一中学2019届高三上学期第三次月考理科综合化学试题山东省商河市第一中学2019届高三上学期11月月考理科综合化学试题山东省滨州市北镇中学2019届高三上学期12月份质量检测化学试题江西省九江市同文中学2019届高三上学期期中考试化学试题山东省济宁市微山县亚马逊中学2019届高三上学期11月月考化学试题江西省上饶市横峰中学2018-2019学年高一下学期开学考试化学试题吉林省东辽五中2020届高三上学期9月月考化学试题江西省临川第二中学2020届高三10月月考化学试题吉林省白城市通榆县第一中学2020届高三上学期第二次月考化学试题山东省济宁市2020届高三10月月考化学试卷山东省济宁市邹城第一中学2020届高三10月月考化学试题甘肃省兰州市第一中学2020届高三上学期9月月考化学试题山东省莱阳市第一中学2020届高三10月月考化学试题吉林省长春市东北师范大学附中2020届高三上学期第一次摸底考试化学试题山东省肥城市泰西中学2019-2020学年高三上学期第一次月考化学试题新疆乌鲁木齐县柴窝堡林场中学2019届高三第三次模拟考试理科综合化学试题陕西省汉中市龙岗学校2019-2020学年高一上学期期中考试化学试题福建省厦门市湖滨中学2020届高三上学期期中考试化学试题四川省宜宾市叙州区第二中学校2019-2020学年高一下学期第一次在线月考化学试题(已下线)【南昌新东方】2018-2019莲塘一中 高三12月 014(已下线)专题3.4 金属材料及金属矿物的开发利用(练)——2020年高考化学一轮复习讲练测吉林省长春外国语学校2020-2021学年高三上学期期初考试化学试题河南省郑州市第一中学2021届高三上学期开学测试化学试题福建省永安市第三中学2021届高三9月月考化学试题吉林省大安市第一中学校2021届高三上学期第二次月考化学试题(已下线)第二章 元素与物质世界(能力提升)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)四川省乐山沫若中学2021届高三上学期第二次理综化学试题江西省高安中学2020-2021学年高一上学期期中考试化学试题广东省中山纪念中学2021届高三上学期第一次月考化学试题湖南省/(常德市芷兰实验中学2020-2021学年高一上学期第二次月考化学试题河南省信阳高级中学2020-2021学年高一上学期1月月考化学试题福建省莆田第十五中学2020届高三9月月考化学试题(已下线)解密07 非金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密07 非金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练云南省昭通市昭阳区第一中学2020-2021学年高一上学期第三次月考化学试题(已下线)【一飞冲天】名家原创卷1河北省廊坊市河北省三河市第一中学2020-2021学年高一下学期第二次阶段考化学试题吉林省辉南县第六中学2022届高三上学期第一次月考化学试题内蒙古自治区科尔沁左翼中旗实验高级中学2023-2024学年高三上学期11月月考化学试题
10 . Ⅰ、含氮废水是造成水体污染的重要原因之一、研究含氮废水的处理对水体净化有重要意义。利用 O2 和 H2 可高效去除水体中同时存在的 NH 和 NO
和 NO 。
。
具体方法是:①先利用氧气将 NH 氧化成 NO
氧化成 NO ,
,
②再利用 H2 将 NO 还原为N2 (2NO
还原为N2 (2NO +5H2
+5H2 N2+2OH-+4H2O)。
N2+2OH-+4H2O)。
(1)反应①中氧化剂与还原剂物质的量之比为___________ 。
(2)若完全处理 100g 含 NH4NO3 4%的废水,至少需要标准状况下的 H2___________ L。
(3)该污水处理的好处是___________ (列举一条即可)
Ⅱ、焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4Cl、FeCl3、N2、Fe2O3、Fe和X。
(1)根据题意,可判断出X是___________ (写化学式)。
(2)写出并配平该反应的化学方程式:___________ ;
(3)发生还原反应的物质是___________ ,反应中2mol氧化剂能___________ (填“失去”或“得到”)___________ mol电子。
(4)反应中产生5.6L(标准状况)的气体时,被还原的物质的质量为___________ 。
 和 NO
和 NO 。
。具体方法是:①先利用氧气将 NH
 氧化成 NO
氧化成 NO ,
,②再利用 H2 将 NO
 还原为N2 (2NO
还原为N2 (2NO +5H2
+5H2 N2+2OH-+4H2O)。
N2+2OH-+4H2O)。(1)反应①中氧化剂与还原剂物质的量之比为
(2)若完全处理 100g 含 NH4NO3 4%的废水,至少需要标准状况下的 H2
(3)该污水处理的好处是
Ⅱ、焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4Cl、FeCl3、N2、Fe2O3、Fe和X。
(1)根据题意,可判断出X是
(2)写出并配平该反应的化学方程式:
(3)发生还原反应的物质是
(4)反应中产生5.6L(标准状况)的气体时,被还原的物质的质量为
您最近一年使用:0次



