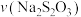解题方法
1 . 某小组同学为探究FeSO4的性质设计了如下实验。
Ⅰ.新配制0.1 mol·L−1 FeSO4溶液450 mL:
(1)配制0.1 mol·L−1 FeSO4溶液450 mL,需用托盘天平准确称取绿矾(FeSO4·7H2O)
_______ g,其部分实验操作示意图如下,正确的步骤顺序为_______ (填序号)。
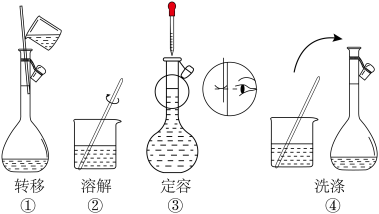
Ⅱ.取2 mL新配制的FeSO4溶液,按下图进行实验并观察到如下现象:
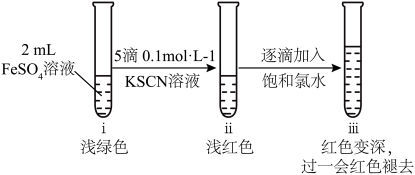
(2)ⅱ中溶液呈浅红色,说明FeSO4溶液中存在_______ (填离子符号)。
(3)ⅲ中溶液红色变深的主要原因是_______ (用离子方程式表示)。
Ⅲ.探究ⅲ中“红色褪去”的原因:
查阅资料:SCN−具有还原性,能被氯气氧化为(SCN)2。
根据查阅资料,甲、乙两位同学提出了如下猜想:
(4)乙同学的猜想是_______ 。为验证甲、乙两位同学的猜想,设计如下实验:将褪色后的溶液分为两等份,一份滴加KSCN溶液,呈血红色;另一份加入氯化铁溶液,无明显现象,则_______ 同学猜想是正确的。
Ⅳ.丙和丁同学探究无水FeSO4在450 ℃、不同氛围中的分解产物:
① 丙同学在450 ℃、空气氛围中加热15.2 g FeSO4,直至固体质量不变,得到纯净的红棕色固体m g,产生的气体通入品红溶液,无明显变化,通入氯化钡溶液中有白色沉淀生成;
② 丁同学在450 ℃、氮气氛围中加热15.2 g FeSO4,直至固体质量不变,得到纯净的红棕色固体也是m g,产生的气体依次通入氯化钡溶液和品红溶液,氯化钡溶液中有白色沉淀,品红溶液褪色。
(5)则m =_______ g,FeSO4固体在空气氛围中加热时反应的化学方程式为_______ 。
Ⅰ.新配制0.1 mol·L−1 FeSO4溶液450 mL:
(1)配制0.1 mol·L−1 FeSO4溶液450 mL,需用托盘天平准确称取绿矾(FeSO4·7H2O)

Ⅱ.取2 mL新配制的FeSO4溶液,按下图进行实验并观察到如下现象:

(2)ⅱ中溶液呈浅红色,说明FeSO4溶液中存在
(3)ⅲ中溶液红色变深的主要原因是
Ⅲ.探究ⅲ中“红色褪去”的原因:
查阅资料:SCN−具有还原性,能被氯气氧化为(SCN)2。
根据查阅资料,甲、乙两位同学提出了如下猜想:
| 猜想 | |
| 甲 | +3价铁又被还原成+2价铁 |
| 乙 |
(4)乙同学的猜想是
Ⅳ.丙和丁同学探究无水FeSO4在450 ℃、不同氛围中的分解产物:
① 丙同学在450 ℃、空气氛围中加热15.2 g FeSO4,直至固体质量不变,得到纯净的红棕色固体m g,产生的气体通入品红溶液,无明显变化,通入氯化钡溶液中有白色沉淀生成;
② 丁同学在450 ℃、氮气氛围中加热15.2 g FeSO4,直至固体质量不变,得到纯净的红棕色固体也是m g,产生的气体依次通入氯化钡溶液和品红溶液,氯化钡溶液中有白色沉淀,品红溶液褪色。
(5)则m =
您最近一年使用:0次
解题方法
2 . SO2是硫元素中一种重要物质,在生产生活中有重要用途。
(1)某研究小组用如图装置进行SO2与 溶液反应的相关实验(夹持装置已略去)
溶液反应的相关实验(夹持装置已略去)_________ 。
②根据以上现象,该小组同学认为SO2与 溶液发生氧化还原反应。
溶液发生氧化还原反应。
a.写出SO2与 溶液反应的离子方程式:
溶液反应的离子方程式:_________ 。
b.该小组同学向C试管反应后的溶液中加入硝酸酸化的 溶液,若出现白色沉淀,即可证明反应生成了
溶液,若出现白色沉淀,即可证明反应生成了 。该做法
。该做法_________ (填“合理”或“不合理”),理由是_________ 。
③为了验证SO2具有还原性,实验中可以代替 溶液的试剂有
溶液的试剂有_________ (填字母)。
A.浓硫酸 B.酸性 溶液 C.碘水 D.NaCl溶液
溶液 C.碘水 D.NaCl溶液
(2)某同学利用如图所示的装置研究SO2的性质:(熔点:SO2为 ,
, 为16.8℃,沸点:SO2为-10℃,
为16.8℃,沸点:SO2为-10℃, 为45℃)
为45℃)_________ 。
②装置Ⅱ的作用_________ 。
③甲同学按I、Ⅱ、Ⅲ、IV的顺序连接装置,装置Ⅲ中溶液逐渐褪色,生成Mn2+,同时酸性增强,则该反应的离子方程式是_________ (忽略 的影响)。
的影响)。
(1)某研究小组用如图装置进行SO2与
 溶液反应的相关实验(夹持装置已略去)
溶液反应的相关实验(夹持装置已略去)
②根据以上现象,该小组同学认为SO2与
 溶液发生氧化还原反应。
溶液发生氧化还原反应。a.写出SO2与
 溶液反应的离子方程式:
溶液反应的离子方程式:b.该小组同学向C试管反应后的溶液中加入硝酸酸化的
 溶液,若出现白色沉淀,即可证明反应生成了
溶液,若出现白色沉淀,即可证明反应生成了 。该做法
。该做法③为了验证SO2具有还原性,实验中可以代替
 溶液的试剂有
溶液的试剂有A.浓硫酸 B.酸性
 溶液 C.碘水 D.NaCl溶液
溶液 C.碘水 D.NaCl溶液(2)某同学利用如图所示的装置研究SO2的性质:(熔点:SO2为
 ,
, 为16.8℃,沸点:SO2为-10℃,
为16.8℃,沸点:SO2为-10℃, 为45℃)
为45℃)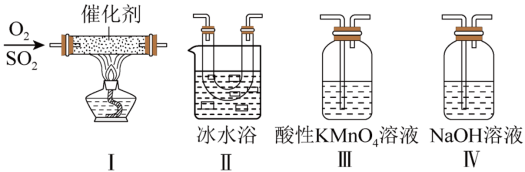
②装置Ⅱ的作用
③甲同学按I、Ⅱ、Ⅲ、IV的顺序连接装置,装置Ⅲ中溶液逐渐褪色,生成Mn2+,同时酸性增强,则该反应的离子方程式是
 的影响)。
的影响)。
您最近一年使用:0次
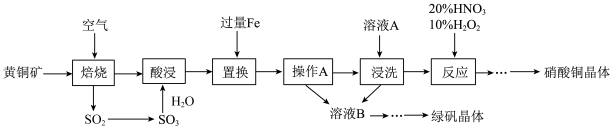
3 . 研究人员拟设计黄铜矿(主要含CuFeS2)制备硝酸铜和绿矾晶体的流程如下:
(1)CuFeS2中铁元素的化合价为___________ 价,已知“焙烧”生成SO2、CuO和)Fe2O3则其化学反应方程式为___________ 。
(2)“置换”步骤中发生的所有反应的离子方程式有Fe+Cu2+=Fe2++Cu Fe+2H+=Fe2++H2↑、___________ 。
(3)流程中“操作 A”所需的玻璃仪器有烧杯、玻璃棒、___________ 。
(4)“浸洗”步骤中加溶液A 的目的是___________ 。
(5)“反应”步骤中,10%H2O2为氧化剂,20%HNO3提供H+,可以避免污染性气体的产生,写出该“反应”的离子方程式:___________ 。
(6)绿矾晶体(FeSO4·7H2O)在空气中极易变质; 验证绿矾晶体已变质的操作为___________ 。
(1)CuFeS2中铁元素的化合价为
(2)“置换”步骤中发生的所有反应的离子方程式有Fe+Cu2+=Fe2++Cu Fe+2H+=Fe2++H2↑、
(3)流程中“操作 A”所需的玻璃仪器有烧杯、玻璃棒、
(4)“浸洗”步骤中加溶液A 的目的是
(5)“反应”步骤中,10%H2O2为氧化剂,20%HNO3提供H+,可以避免污染性气体的产生,写出该“反应”的离子方程式:
(6)绿矾晶体(FeSO4·7H2O)在空气中极易变质; 验证绿矾晶体已变质的操作为
您最近一年使用:0次
名校
解题方法
4 . 下列离子方程式书写正确的是
A.铁粉溶于过量稀硝酸: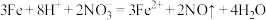 |
B.将SO2通入BaCl2溶液中: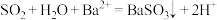 |
C.氯气与水反应: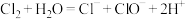 |
D.氯化铁溶液中通入SO2: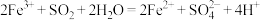 |
您最近一年使用:0次
解题方法
5 . 能正确描述下列反应的离子方程式为
A.用 溶液腐蚀印刷电路板: 溶液腐蚀印刷电路板: |
B. 溶液与少量 溶液与少量 溶液反应: 溶液反应: |
C.用 溶液吸收 溶液吸收 气体: 气体: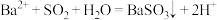 |
D.将 通入含 通入含 的溶液中: 的溶液中: |
您最近一年使用:0次
解题方法
6 . 某酸性废液中含有 四种金属离子。有同学设计下列方案对废液进行处理(所加试剂均稍过量),减少对环境的污染,流程如图所示:
四种金属离子。有同学设计下列方案对废液进行处理(所加试剂均稍过量),减少对环境的污染,流程如图所示:

回答下列问题:
(1)该酸性废液中可能大量含有的阴离子是 (填标号)。
A. | B. | C. | D. |
(2)沉淀
 的化学式是
的化学式是 的化学式是
的化学式是(3)已知氧化性强弱:
 ,加入铁屑发生的离子反应有:
,加入铁屑发生的离子反应有:① ;
;
②
③
(4)判断铁屑过量的实验现象是
(5)检验溶液
 中不含
中不含 的操作及现象是
的操作及现象是(6)向溶液
 中逐滴加入稀盐酸,理论上先后参与反应的离子依次是
中逐滴加入稀盐酸,理论上先后参与反应的离子依次是 。
。
您最近一年使用:0次
名校
解题方法
7 . 某化学实验室产生的废液中含有 Fe3+、Cu2+、Ag+三种金属离子,甲同学设计了如图所示的方案对废液进行处理,以回收金属,下列说法正确的是
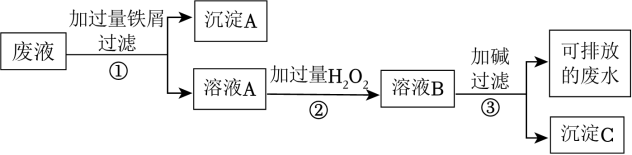

| A.沉淀A中含有2种金属单质 |
| B.可用KSCN溶液来检验溶液B中所含的金属离子 |
| C.溶液A若只经过操作③最终将无法得到沉淀C |
| D.操作①②③中都需要用到玻璃棒、漏斗 |
您最近一年使用:0次
2024-03-19更新
|
88次组卷
|
20卷引用:四川师范大学附属中学2020-2021学年高一上学期12月月考化学试题
四川师范大学附属中学2020-2021学年高一上学期12月月考化学试题浙江省温州市新力量联盟2018-2019学年高一上学期期末考试化学试题贵州省思南中学2018-2019学年高一下学期期末考试化学试题江西省上高县第二中学2019-2020学年高一上学期第三次月考化学试题河北省安平中学2019-2020学年高一上学期第四次月考化学试题江苏省盐城市大丰区新丰中学2019-2020学年高一上学期期末考试化学试题河北省保定市涞水波峰中学2019-2020学年高一下学期第三次质检考试化学试题山西省太原市第五中学2020-2021学年高一上学期12月阶段性检测化学试题宁夏石嘴山市第三中学2020-2021学年高一上学期第二次月考化学试题(已下线)【浙江新东方】在线化学 (14)(已下线)练习9 铁的多样性-2020-2021学年【补习教材·寒假作业】高一化学(鲁科版2019)(已下线)【浙江新东方】在线化学33浙江省淳安县汾口中学2020-2021学年高二12月月考化学试题云南省楚雄天人中学2019-2020学年高一上学期12月月考化学试题云南省玉溪师范学院附属中学2021-2022学年高一下学期开学测试化学试题湖南省常德市桃源县第一中学2022-2023学年高三上学期9月月考化学试题河北省廊坊市第一中学2022~2023 学年高一上学期期末考试化学试题甘肃省张掖市高台县第一中学2022-2023学年高一下学期开学检测化学试题广东省广州天省实验学校2022-2023学年高一上学期期末考试化学试卷浙江省淳安县汾口中学2023-2024学年高二上学期12月检测化学试题
8 . I.某实验小组采用下列实验探究外界条件对化学反应速率及其化学平衡的影响。
(1)室温下,向盛有 溶液的试管中加入
溶液的试管中加入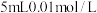 的
的 溶液,溶液变为
溶液,溶液变为_________ 色。发生反应的离子方程式为____________________________________________________ 。
(2)现将上述溶液均分为两份置于甲、乙两支试管中;
①向甲试管中加入4滴饱和 溶液,平衡
溶液,平衡______ (填“正向移动”、“逆向移动”或“不移动”);溶液中的 浓度
浓度
______ (填“增大”、“减小”或“不变”,下同),重新达到平衡时 转化率
转化率______ 。
②向乙试管中加入 固体,平衡
固体,平衡______ (填“正向移动”、“逆向移动”或“不移动”)。
II.该实验小组还利用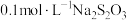 溶液和
溶液和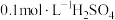 溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如表。请结合表中信息,回答有关问题:
溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如表。请结合表中信息,回答有关问题:
(3)该反应的离子方程式为____________________________________________ 。
(4)在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件,其中:
①能说明温度对该反应速率影响的组合是______ (填实验序号,下同);
②实验Ⅱ和Ⅲ探究的是_______ (填外部因素)对化学反应速率的影响,其中实验Ⅲ中 =
=_______ 。
(1)室温下,向盛有
 溶液的试管中加入
溶液的试管中加入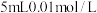 的
的 溶液,溶液变为
溶液,溶液变为(2)现将上述溶液均分为两份置于甲、乙两支试管中;
①向甲试管中加入4滴饱和
 溶液,平衡
溶液,平衡 浓度
浓度
 转化率
转化率②向乙试管中加入
 固体,平衡
固体,平衡II.该实验小组还利用
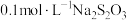 溶液和
溶液和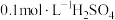 溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如表。请结合表中信息,回答有关问题:
溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如表。请结合表中信息,回答有关问题:实验序号 | 反应温度 |
|
|
| 出现沉淀所需的时间 |
I | 0℃ | 5mL | 5mL | 10mL | 12s |
II | 30℃ | 5mL | 10mL | 5mL | 8s |
III | 30℃ | 5mL | 7mL |
| 10s |
IV | 30℃ | 5mL | 5mL | 10mL | 10s |
(4)在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件,其中:
①能说明温度对该反应速率影响的组合是
②实验Ⅱ和Ⅲ探究的是
 =
=
您最近一年使用:0次
名校
解题方法
9 . 小组同学用FeSO4·7H2O晶体和蒸馏水配制100 mL 0.5 mol·L−1 FeSO4溶液(pH为3.3), 再进行性质探究实验。
Ⅰ.配制溶液
(1)用到的仪器有:天平、药匙、量筒、烧杯、玻璃棒、胶头滴管和_______ 。
(2)计算需要FeSO4·7H2O晶体的质量是_____ g。
(3)下列情况中,会使所配溶液浓度不准确 的是___________ (填字母)。
a.称量晶体后,加入盛有100 mL 水的烧杯中
b.转移时,洗涤烧杯和玻璃棒
c.定容时,眼睛俯视刻度线
d.定容时,发现液面高于刻度线,将多余溶液倒出
Ⅱ.性质探究。
立即取出一定量配制好的溶液放入2个试管中,分别进行如下实验:
实验i:滴加氢氧化钠溶液,观察到产生白色沉淀,最后变为红褐色。
实验ii:滴加高锰酸钾溶液,溶液褪色
(4)生成红褐色沉淀的化学方程式是___________ 。
(5)实验ii中高锰酸钾将Fe2+转化为_______ 。
Ⅲ.对异常现象的探究。
配制好的溶液放置1 h后,溶液变黄。24 h后,产生黄褐色沉淀,测得上层清液pH为1.4。
(6)取少量黄色溶液,_______ (填操作和现象),证明黄色溶液中含有Fe3+。
(7)通过下列实验证实,黄褐色沉淀中含有 。
。

①证实黄褐色沉淀中含有 的证据是
的证据是_________ 。
②洗涤黄褐色沉淀的目的是_______ 。
Ⅳ.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,与水反应可生成透明的红褐色胶体。
(8)上述反应的离子方程式如下,请将方程式补写完整______ ,
___ +____H2O=____Fe(OH)3(胶体)+__O2↑+___OH-。
+____H2O=____Fe(OH)3(胶体)+__O2↑+___OH-。
Ⅰ.配制溶液
(1)用到的仪器有:天平、药匙、量筒、烧杯、玻璃棒、胶头滴管和
(2)计算需要FeSO4·7H2O晶体的质量是
(3)下列情况中,会使所配溶液浓度
a.称量晶体后,加入盛有100 mL 水的烧杯中
b.转移时,洗涤烧杯和玻璃棒
c.定容时,眼睛俯视刻度线
d.定容时,发现液面高于刻度线,将多余溶液倒出
Ⅱ.性质探究。
立即取出一定量配制好的溶液放入2个试管中,分别进行如下实验:
实验i:滴加氢氧化钠溶液,观察到产生白色沉淀,最后变为红褐色。
实验ii:滴加高锰酸钾溶液,溶液褪色
(4)生成红褐色沉淀的化学方程式是
(5)实验ii中高锰酸钾将Fe2+转化为
Ⅲ.对异常现象的探究。
配制好的溶液放置1 h后,溶液变黄。24 h后,产生黄褐色沉淀,测得上层清液pH为1.4。
(6)取少量黄色溶液,
(7)通过下列实验证实,黄褐色沉淀中含有
 。
。
①证实黄褐色沉淀中含有
 的证据是
的证据是②洗涤黄褐色沉淀的目的是
Ⅳ.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,与水反应可生成透明的红褐色胶体。
(8)上述反应的离子方程式如下,请将方程式补写完整
___
 +____H2O=____Fe(OH)3(胶体)+__O2↑+___OH-。
+____H2O=____Fe(OH)3(胶体)+__O2↑+___OH-。
您最近一年使用:0次
10 . 下列实验中,对应的现象以及解释或结论都正确,且两者具有因果关系的是
| 实验操作 | 实验现象 | 结论或解释 | |
| A | 取久置的 粉末,向其中滴加过量的盐酸 粉末,向其中滴加过量的盐酸 | 产生无色气体 |  粉末没有变质 粉末没有变质 |
| B | 用铂丝蘸取某样品进行焰色试验 | 产生黄色火焰 | 该样品所含金属元素只有钠 |
| C | 向装有鲜花的集气瓶中通入 | 鲜花变色 |  具有漂白性 具有漂白性 |
| D | 向 溶液中加入少量铜粉 溶液中加入少量铜粉 | 固体溶解 | 氧化性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次