名校
1 .  是生产金属钛及其化合物的重要中间体。工业上以高钛渣(主要成分是
是生产金属钛及其化合物的重要中间体。工业上以高钛渣(主要成分是 )为原料生产
)为原料生产 的反应原理为:
的反应原理为: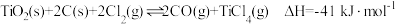 。回答下列问题:
。回答下列问题:
(1)已知: ,
, 的燃烧热为
的燃烧热为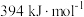 ,则表示
,则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为_______ 。
(2) 时,将足量的
时,将足量的 和C加入一恒容密闭容器中,并通入一定量的
和C加入一恒容密闭容器中,并通入一定量的 和
和 的混合气体,
的混合气体, 不参与化学反应。容器中只发生反应:
不参与化学反应。容器中只发生反应: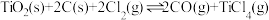 ,测得容器中的总压强(p总压)与
,测得容器中的总压强(p总压)与 的转化率(
的转化率( )随时间的变化关系如图所示:
)随时间的变化关系如图所示:
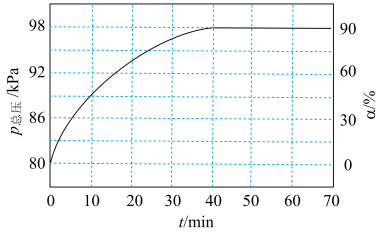
① 时,该反应的平衡常数
时,该反应的平衡常数
_______  (分压=总压×物质的量分数)。
(分压=总压×物质的量分数)。
②保持温度和起始总压相同,若向恒容密闭容器中通入的 不含
不含 ,与含
,与含 相比,
相比, 的平衡转化率将
的平衡转化率将_______ (填“>”“=”或“<”)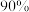 ,其原因是
,其原因是_______ 。
(3)利用 制得
制得 ,焙烧
,焙烧 可得纳米
可得纳米 。书写用
。书写用 溶液制备
溶液制备 反应的化学方程式:
反应的化学方程式:_______ 。
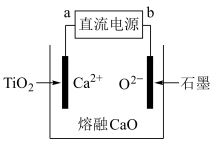
(4)电解法生产钛的原理如图所示,电解过程中,被还原的 进一步还原
进一步还原 得到钛。其中,直流电源a为
得到钛。其中,直流电源a为_______ (填“正”或“负”)极,用化学用语表示制钛的过程:_______ 、_______ 。石墨电极需要定期更换的原因是_______ 。
 是生产金属钛及其化合物的重要中间体。工业上以高钛渣(主要成分是
是生产金属钛及其化合物的重要中间体。工业上以高钛渣(主要成分是 )为原料生产
)为原料生产 的反应原理为:
的反应原理为: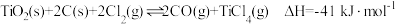 。回答下列问题:
。回答下列问题:(1)已知:
 ,
, 的燃烧热为
的燃烧热为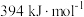 ,则表示
,则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为(2)
 时,将足量的
时,将足量的 和C加入一恒容密闭容器中,并通入一定量的
和C加入一恒容密闭容器中,并通入一定量的 和
和 的混合气体,
的混合气体, 不参与化学反应。容器中只发生反应:
不参与化学反应。容器中只发生反应: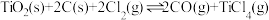 ,测得容器中的总压强(p总压)与
,测得容器中的总压强(p总压)与 的转化率(
的转化率( )随时间的变化关系如图所示:
)随时间的变化关系如图所示:
①
 时,该反应的平衡常数
时,该反应的平衡常数
 (分压=总压×物质的量分数)。
(分压=总压×物质的量分数)。②保持温度和起始总压相同,若向恒容密闭容器中通入的
 不含
不含 ,与含
,与含 相比,
相比, 的平衡转化率将
的平衡转化率将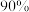 ,其原因是
,其原因是(3)利用
 制得
制得 ,焙烧
,焙烧 可得纳米
可得纳米 。书写用
。书写用 溶液制备
溶液制备 反应的化学方程式:
反应的化学方程式:(4)电解法生产钛的原理如图所示,电解过程中,被还原的
 进一步还原
进一步还原 得到钛。其中,直流电源a为
得到钛。其中,直流电源a为
您最近一年使用:0次
名校
解题方法
2 . 萘类物质的加成反应,可以合成多种环状结构的异构体,并在工业中有重要应用,利用1-甲基萘(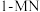 )制备四氢萘类物质(
)制备四氢萘类物质( ,包括
,包括 和
和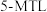 )。反应过程中伴有生成十氢萘(
)。反应过程中伴有生成十氢萘(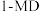 )的副反应,涉及反应如图:
)的副反应,涉及反应如图:
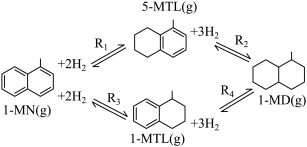
请回答下列问题:
(1)已知一定条件下反应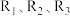 的焓变分别为
的焓变分别为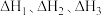 ,则反应
,则反应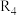 的焓变
的焓变
______ (用含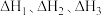 的代数式表示)。
的代数式表示)。
(2)根据 和
和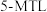 的结构及命名方式,
的结构及命名方式, 和
和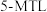 的一种同分异构体
的一种同分异构体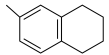 的名称为
的名称为______  。
。
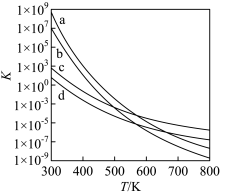
(3)四个平衡体系的平衡常数与温度的关系如图所示。
①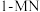 ,
, ,
,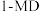 中最稳定的是
中最稳定的是______ 。
②不考虑生成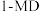 ,从反应进行程度上考虑,利于生成
,从反应进行程度上考虑,利于生成 的条件是
的条件是______ 。
③若曲线c、d分别代表反应 、
、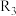 的平衡常数随温度的变化,则表示反应
的平衡常数随温度的变化,则表示反应 的平衡常数随温度变化的曲线为
的平衡常数随温度变化的曲线为______ 。
(4)某温度下,将一定量的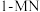 、投入一密闭容器中,检测到四种有机物的物质的量随时间的变化关系如图乙所示。
、投入一密闭容器中,检测到四种有机物的物质的量随时间的变化关系如图乙所示。
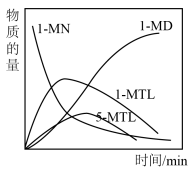
在此温度下,如何更多的得到
______ 。
a.延长反应时间
b.增大压强
c.使用选择性更高的催化剂
d反应初期生成较多 时,及时分离出
时,及时分离出
(5) 时,在体积恒定的密闭容器中投入一定量的
时,在体积恒定的密闭容器中投入一定量的 ,假定只发生
,假定只发生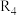 过程,
过程, 足量,且反应过程中氢气的浓度恒定为
足量,且反应过程中氢气的浓度恒定为 ,当
,当 的转化率为a时,反应的平衡常数为
的转化率为a时,反应的平衡常数为______ 。
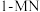 )制备四氢萘类物质(
)制备四氢萘类物质( ,包括
,包括 和
和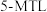 )。反应过程中伴有生成十氢萘(
)。反应过程中伴有生成十氢萘(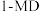 )的副反应,涉及反应如图:
)的副反应,涉及反应如图:
请回答下列问题:
(1)已知一定条件下反应
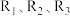 的焓变分别为
的焓变分别为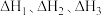 ,则反应
,则反应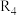 的焓变
的焓变
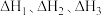 的代数式表示)。
的代数式表示)。(2)根据
 和
和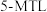 的结构及命名方式,
的结构及命名方式, 和
和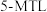 的一种同分异构体
的一种同分异构体 的名称为
的名称为 。
。(3)四个平衡体系的平衡常数与温度的关系如图所示。

①
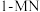 ,
, ,
,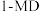 中最稳定的是
中最稳定的是②不考虑生成
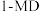 ,从反应进行程度上考虑,利于生成
,从反应进行程度上考虑,利于生成 的条件是
的条件是③若曲线c、d分别代表反应
 、
、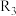 的平衡常数随温度的变化,则表示反应
的平衡常数随温度的变化,则表示反应 的平衡常数随温度变化的曲线为
的平衡常数随温度变化的曲线为(4)某温度下,将一定量的
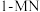 、投入一密闭容器中,检测到四种有机物的物质的量随时间的变化关系如图乙所示。
、投入一密闭容器中,检测到四种有机物的物质的量随时间的变化关系如图乙所示。
在此温度下,如何更多的得到

a.延长反应时间
b.增大压强
c.使用选择性更高的催化剂
d反应初期生成较多
 时,及时分离出
时,及时分离出
(5)
 时,在体积恒定的密闭容器中投入一定量的
时,在体积恒定的密闭容器中投入一定量的 ,假定只发生
,假定只发生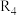 过程,
过程, 足量,且反应过程中氢气的浓度恒定为
足量,且反应过程中氢气的浓度恒定为 ,当
,当 的转化率为a时,反应的平衡常数为
的转化率为a时,反应的平衡常数为
您最近一年使用:0次
2023-12-08更新
|
396次组卷
|
2卷引用:湖北省恩施土家族苗族自治州利川市第一中学2023-2024学年高二下学期开学化学试题
解题方法
3 . 氨基甲酸铵(H2NCOONH4)为尿素生产过程的中间产物,易分解。某小组对氨基甲酸铵的分解实验进行探究。
已知:Ⅰ.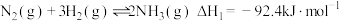
Ⅱ.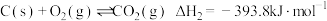
Ⅲ.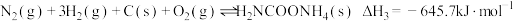
回答下列问题:
(1) 分子中含有键
分子中含有键___________ (填“极性”或“非极性”),写出二氧化碳的电子式___________ 。
(2)写出 分解生成
分解生成 与
与 气体的热化学方程式:
气体的热化学方程式:___________ 。
(3)在一定温度下,向 密闭容器中,加入
密闭容器中,加入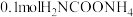 ,实验测得
,实验测得 物质的量变化如下表所示:
物质的量变化如下表所示:
从反应开始到2min,用 的浓度变化表示的化学反应速率为
的浓度变化表示的化学反应速率为___________ ;平衡后, 的转化率为
的转化率为___________ 。
(4)若在恒温恒压条件下进行反应,下列能够说明该反应已达到化学平衡状态的是___________。
(5)对该反应,改变某一条件,对化学反应速率的影响及解释不正确的是___________ 。
A.升高温度,使单位体积内活化分子百分数增加,反应速率加快
B.增加反应物的量,使活化分子百分数增加,有效碰撞增多,反应速率加快
C.使用催化剂能降低反应活化能,使单位体积内活化分子百分数增加,反应速率加快
已知:Ⅰ.
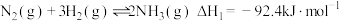
Ⅱ.
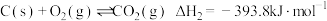
Ⅲ.
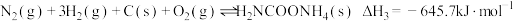
回答下列问题:
(1)
 分子中含有键
分子中含有键(2)写出
 分解生成
分解生成 与
与 气体的热化学方程式:
气体的热化学方程式:(3)在一定温度下,向
 密闭容器中,加入
密闭容器中,加入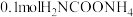 ,实验测得
,实验测得 物质的量变化如下表所示:
物质的量变化如下表所示: | 0 | 1 | 2 | 3 | 4 |
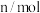 | 0 | a | b | c | c |
 的浓度变化表示的化学反应速率为
的浓度变化表示的化学反应速率为 的转化率为
的转化率为(4)若在恒温恒压条件下进行反应,下列能够说明该反应已达到化学平衡状态的是___________。
A. 的浓度不再改变 的浓度不再改变 | B.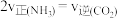 |
| C.容器体积不再改变 | D.容器内密度不再改变 |
A.升高温度,使单位体积内活化分子百分数增加,反应速率加快
B.增加反应物的量,使活化分子百分数增加,有效碰撞增多,反应速率加快
C.使用催化剂能降低反应活化能,使单位体积内活化分子百分数增加,反应速率加快
您最近一年使用:0次
解题方法
4 . 氨的用途十分广泛,是现代工业、农业生产最基础的化工原料之一。
I.以氨为原料可生产尿素:2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g) ΔH, 其反应分两步进行:
CO(NH2)2(l)+H2O(g) ΔH, 其反应分两步进行:
①2NH3(g)+CO2(g) NH2COONH4(l) ΔH1=−117kJ·mol−1
NH2COONH4(l) ΔH1=−117kJ·mol−1
②NH2COONH4(l) CO(NH2)2(l)+H2O(g) ΔH2=+15kJ·mol−1
CO(NH2)2(l)+H2O(g) ΔH2=+15kJ·mol−1
(1)生产尿素的决速步骤是第二步,可判断活化能较小的是_______ (填“①”或“②”)。
(2)总反应的ΔH=_______ 。
Ⅱ.传统的“哈伯法”合成氨原理为:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ·mol−1 ΔS=−200J·K−1·mol−1
2NH3(g) ΔH=-92.4kJ·mol−1 ΔS=−200J·K−1·mol−1
(3)上述反应在常温下_______ (填“能”或“不能”)自发进行。
(4)一定条件下,在恒温恒容的密闭容器中充入等物质的量的N2和H2发生反应生成NH3下列状态能说明反应达到平衡的是_______(填标号)。
(5)科研小组模拟不同条件下的合成氨反应,向体积可变的密闭容器中充入6mol N2和10mol H2,不同温度下平衡时氨气的体积分数与总压强(p)的关系如图所示。
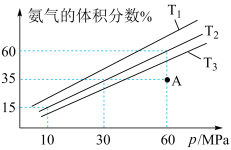
①T1、T2、T3由小到大的顺序为_______ 。
②在T2、60MPa条件下,平衡时N2的转化率为_______ %;平衡常数Kp=_______ (保留两位有效数字)。(用平衡分压代替平衡浓度,分压=总压x物质的量分数)
I.以氨为原料可生产尿素:2NH3(g)+CO2(g)
 CO(NH2)2(l)+H2O(g) ΔH, 其反应分两步进行:
CO(NH2)2(l)+H2O(g) ΔH, 其反应分两步进行:①2NH3(g)+CO2(g)
 NH2COONH4(l) ΔH1=−117kJ·mol−1
NH2COONH4(l) ΔH1=−117kJ·mol−1②NH2COONH4(l)
 CO(NH2)2(l)+H2O(g) ΔH2=+15kJ·mol−1
CO(NH2)2(l)+H2O(g) ΔH2=+15kJ·mol−1(1)生产尿素的决速步骤是第二步,可判断活化能较小的是
(2)总反应的ΔH=
Ⅱ.传统的“哈伯法”合成氨原理为:N2(g)+3H2(g)
 2NH3(g) ΔH=-92.4kJ·mol−1 ΔS=−200J·K−1·mol−1
2NH3(g) ΔH=-92.4kJ·mol−1 ΔS=−200J·K−1·mol−1(3)上述反应在常温下
(4)一定条件下,在恒温恒容的密闭容器中充入等物质的量的N2和H2发生反应生成NH3下列状态能说明反应达到平衡的是_______(填标号)。
| A.容器内气体的平均摩尔质量不变 | B.N2的体积分数不变 |
| C.混合气体的颜色不再改变 | D.3v正(NH3)=2v逆(H2) |

①T1、T2、T3由小到大的顺序为
②在T2、60MPa条件下,平衡时N2的转化率为
您最近一年使用:0次
名校
解题方法
5 .  的排放是形成酸雨的重要原因之一,工业上可采用多种方法减少
的排放是形成酸雨的重要原因之一,工业上可采用多种方法减少 的排放。回答下列问题:
的排放。回答下列问题:
(1) 还原法:
还原法:
已知: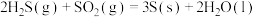
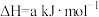 ;
; 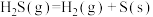
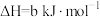 。
。
则 和
和 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为_______ 。
(2)碘循环法的循环过程如图所示,反应①的化学方程式为_______ ,在整个循环系统中做催化剂的物质是_______ (填化学式)。
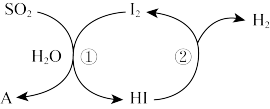
(3)钠碱循环法:用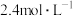 的
的 溶液吸收尾气中的
溶液吸收尾气中的 。
。
①上述 溶液中:
溶液中: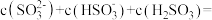
_______  ;
;
_______ 。
②室温下,当溶液的pH约为6时, 溶液吸收
溶液吸收 能力显著下降,此时溶液中
能力显著下降,此时溶液中 的浓度是
的浓度是 ,则此时溶液中各离子浓度由大到小的顺序为
,则此时溶液中各离子浓度由大到小的顺序为_______ 。
(4)氨石灰水法:
第一步:用过量的浓氨水吸收 ,并在空气中氧化;
,并在空气中氧化;
第二步:加入澄清石灰水。
已知:室温下,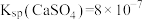 ,
,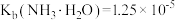 ,则室温下,第二步反应:
,则室温下,第二步反应: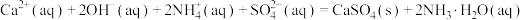 的平衡常数
的平衡常数
_______ 。
 的排放是形成酸雨的重要原因之一,工业上可采用多种方法减少
的排放是形成酸雨的重要原因之一,工业上可采用多种方法减少 的排放。回答下列问题:
的排放。回答下列问题:(1)
 还原法:
还原法:已知:
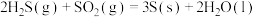
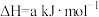 ;
; 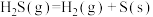
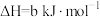 。
。则
 和
和 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为(2)碘循环法的循环过程如图所示,反应①的化学方程式为

(3)钠碱循环法:用
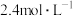 的
的 溶液吸收尾气中的
溶液吸收尾气中的 。
。①上述
 溶液中:
溶液中: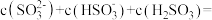
 ;
;
②室温下,当溶液的pH约为6时,
 溶液吸收
溶液吸收 能力显著下降,此时溶液中
能力显著下降,此时溶液中 的浓度是
的浓度是 ,则此时溶液中各离子浓度由大到小的顺序为
,则此时溶液中各离子浓度由大到小的顺序为(4)氨石灰水法:
第一步:用过量的浓氨水吸收
 ,并在空气中氧化;
,并在空气中氧化;第二步:加入澄清石灰水。
已知:室温下,
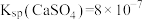 ,
,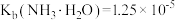 ,则室温下,第二步反应:
,则室温下,第二步反应: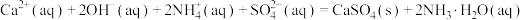 的平衡常数
的平衡常数
您最近一年使用:0次
2023-01-15更新
|
139次组卷
|
4卷引用:湖北省恩施土家族苗族自治州巴东县2022-2023学年高二下学期6月月考化学试题
名校
解题方法
6 . 诺贝尔化学奖获得者GeorgeA.Olah提出了“甲醇经济”的概念,他建议用甲醇来代替目前广泛使用的化石燃料。工业上用天然气为原料,分为两个阶段制备甲醇:
(i)制备合成气:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=+206.0 kJ·mol-1
CO(g)+3H2(g) ΔH=+206.0 kJ·mol-1
(ii)合成甲醇:CO(g)+2H2(g) CH3OH(g) ΔH=-90.67 kJ·mol-1
CH3OH(g) ΔH=-90.67 kJ·mol-1
回答下列问题:
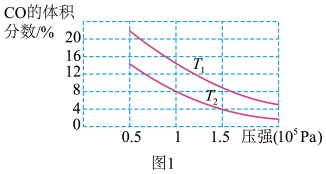
(1)制备合成气反应中,平衡混合物中CO的体积分数与压强的关系如图1所示,判断T1和T2的大小关系:T1_______ T2(填“<”或“=”),理由是_______ 。
(2)工业生产中为解决合成气中H2过量而CO不足的问题,原料气中需添加CO2,发生反应CO2(g)+H2(g) CO(g)+H2O(g) ΔH=+41.17 kJ·mol-1,为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳的体积比为
CO(g)+H2O(g) ΔH=+41.17 kJ·mol-1,为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳的体积比为_______ 。
(3)在体积不变的密闭容器中投入0.5 mol CO和1 mol H2,不同条件下发生反应:CO(g)+2H2(g) CH3OH(g) ΔH。实验测得平衡时H2的转化率随温度、压强的变化如图2所示。
CH3OH(g) ΔH。实验测得平衡时H2的转化率随温度、压强的变化如图2所示。
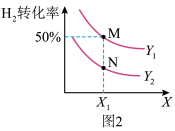
①图2中X代表_______ (填“温度”或“压强”)。图3中正确表示该反应的平衡常数的负对数pK(pK=-lgK)与X的关系的曲线_______ (填“AC”或“AB”)。
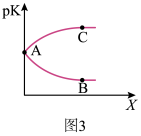
②若图2中M点对应的容器体积为5 L,此时容器的压强为b kPa,则N点的压强平衡常数Kp为_______ 。
(4)为节约化石能源,用CO2代替CO作为制备甲醇的碳源正成为当前研究的焦点。
①二氧化碳加氢合成甲醇和水蒸气的热化学方程式为_______ 。
②研究表明在二氧化碳合成甲醇的原料气中加入CO可以降低CO2与H2反应的活化能。在200~360℃、9MPa时,合成气初始组成H2、CO、CO2物质的量之比为7:2:1的条件下研究甲醇的合成反应(如图所示)。
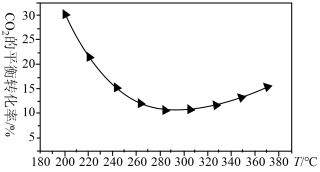
CO2的平衡转化率随温度的升高先减小后增大,请分析可能的原因_______ 。
(i)制备合成气:CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH=+206.0 kJ·mol-1
CO(g)+3H2(g) ΔH=+206.0 kJ·mol-1(ii)合成甲醇:CO(g)+2H2(g)
 CH3OH(g) ΔH=-90.67 kJ·mol-1
CH3OH(g) ΔH=-90.67 kJ·mol-1回答下列问题:
(1)制备合成气反应中,平衡混合物中CO的体积分数与压强的关系如图1所示,判断T1和T2的大小关系:T1

(2)工业生产中为解决合成气中H2过量而CO不足的问题,原料气中需添加CO2,发生反应CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH=+41.17 kJ·mol-1,为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳的体积比为
CO(g)+H2O(g) ΔH=+41.17 kJ·mol-1,为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳的体积比为(3)在体积不变的密闭容器中投入0.5 mol CO和1 mol H2,不同条件下发生反应:CO(g)+2H2(g)
 CH3OH(g) ΔH。实验测得平衡时H2的转化率随温度、压强的变化如图2所示。
CH3OH(g) ΔH。实验测得平衡时H2的转化率随温度、压强的变化如图2所示。
①图2中X代表

②若图2中M点对应的容器体积为5 L,此时容器的压强为b kPa,则N点的压强平衡常数Kp为
(4)为节约化石能源,用CO2代替CO作为制备甲醇的碳源正成为当前研究的焦点。
①二氧化碳加氢合成甲醇和水蒸气的热化学方程式为
②研究表明在二氧化碳合成甲醇的原料气中加入CO可以降低CO2与H2反应的活化能。在200~360℃、9MPa时,合成气初始组成H2、CO、CO2物质的量之比为7:2:1的条件下研究甲醇的合成反应(如图所示)。

CO2的平衡转化率随温度的升高先减小后增大,请分析可能的原因
您最近一年使用:0次
2023-01-12更新
|
135次组卷
|
3卷引用:湖北省部分重点中学2023届高三上学期第二次联考化学试题
7 . 天然气的主要成分为CH4,一般还含有C2H6等烃类,是重要的燃料和化工原料。
(1)乙烷在一定条件可发生如下反应:C2H6(g)=C2H4(g)+H2(g) ΔH1,相关物质的燃烧热数据如下表所示:
①ΔH1=_______ kJ·mol-1。
②提高该反应平衡转化率的方法有_______ 、_______ 。
③容器中通入等物质的量的乙烷和氢气,在等压下(p)发生上述反应,乙烷的平衡转化率为α。反应的平衡常数Kp=_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)高温下,甲烷生成乙烷的反应如下:2CH4 C2H6+H2。反应在初期阶段的速率方程为v=k×c(CH4),其中k为反应速率常数。
C2H6+H2。反应在初期阶段的速率方程为v=k×c(CH4),其中k为反应速率常数。
①设反应开始时的反应速率为r1,甲烷的转化率为α时的反应速率为r2,则r2=_______ r1。
②对于处于初期阶段的该反应,下列说法正确的是_______ 。
A.增加甲烷浓度,r增大 B.增加H2浓度,r增大
C.乙烷的生成速率逐渐增大 D.降低反应温度,k减小
(3)甲烷-空气燃料电池是一种高效能、低污染电池,利用此电池可作电源,则在酸性介质中此电池负极的电极反应式为_______ 。
(1)乙烷在一定条件可发生如下反应:C2H6(g)=C2H4(g)+H2(g) ΔH1,相关物质的燃烧热数据如下表所示:
| 物质 | C2H6(g) | C2H4(g) | H2(g) |
| 燃烧热ΔH(kJ·mol-1) | -1560 | -1411 | -286 |
②提高该反应平衡转化率的方法有
③容器中通入等物质的量的乙烷和氢气,在等压下(p)发生上述反应,乙烷的平衡转化率为α。反应的平衡常数Kp=
(2)高温下,甲烷生成乙烷的反应如下:2CH4
 C2H6+H2。反应在初期阶段的速率方程为v=k×c(CH4),其中k为反应速率常数。
C2H6+H2。反应在初期阶段的速率方程为v=k×c(CH4),其中k为反应速率常数。①设反应开始时的反应速率为r1,甲烷的转化率为α时的反应速率为r2,则r2=
②对于处于初期阶段的该反应,下列说法正确的是
A.增加甲烷浓度,r增大 B.增加H2浓度,r增大
C.乙烷的生成速率逐渐增大 D.降低反应温度,k减小
(3)甲烷-空气燃料电池是一种高效能、低污染电池,利用此电池可作电源,则在酸性介质中此电池负极的电极反应式为
您最近一年使用:0次
8 . I.钛(Ti)因具有硬度大、熔点高、耐酸腐蚀等优点而被应用于航空、电子等领域,由金红石(TiO2)制取单质Ti的步骤如下:
TiO2→TiCl4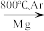 Ti
Ti
已知:i. C(s)+O2(g)=CO2(g) ΔH=−393.5 kJ∙mol−1
ii. 2CO(g)+O2(g)=2CO2(g) ΔH=−566 kJ∙mol−1
ⅲ. TiO2(s)+2Cl2(g)=TiCl(s)+O2(g) ΔH=+141 kJ∙mol−1
(1)TiO2(s)+2Cl2(g)+2 C(s)=TiCl(s)+2CO(g)的ΔH=_______
(2)反应TiCl4+2Mg 2MgCl2+Ti在Ar气氛中进行的理由是
2MgCl2+Ti在Ar气氛中进行的理由是_______
Ⅱ. 50mL 0.50 mol∙L−1盐酸与50mL 0.55 mol∙L−1 NaOH溶液在简易量热计中进行中和反应,假设盐酸和氢氧化钠溶液的密度都是1g·cm−3,又知中和反应后生成溶液的比热容c=4.18J·g−1·℃−1。为了计算中和热,某学生实验记录的数据如下:
(3)依据该学生的实验数据计算,该实验测得的中和热ΔH=_______ (结果保留一位小数)。如用0.5 mol∙L−1的盐酸与NaOH固体进行实验,则实验中测得的中和热数值将_______ (填“偏大”、“偏小”或“不变”)。
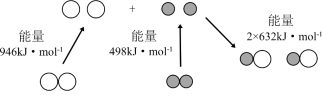
Ⅲ.25℃时,在体积为2L的密闭容器中,气态物质A、B、C的物质的量n随时间t的变化如图1所示,已知达到平衡后,降低温度,A的转化率将增大。
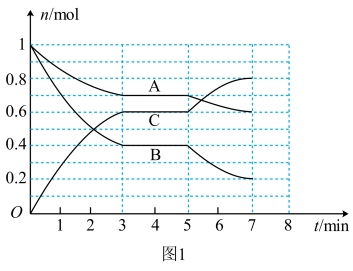
(4)根据图1数据,写出该反应的化学方程式:_______ 。此反应的平衡常数表达式K=_______ 。
(5)在5~7min内,若K不变,则此处曲线变化的原因是_______ 。
(6)此反应的反应速率v和时间t的关系如图2,各阶段的平衡常数如表所示。K1、K2、K3、K4之间的关系为_______ (用“>”、“<”或“=”连接)
TiO2→TiCl4
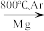 Ti
Ti已知:i. C(s)+O2(g)=CO2(g) ΔH=−393.5 kJ∙mol−1
ii. 2CO(g)+O2(g)=2CO2(g) ΔH=−566 kJ∙mol−1
ⅲ. TiO2(s)+2Cl2(g)=TiCl(s)+O2(g) ΔH=+141 kJ∙mol−1
(1)TiO2(s)+2Cl2(g)+2 C(s)=TiCl(s)+2CO(g)的ΔH=
(2)反应TiCl4+2Mg
 2MgCl2+Ti在Ar气氛中进行的理由是
2MgCl2+Ti在Ar气氛中进行的理由是Ⅱ. 50mL 0.50 mol∙L−1盐酸与50mL 0.55 mol∙L−1 NaOH溶液在简易量热计中进行中和反应,假设盐酸和氢氧化钠溶液的密度都是1g·cm−3,又知中和反应后生成溶液的比热容c=4.18J·g−1·℃−1。为了计算中和热,某学生实验记录的数据如下:
| 试验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
Ⅲ.25℃时,在体积为2L的密闭容器中,气态物质A、B、C的物质的量n随时间t的变化如图1所示,已知达到平衡后,降低温度,A的转化率将增大。

(4)根据图1数据,写出该反应的化学方程式:
(5)在5~7min内,若K不变,则此处曲线变化的原因是
(6)此反应的反应速率v和时间t的关系如图2,各阶段的平衡常数如表所示。K1、K2、K3、K4之间的关系为

| t2~t3 | t4~t5 | t5~t6 | t7~t8 |
| K1 | K2 | K3 | K4 |
您最近一年使用:0次
解题方法
9 . “绿水青山就是金山银山”,运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
(1)汽车是近代重要的交通运输工具,随着汽车量的激增,汽车尾气造成的环境污染也日益严重。汽车尾气中的有害成分主要有CO、NO、SO2、颗粒物和臭氧等。
①汽车尾气中NO生成过程中的能量变化如图所示。1 mol N2和1 mol O2完全反应生成NO会_______ (填“吸收”或“放出”)_______ kJ能量。
②一种新型催化剂用于NO和CO的反应:NO+2CO2 CO2+N2为了测定在某种催化剂作用下该反应的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下表:
CO2+N2为了测定在某种催化剂作用下该反应的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下表:
前2 s内的平均反应速率v(N2)=_______ 。(保留小数点后一位)
③在容积固定的绝热容器中发生反应2NO+2CO 2CO2+N2,下列能说明该反应已达到平衡状态的是
2CO2+N2,下列能说明该反应已达到平衡状态的是_______ (填标号)
A.容器内混合气体温度不再变化 B.容器内的气体压强保持不变
C.2v逆(NO)=v正(N2) D.容器内混合气体密度保持不变
(2)煤燃烧排放的烟气中含有SO2和NO2,会形成酸雨,污染大气。
①NaClO2溶液在碱性条件下可对烟气进行脱硫、脱硝,效果非常好。完成下列对烟气脱氮过程的离子方程式:_______
_______ +_______NO+__________=_______Cl-+_______
+_______NO+__________=_______Cl-+_______ +______________。
+______________。
②针对含SO2的工业废气可以采用“钙基固硫法”。例如将生石灰与含硫的煤混合后再燃烧,可以将SO2最终转化为CaSO4,请写出生石灰将SO2转化为CaSO4的反应的化学方程式:_______
③将SO2转化为重要的化工原料H2SO4的原理示意图如图。
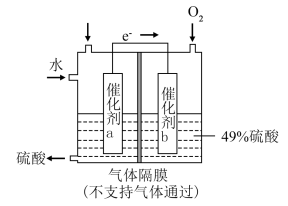
催化剂a表面的电极反应式为_______ 。若得到的硫酸质量分数仍为49%,则理论上参加反应的SO2与加入的H2O的质量比为_______ 。
(1)汽车是近代重要的交通运输工具,随着汽车量的激增,汽车尾气造成的环境污染也日益严重。汽车尾气中的有害成分主要有CO、NO、SO2、颗粒物和臭氧等。
①汽车尾气中NO生成过程中的能量变化如图所示。1 mol N2和1 mol O2完全反应生成NO会

②一种新型催化剂用于NO和CO的反应:NO+2CO2
 CO2+N2为了测定在某种催化剂作用下该反应的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下表:
CO2+N2为了测定在某种催化剂作用下该反应的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/(10-4 mol·L-1) | 10 | 4.5 | 2.5 | 1.5 | 1.0 | 1.0 |
| c(CO)/(10-3 mol·L-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
前2 s内的平均反应速率v(N2)=
③在容积固定的绝热容器中发生反应2NO+2CO
 2CO2+N2,下列能说明该反应已达到平衡状态的是
2CO2+N2,下列能说明该反应已达到平衡状态的是A.容器内混合气体温度不再变化 B.容器内的气体压强保持不变
C.2v逆(NO)=v正(N2) D.容器内混合气体密度保持不变
(2)煤燃烧排放的烟气中含有SO2和NO2,会形成酸雨,污染大气。
①NaClO2溶液在碱性条件下可对烟气进行脱硫、脱硝,效果非常好。完成下列对烟气脱氮过程的离子方程式:
_______
 +_______NO+__________=_______Cl-+_______
+_______NO+__________=_______Cl-+_______ +______________。
+______________。②针对含SO2的工业废气可以采用“钙基固硫法”。例如将生石灰与含硫的煤混合后再燃烧,可以将SO2最终转化为CaSO4,请写出生石灰将SO2转化为CaSO4的反应的化学方程式:
③将SO2转化为重要的化工原料H2SO4的原理示意图如图。

催化剂a表面的电极反应式为
您最近一年使用:0次
解题方法
10 . 丁二烯、异丁烯均是重要的有机化工原料,广泛用于有机合成和精细化工。
I.正丁烷催化氧化制1.3-丁二烯的一种反应途径如图所示。
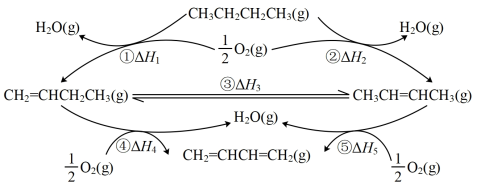
(1)已知: ,则
,则
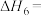
______ ,相同条件下,稳定性:1-丁烯______ (填“>”、“<”或“=”)2-丁烯。
(2)在某恒温恒容密闭容器中通入等物质的量的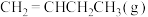 和
和 ,仅发生反应④(该反应为可逆反应),下列描述能说明反应已经达到平衡状态的是______(填标号)。
,仅发生反应④(该反应为可逆反应),下列描述能说明反应已经达到平衡状态的是______(填标号)。
II.正丁烷脱氢异构制异丁烯。
温度为T℃,向体积不等的恒容密闭容器中均充入1 mol正丁烷,发生反应:

 ,反应均进行10 min,测得各容器中正丁烷的转化率与容器体积的关系如图所示。
,反应均进行10 min,测得各容器中正丁烷的转化率与容器体积的关系如图所示。
(3)A点时
______ (填“>”、“=”或“<”,同) ;正反应速率:
;正反应速率:
______ 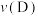 。
。
(4)若C点为平衡点且容器总压强为0.4 MPa,则该条件下,反应的平衡常数
______ MPa(以分压表示的平衡常数为 ,分压=总压×物质的量分数)。
,分压=总压×物质的量分数)。
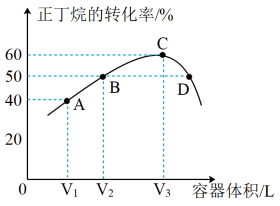
(5)向A点对应的反应体系中再充入一定量的正丁烷,达到平衡时,正丁烷的转化率______ (填“增大”、“减小”或“不变”)。
(6)
______ 。
I.正丁烷催化氧化制1.3-丁二烯的一种反应途径如图所示。

(1)已知:
 ,则
,则
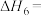
(2)在某恒温恒容密闭容器中通入等物质的量的
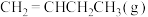 和
和 ,仅发生反应④(该反应为可逆反应),下列描述能说明反应已经达到平衡状态的是______(填标号)。
,仅发生反应④(该反应为可逆反应),下列描述能说明反应已经达到平衡状态的是______(填标号)。| A.混合气体的密度不再改变 |
| B.混合气体平均摩尔质量不再改变 |
C.丁二烯和 的物质的量之比不再改变 的物质的量之比不再改变 |
D.1-丁烯和 的物质的量之比不再改变 的物质的量之比不再改变 |
II.正丁烷脱氢异构制异丁烯。
温度为T℃,向体积不等的恒容密闭容器中均充入1 mol正丁烷,发生反应:

 ,反应均进行10 min,测得各容器中正丁烷的转化率与容器体积的关系如图所示。
,反应均进行10 min,测得各容器中正丁烷的转化率与容器体积的关系如图所示。(3)A点时

 ;正反应速率:
;正反应速率:
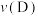 。
。(4)若C点为平衡点且容器总压强为0.4 MPa,则该条件下,反应的平衡常数

 ,分压=总压×物质的量分数)。
,分压=总压×物质的量分数)。
(5)向A点对应的反应体系中再充入一定量的正丁烷,达到平衡时,正丁烷的转化率
(6)

您最近一年使用:0次



