1 . 2021年3月5日,国务院政府工作报告中指出,扎实做好碳达峰、碳中和各项工作。为了达到碳中和,研发二氧化碳的利用技术成为热点。
(1)CH4—CO2催化重整可得到合成气(CO和H2),其工艺过程中涉及如下反应:
反应①:CO2(g)+H2(g) CO(g)+H2O(g) △H1=+41.2kJ·mol-1
CO(g)+H2O(g) △H1=+41.2kJ·mol-1
反应②:CH4(g)+ O2(g)
O2(g) CO(g)+2H2(g) △H2=-36.0kJ·mol-1
CO(g)+2H2(g) △H2=-36.0kJ·mol-1
反应③: O2(g)+H2(g)
O2(g)+H2(g) H2O(g) △H3=-241.8kJ·mol-1
H2O(g) △H3=-241.8kJ·mol-1
则反应④:CH4(g)+CO2(g) 2CO(g)+2H2(g) △H4=
2CO(g)+2H2(g) △H4=__ kJ·mol-1
(2)在催化剂作用下合成气可发生反应:CO(g)+2H2(g) CH3OH(g),在a、b、c容积不等的恒容密闭容器中(其中容器b容积为1L),均充入0.1molCO和0.2molH2,充分反应后测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图1所示:
CH3OH(g),在a、b、c容积不等的恒容密闭容器中(其中容器b容积为1L),均充入0.1molCO和0.2molH2,充分反应后测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图1所示:
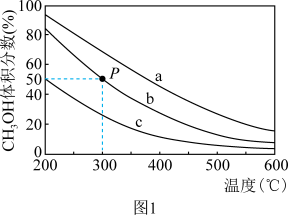
①容器的容积a___ c(填“>”“<”或“=”)。
②P点时,H2的转化率为____ ;若其他条件不变,将恒容密闭容器改为恒压密闭容器,平衡后H2的转化率将____ (填“增大”、“减小”或“不变”)。
③当温度为300℃时,该反应的化学平衡常数K=____ 。
(3)利用电化学方法可以将CO2有效地转化为HCOO-,装置如图2所示。
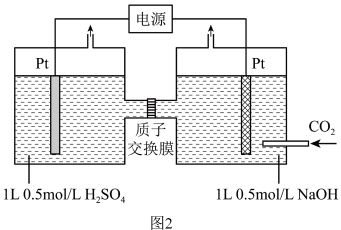
①在该装置中,右侧Pt电极的电极反应式为____ 。
②装置工作时,阴极除有HCOO-生成外,还可能生成副产物降低电解效率(电解效率=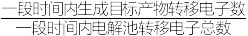 ×100%),标准状况下,当阳极生成氧气体积为448mL时,测得阴极区内的c(HCOO-)=0.03mol/L,电解效率为
×100%),标准状况下,当阳极生成氧气体积为448mL时,测得阴极区内的c(HCOO-)=0.03mol/L,电解效率为____ (忽略电解前后溶液的体积变化)。
(1)CH4—CO2催化重整可得到合成气(CO和H2),其工艺过程中涉及如下反应:
反应①:CO2(g)+H2(g)
 CO(g)+H2O(g) △H1=+41.2kJ·mol-1
CO(g)+H2O(g) △H1=+41.2kJ·mol-1反应②:CH4(g)+
 O2(g)
O2(g) CO(g)+2H2(g) △H2=-36.0kJ·mol-1
CO(g)+2H2(g) △H2=-36.0kJ·mol-1反应③:
 O2(g)+H2(g)
O2(g)+H2(g) H2O(g) △H3=-241.8kJ·mol-1
H2O(g) △H3=-241.8kJ·mol-1则反应④:CH4(g)+CO2(g)
 2CO(g)+2H2(g) △H4=
2CO(g)+2H2(g) △H4=(2)在催化剂作用下合成气可发生反应:CO(g)+2H2(g)
 CH3OH(g),在a、b、c容积不等的恒容密闭容器中(其中容器b容积为1L),均充入0.1molCO和0.2molH2,充分反应后测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图1所示:
CH3OH(g),在a、b、c容积不等的恒容密闭容器中(其中容器b容积为1L),均充入0.1molCO和0.2molH2,充分反应后测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图1所示:
①容器的容积a
②P点时,H2的转化率为
③当温度为300℃时,该反应的化学平衡常数K=
(3)利用电化学方法可以将CO2有效地转化为HCOO-,装置如图2所示。

①在该装置中,右侧Pt电极的电极反应式为
②装置工作时,阴极除有HCOO-生成外,还可能生成副产物降低电解效率(电解效率=
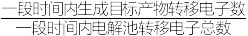 ×100%),标准状况下,当阳极生成氧气体积为448mL时,测得阴极区内的c(HCOO-)=0.03mol/L,电解效率为
×100%),标准状况下,当阳极生成氧气体积为448mL时,测得阴极区内的c(HCOO-)=0.03mol/L,电解效率为
您最近一年使用:0次
2 . 合成氨的反应对人类解决粮食问题贡献巨大,德国化学家F.Haber因合成氨而获得诺贝尔奖。合成氨反应热化学方程式如下:N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol
(1)已知N2(g)+3H2(g) 2NH3(g)不加入催化剂时正反应的活化能为326kJ/mol,则该反应逆反应的活化能为
2NH3(g)不加入催化剂时正反应的活化能为326kJ/mol,则该反应逆反应的活化能为_______ kJ/mol。
(2)已知N2(g)+O2(g)=2NO(g) △H=+180kJ/mol
H2的燃烧热△H=-285.8kJ/mol
则NH3(g)+ O2(g)=NO(g)+
O2(g)=NO(g)+ H2O(l) △H=
H2O(l) △H=_______ kJ/mol。
(3)一定温度下,向恒容的密闭容器中充入一定量的N2和H2发生反应,测得各组分浓度随时间变化如图所示。
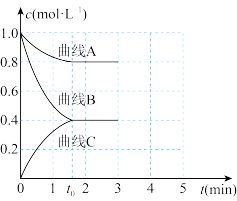
①表示c(H2)变化的曲线是_______ (填“曲线A”“曲线B”或“曲线C”)。
②0~t0时用NH3表示的化学反应速率为v(NH3)=_______ mol·L-1·min-1。
③下列能说明该反应达到平衡状态的是_______ (填标号)。
A.容器中混合气体的密度不随时间变化
B.容器中的n(N2)与n(H2)的比值不随时间变化
C.断裂3molH-H的同时断裂6molN-H键
D.3v正(H2)=2v逆(NH3)
(4)合成氨反应在某催化剂条件下的相对能量-反应历程如图所示(ad为吸附态):
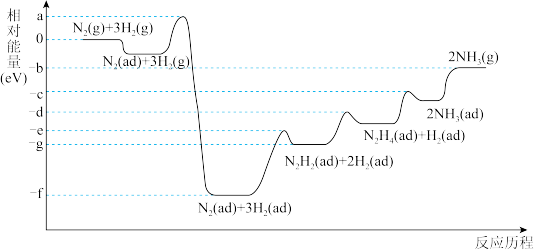
①该过程中含氮的中间产物有_______ 种(填数字)。
②活化能最大的那一步基元反应方程式为_______ 。
③下列说法正确的是_______ (填标号)。
A.最后一步NH3(ad)变为NH3(g)为吸热过程。
B.催化剂参与反应,但不改变合成氨反应的△H
C.催化剂和升温都能降低反应的活化能,加快合成氨的反应速率
D.使用催化剂和压缩容器体积加压都能增大活化分子百分数,加快合成氨反应速率
 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol(1)已知N2(g)+3H2(g)
 2NH3(g)不加入催化剂时正反应的活化能为326kJ/mol,则该反应逆反应的活化能为
2NH3(g)不加入催化剂时正反应的活化能为326kJ/mol,则该反应逆反应的活化能为(2)已知N2(g)+O2(g)=2NO(g) △H=+180kJ/mol
H2的燃烧热△H=-285.8kJ/mol
则NH3(g)+
 O2(g)=NO(g)+
O2(g)=NO(g)+ H2O(l) △H=
H2O(l) △H=(3)一定温度下,向恒容的密闭容器中充入一定量的N2和H2发生反应,测得各组分浓度随时间变化如图所示。

①表示c(H2)变化的曲线是
②0~t0时用NH3表示的化学反应速率为v(NH3)=
③下列能说明该反应达到平衡状态的是
A.容器中混合气体的密度不随时间变化
B.容器中的n(N2)与n(H2)的比值不随时间变化
C.断裂3molH-H的同时断裂6molN-H键
D.3v正(H2)=2v逆(NH3)
(4)合成氨反应在某催化剂条件下的相对能量-反应历程如图所示(ad为吸附态):

①该过程中含氮的中间产物有
②活化能最大的那一步基元反应方程式为
③下列说法正确的是
A.最后一步NH3(ad)变为NH3(g)为吸热过程。
B.催化剂参与反应,但不改变合成氨反应的△H
C.催化剂和升温都能降低反应的活化能,加快合成氨的反应速率
D.使用催化剂和压缩容器体积加压都能增大活化分子百分数,加快合成氨反应速率
您最近一年使用:0次
3 . 2020年已提出:我国将力争2030年前实现碳达峰、2060年前实现碳中和。研究 的转化和
的转化和 资源化利用对缓解碳减排压力和推进能源绿色转型,实现“碳达峰、碳中和”具有重要意义。
资源化利用对缓解碳减排压力和推进能源绿色转型,实现“碳达峰、碳中和”具有重要意义。
(1) 与
与 催化重整制合成气是研究热点之一。发生的主要反应有:
催化重整制合成气是研究热点之一。发生的主要反应有:
反应①: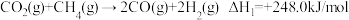
反应②: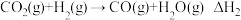
有关化学键键能数据如表:
则反应②的反应热
_______  。
。
(2)对于上述反应体系,下列说法错误的是_______ 。
A.增大 的浓度,反应①②的正反应速率均增加
的浓度,反应①②的正反应速率均增加
B.恒容密闭容器中当气体密度不变时,反应达到平衡状态
C.加入催化剂,可提高 的平衡转化率
的平衡转化率
(3)在体积为 的刚性容器中进行“合成气催化重整”,反应的化学方程式为
的刚性容器中进行“合成气催化重整”,反应的化学方程式为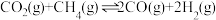 。当投料比,
。当投料比,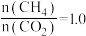 时,
时, 的平衡转化率(
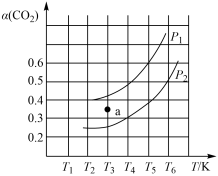
的平衡转化率( )与温度(T)、初始压强(p)的关系如图所示。压强
)与温度(T)、初始压强(p)的关系如图所示。压强
_______ (填“>”“<”或“=”,下同) ;当温度为
;当温度为 、压强为
、压强为 时,a点时的v(正)
时,a点时的v(正)_______ v(逆);起始时向容器中加入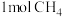 和
和 ,在温度为
,在温度为 、初始压强为
、初始压强为 时反应,该反应的
时反应,该反应的
_______ 。
(4)科学家利用电化学装置实现 和
和 两种分子的耦合转化来达到减碳的目的,其原理如图所示:
两种分子的耦合转化来达到减碳的目的,其原理如图所示:
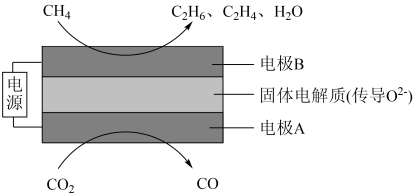
①电极A上的电极反应式为_______ 。
②若生成的乙烯和乙烷的物质的量比为1∶1,则消耗的 和
和 的物质的量之比为
的物质的量之比为_______ 。
 的转化和
的转化和 资源化利用对缓解碳减排压力和推进能源绿色转型,实现“碳达峰、碳中和”具有重要意义。
资源化利用对缓解碳减排压力和推进能源绿色转型,实现“碳达峰、碳中和”具有重要意义。(1)
 与
与 催化重整制合成气是研究热点之一。发生的主要反应有:
催化重整制合成气是研究热点之一。发生的主要反应有:反应①:
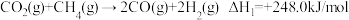
反应②:
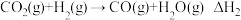
有关化学键键能数据如表:
| 化学键 |  |  |  |  |
键能/ | 436 | 463 | 803 | 1076 |

 。
。(2)对于上述反应体系,下列说法错误的是
A.增大
 的浓度,反应①②的正反应速率均增加
的浓度,反应①②的正反应速率均增加B.恒容密闭容器中当气体密度不变时,反应达到平衡状态
C.加入催化剂,可提高
 的平衡转化率
的平衡转化率(3)在体积为
 的刚性容器中进行“合成气催化重整”,反应的化学方程式为
的刚性容器中进行“合成气催化重整”,反应的化学方程式为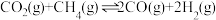 。当投料比,
。当投料比,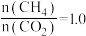 时,
时, 的平衡转化率(
的平衡转化率( )与温度(T)、初始压强(p)的关系如图所示。压强
)与温度(T)、初始压强(p)的关系如图所示。压强
 ;当温度为
;当温度为 、压强为
、压强为 时,a点时的v(正)
时,a点时的v(正)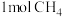 和
和 ,在温度为
,在温度为 、初始压强为
、初始压强为 时反应,该反应的
时反应,该反应的

(4)科学家利用电化学装置实现
 和
和 两种分子的耦合转化来达到减碳的目的,其原理如图所示:
两种分子的耦合转化来达到减碳的目的,其原理如图所示:
①电极A上的电极反应式为
②若生成的乙烯和乙烷的物质的量比为1∶1,则消耗的
 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解题方法
4 . 回答下列问题:
(1)已知稀溶液中,1mol H2SO4与2mol NaOH恰好完全反应时,放出114.6kJ热量,写出该反应表示中和热的热化学方程式:_______ 。
(2)利用甲烷的还原性,可以对大气中的氮氧化合物进行处理。已知一定条件下:
①4NO(g)=2NO2(g)+N2(g) ∆H1= -293kJ·mol-l
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ∆H2= -1160kJ·mol-1
则CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ∆H=_______ kJ·mol-1,该反应能在_______ 下自发进行。(选填“低温”、“高温”或“任何温度”)
(3)①恒温恒容的密闭容器中,发生反应CO (g) +H2S (g) COS (g) +H2 (g), 若反应前只充10mol CO和x mol H2S,达到平衡时CO的物质的量为8mol,且化学平衡常数为0.1,则x=
COS (g) +H2 (g), 若反应前只充10mol CO和x mol H2S,达到平衡时CO的物质的量为8mol,且化学平衡常数为0.1,则x=_______ mol。
②恒温恒容时,能表明Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)达平衡状态的是
2Fe(s)+3CO2(g)达平衡状态的是_______ ( 填字母)。
A.单位时间内生成n mol CO同时消耗n mol CO2
B. c(CO)不随时间改变
C. CO2的体积分数不变
D. Fe 的浓度不变
(4)某种新工艺装置是氯碱工业装置和另一种电化学装置组合而成,相关物料的传输与转化关系如图所示,其中电极未标出,所用的离子交换膜都只允许阳离子通过。
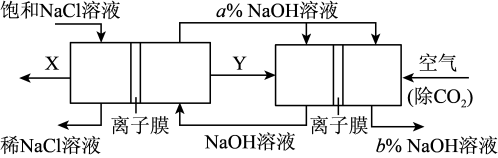
图中物质Y的电子式_______ , 图中b%_______ a%(填“<”或“>”或“=”),通入除去CO2的空气一极的电极反应式为_______ 。
(1)已知稀溶液中,1mol H2SO4与2mol NaOH恰好完全反应时,放出114.6kJ热量,写出该反应表示中和热的热化学方程式:
(2)利用甲烷的还原性,可以对大气中的氮氧化合物进行处理。已知一定条件下:
①4NO(g)=2NO2(g)+N2(g) ∆H1= -293kJ·mol-l
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ∆H2= -1160kJ·mol-1
则CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ∆H=
(3)①恒温恒容的密闭容器中,发生反应CO (g) +H2S (g)
 COS (g) +H2 (g), 若反应前只充10mol CO和x mol H2S,达到平衡时CO的物质的量为8mol,且化学平衡常数为0.1,则x=
COS (g) +H2 (g), 若反应前只充10mol CO和x mol H2S,达到平衡时CO的物质的量为8mol,且化学平衡常数为0.1,则x=②恒温恒容时,能表明Fe2O3(s)+3CO(g)
 2Fe(s)+3CO2(g)达平衡状态的是
2Fe(s)+3CO2(g)达平衡状态的是A.单位时间内生成n mol CO同时消耗n mol CO2
B. c(CO)不随时间改变
C. CO2的体积分数不变
D. Fe 的浓度不变
(4)某种新工艺装置是氯碱工业装置和另一种电化学装置组合而成,相关物料的传输与转化关系如图所示,其中电极未标出,所用的离子交换膜都只允许阳离子通过。

图中物质Y的电子式
您最近一年使用:0次
解题方法
5 . 碳单质及其化合物在生产生活中用途广泛。回答以下问题:
(1)以焦炭为原料,在高温下与水蒸气反应可制得水煤气,涉及反应如下:
a.主反应
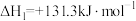
b.副反应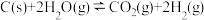

已知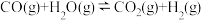 中逆反应的活化能为89kJ/mol,则该反应的正反应活化能为
中逆反应的活化能为89kJ/mol,则该反应的正反应活化能为___________ kJ/mol。对于反应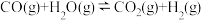 ,测得在不同温度下
,测得在不同温度下 的平衡转化率为
的平衡转化率为 ,则温度T1、T2、T3由大到小关系为
,则温度T1、T2、T3由大到小关系为___________ 。
(2)以水煤气制备甲烷的反应为: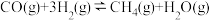 。下图是使用某种催化剂时转化过程中的能量变化(部分物质省略)。
。下图是使用某种催化剂时转化过程中的能量变化(部分物质省略)。
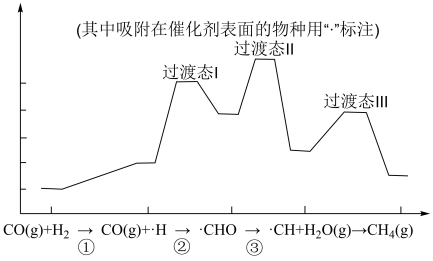
下列说法正确的是_________
A.步骤①只有非极性键断裂
B.步骤②的原子利用率为100%
C.过渡态Ⅱ能量最高,因此其对应的步骤③反应速率最慢
D.该方法可以清除剧毒气体CO,从而保护环境
该反应的正反应速率表达式为v正=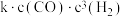 ,k为速率常数,在某温度下测得实验数据如表所示:
,k为速率常数,在某温度下测得实验数据如表所示:
由上述数据可得该温度下,c2=___________ mol/L,该反应的正反应速率常数k=___________ 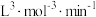 。若某温度下,在刚性密闭容器中加入CO(g)和
。若某温度下,在刚性密闭容器中加入CO(g)和 ,两者物质的量之比为1:2,起始压强为9MPa,平衡时压强为6MPa,该反应的压强平衡常数Kp=
,两者物质的量之比为1:2,起始压强为9MPa,平衡时压强为6MPa,该反应的压强平衡常数Kp=___________  (分压=总压×物质的量分数;结果保留两位有效数字)。
(分压=总压×物质的量分数;结果保留两位有效数字)。
(1)以焦炭为原料,在高温下与水蒸气反应可制得水煤气,涉及反应如下:
a.主反应

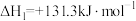
b.副反应
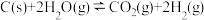

已知
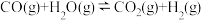 中逆反应的活化能为89kJ/mol,则该反应的正反应活化能为
中逆反应的活化能为89kJ/mol,则该反应的正反应活化能为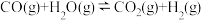 ,测得在不同温度下
,测得在不同温度下 的平衡转化率为
的平衡转化率为 ,则温度T1、T2、T3由大到小关系为
,则温度T1、T2、T3由大到小关系为(2)以水煤气制备甲烷的反应为:
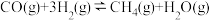 。下图是使用某种催化剂时转化过程中的能量变化(部分物质省略)。
。下图是使用某种催化剂时转化过程中的能量变化(部分物质省略)。
下列说法正确的是
A.步骤①只有非极性键断裂
B.步骤②的原子利用率为100%
C.过渡态Ⅱ能量最高,因此其对应的步骤③反应速率最慢
D.该方法可以清除剧毒气体CO,从而保护环境
该反应的正反应速率表达式为v正=
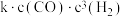 ,k为速率常数,在某温度下测得实验数据如表所示:
,k为速率常数,在某温度下测得实验数据如表所示:| CO浓度/(mol/L) | 浓度/(mol/L) | 正反应速率/( ) ) |
| 0.1 | c1 | 8.0 |
| c2 | c1 | 16.0 |
| c2 | 0.15 | 6.75 |
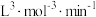 。若某温度下,在刚性密闭容器中加入CO(g)和
。若某温度下,在刚性密闭容器中加入CO(g)和 ,两者物质的量之比为1:2,起始压强为9MPa,平衡时压强为6MPa,该反应的压强平衡常数Kp=
,两者物质的量之比为1:2,起始压强为9MPa,平衡时压强为6MPa,该反应的压强平衡常数Kp= (分压=总压×物质的量分数;结果保留两位有效数字)。
(分压=总压×物质的量分数;结果保留两位有效数字)。
您最近一年使用:0次
2022-03-14更新
|
118次组卷
|
2卷引用:湖北省部分普通高中联合体2021-2022学年高二下学期期中联考化学试题
6 . 载人航天器中,可将航天员呼出的CO2转化为 H2O,再通过电解 H2O 获得 O2,实现 O2的再 生,同时还能制备 CH4.已知:
①CO2(g)+4H2(g)=CH4(g)+2H2O(l) ∆H =-252.9kJ/mol
②2H2O(l)=2H2(g)+O2(g) ∆H =571.6kJ/mol
请回答下列问题:
(1)反应①属于_______ (填“吸热”或“放热”)反应。
(2)反应CH4(g)+2O2(g)=CO2(g)+2H2O(l) ∆H =_______ kJ/mol。
(3)利用 CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如表:
①已知2CH4(g)=C2H4(g)+2H2(g) ΔH =+167kJ/mol,则a=_______ 。
②已知5C2H4(g)+12 (aq)+36H+ (aq)=12Mn2+ (aq)+10CO2 (g)+28H2O(l) ΔH =-m kJ·mol-1,当放出的热量为n kJ时,该反应转移电子的物质的量为
(aq)+36H+ (aq)=12Mn2+ (aq)+10CO2 (g)+28H2O(l) ΔH =-m kJ·mol-1,当放出的热量为n kJ时,该反应转移电子的物质的量为_______ mol。(用含m、n 的代数式表示)
③制备合成气反应历程分两步,步骤Ⅰ:CH4(g)⇌ C(ads)+2H2(g);步骤Ⅱ:C(ads)+ CO2(g)⇌ 2CO(g)。上述反应中 C(ads)为吸附性活性炭,反应历程的能量变化如图
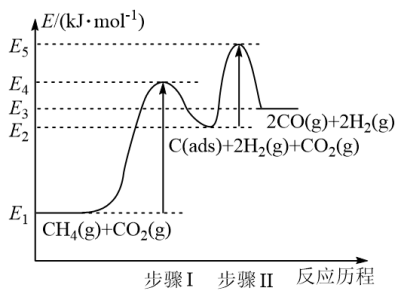
E4-E1表示步骤Ⅰ正反应的_______ ,制备合成气反应可在_______ (填“高温” 或“低温”)下自发进行。
①CO2(g)+4H2(g)=CH4(g)+2H2O(l) ∆H =-252.9kJ/mol
②2H2O(l)=2H2(g)+O2(g) ∆H =571.6kJ/mol
请回答下列问题:
(1)反应①属于
(2)反应CH4(g)+2O2(g)=CO2(g)+2H2O(l) ∆H =
(3)利用 CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如表:
| 化学键 | H-H | C=C | C-C | C-H |
| E(kJ/mol) | 436 | a | 348 | 413 |
②已知5C2H4(g)+12
 (aq)+36H+ (aq)=12Mn2+ (aq)+10CO2 (g)+28H2O(l) ΔH =-m kJ·mol-1,当放出的热量为n kJ时,该反应转移电子的物质的量为
(aq)+36H+ (aq)=12Mn2+ (aq)+10CO2 (g)+28H2O(l) ΔH =-m kJ·mol-1,当放出的热量为n kJ时,该反应转移电子的物质的量为③制备合成气反应历程分两步,步骤Ⅰ:CH4(g)⇌ C(ads)+2H2(g);步骤Ⅱ:C(ads)+ CO2(g)⇌ 2CO(g)。上述反应中 C(ads)为吸附性活性炭,反应历程的能量变化如图

E4-E1表示步骤Ⅰ正反应的
您最近一年使用:0次
2021-12-06更新
|
255次组卷
|
2卷引用:湖北省部分省级示范高中2021-2022学年高二上学期期中测试化学试题
解题方法
7 . 铁及其化合物在生产、生活中有广泛的应用。回答下列问题:
(1)复合氧化物铁酸锰( )可用于热化学循环分解制氢气,原理如下:
)可用于热化学循环分解制氢气,原理如下:
①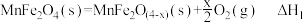 ;
;
②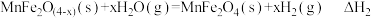 ;
;
③
则
___________ (用 、
、 表示)。
表示)。
(2)用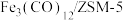 催化
催化 加氢合成低碳烯烃反应,反应过程如图。催化剂中添加助剂Na、K、Cu(也起催化作用)后可改变反应的选择性。
加氢合成低碳烯烃反应,反应过程如图。催化剂中添加助剂Na、K、Cu(也起催化作用)后可改变反应的选择性。
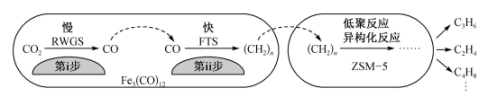
①第i步所发生反应的化学方程式为___________ 。
②下列说法错误的是___________ (填字母)。
A.第i步反应的活化能高于第ii步反应的活化能
B.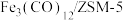 使
使 加氢合成低碳烯烃的
加氢合成低碳烯烃的 减小
减小
C.添加不同助剂后,各反应的平衡常数不变
(3)纳米铁是重要的储氢材料,可用反应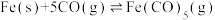 制得。在1 L恒容密闭容器中加入足量铁粉和0.48 mol CO,在
制得。在1 L恒容密闭容器中加入足量铁粉和0.48 mol CO,在 、
、 不同温度下进行反应,测得
不同温度下进行反应,测得 与温度、时间的关系如图所示。
与温度、时间的关系如图所示。
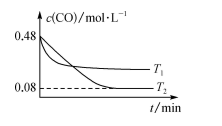
①
___________ (填“>”或“<”,下同) ,
,
___________ 0。
② 温度下,平衡时体系的压强为p,反应的标准平衡常数
温度下,平衡时体系的压强为p,反应的标准平衡常数
___________ {已知:标准平衡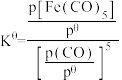 ,其中
,其中 为标准压强(
为标准压强(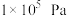 ),
),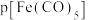 、
、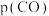 为各组分的平衡分压}。
为各组分的平衡分压}。
(1)复合氧化物铁酸锰(
 )可用于热化学循环分解制氢气,原理如下:
)可用于热化学循环分解制氢气,原理如下:①
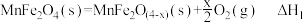 ;
;②
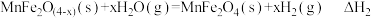 ;
;③

则

 、
、 表示)。
表示)。(2)用
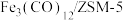 催化
催化 加氢合成低碳烯烃反应,反应过程如图。催化剂中添加助剂Na、K、Cu(也起催化作用)后可改变反应的选择性。
加氢合成低碳烯烃反应,反应过程如图。催化剂中添加助剂Na、K、Cu(也起催化作用)后可改变反应的选择性。
①第i步所发生反应的化学方程式为
②下列说法错误的是
A.第i步反应的活化能高于第ii步反应的活化能
B.
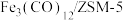 使
使 加氢合成低碳烯烃的
加氢合成低碳烯烃的 减小
减小C.添加不同助剂后,各反应的平衡常数不变
(3)纳米铁是重要的储氢材料,可用反应
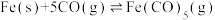 制得。在1 L恒容密闭容器中加入足量铁粉和0.48 mol CO,在
制得。在1 L恒容密闭容器中加入足量铁粉和0.48 mol CO,在 、
、 不同温度下进行反应,测得
不同温度下进行反应,测得 与温度、时间的关系如图所示。
与温度、时间的关系如图所示。
①

 ,
,
②
 温度下,平衡时体系的压强为p,反应的标准平衡常数
温度下,平衡时体系的压强为p,反应的标准平衡常数
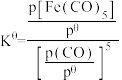 ,其中
,其中 为标准压强(
为标准压强(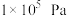 ),
),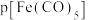 、
、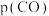 为各组分的平衡分压}。
为各组分的平衡分压}。
您最近一年使用:0次
解题方法
8 . 研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
Ⅰ.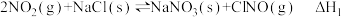 ;
;
Ⅱ.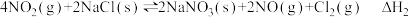 ;
;
Ⅲ. 。
。
回答下列问题:
(1)根据盖斯定律,写出表示 、
、 、
、 关系的等式:
关系的等式:___________ 。
(2)已知反应Ⅰ、Ⅱ、Ⅲ的平衡常数分别为 、
、 、
、 ,则
,则
___________ (用 、
、 表示)。
表示)。
(3)25 ℃时,向体积为1 L且带气压计的恒容密闭容器中通入0.04 mol NO和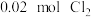 发生反应Ⅲ。
发生反应Ⅲ。
①下列描述能说明该反应已达到平衡状态的是___________ (填字母)。
A.容器内气体压强保持不变
B.容器内混合气体的体积保持不变
C.容器内混合气体的密度保持不变
D.容器内混合气体的平均相对分子质量保持不变
②若该反应达到化学平衡时,测得NO的浓度为 ,则该温度下的化学平衡常数
,则该温度下的化学平衡常数
___________ 。降低温度,化学平衡向___________ (填“正反应”或“逆反应”)方向移动。
Ⅰ.
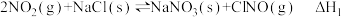 ;
;Ⅱ.
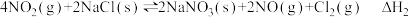 ;
;Ⅲ.
 。
。回答下列问题:
(1)根据盖斯定律,写出表示
 、
、 、
、 关系的等式:
关系的等式:(2)已知反应Ⅰ、Ⅱ、Ⅲ的平衡常数分别为
 、
、 、
、 ,则
,则
 、
、 表示)。
表示)。(3)25 ℃时,向体积为1 L且带气压计的恒容密闭容器中通入0.04 mol NO和
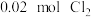 发生反应Ⅲ。
发生反应Ⅲ。①下列描述能说明该反应已达到平衡状态的是
A.容器内气体压强保持不变
B.容器内混合气体的体积保持不变
C.容器内混合气体的密度保持不变
D.容器内混合气体的平均相对分子质量保持不变
②若该反应达到化学平衡时,测得NO的浓度为
 ,则该温度下的化学平衡常数
,则该温度下的化学平衡常数
您最近一年使用:0次
解题方法
9 . 已知:
反应Ⅰ: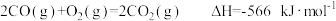 ;
;
反应Ⅱ: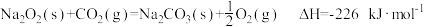 。
。
回答下列问题:
(1)能否通过反应Ⅰ判断等物质的量的CO、 具有能量的高低?
具有能量的高低?___________ (填“能”或“不能”)。
(2)CO的燃烧热
___________  。
。
(3)下列各图中表示反应Ⅱ能量变化的是___________(填字母)。
(4) 与
与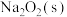 反应生成
反应生成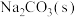 ,该反应的热化学方程式为
,该反应的热化学方程式为___________ 。
(5)依据反应Ⅱ,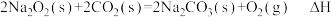
___________ (填“>”“<”或“=”)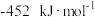 。
。
反应Ⅰ:
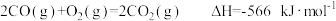 ;
;反应Ⅱ:
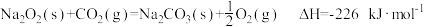 。
。回答下列问题:
(1)能否通过反应Ⅰ判断等物质的量的CO、
 具有能量的高低?
具有能量的高低?(2)CO的燃烧热

 。
。(3)下列各图中表示反应Ⅱ能量变化的是___________(填字母)。
A.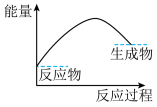 | B.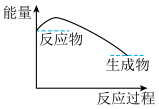 |
C.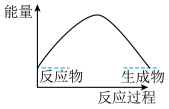 | D.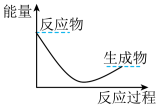 |
 与
与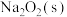 反应生成
反应生成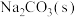 ,该反应的热化学方程式为
,该反应的热化学方程式为(5)依据反应Ⅱ,
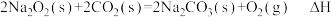
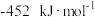 。
。
您最近一年使用:0次
10 . 2021年6月17日神舟天和成功对接,中国宇航员入驻空间站。空间站处理CO2的一种重要方法是CO2的收集与浓缩、CO2的还原。H2还原CO2制CH4的部分反应如下:
I.CO2(g)+H2(g) CO(g)+H2O(g) ∆H1=+41kJ/mol
CO(g)+H2O(g) ∆H1=+41kJ/mol
II.CO(g)+3H2(g) CH4(g)+H2O(g) ∆H2=-246kJ/mol
CH4(g)+H2O(g) ∆H2=-246kJ/mol
III.CO(g)+H2(g) C(s)+H2O(g) ∆H3=-131kJ/mol
C(s)+H2O(g) ∆H3=-131kJ/mol
回答下列问题:
(1)反应2C(s)+2H2O(g) CH4(g)+CO2(g)的∆H=
CH4(g)+CO2(g)的∆H=___________ kJ/mol。
(2)循环系统中可利用弱碱性的固态胺离子树脂(R1NHR2吸收舱内空气中的CO2、H2O生成酸式碳酸盐。该反应的化学方程式为___________ ;再解吸出CO2的简单方法是___________ 。
(3)控制起始时n(H2)/n(CO2)=4,p=1atm (atm表示标准大气压),在恒容密闭容器中,若只反生反应I、II,平衡时各物质的量分数随温度的变化如下图所示:
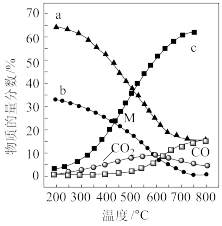
①图中代表的物质:a___________ ,(填化学式,下同),b___________ 。
②温度高于500℃时,CO的物质的量分数不断增大的原因是___________ 。
③M点时,平衡分压p(CO2)=___________ atm。反应CO2(g)+4H2(g) CH4(g)+2H2O(g)的平衡常数Kp=
CH4(g)+2H2O(g)的平衡常数Kp=___________ atm-2(以分压表示,分压=总压×物质的量分数)。
I.CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H1=+41kJ/mol
CO(g)+H2O(g) ∆H1=+41kJ/molII.CO(g)+3H2(g)
 CH4(g)+H2O(g) ∆H2=-246kJ/mol
CH4(g)+H2O(g) ∆H2=-246kJ/molIII.CO(g)+H2(g)
 C(s)+H2O(g) ∆H3=-131kJ/mol
C(s)+H2O(g) ∆H3=-131kJ/mol回答下列问题:
(1)反应2C(s)+2H2O(g)
 CH4(g)+CO2(g)的∆H=
CH4(g)+CO2(g)的∆H=(2)循环系统中可利用弱碱性的固态胺离子树脂(R1NHR2吸收舱内空气中的CO2、H2O生成酸式碳酸盐。该反应的化学方程式为
(3)控制起始时n(H2)/n(CO2)=4,p=1atm (atm表示标准大气压),在恒容密闭容器中,若只反生反应I、II,平衡时各物质的量分数随温度的变化如下图所示:

①图中代表的物质:a
②温度高于500℃时,CO的物质的量分数不断增大的原因是
③M点时,平衡分压p(CO2)=
 CH4(g)+2H2O(g)的平衡常数Kp=
CH4(g)+2H2O(g)的平衡常数Kp=
您最近一年使用:0次



