1 .  是存在于燃气中的一种有害气体,脱除
是存在于燃气中的一种有害气体,脱除 的方法有多种。回答下列问题:
的方法有多种。回答下列问题:
(1)Claus氧化回收硫的反应原理为:
①
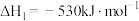 ;
;
②
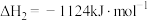 ;
;
③
 。
。
则
___________  。
。
(2)化学反应的焓变与反应物和生成物的键能(气态分子中 化学键解离成气态原子所吸收的能量)有关。已知某些化学键的键能如下表所示:
化学键解离成气态原子所吸收的能量)有关。已知某些化学键的键能如下表所示:
结合(1)中反应原理,
___________ 。
(3)电解法治理 是先用
是先用 溶液吸收含
溶液吸收含 的工业废气,所得溶液用情性电极电解,阳极区所得溶液循环利用。
的工业废气,所得溶液用情性电极电解,阳极区所得溶液循环利用。
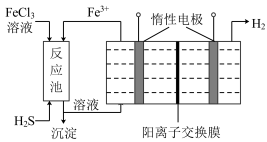
①进入电解池的溶液中,溶质是_______ (填化学式)。
②阳极的电极反应式为___________ 。
(4)工业上采用高温热分解 的方法制取
的方法制取 ,在膜反应器中分离出
,在膜反应器中分离出 。
。 下,
下, 分解:
分解: 。保持压强不变,反应达到平衡时,气体的体积分数
。保持压强不变,反应达到平衡时,气体的体积分数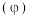 随温度的变化曲线如图:
随温度的变化曲线如图:

①在密闭容器中,关于上述反应的说法正确的是_______ (填字母)。
A. 随温度的升高而增大
随温度的升高而增大
B.低压有利于提高 的平衡分解率
的平衡分解率
C.维持温度、气体总压强不变时,向平衡体系中通入氩气,则v(正)<v(逆)
D.在恒容密闭容器中进行反应,当气体密度不再变化时,反应达到平衡状态
②图中 点:
点: 的平衡转化率为
的平衡转化率为_______ ;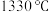 时,反应
时,反应 的
的
_______  (
( 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
 是存在于燃气中的一种有害气体,脱除
是存在于燃气中的一种有害气体,脱除 的方法有多种。回答下列问题:
的方法有多种。回答下列问题:(1)Claus氧化回收硫的反应原理为:
①

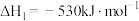 ;
;②

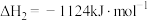 ;
;③

 。
。则

 。
。(2)化学反应的焓变与反应物和生成物的键能(气态分子中
 化学键解离成气态原子所吸收的能量)有关。已知某些化学键的键能如下表所示:
化学键解离成气态原子所吸收的能量)有关。已知某些化学键的键能如下表所示:| 共价键 |  |  |  |  |
键能 | 339 | 246 |  | 120 |

(3)电解法治理
 是先用
是先用 溶液吸收含
溶液吸收含 的工业废气,所得溶液用情性电极电解,阳极区所得溶液循环利用。
的工业废气,所得溶液用情性电极电解,阳极区所得溶液循环利用。
①进入电解池的溶液中,溶质是
②阳极的电极反应式为
(4)工业上采用高温热分解
 的方法制取
的方法制取 ,在膜反应器中分离出
,在膜反应器中分离出 。
。 下,
下, 分解:
分解: 。保持压强不变,反应达到平衡时,气体的体积分数
。保持压强不变,反应达到平衡时,气体的体积分数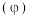 随温度的变化曲线如图:
随温度的变化曲线如图:
①在密闭容器中,关于上述反应的说法正确的是
A.
 随温度的升高而增大
随温度的升高而增大B.低压有利于提高
 的平衡分解率
的平衡分解率C.维持温度、气体总压强不变时,向平衡体系中通入氩气,则v(正)<v(逆)
D.在恒容密闭容器中进行反应,当气体密度不再变化时,反应达到平衡状态
②图中
 点:
点: 的平衡转化率为
的平衡转化率为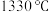 时,反应
时,反应 的
的
 (
( 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
您最近一年使用:0次
2023-12-31更新
|
79次组卷
|
3卷引用:陕西省榆林市府谷县府谷中学2023-2024学年高二下学期开学化学试题
名校
解题方法
2 . 甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、 和
和 )在催化剂作用下可合成甲醇,发生的主要反应如下:
)在催化剂作用下可合成甲醇,发生的主要反应如下:
Ⅰ.
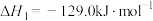 ;
;
Ⅱ.
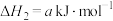 ;
;
Ⅲ.
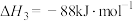 。
。
(1)
______ 。
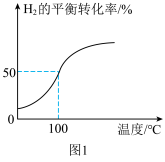
(2)将2.0 mol 和3.0mol
和3.0mol  通入容积为3L的恒容密闭容器中,在一定条件下发生反应Ⅱ,测得
通入容积为3L的恒容密闭容器中,在一定条件下发生反应Ⅱ,测得 的平衡转化率与温度的关系如图1所示。
的平衡转化率与温度的关系如图1所示。
①100℃时反应达到平衡所需的时间为5 min,则反应从起始至5 min内,用 表示该反应的平均反应速率为
表示该反应的平均反应速率为______  ;平衡后向容器中再通入3 mol Ar,平衡
;平衡后向容器中再通入3 mol Ar,平衡______ (填“正向”“逆向”或“不”)移动。
②100℃时,反应Ⅱ的平衡常数
______ 。
(3)甲醇会对水质造成一定的污染,有一种电化学法可消除这种污染,其原理如下:通电后,将 氧化成
氧化成 ,然后以
,然后以 作氧化剂,将水中的甲醇氧化成
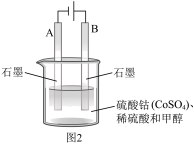
作氧化剂,将水中的甲醇氧化成 而净化。实验室用如图2装置模拟上述过程。
而净化。实验室用如图2装置模拟上述过程。
①图2中石墨A的电极名称为______ ;写出阳极的电极反应式:______ 。
②写出除去甲醇的离子方程式:______ 。
 和
和 )在催化剂作用下可合成甲醇,发生的主要反应如下:
)在催化剂作用下可合成甲醇,发生的主要反应如下:Ⅰ.

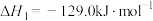 ;
;Ⅱ.

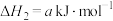 ;
;Ⅲ.

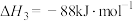 。
。(1)

(2)将2.0 mol
 和3.0mol
和3.0mol  通入容积为3L的恒容密闭容器中,在一定条件下发生反应Ⅱ,测得
通入容积为3L的恒容密闭容器中,在一定条件下发生反应Ⅱ,测得 的平衡转化率与温度的关系如图1所示。
的平衡转化率与温度的关系如图1所示。①100℃时反应达到平衡所需的时间为5 min,则反应从起始至5 min内,用
 表示该反应的平均反应速率为
表示该反应的平均反应速率为 ;平衡后向容器中再通入3 mol Ar,平衡
;平衡后向容器中再通入3 mol Ar,平衡②100℃时,反应Ⅱ的平衡常数



(3)甲醇会对水质造成一定的污染,有一种电化学法可消除这种污染,其原理如下:通电后,将
 氧化成
氧化成 ,然后以
,然后以 作氧化剂,将水中的甲醇氧化成
作氧化剂,将水中的甲醇氧化成 而净化。实验室用如图2装置模拟上述过程。
而净化。实验室用如图2装置模拟上述过程。①图2中石墨A的电极名称为
②写出除去甲醇的离子方程式:
您最近一年使用:0次
3 . 由乙烯制备环氧乙烷( )涉及反应如下:
)涉及反应如下:
Ⅰ.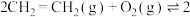 (
(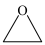 )
)
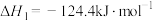
Ⅱ.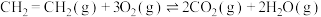

回答下列问题:
(1)反应2( )
)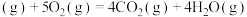

___________  。
。
(2)以Ag为催化剂制备 时,发生反应Ⅰ、反应Ⅱ,其中反应Ⅰ机理如下:
时,发生反应Ⅰ、反应Ⅱ,其中反应Ⅰ机理如下:
ⅰ.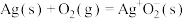 慢
慢
ⅱ.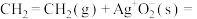 (
(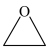 )
)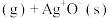 快
快
①活化能较大的是___________ (填“ⅰ”或“ⅱ”)。
②下列措施可能显著提高反应Ⅰ速率的是___________ (填字母)。
A.通入惰性气体 B.升高温度、
C.增大 浓度 D.增大
浓度 D.增大 浓度
浓度
(3)某密闭容器中由 、
、 制备
制备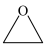 ,同时发生反应Ⅰ、反应Ⅱ,相同时间内
,同时发生反应Ⅰ、反应Ⅱ,相同时间内 的转化率和
的转化率和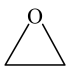 的选择性[
的选择性[ ]与温度的关系如图所示。
]与温度的关系如图所示。

①随着温度升高, 的转化率升高,其原因是
的转化率升高,其原因是___________ 。
②环氧乙烷的选择性随温度升高面下降的原因可能是___________ 。
(4)某温度下,向密闭容器中通入 和
和 仅发生反应Ⅰ,经过20min达到平衡状态,此时乙烯的转化率为50%,c(
仅发生反应Ⅰ,经过20min达到平衡状态,此时乙烯的转化率为50%,c(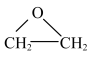 )
)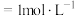 。
。
①前20min反应速率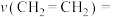
___________  。
。
②该温度下反应Ⅰ的平衡常数
___________ (保留两位有效数字)。
③能够提高 平衡产率的措施有
平衡产率的措施有___________ (写一项即可)。
 )涉及反应如下:
)涉及反应如下:Ⅰ.
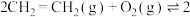 (
( )
)
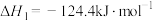
Ⅱ.
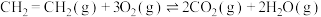

回答下列问题:
(1)反应2(
 )
)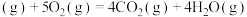

 。
。(2)以Ag为催化剂制备
 时,发生反应Ⅰ、反应Ⅱ,其中反应Ⅰ机理如下:
时,发生反应Ⅰ、反应Ⅱ,其中反应Ⅰ机理如下:ⅰ.
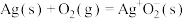 慢
慢ⅱ.
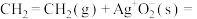 (
( )
)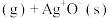 快
快①活化能较大的是
②下列措施可能显著提高反应Ⅰ速率的是
A.通入惰性气体 B.升高温度、
C.增大
 浓度 D.增大
浓度 D.增大 浓度
浓度(3)某密闭容器中由
 、
、 制备
制备 ,同时发生反应Ⅰ、反应Ⅱ,相同时间内
,同时发生反应Ⅰ、反应Ⅱ,相同时间内 的转化率和
的转化率和 的选择性[
的选择性[ ]与温度的关系如图所示。
]与温度的关系如图所示。
①随着温度升高,
 的转化率升高,其原因是
的转化率升高,其原因是②环氧乙烷的选择性随温度升高面下降的原因可能是
(4)某温度下,向密闭容器中通入
 和
和 仅发生反应Ⅰ,经过20min达到平衡状态,此时乙烯的转化率为50%,c(
仅发生反应Ⅰ,经过20min达到平衡状态,此时乙烯的转化率为50%,c( )
)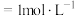 。
。①前20min反应速率
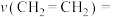
 。
。②该温度下反应Ⅰ的平衡常数

③能够提高
 平衡产率的措施有
平衡产率的措施有
您最近一年使用:0次
4 .  是一种温室气体,研究
是一种温室气体,研究 的利用对促进低碳社会构建具有重要意义,我国科学家利用
的利用对促进低碳社会构建具有重要意义,我国科学家利用 作为催化剂,实现了
作为催化剂,实现了 加氢制
加氢制 .
.
主反应为:Ⅰ.

同时伴随发生副反应:Ⅱ.

(1)已知
 ,则
,则
______  .
.
(2)一定温度下,向某容器中充入2mol 和6mol
和6mol ,假设只发生上述反应Ⅰ,一段时间后达到平衡.
,假设只发生上述反应Ⅰ,一段时间后达到平衡.
①关于上述反应体系的分析,下列说法正确的是______ .
A.当 时,反应达到平衡状态
时,反应达到平衡状态
B.恒温恒压下,当混合气体的密度恒定时,反应达到平衡状态
C.保持容器的容积不变,向体系中充入氩气,平衡不移动
D.改加高效催化剂,可以提高 的平衡转化率
的平衡转化率
②恒容条件下,测得反应过程中 和
和 的物质的量浓度随时间的变化如图所示,该温度下的平衡常数
的物质的量浓度随时间的变化如图所示,该温度下的平衡常数
______ (保留小数点后两位).

(3)在恒温恒容的密闭容器中,加入一定量的 和足量的
和足量的 ,同时发生主、副反应.体系中
,同时发生主、副反应.体系中 的选择性(指转化为
的选择性(指转化为 的
的 占发生反应的
占发生反应的 的百分比)随温度、压强的变化曲线如图所示:
的百分比)随温度、压强的变化曲线如图所示:
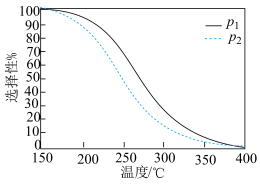
①
______ 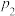 (填“>”或“=”或“<”).
(填“>”或“=”或“<”).
② 的选择性随温度升高而降低的原因可能是
的选择性随温度升高而降低的原因可能是______ .
③科学家研究了用电解法把 转化为
转化为 ,从而消除
,从而消除 对环境的影响,其原理如图所示:
对环境的影响,其原理如图所示:

则图中A电极接电源______ 极.已知B电极为惰性电极,则在水溶液中,该极的电极反应式为______ .
 是一种温室气体,研究
是一种温室气体,研究 的利用对促进低碳社会构建具有重要意义,我国科学家利用
的利用对促进低碳社会构建具有重要意义,我国科学家利用 作为催化剂,实现了
作为催化剂,实现了 加氢制
加氢制 .
.主反应为:Ⅰ.


同时伴随发生副反应:Ⅱ.


(1)已知

 ,则
,则
 .
.(2)一定温度下,向某容器中充入2mol
 和6mol
和6mol ,假设只发生上述反应Ⅰ,一段时间后达到平衡.
,假设只发生上述反应Ⅰ,一段时间后达到平衡.①关于上述反应体系的分析,下列说法正确的是
A.当
 时,反应达到平衡状态
时,反应达到平衡状态B.恒温恒压下,当混合气体的密度恒定时,反应达到平衡状态
C.保持容器的容积不变,向体系中充入氩气,平衡不移动
D.改加高效催化剂,可以提高
 的平衡转化率
的平衡转化率②恒容条件下,测得反应过程中
 和
和 的物质的量浓度随时间的变化如图所示,该温度下的平衡常数
的物质的量浓度随时间的变化如图所示,该温度下的平衡常数

(3)在恒温恒容的密闭容器中,加入一定量的
 和足量的
和足量的 ,同时发生主、副反应.体系中
,同时发生主、副反应.体系中 的选择性(指转化为
的选择性(指转化为 的
的 占发生反应的
占发生反应的 的百分比)随温度、压强的变化曲线如图所示:
的百分比)随温度、压强的变化曲线如图所示:
①

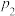 (填“>”或“=”或“<”).
(填“>”或“=”或“<”).②
 的选择性随温度升高而降低的原因可能是
的选择性随温度升高而降低的原因可能是③科学家研究了用电解法把
 转化为
转化为 ,从而消除
,从而消除 对环境的影响,其原理如图所示:
对环境的影响,其原理如图所示:
则图中A电极接电源
您最近一年使用:0次
2023-12-21更新
|
305次组卷
|
3卷引用:陕西省汉中市2023-2024学年高三上学期第一次质量检测化学试题
名校
5 . 甲烷化反应即为氢气和碳氧化物反应生成甲烷,有利于实现碳循环利用.
已知涉及的反应如下:
反应Ⅰ: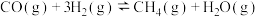

反应Ⅱ:

反应Ⅲ:

回答下列问题:
(1)
______ 
(2)在 时,在固定容积的密闭容器中进行上述反应,平衡时
时,在固定容积的密闭容器中进行上述反应,平衡时 和
和 的转化率及
的转化率及 和
和 的产率随
的产率随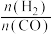 变化的情况如图1所示.
变化的情况如图1所示.

图中表示 转化率、
转化率、 产率变化的曲线分别是
产率变化的曲线分别是______ 、______ (填标号), 、
、 两点
两点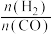 的值相同,
的值相同, 点通过改变温度达到
点通过改变温度达到 点,则
点,则 、
、 、
、 三点温度由大到小的顺序是
三点温度由大到小的顺序是______ 。
②一定温度下,向恒容容器内充入 和
和 ,初始压强为
,初始压强为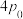 ,发生上述3个反应,达到平衡时
,发生上述3个反应,达到平衡时 的分压为
的分压为 ,
, 的分压为
的分压为 ,则
,则 的选择性=
的选择性=______ [ 的选择性
的选择性 用
用 ,
, ,
, 表示,下同],反应Ⅱ的
表示,下同],反应Ⅱ的
______ (用分压表示,分压=总压×物质的量分数)。
(3)已知常温下, 的溶度积常数为
的溶度积常数为 ,
, 的二级电离常数为
的二级电离常数为 。
。 溶于水除了沉淀溶解平衡,还存在碳酸根的水解(忽略二级水解).则常温下,
溶于水除了沉淀溶解平衡,还存在碳酸根的水解(忽略二级水解).则常温下, 的实际溶解度比理论值
的实际溶解度比理论值______ (填“大”或者“小”).若溶液 已知,则钙离子的实际浓度为
已知,则钙离子的实际浓度为______  [用含
[用含 ,
, ,
, 的式子表达]。
的式子表达]。
(4)用电解法可将 转化为多种原料,原理如图.若铜电极上只产生
转化为多种原料,原理如图.若铜电极上只产生 和
和 气体,请写出产生
气体,请写出产生 的电极反应式
的电极反应式__________________ ;电解后溶液的
______ (填“变大”、“变小”或“不变”).

已知涉及的反应如下:
反应Ⅰ:
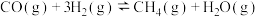

反应Ⅱ:


反应Ⅲ:


回答下列问题:
(1)


(2)在
 时,在固定容积的密闭容器中进行上述反应,平衡时
时,在固定容积的密闭容器中进行上述反应,平衡时 和
和 的转化率及
的转化率及 和
和 的产率随
的产率随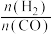 变化的情况如图1所示.
变化的情况如图1所示.
图中表示
 转化率、
转化率、 产率变化的曲线分别是
产率变化的曲线分别是 、
、 两点
两点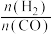 的值相同,
的值相同, 点通过改变温度达到
点通过改变温度达到 点,则
点,则 、
、 、
、 三点温度由大到小的顺序是
三点温度由大到小的顺序是②一定温度下,向恒容容器内充入
 和
和 ,初始压强为
,初始压强为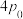 ,发生上述3个反应,达到平衡时
,发生上述3个反应,达到平衡时 的分压为
的分压为 ,
, 的分压为
的分压为 ,则
,则 的选择性=
的选择性= 的选择性
的选择性 用
用 ,
, ,
, 表示,下同],反应Ⅱ的
表示,下同],反应Ⅱ的
(3)已知常温下,
 的溶度积常数为
的溶度积常数为 ,
, 的二级电离常数为
的二级电离常数为 。
。 溶于水除了沉淀溶解平衡,还存在碳酸根的水解(忽略二级水解).则常温下,
溶于水除了沉淀溶解平衡,还存在碳酸根的水解(忽略二级水解).则常温下, 的实际溶解度比理论值
的实际溶解度比理论值 已知,则钙离子的实际浓度为
已知,则钙离子的实际浓度为 [用含
[用含 ,
, ,
, 的式子表达]。
的式子表达]。(4)用电解法可将
 转化为多种原料,原理如图.若铜电极上只产生
转化为多种原料,原理如图.若铜电极上只产生 和
和 气体,请写出产生
气体,请写出产生 的电极反应式
的电极反应式

您最近一年使用:0次
名校
6 . CO2的资源化可以推动经济高质量发展和生态环境质量的持续改善,回答下列问题:
(1) CO2和乙烷反应制备乙烯。常温常压时,相关物质的相对能量如图所示: 的
的 计算如下:
计算如下: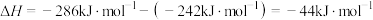
则CO2和乙烷反应生成乙烯、CO和液态水的热化学方程式为___________ 。
(2) CO2和 反应制备
反应制备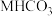 ,某学习兴趣小组为了研究该反应,将足量的某碳酸氢盐
,某学习兴趣小组为了研究该反应,将足量的某碳酸氢盐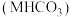 固体置于真空恒容密闭容器中,发生如下反应:
固体置于真空恒容密闭容器中,发生如下反应: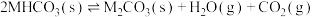 。反应达平衡时体系的总压为
。反应达平衡时体系的总压为 ,保持温度不变,开始时在体系中先通入一定量的
,保持温度不变,开始时在体系中先通入一定量的 ,再加入足量
,再加入足量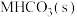 ,欲使平衡时体系中水蒸气的分压小于
,欲使平衡时体系中水蒸气的分压小于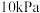 ,则
,则 的初始压强应大于
的初始压强应大于________  。
。
(3) 和
和 制备甲醇,反应体系中涉及以下两个反应:
制备甲醇,反应体系中涉及以下两个反应:
I.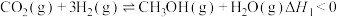
Ⅱ.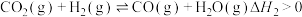
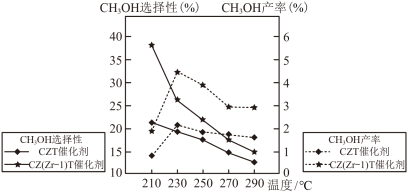
将CO2和H+按物质的量之比1∶3混合通入刚性密闭容器中,在催化剂作用下发生反应I和反应Ⅱ,在相同的时间内CH3OH的选择性和产率随温度的变化如图所示。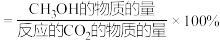
①在上述条件下合成甲醇的工业条件是___________ (填标号)。
A.210℃ B.230℃ C.催化CZT D.催化剂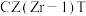
② 以上,升高温度导致CO2的转化率增大,甲醇的产率降低。可能的原因是
以上,升高温度导致CO2的转化率增大,甲醇的产率降低。可能的原因是___________ 。
③ 时,容器内压强随时间的变化如下表所示:
时,容器内压强随时间的变化如下表所示:
反应I的速率可表示为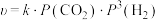 (k为常数),平衡时
(k为常数),平衡时 ,则反应在
,则反应在 时
时
___________ (用含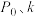 的式子表示)。达平衡时
的式子表示)。达平衡时 的选择性=
的选择性=___________ ,反应Ⅱ的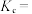
___________ 。
(1) CO2和乙烷反应制备乙烯。常温常压时,相关物质的相对能量如图所示:
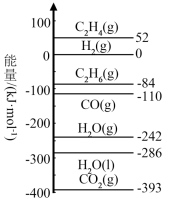
 的
的 计算如下:
计算如下: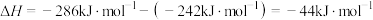
则CO2和乙烷反应生成乙烯、CO和液态水的热化学方程式为
(2) CO2和
 反应制备
反应制备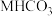 ,某学习兴趣小组为了研究该反应,将足量的某碳酸氢盐
,某学习兴趣小组为了研究该反应,将足量的某碳酸氢盐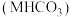 固体置于真空恒容密闭容器中,发生如下反应:
固体置于真空恒容密闭容器中,发生如下反应: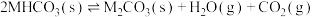 。反应达平衡时体系的总压为
。反应达平衡时体系的总压为 ,保持温度不变,开始时在体系中先通入一定量的
,保持温度不变,开始时在体系中先通入一定量的 ,再加入足量
,再加入足量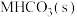 ,欲使平衡时体系中水蒸气的分压小于
,欲使平衡时体系中水蒸气的分压小于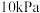 ,则
,则 的初始压强应大于
的初始压强应大于 。
。(3)
 和
和 制备甲醇,反应体系中涉及以下两个反应:
制备甲醇,反应体系中涉及以下两个反应:I.
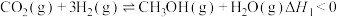
Ⅱ.
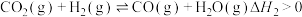
将CO2和H+按物质的量之比1∶3混合通入刚性密闭容器中,在催化剂作用下发生反应I和反应Ⅱ,在相同的时间内CH3OH的选择性和产率随温度的变化如图所示。
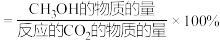
①在上述条件下合成甲醇的工业条件是
A.210℃ B.230℃ C.催化CZT D.催化剂
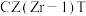
②
 以上,升高温度导致CO2的转化率增大,甲醇的产率降低。可能的原因是
以上,升高温度导致CO2的转化率增大,甲醇的产率降低。可能的原因是③
 时,容器内压强随时间的变化如下表所示:
时,容器内压强随时间的变化如下表所示:时间 | 0 | 20 | 40 | 60 | 80 |
压强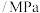 |  | 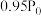 | 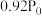 |  |  |
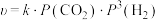 (k为常数),平衡时
(k为常数),平衡时 ,则反应在
,则反应在 时
时
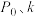 的式子表示)。达平衡时
的式子表示)。达平衡时 的选择性=
的选择性=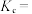
您最近一年使用:0次
2023-12-19更新
|
301次组卷
|
7卷引用:2024届陕西省西安市第一中学高三上学期模拟测试理科综合试题-高中化学
2024届陕西省西安市第一中学高三上学期模拟测试理科综合试题-高中化学安徽省黄山市2022届高三第二次质量检测理科综合化学试题(已下线)专项16 化学反应原理综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)化学(山东A卷)-学易金卷:2023年高考第一次模拟考试卷山东省实验中学2022-2023学年高三下学期开学考试化学试题 山东省济宁市第一中学2023-2024学年高三上学期12月月考化学试题(已下线)江苏省南通市如皋中学2024届高三下学期第三次适应性考试化学试题
7 . 四氯化钛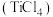 是生产金属钛及其化合物的重要中间体,工业上以高钛渣(主要成分为
是生产金属钛及其化合物的重要中间体,工业上以高钛渣(主要成分为 )为原料生产
)为原料生产 的化学反应原理为
的化学反应原理为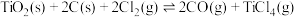

 。请回答下列问题:
。请回答下列问题:
(1)已知: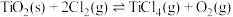
 、C(s)的燃烧热
、C(s)的燃烧热 为
为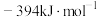 ,则CO的燃烧热
,则CO的燃烧热 为
为______  。
。
(2)T℃时,将足量的 、C加入某恒容密闭容器中,并通入一定量的
、C加入某恒容密闭容器中,并通入一定量的 和
和 (
( 不参与反应)只发生反应:
不参与反应)只发生反应: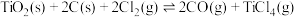 ,测得容器内总压强(
,测得容器内总压强(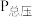 )和
)和 的转化率(
的转化率( )随时间的变化关系如图所示:
)随时间的变化关系如图所示:
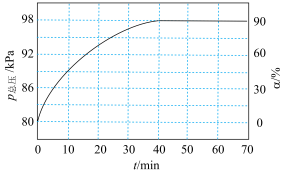
①T℃时,反应的平衡常数
______ kPa( 为以各组分的平衡分压表示的平衡常数,分压=总压×物质的量分数)。
为以各组分的平衡分压表示的平衡常数,分压=总压×物质的量分数)。
②保持温度和起始总压相同,若向恒容密闭容器中通入的 中不含氮气,与含有氮气相比,
中不含氮气,与含有氮气相比, 的平衡转化率
的平衡转化率
______ (填“增大”“减小”或“不变”),其原因为____________ 。
(3)利用 先制得
先制得 ,焙烧
,焙烧 可获得纳米
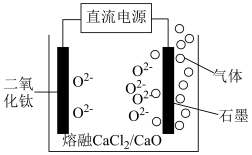
可获得纳米 。用电解法生产钛的原理如图所示。电解过程中,被还原的Ca进一步还原
。用电解法生产钛的原理如图所示。电解过程中,被还原的Ca进一步还原 得到钛,用化学用语表示制钛过程:
得到钛,用化学用语表示制钛过程:______ 、____________ ;石墨电极需要定期更换的原因为______ 。
 是生产金属钛及其化合物的重要中间体,工业上以高钛渣(主要成分为
是生产金属钛及其化合物的重要中间体,工业上以高钛渣(主要成分为 )为原料生产
)为原料生产 的化学反应原理为
的化学反应原理为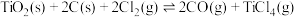

 。请回答下列问题:
。请回答下列问题:(1)已知:
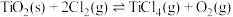
 、C(s)的燃烧热
、C(s)的燃烧热 为
为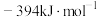 ,则CO的燃烧热
,则CO的燃烧热 为
为 。
。(2)T℃时,将足量的
 、C加入某恒容密闭容器中,并通入一定量的
、C加入某恒容密闭容器中,并通入一定量的 和
和 (
( 不参与反应)只发生反应:
不参与反应)只发生反应: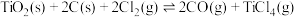 ,测得容器内总压强(
,测得容器内总压强(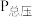 )和
)和 的转化率(
的转化率( )随时间的变化关系如图所示:
)随时间的变化关系如图所示:
①T℃时,反应的平衡常数

 为以各组分的平衡分压表示的平衡常数,分压=总压×物质的量分数)。
为以各组分的平衡分压表示的平衡常数,分压=总压×物质的量分数)。②保持温度和起始总压相同,若向恒容密闭容器中通入的
 中不含氮气,与含有氮气相比,
中不含氮气,与含有氮气相比, 的平衡转化率
的平衡转化率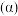
(3)利用
 先制得
先制得 ,焙烧
,焙烧 可获得纳米
可获得纳米 。用电解法生产钛的原理如图所示。电解过程中,被还原的Ca进一步还原
。用电解法生产钛的原理如图所示。电解过程中,被还原的Ca进一步还原 得到钛,用化学用语表示制钛过程:
得到钛,用化学用语表示制钛过程:
您最近一年使用:0次
2023-12-13更新
|
249次组卷
|
3卷引用:陕西省安康市高新中学2023-2024学年高三上学期阶段性测试四化学试题
8 . 一定条件下, 在某密闭容器中发生的反应有:
在某密闭容器中发生的反应有:
反应I.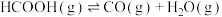


反应Ⅱ.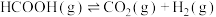

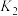
回答下列问题:
(1)对于反应

 ,
,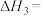
___________ (用含 、
、 的式子表示),
的式子表示),
___________ (用含 、
、 的式子表示)。
的式子表示)。
(2)常温下,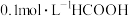 (甲酸)溶液中[已知:
(甲酸)溶液中[已知: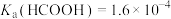 ]:
]:
①HCOOH的电离方程式为___________ 。
②该溶液中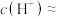
___________  。
。
③此温度下,若将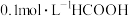 溶液加水稀释至
溶液加水稀释至 ,此时
,此时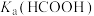
___________ (填“变大”、“变小”或“不变”,下同),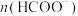
___________ 。
(3)某温度下,往某一恒容密闭容器中通入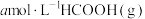 ,仅发生反应I和反应Ⅱ,
,仅发生反应I和反应Ⅱ, 后反应达到平衡,此时测得CO、HCOOH的浓度分别为
后反应达到平衡,此时测得CO、HCOOH的浓度分别为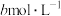 、
、 (不考虑碳元素的其他存在形式,
(不考虑碳元素的其他存在形式,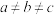 )。则
)。则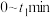 内
内
___________  (用含a、b、c的式子表示,下同),
(用含a、b、c的式子表示,下同), 的物质的量分数为
的物质的量分数为___________ ,反应Ⅱ的平衡常数为___________ 。
 在某密闭容器中发生的反应有:
在某密闭容器中发生的反应有:反应I.
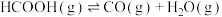


反应Ⅱ.
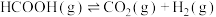

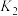
回答下列问题:
(1)对于反应


 ,
,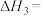
 、
、 的式子表示),
的式子表示),
 、
、 的式子表示)。
的式子表示)。(2)常温下,
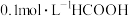 (甲酸)溶液中[已知:
(甲酸)溶液中[已知: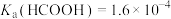 ]:
]:①HCOOH的电离方程式为
②该溶液中
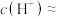
 。
。③此温度下,若将
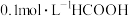 溶液加水稀释至
溶液加水稀释至 ,此时
,此时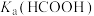
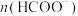
(3)某温度下,往某一恒容密闭容器中通入
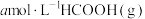 ,仅发生反应I和反应Ⅱ,
,仅发生反应I和反应Ⅱ, 后反应达到平衡,此时测得CO、HCOOH的浓度分别为
后反应达到平衡,此时测得CO、HCOOH的浓度分别为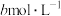 、
、 (不考虑碳元素的其他存在形式,
(不考虑碳元素的其他存在形式,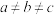 )。则
)。则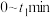 内
内
 (用含a、b、c的式子表示,下同),
(用含a、b、c的式子表示,下同), 的物质的量分数为
的物质的量分数为
您最近一年使用:0次
2023-12-05更新
|
131次组卷
|
2卷引用:陕西省西安市莲湖区2023-2024学年高二上学期期中联考化学试题
9 . 研究 、
、 、CO等气体的无害化处理对治理大气污染、建设生态文明具有重要意义。已知:
、CO等气体的无害化处理对治理大气污染、建设生态文明具有重要意义。已知:
反应I.
 ;
;
反应Ⅱ.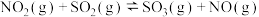
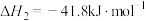 。
。
(1)则反应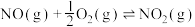

___________  ;该反应的平衡常数表达式为
;该反应的平衡常数表达式为___________ 。
(2)在某一恒容密闭容器中,通入一定量的 和
和 ,仅发生反应
,仅发生反应 :
:
①下列能说明该反应达到平衡状态的是___________ (填标号)。
A.当混合气体的密度不再随时间变化而改变时,该反应达到平衡
B.当混合气体的平均相对分子质量不再随时间变化而改变时,该反应达到平衡
C.当 不再随时间变化而改变时,该反应达到平衡
不再随时间变化而改变时,该反应达到平衡
D.当 的质量分数不再随时间变化而改变时,该反应达到平衡
的质量分数不再随时间变化而改变时,该反应达到平衡
②既能加快反应 的反应速率,又能提高
的反应速率,又能提高 的平衡转化率,可采取的措施有
的平衡转化率,可采取的措施有___________ (填标号)。
A.使用合适的催化剂 B.通入适量的
C.及时抽走部分NO D.升高温度
(3) 下,在2L的恒容密闭容器中,充入
下,在2L的恒容密闭容器中,充入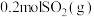 和
和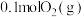 ,仅发生反应
,仅发生反应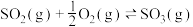 ,tmin时,该反应达到平衡,此时测得容器中混合气体的压强为起始时混合气体压强的80%:
,tmin时,该反应达到平衡,此时测得容器中混合气体的压强为起始时混合气体压强的80%:
①___________ (填“低温”、“高温”或“任意温度”)下,有利于该反应自发进行。
②保持其他条件不变,仅改变温度, ,仅发生该反应,反应达到平衡时,该反应的平衡常数
,仅发生该反应,反应达到平衡时,该反应的平衡常数 ,则
,则
___________ (填“>”或“<”) 。
。
③该反应达到平衡后,保持其他条件不变,仅再通入 、
、 和
和 ,则此时
,则此时
________ (填“>”、“<”或“=”) ,判断的理由为
,判断的理由为_________ 。
 、
、 、CO等气体的无害化处理对治理大气污染、建设生态文明具有重要意义。已知:
、CO等气体的无害化处理对治理大气污染、建设生态文明具有重要意义。已知:反应I.

 ;
;反应Ⅱ.
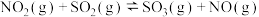
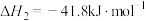 。
。(1)则反应
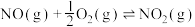

 ;该反应的平衡常数表达式为
;该反应的平衡常数表达式为(2)在某一恒容密闭容器中,通入一定量的
 和
和 ,仅发生反应
,仅发生反应 :
:①下列能说明该反应达到平衡状态的是
A.当混合气体的密度不再随时间变化而改变时,该反应达到平衡
B.当混合气体的平均相对分子质量不再随时间变化而改变时,该反应达到平衡
C.当
 不再随时间变化而改变时,该反应达到平衡
不再随时间变化而改变时,该反应达到平衡D.当
 的质量分数不再随时间变化而改变时,该反应达到平衡
的质量分数不再随时间变化而改变时,该反应达到平衡②既能加快反应
 的反应速率,又能提高
的反应速率,又能提高 的平衡转化率,可采取的措施有
的平衡转化率,可采取的措施有A.使用合适的催化剂 B.通入适量的

C.及时抽走部分NO D.升高温度
(3)
 下,在2L的恒容密闭容器中,充入
下,在2L的恒容密闭容器中,充入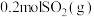 和
和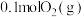 ,仅发生反应
,仅发生反应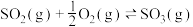 ,tmin时,该反应达到平衡,此时测得容器中混合气体的压强为起始时混合气体压强的80%:
,tmin时,该反应达到平衡,此时测得容器中混合气体的压强为起始时混合气体压强的80%:①
②保持其他条件不变,仅改变温度,
 ,仅发生该反应,反应达到平衡时,该反应的平衡常数
,仅发生该反应,反应达到平衡时,该反应的平衡常数 ,则
,则
 。
。③该反应达到平衡后,保持其他条件不变,仅再通入
 、
、 和
和 ,则此时
,则此时
 ,判断的理由为
,判断的理由为
您最近一年使用:0次
名校
解题方法
10 . 温室气体让地球发烧,倡导低碳生活,是一种可持续发展的环保责任,将 应用于生产中实现其综合利用是目前的研究热点。
应用于生产中实现其综合利用是目前的研究热点。
Ⅰ.在催化作用下由 和
和 转化为
转化为 的反应历程示意图如图。
的反应历程示意图如图。
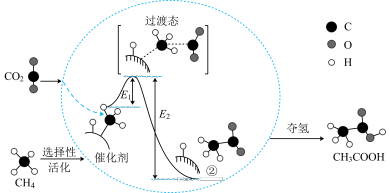
(1)在合成 的反应历程中,下列有关说法正确的是___________(填字母)。
的反应历程中,下列有关说法正确的是___________(填字母)。
Ⅱ.以 、
、 为原料制备“21世纪的清洁燃料”二甲醚(
为原料制备“21世纪的清洁燃料”二甲醚( )涉及的主要反应如下:
)涉及的主要反应如下:
①
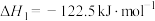
②
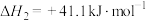
(2)反应 的
的
___________ 。
(3)在压强、 和
和 的起始投料一定的条件下,发生反应①、②,实验测得
的起始投料一定的条件下,发生反应①、②,实验测得 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图所示。
的选择性随温度的变化如图所示。
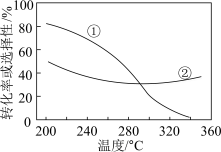
已知: ,其中表示平衡时
,其中表示平衡时 的选择性的是曲线
的选择性的是曲线___________ (填“①”或“②”);温度高于300℃时,曲线②随温度升高而升高的原因是______________________ ;为同时提高 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性,应选择的反应条件为
的选择性,应选择的反应条件为___________ (填字母)。
a.低温、低压 b.高温、高压 c.高温、低压 d.低温、高压
Ⅲ.以CO2、C2H6为原料合成的主要反应为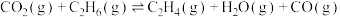
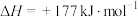 。
。
(4)某温度下,在0.1MPa恒压密闭容器中充入等物质的量的 和
和 ,达到平衡时
,达到平衡时 的物质的量分数为20%,该温度下反应的平衡常数
的物质的量分数为20%,该温度下反应的平衡常数
___________ MPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 应用于生产中实现其综合利用是目前的研究热点。
应用于生产中实现其综合利用是目前的研究热点。Ⅰ.在催化作用下由
 和
和 转化为
转化为 的反应历程示意图如图。
的反应历程示意图如图。
(1)在合成
 的反应历程中,下列有关说法正确的是___________(填字母)。
的反应历程中,下列有关说法正确的是___________(填字母)。| A.该催化剂使反应的平衡常数增大 |
B. → → 过程中,有C-H断裂和C-C形成 过程中,有C-H断裂和C-C形成 |
| C.生成乙酸的反应原子利用率为100% |
D.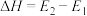 |
Ⅱ.以
 、
、 为原料制备“21世纪的清洁燃料”二甲醚(
为原料制备“21世纪的清洁燃料”二甲醚( )涉及的主要反应如下:
)涉及的主要反应如下:①

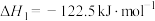
②

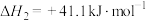
(2)反应
 的
的
(3)在压强、
 和
和 的起始投料一定的条件下,发生反应①、②,实验测得
的起始投料一定的条件下,发生反应①、②,实验测得 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图所示。
的选择性随温度的变化如图所示。
已知:
 ,其中表示平衡时
,其中表示平衡时 的选择性的是曲线
的选择性的是曲线 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性,应选择的反应条件为
的选择性,应选择的反应条件为a.低温、低压 b.高温、高压 c.高温、低压 d.低温、高压
Ⅲ.以CO2、C2H6为原料合成的主要反应为
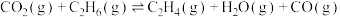
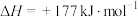 。
。(4)某温度下,在0.1MPa恒压密闭容器中充入等物质的量的
 和
和 ,达到平衡时
,达到平衡时 的物质的量分数为20%,该温度下反应的平衡常数
的物质的量分数为20%,该温度下反应的平衡常数
您最近一年使用:0次



