1 . 还原法处理氮的氧化物是环境科学研究的热点课题
(1)汽车尾气中CO、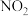 在一定条件下可以发生反应:
在一定条件下可以发生反应: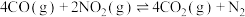
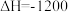
 。在一定温度下,向容积固定为2 L的密闭容器中充入1.2 mol CO和一定量的
。在一定温度下,向容积固定为2 L的密闭容器中充入1.2 mol CO和一定量的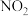 ,
,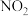 的物质的量随时间的变化曲线如图所示。
的物质的量随时间的变化曲线如图所示。
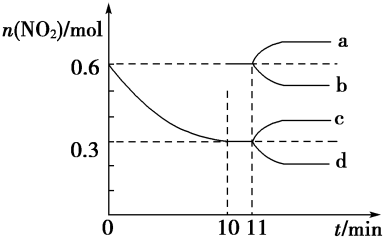
①恒温恒容条件下,不能说明该反应已达到平衡状态的是_______ (填标号)。
A.容器内混合气体颜色不再变化 B.
C.容器内的压强保持不变 D.容器内混合气体密度保持不变
②0~10 min内该反应的平均速率
_______ ,从11 min起其他条件不变,压缩容器的容积变为1 L,则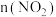 的变化曲线可能为图中的
的变化曲线可能为图中的_______ (填字母)。
③对于该反应,温度不同( )、其他条件相同时,下列图象表示正确的是
)、其他条件相同时,下列图象表示正确的是_______ (填序号)。
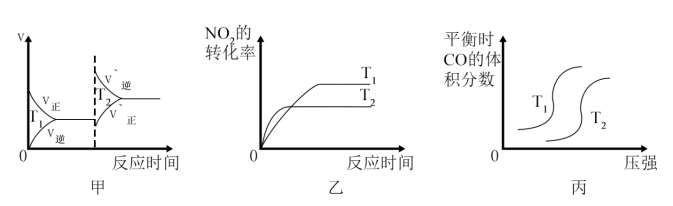
(2)碳单质可应用于脱硝。向容积为2 L的密闭容器中加入炭(足量)和2.0 mol NO,模拟发生脱硝反应: ,测得不同温度下,NO的物质的量随时间的变化如下图所示。
,测得不同温度下,NO的物质的量随时间的变化如下图所示。

① 温度时,若起始向容器中充入
温度时,若起始向容器中充入 (g)和
(g)和 (g)各1 mol,平衡时,NO的体积分数为
(g)各1 mol,平衡时,NO的体积分数为_______ 。
② 温度时该反应的平衡常数为
温度时该反应的平衡常数为_______ 。
③ 温度下,向平衡后的容器内再加入2 mol
温度下,向平衡后的容器内再加入2 mol  和2 mol NO,则平衡
和2 mol NO,则平衡_______ (填“向右移动”“向左移动”或“不移动”)。
(1)汽车尾气中CO、
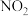 在一定条件下可以发生反应:
在一定条件下可以发生反应: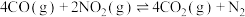
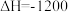
 。在一定温度下,向容积固定为2 L的密闭容器中充入1.2 mol CO和一定量的
。在一定温度下,向容积固定为2 L的密闭容器中充入1.2 mol CO和一定量的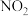 ,
,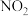 的物质的量随时间的变化曲线如图所示。
的物质的量随时间的变化曲线如图所示。
①恒温恒容条件下,不能说明该反应已达到平衡状态的是
A.容器内混合气体颜色不再变化 B.

C.容器内的压强保持不变 D.容器内混合气体密度保持不变
②0~10 min内该反应的平均速率

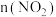 的变化曲线可能为图中的
的变化曲线可能为图中的③对于该反应,温度不同(
 )、其他条件相同时,下列图象表示正确的是
)、其他条件相同时,下列图象表示正确的是
(2)碳单质可应用于脱硝。向容积为2 L的密闭容器中加入炭(足量)和2.0 mol NO,模拟发生脱硝反应:
 ,测得不同温度下,NO的物质的量随时间的变化如下图所示。
,测得不同温度下,NO的物质的量随时间的变化如下图所示。
①
 温度时,若起始向容器中充入
温度时,若起始向容器中充入 (g)和
(g)和 (g)各1 mol,平衡时,NO的体积分数为
(g)各1 mol,平衡时,NO的体积分数为②
 温度时该反应的平衡常数为
温度时该反应的平衡常数为③
 温度下,向平衡后的容器内再加入2 mol
温度下,向平衡后的容器内再加入2 mol  和2 mol NO,则平衡
和2 mol NO,则平衡
您最近一年使用:0次
名校
2 .  资源化在推进能源绿色转型,实现“碳达峰、碳中和”中具有重要意义。
资源化在推进能源绿色转型,实现“碳达峰、碳中和”中具有重要意义。
Ⅰ. 与
与 催化重整制合成气是研究热点之一、发生的主要反应有:
催化重整制合成气是研究热点之一、发生的主要反应有:
反应①:
反应②: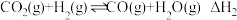
(1)有关化学键键能数据如表:
则反应②的反应热
_______  。
。
(2)对于上述反位体系,下列说法错误的是_______ 。
A.增大 的浓度,反应①②的正反应速率均增加
的浓度,反应①②的正反应速率均增加
B.恒容密闭容器中当气体密度不变时,反应达到平衡状态
C.加入催化剂,可提高 的平衡转化率
的平衡转化率
(3)恒压下进行 与
与 催化重整实验。初始压强为
催化重整实验。初始压强为 ,起始投料
,起始投料 ,
, 和
和 的平衡转化率随温度变化曲线如图所示。
的平衡转化率随温度变化曲线如图所示。
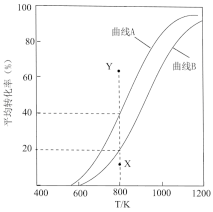
①曲线_______ (填“A”或“B”)表示 的平衡转化率。
的平衡转化率。
②800K,反应至 转化率达到X点时,v(正)
转化率达到X点时,v(正)_______ v(逆)(填“>”、“<”或“=”)。若要使 的转化率由X点达到Y点,改变的外界条件可以是
的转化率由X点达到Y点,改变的外界条件可以是_______ (答一条即可)。
③800K,反应①的分压平衡常数
_______ (分压=总压×物质的量分数)。
Ⅱ.利用电化学装置可实现 和
和 两种分子的耦合转化,其原理如图所示。
两种分子的耦合转化,其原理如图所示。
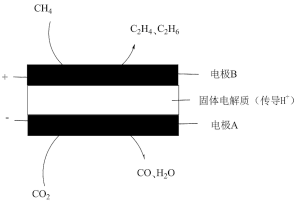
(4)阴极的电极反应式为_______ 。
 资源化在推进能源绿色转型,实现“碳达峰、碳中和”中具有重要意义。
资源化在推进能源绿色转型,实现“碳达峰、碳中和”中具有重要意义。Ⅰ.
 与
与 催化重整制合成气是研究热点之一、发生的主要反应有:
催化重整制合成气是研究热点之一、发生的主要反应有:反应①:

反应②:
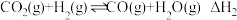
(1)有关化学键键能数据如表:
| 化学键 |  | H-O | C=O |  |
键能/ | 436 | 463 | 803 | 1076 |

 。
。(2)对于上述反位体系,下列说法错误的是
A.增大
 的浓度,反应①②的正反应速率均增加
的浓度,反应①②的正反应速率均增加B.恒容密闭容器中当气体密度不变时,反应达到平衡状态
C.加入催化剂,可提高
 的平衡转化率
的平衡转化率(3)恒压下进行
 与
与 催化重整实验。初始压强为
催化重整实验。初始压强为 ,起始投料
,起始投料 ,
, 和
和 的平衡转化率随温度变化曲线如图所示。
的平衡转化率随温度变化曲线如图所示。
①曲线
 的平衡转化率。
的平衡转化率。②800K,反应至
 转化率达到X点时,v(正)
转化率达到X点时,v(正) 的转化率由X点达到Y点,改变的外界条件可以是
的转化率由X点达到Y点,改变的外界条件可以是③800K,反应①的分压平衡常数

Ⅱ.利用电化学装置可实现
 和
和 两种分子的耦合转化,其原理如图所示。
两种分子的耦合转化,其原理如图所示。
(4)阴极的电极反应式为
您最近一年使用:0次
2022-01-24更新
|
593次组卷
|
4卷引用:安徽省合肥市2022届高三上学期第一次教学质量检测化学试题
安徽省合肥市2022届高三上学期第一次教学质量检测化学试题(已下线)专项16 化学反应原理综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)甘肃省武威第六中学2022届高三下学期第八次诊断考试理综化学试题四川省成都艺术高级中学2021-2022学年高三下学期模拟考试理科综合化学部分试题(三)
名校
3 . 下列事实不能用勒夏特列原理解释的是
| A.打开可乐瓶盖后看到有大量气泡逸出 |
| B.H2、I2、HI三者的平衡混合气,加压(缩小容器体积)后颜色变深 |
| C.新制的氯水在光照条件下颜色变浅,溶液的pH减小 |
| D.实验室可用向浓氨水中加入一定量的氢氧化钠固体来快速制取氨气 |
您最近一年使用:0次
2022-01-23更新
|
392次组卷
|
3卷引用:安徽省合肥市肥东县综合高中2021-2022学年高二下学期5月月考化学试题
4 . 《天工开物》中记载:“象牙色,栌木煎水薄染;金黄色,栌木煎水染,复用麻蒿灰淋,碱水漂”。下列说法错误的是
| A.该染色过程伴随化学变化 | B.记载中颜色的变化说明发生了化学平衡的移动 |
| C.麻蒿灰中含有碳酸钾,水溶液显碱性 | D.植物染料色素(栌木中的黄木素)难溶于水 |
您最近一年使用:0次
2022-01-20更新
|
255次组卷
|
3卷引用:安徽省部分省示范高中2021~2022学年高二上学期期末联考化学试题
安徽省部分省示范高中2021~2022学年高二上学期期末联考化学试题(已下线)卷01 化学与STSE-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)河南省三门峡市2022-2023学年高二上学期期末考试化学试题
5 . 下列实验操作、现象和结论均正确的是
| 选项 | 操作 | 现象 | 结论或解释 |
| A | 取一支试管装入2mL2mol/LNaOH溶液,先滴加1mL1mol/LMgCl2溶液,再滴几滴1mol/LCuCl2溶液 | 先生成白色沉淀,后沉淀变为蓝色 | Ksp[Cu(OH)2]<Ksp[Mg(OH)2] |
| B | 在FeCl3+3KSCN⇌Fe(SCN)3+3KCl平衡体系中加入KCl固体 | 溶液颜色变浅 | 加入生成物该化学平衡向逆反应方向移动 |
| C | 常温下,用pH计测定1mol/LCH3COONH4溶液 | 测得pH=7 | CH3COONH4溶液对水的电离程度无影响 |
| D | 滴有酚酞的Na2CO3溶液中加入BaCl2固体 | 溶液红色变浅 | Na2CO3溶液中存在水解平衡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-19更新
|
168次组卷
|
2卷引用:安徽省芜湖市2021-2022学年高二上学期期末考试化学试题
解题方法
6 . 反应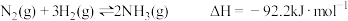 达到平衡状态后,改变某一条件,下列图像与条件变化相悖的是
达到平衡状态后,改变某一条件,下列图像与条件变化相悖的是
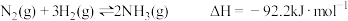 达到平衡状态后,改变某一条件,下列图像与条件变化相悖的是
达到平衡状态后,改变某一条件,下列图像与条件变化相悖的是| A.增大N2浓度 | B.升高温度 | C.改变压强 | D.加入催化剂 |
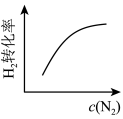 |  | 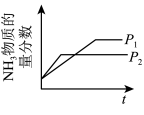 | 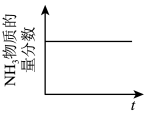 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-17更新
|
82次组卷
|
2卷引用:安徽省宿州市十三所重点中学2021-2022学年高二上学期期末质量检测化学(理科)试题
名校
7 . 将BaO2放入密闭真空容器中,反应2BaO2(s)⇌2BaO(s)+O2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
| A.平衡常数减小 | B.BaO量不变 | C.容器内压强增大 | D.O2浓度不变 |
您最近一年使用:0次
8 . CuCl是一种白色固体,溶于氨水,碱性条件下水解,可用于一氧化碳和乙炔的气体分析中。回答下列问题:
(1)制备CuCl的方法很多,如可用CuSO4溶液、Na2SO3溶液及NaCl反应制取,其他条件一定时,实验测得CuCl产率与溶液pH的关系如图所示:
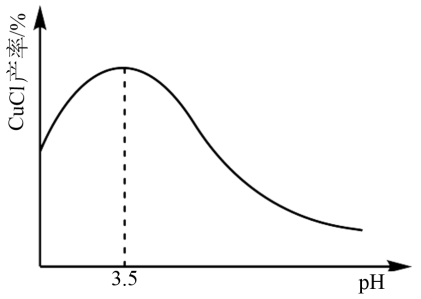
①制备CuCl反应的化学方程式为___________ 。
②由图可知,pH<3.5,随着pH增大,CuCl产率增大,其原因是___________ ,pH>3.5,随着pH增大,CuCl产率减少,其原因是___________ 。
(2)CuCl溶于氨水的反应为CuCl+2NH3∙H2O Cu(NH3)2Cl+2H2O。向反应后溶液中滴加稀H2SO4观察到的现象是
Cu(NH3)2Cl+2H2O。向反应后溶液中滴加稀H2SO4观察到的现象是___________ ;含氨的Cu(NH3)2Cl溶液久置会转化为Cu(NH3)4Cl2溶液,其反应的离子方程式为___________ 。
(3)利用盛放如下试剂的装置,可测量混合气体中N2、CO2、CO、O2的含量,其气体经过装置顺序:混合气体→b→___________ →___________ →d(填字母)。
a.氯化亚铜酸溶液吸收CO;b.KOH溶液吸收CO2;c.含焦性没食子酸的KOH溶液吸收O2;d.排水法收集N2。
(1)制备CuCl的方法很多,如可用CuSO4溶液、Na2SO3溶液及NaCl反应制取,其他条件一定时,实验测得CuCl产率与溶液pH的关系如图所示:

①制备CuCl反应的化学方程式为
②由图可知,pH<3.5,随着pH增大,CuCl产率增大,其原因是
(2)CuCl溶于氨水的反应为CuCl+2NH3∙H2O
 Cu(NH3)2Cl+2H2O。向反应后溶液中滴加稀H2SO4观察到的现象是
Cu(NH3)2Cl+2H2O。向反应后溶液中滴加稀H2SO4观察到的现象是(3)利用盛放如下试剂的装置,可测量混合气体中N2、CO2、CO、O2的含量,其气体经过装置顺序:混合气体→b→
a.氯化亚铜酸溶液吸收CO;b.KOH溶液吸收CO2;c.含焦性没食子酸的KOH溶液吸收O2;d.排水法收集N2。
您最近一年使用:0次
名校
9 .  温度时,在容积为1L的密闭容器中,X、Y、Z三种气体的浓度随时间变化如图Ⅰ。其它条件不变,当温度分别为
温度时,在容积为1L的密闭容器中,X、Y、Z三种气体的浓度随时间变化如图Ⅰ。其它条件不变,当温度分别为 和
和 时,Y的体积分数与时间关系如图Ⅱ。
时,Y的体积分数与时间关系如图Ⅱ。

(1)写出容器中发生反应的方程式___________ ;正反应为___________ 反应(填“放热”或“吸热”)。
(2)当 时,该反应
时,该反应___________ 达到平衡状态(填“已”或“未”);由图Ⅰ,若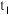 为10min,则
为10min,则 时间内,
时间内,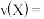
___________ ; 时平衡常数K=
时平衡常数K=___________ (保留小数点后一位)。
(3)其它条件不变,再充入一定量X,平衡___________ 移动(填“正向”、“逆向”、或“不”),X的转化率___________ (填“增大”、“减小”、或“不变”)。
 温度时,在容积为1L的密闭容器中,X、Y、Z三种气体的浓度随时间变化如图Ⅰ。其它条件不变,当温度分别为
温度时,在容积为1L的密闭容器中,X、Y、Z三种气体的浓度随时间变化如图Ⅰ。其它条件不变,当温度分别为 和
和 时,Y的体积分数与时间关系如图Ⅱ。
时,Y的体积分数与时间关系如图Ⅱ。
(1)写出容器中发生反应的方程式
(2)当
 时,该反应
时,该反应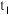 为10min,则
为10min,则 时间内,
时间内,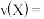
 时平衡常数K=
时平衡常数K=(3)其它条件不变,再充入一定量X,平衡
您最近一年使用:0次
2021-12-18更新
|
226次组卷
|
4卷引用:安徽省黄山市屯溪第一中学2021-2022学年高二上学期期中考试化学试题
名校
解题方法
10 . 使用SNCR脱硝技术的原理是6NO(g)+4NH3(g) 5N2(g)+6H2O(g),如图是其在密闭体系中研究反应条件对烟气脱硝效率的实验结果。下列说法正确的是
5N2(g)+6H2O(g),如图是其在密闭体系中研究反应条件对烟气脱硝效率的实验结果。下列说法正确的是

 5N2(g)+6H2O(g),如图是其在密闭体系中研究反应条件对烟气脱硝效率的实验结果。下列说法正确的是
5N2(g)+6H2O(g),如图是其在密闭体系中研究反应条件对烟气脱硝效率的实验结果。下列说法正确的是
| A.从图1判断,该反应的正反应方向是放热反应 |
| B.从图2判断,减少氨气的浓度有助于提高NO的转化率 |
| C.从图1判断,脱硝的最佳温度约为900℃ |
| D.从图2判断,综合考虑脱硝效率和运行成本最佳氨氮摩尔比应为1.5-2.0 |
您最近一年使用:0次
2021-12-13更新
|
167次组卷
|
2卷引用:安徽省亳州市第二中学2021-2022学年高二上学期期中考试化学试题



