名校
1 . 关节炎首次发作一般在寒冷季节,原因是关节滑液中形成了尿酸钠晶体(NaUr),易诱发关节疼痛,其化学机理是:①HUr(aq)+H2O(l)⇌Ur-(aq)+H3O+(aq)②Ur-(aq)+Na+(aq)⇌NaUr(s)。下列叙述错误的是( )
| A.反应①是尿酸电离的方程式 |
| B.反应①②的正反应均为吸热反应 |
| C.降低关节滑液中HUr及Na+含量是治疗方法之一 |
| D.关节保暖可以缓解疼痛,原理是平衡②逆向移动 |
您最近一年使用:0次
2020-04-05更新
|
284次组卷
|
7卷引用:福建省连城县第一中学2020-2021学年高二上学期第二次月考化学(高考科)试题
名校
解题方法
2 . 下列叙述中正确的是( )
| A.升温或加压均能提高反应体系单位体积内活化分子的百分数 |
| B.恒温恒容H2(g)+I2(g)⇌2HI(g)平衡体系中充入气体H2或He均可提高I2的转化率 |
| C.明矾净水、纯碱去油污和NH4Cl作焊药去除铁锈,均运用了盐类水解原理 |
| D.用惰性电极电解熔融态的NaCl、AlCl3、SiCl4,均可冶炼制取Na、Al、Si |
您最近一年使用:0次
2020-04-05更新
|
119次组卷
|
3卷引用:福建省连城县第一中学2020-2021学年高二上学期第二次月考化学(高考科)试题
名校
3 . 下列事实不能用化学平衡移动原理解释的是
| A.光照新制的氯水时,溶液的pH逐渐减小 |
| B.在铂铑合金催化下缩短N2和H2合成氨的时间 |
| C.可用浓氨水和氢氧化钠固体快速制取氨气 |
| D.红棕色的NO2,加压后颜色先变深后变浅 |
您最近一年使用:0次
2019-12-25更新
|
72次组卷
|
2卷引用:福建省漳平市第一中学2019-2020学年高二上学期第二次月考化学试题
11-12高二·福建龙岩·期末
4 . 下列措施或事实不能 用勒夏特列原理解释的是( )
| A.滴加酚酞的氨水中加入氯化铵固体后红色变浅 |
B.棕红色的NO2加压后颜色先变深后变浅(已知:2NO2(g) N2O4(g)) N2O4(g)) |
| C.煅烧粉碎的硫铁矿利于SO2的生成 |
| D.工业上生产硫酸的过程中,使用过量的空气以提高SO2的利用率 |
您最近一年使用:0次
2019-11-05更新
|
116次组卷
|
4卷引用:2011-2012学年福建省龙岩一中高二期末考试化学试卷
(已下线)2011-2012学年福建省龙岩一中高二期末考试化学试卷(已下线)2012-2013学年山东东阿一中高二上学期第一次模块测试化学试卷甘肃省白银市会宁县第四中学2019-2020学年高二上学期期中考试化学试题广西壮族自治区百色市田阳高中2019-2020学年高二上学期12月月考理科综合化学试题
5 . CO2是一种常用的化工原料。
Ⅰ.以CO2与NH3为原料可以合成尿素[CO(NH2)2]。合成尿素的反应为2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)。
CO(NH2)2(s)+H2O(g)。
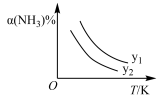
(1)在不同温度及不同y值下合成尿素,达到平衡时,氨气转化率变化情况如图所示。该反应的ΔH_____ 0(填“>”、“<”或“=”,下同),若y表示压强,则y1_______ y2 , 若y表示反应开始时的水碳比[n(NH3)/n(CO2)],则y1_______ y2。
(2)t℃时,若向容积为2L的密闭容器中加入3molNH3和1molCO2,达到平衡时,容器内压强为开始时的0.75倍。若保持条件不变,再向该容器中加入0.5molCO2和1molH2O,NH3的转化率将__________ (填“增大”、“减小”或“不变”)。
Ⅱ.CO2与H2反应可用于生产甲醇。
(3)已知氢气与甲醇的燃烧热分别为-285.8 kJ·mol-1、-726.5kJ·mol-1,则CO2与H2反应产生液态甲醇与液态水的热化学方程式为________________ 。
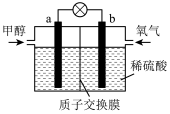
(4)下图是某甲醇燃料电池工作的示意图。质子交换膜(只有质子能够通过)左右两侧的溶液均为1L 2mol·L-1 H2SO4溶液。电极a上发生的电极反应式为________________________ ,当电池中有1mol e-发生转移时左右两侧溶液的质量之差为______ g (假设反应物耗尽,忽略气体的溶解)。
Ⅰ.以CO2与NH3为原料可以合成尿素[CO(NH2)2]。合成尿素的反应为2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g)。
CO(NH2)2(s)+H2O(g)。 (1)在不同温度及不同y值下合成尿素,达到平衡时,氨气转化率变化情况如图所示。该反应的ΔH

(2)t℃时,若向容积为2L的密闭容器中加入3molNH3和1molCO2,达到平衡时,容器内压强为开始时的0.75倍。若保持条件不变,再向该容器中加入0.5molCO2和1molH2O,NH3的转化率将
Ⅱ.CO2与H2反应可用于生产甲醇。
(3)已知氢气与甲醇的燃烧热分别为-285.8 kJ·mol-1、-726.5kJ·mol-1,则CO2与H2反应产生液态甲醇与液态水的热化学方程式为
(4)下图是某甲醇燃料电池工作的示意图。质子交换膜(只有质子能够通过)左右两侧的溶液均为1L 2mol·L-1 H2SO4溶液。电极a上发生的电极反应式为

您最近一年使用:0次
2019-02-20更新
|
136次组卷
|
2卷引用:福建省连城县第一中学2020-2021学年高二上学期第二次月考化学(高考科)试题
6 . 人体血液内的血红蛋白(Hb)易与O2结合生成HbO2,因此具有输氧能力,CO吸入肺中发生反应:CO+HbO2 O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是
O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是
 O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是
O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是A.CO与HbO2反应的平衡常数K=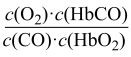 |
| B.人体吸入的CO越多,与血红蛋白结合的O2越少 |
| C.当吸入的CO与O2浓度之比大于或等于0.02时,人的智力才会受损 |
| D.把CO中毒的病人放入高压氧仓中解毒,其原理是使上述平衡向逆反应方向移动 |
您最近一年使用:0次
2019-01-30更新
|
1624次组卷
|
33卷引用:2011-2012学年福建省龙岩一中高二期末考试化学试卷
(已下线)2011-2012学年福建省龙岩一中高二期末考试化学试卷2009年普通高等学校招生统一考试理综试题化学部分(天津卷)(已下线)09-10年湖北恩施高二下学期期末测试化学卷(已下线)2010年江西省九江一中高二上学期第一次月考(化学)(已下线)2010年河北省邯郸市高二上学期期末考试化学试卷(已下线)2011-2012学年浙江省台州中学高二下学期第一次统练化学试卷(已下线)2011-2012学年浙江省温州四中高二下学期期中考试化学试卷(已下线)2013-2014学年湖北省荆州中学高二上学期期中考试化学试卷(已下线)2014-2015学年浙江省东阳外国语学校高二上学期期中化学试卷2015-2016学年浙江省东阳中学高二上学期12月阶段测化学试卷2016-2017学年辽宁省鞍山一中高二上期中化学试卷福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题北京市第161中学2017-2018学年高二上学期期中适应性训练化学试题【校级联考】福建省平和一中、南靖一中等五校2018-2019学年高二上学期第一次联考化学试题【全国百强校】福建省三明市第一中学2018-2019学年高二(理)上学期期中考试化学试题【全国百强校】黑龙江省鹤岗市第一中学2018-2019学年高二下学期第一次月考(开学)化学试题山西大学附属中学2019-2020学年高二10月月考化学试题河北省临漳县第一中学2019-2020学年高二上学期期中考试化学试题云南省楚雄市实验中学2018—2019学年高二上学期11月月考化学试题鲁科版(2019)选择性必修1化学反应原理 综合训练高中必刷题高二选择性必修1化学反应原理综合训练四川省广安市武胜烈面中学校2020-2021学年高二上学期10月月考化学试题广东省汕头市澄海中学2020-2021学年高二上学期期中考试化学(选考)试题选择性必修1 化学反应原理综合训练重庆实验外国语学校2022届高三上学期开学考试化学试题河北省衡水市第十四中学2021-2022学年高二上学期二调考试化学试题(已下线)2.4 化学反应的调控(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)广东实验中学2021-2022学年高二上学期期中考试化学试题(已下线)2.2.3 化学平衡常数(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)辽宁省沈阳市铁西区重点协作校2021-2022学年高二上学期期中考试化学试题山东省德州市第一中学2022-2023学年高二上学期10月月考化学试题云南省龙陵县第一中学2022-2023学年高二下学期期末考试化学试题福建省莆田第一中学2023-2024学年高二上学期期中考试化学试题
7 . COCl2(g)⇌CO(g)+Cl2(g)∆H>0,当反应达到平衡时,下列措施:①升温,②恒压通入惰性气体,③增加CO的浓度,④减压,⑤加催化剂,⑥恒容通入惰性气体;能提高COCl2转化率的是( )
| A.①②④ | B.①④⑥ | C.②③⑥ | D.③⑤⑥ |
您最近一年使用:0次
2019-01-30更新
|
1252次组卷
|
74卷引用:2016-2017学年福建省龙岩四校高二上学期期中联考化学试卷
2016-2017学年福建省龙岩四校高二上学期期中联考化学试卷2010年普通高等学校招生全国统一考试理综化学部分(重庆卷)2010年高考化学试题分项专题八 化学反应速率和化学平衡(已下线)09~10年瑞安中学高一下学期期末考试(理)化学卷(已下线)2012年武警院校招生统考模拟卷(一)化学试卷(已下线)2011-2012学年山东省沂南一中高二上学期期中模块学分认定考试化学试卷(已下线)2010-2011学年浙江省绍兴一中高二下学期期末考试化学试卷(已下线)2011-2012学年福建省南安市侨光中学高二上学期期末考试化学试卷(已下线)2011-2012学年贵州省遵义四中高二上学期期末检测化学试卷(已下线)2011—2012学年度黑龙江大庆实验中学高二上学期期末考试化学试卷(已下线)2011-2012年浙江永嘉县普高联合体高二下学期期中联考化学试卷(已下线)2011-2012学年福建省福州文博中学高二下学期期中考试化学试卷(已下线)2011-2012学年河北省辛集三中高二化学选修四期中试卷(已下线)2012-2013学年辽宁省沈阳铁路实验中学高一下学期期末考试化学试卷(已下线)2013届安徽省黄山市高中毕业班第一次质量检测化学试卷(已下线)2013-2014学年江苏省淮安市高中协作体高二下学期期中考试化学试卷(已下线)2014届黑龙江省哈师大附中高二上学期期末考试化学试卷(已下线)2014-2015学年湖南省娄底市高二上学期期中联考化学试卷(已下线)2014-2015湖南省新化一中高二上学期期中化学试卷(已下线)2014-2015学年辽宁师范大学附中高二10月模考化学试卷2015-2016学年河北省故城县高级中学高二9月月考化学试卷2016届浙江省东阳市第二高级中学高三上学期12月月考化学试卷2015-2016学年浙江余姚中学高二上学期期中考试化学试卷2016届宁夏银川市第二中学高三上学期统练(三)化学试卷2015-2016学年陕西省西安一中高二上10月月考化学试卷2015-2016学年西藏日喀则高级中学高二上期末化学试卷2015-2016学年河北省邯郸市曲周一中高一下期中化学试卷2016-2017学年陕西省西安一中高二上10月月考化学卷2016-2017学年四川省新津中学高二上10月月考化学试卷2016-2017学年四川省成都开发区实验中学高二10月月考化学卷2016-2017学年陕西西安中学高二平行班上期中化学卷2016-2017学年黑龙江、吉林省两省六校高二上期中化学试卷河北省正定中学2016-2017学年高一下学期期末考试化学试题黑龙江省大庆中学2017-2018学年高二上学期开学考试化学试题天津市耀华中学2018届高三上学期第一次月考化学试题河南省南阳市第一中学2017-2018学年高二上学期第二次月考化学试题北京师大附中2017-2018学年上学期高二年级期中考试化学试卷福建省清流一中2017-2018学年高二上学期第二阶段(期中)考试化学(理)试题江西省南昌市第二中学2017-2018学年高二上学期期末考试化学试题福建省莆田第一中学2017-2018学年高二下学期期初考试化学试题湖北省沙市中学2017-2018学年高二下学期期中考试化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二(理)10月月考化学试题【全国百强校】江苏省启东中学2018-2019学年高二上学期期中考试化学试题甘肃省白银市靖远县第四中学2018-2019学年高二上学期期中考试化学试题山西省晋中市平遥县第二中学2018-2019学年高二上学期期中考试化学试题山西省忻州二中2018-2019学年高二上学期期中考试化学试题【校级联考】天津市静海区2019届高三上学期12月四校联考化学试题内蒙古自治区巴彦淖尔市临河三中2018-2019学年高二上学期期中考试化学试题河北省唐县第一中学2019届高三上学期期中考试化学试题【市级联考】甘肃省张掖市2018-2019学年高二上学期期末联考化学试题步步为赢 高二化学暑假作业:作业九 化学反应速率和化学平衡黑龙江省哈尔滨市第六中学2019-2020学年高二10月月考化学试题广西宾阳县宾阳中学2019-2020学年高二9月月考化学试题山东省肥城市泰西中学2019-2020学年高二10月月考化学试题陕西省延安市第一中学2019-2020学年高二上学期期中考试化学试题辽宁省大连市旅顺口区2018-2019学年高二上学期期中考试化学试题安徽省池州市第一中学2019-2020学年高二上学期期中考试化学试题湖北省宜昌市葛洲坝中学2019-2020学年高二上学期期中考试化学试题河南省平顶山市郏县第一高级中学2019-2020学年高二上学期第二次月考化学试题河南省南阳市2017-2018学年高二上学期期末考试化学试题云南省玉溪市华宁县第二中学2019-2020学年高二上学期期末考试化学试题云南省迪庆州维西县第二中学2019-2020学年上学期高二期末考试化学试题2020届人教版高三专题基础复习专题7《化学反应速率与化学平衡》测试卷云南省大理白族自治州大理市下关第一中学2019-2020学年高二上学期期末考试化学试题甘肃省甘南藏族自治州合作第一中学2019-2020学年高二上学期期中考试理科化学试题安徽省黄山市屯溪第一中学2019-2020学年高二下学期入学考试化学试题安徽省亳州市涡阳县第九中学2019-2020学年高一7月月考化学试题湖北省荆州市北门中学2019-2020学年高二下学期期末考试化学试题黑龙江省大庆市第四中学2020届高三上学期第一次检测化学试题黑龙江省伊春市伊美区第二中学2020-2021学年高二上学期第一次月考化学试题山西省新绛县第二中学2019-2020学年高二上学期第一次考试化学试题辽宁省大连市一〇三中学2020-2021学年高二10月月考化学试题鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 第2节 化学反应的限度课时2 反应条件对化学平衡的影响福建省福州市第十一中学2020-2021学年高二上学期期中质量检测化学试题
8 . 重铬酸钾是一种重要的化工原料,工业上由铬铁矿(主要成分为FeO·Cr2O3、SiO2等)制备,制备流程如图所示:

已知:
Ⅰ.步骤①的主要反应为2FeO·Cr2O3+4Na2CO3+7NaNO3 4Na2CrO4+Fe2O3+4CO2↑+7NaNO2。
4Na2CrO4+Fe2O3+4CO2↑+7NaNO2。
Ⅱ.2CrO42-+2H+ Cr2O72-+H2O。
Cr2O72-+H2O。
下列说法正确的是

已知:
Ⅰ.步骤①的主要反应为2FeO·Cr2O3+4Na2CO3+7NaNO3
 4Na2CrO4+Fe2O3+4CO2↑+7NaNO2。
4Na2CrO4+Fe2O3+4CO2↑+7NaNO2。Ⅱ.2CrO42-+2H+
 Cr2O72-+H2O。
Cr2O72-+H2O。下列说法正确的是
| A.步骤①熔融、氧化可以在陶瓷容器中进行 |
| B.步骤①中每生成44.8 L CO2共转移7 mol电子 |
| C.步骤④若调节滤液2的pH,使之变小,则有利于生成Cr2O72- |
| D.步骤⑤生成K2Cr2O7晶体,说明该温度下K2Cr2O7的溶解度大于Na2Cr2O7 |
您最近一年使用:0次
2018-12-22更新
|
260次组卷
|
4卷引用:福建省长汀、连城一中等六校2020届高三上学期期中考联考化学试题
12-13高二上·江苏盐城·期末
名校
9 . 25 ℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)  Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是
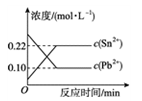
 Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是
| A.往平衡体系中加入金属铅后,c(Pb2+)增大 |
| B.升高温度,平衡体系中c(Pb2+)增大,说明该反应ΔH>0 |
| C.25 ℃时,该反应的平衡常数K=2.2 |
| D.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小 |
您最近一年使用:0次
2017-11-07更新
|
480次组卷
|
47卷引用:2011-2012学年福建省龙岩一中高二第三学段考试化学试卷
(已下线)2011-2012学年福建省龙岩一中高二第三学段考试化学试卷(已下线)2011-2012学年江苏省射阳中学高二上学期期末考试化学(选修)试卷(已下线)2011-2012学年天津一中高二上学期期中考试化学试卷(已下线)2011-2012学年浙江省金华一中高二下学期期中考试化学试卷(已下线)2011-2012学年海南省海南中学高二上学期期末考试理科化学试卷(已下线)2011-2012学年天津市天津一中高二上学期期中考试化学试卷(已下线)2011-2012学年江西省南昌三中高二上学期期中考试化学试卷(已下线)2012-2013学年福建德化三中高二上学期第二次月考理科化学试卷(已下线)2013届甘肃省永昌县第一中学高三上学期期中考试化学试卷(已下线)2013-2014学年湖北省部分重点中学高二上学期期末考试化学试卷(已下线)2014年化学高考课时演练 7-3化学平衡常数化学反应进行方向练习卷(已下线)2013-2014福建省厦门双十中学高三热身考试化学试卷(已下线)2013-2014吉林省吉林一中高一下学期期末考试化学试卷(已下线)2015届福建省福州第八中学高三上学期第二次质量检查化学试卷2014-2015学年甘肃省武威市六中高二上学期期中化学(理)试卷2015届上海理工大学附中高三上学期月考化学试卷2015-2016湖南省衡阳四中高二12月学科联赛化学试卷2015-2016湖南省衡阳县四中高二12月学科联赛化学试卷2014-2015广东省揭阳市第一中学高二上学期期末考试化学理试卷2014-2015学年福建省晋江市平山中学高二下学期期中考试化学试卷2014-2015学年湖北省老河口市第二中学高二下学期期末化学试卷2016届河北省行唐启明中学高三上学期12月月考化学试卷陕西省咸阳市西藏民族学院附属中学2015-2016学年高二上期末化学卷2016届江西省宜春市奉新县第一中学高三上第五次月考化学试卷2015-2016学年湖南省醴陵二中、四中高二上学期期末化学试卷2016届河南省三门峡市陕州中学高三下尖子生专题训练(三)理综化学试卷2016届山西省平遥中学高三第二轮训练三化学试卷2015-2016学年内蒙古包头九中高一下期末化学试题2016-2017学年河北冀州市中学高二上开学调研化学卷2016-2017学年河南省师大附中高二上期中化学试卷2016-2017学年河北省冀州中学高二上期中化学卷2016-2017学年辽宁省瓦房店市高级中学高二上10月月考化学试卷甘肃省会宁县第四中学2017-2018学年高二上学期期中考试化学试题天津市红桥区2017-2018学年高二上学期期中考试化学试题甘肃省民乐县第一中学2017-2018学年高二上学期期中考试化学试题江西省南昌市第二中学2017-2018学年高二上学期第三次月考化学试题四川省眉山市眉山中学2018-2019学年高二上学期10月月考理科综合化学试题【全国百强校】吉林省长春外国语学校2018-2019学年高二上学期期中考试化学试题2【全国百强校】吉林省延边市第二中学2018-2019学年高二下学期开学考试化学试题吉林省吉化第一高级中学校2019-2020学年高二9月月考化学试题河南省南阳市2018-2019学年高二上学期期中质量评估化学试题湖南省长沙市天心区雅礼中学2018-2019学年高二下学期期末考试化学试题吉林省汪清县第六中学2020-2021学年高二上学期期中考试化学试题河南省郑州市第一〇六高级中学2020-2021学年高二上学期11月考试化学试题福建省永安市第一中学2020-2021学年高二上学期第一次月考化学试题湖北省咸宁市通城二中2020-2021学年度高二上学期期中考试化学试题黑龙江省大庆市实验中学2021-2022学年高三上学期开学考试化学试题
10 . 向恒温恒容密闭容器中加入1molHI,发生下列反应2HI(g)  H2(g)+I2(g),△H >0。达到平衡后,往容器中再加入1molHI,有关说法正确的是
H2(g)+I2(g),△H >0。达到平衡后,往容器中再加入1molHI,有关说法正确的是
 H2(g)+I2(g),△H >0。达到平衡后,往容器中再加入1molHI,有关说法正确的是
H2(g)+I2(g),△H >0。达到平衡后,往容器中再加入1molHI,有关说法正确的是| A.平衡不移动,HI平衡转化率不变 |
| B.平衡向右移动,HI平衡转化率不变 |
| C.平衡向左移动,HI平衡转化率减小 |
| D.平衡向右移动,HI平衡转化率增大 |
您最近一年使用:0次



