名校
1 . 下列事实不能用勒夏特列原理解释的是
| A.新制氯水在光照下颜色变浅 |
B.由 、 、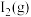 、 、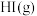 组成的平衡体系加压后颜色变深 组成的平衡体系加压后颜色变深 |
C.对于 ,及时分离出钾蒸气 ,及时分离出钾蒸气 |
D.对于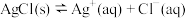 ,选择稀盐酸代替蒸馏水洗涤 ,选择稀盐酸代替蒸馏水洗涤 沉淀 沉淀 |
您最近一年使用:0次
2022-01-23更新
|
183次组卷
|
2卷引用:广东省肇庆市2021-2022学年高二上学期期末考试化学试题
名校
解题方法
2 . 一定温度下,将 和
和 充入
充入 密闭容器中发生反应:
密闭容器中发生反应: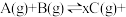
 ,在
,在 时达到平衡。在
时达到平衡。在 、
、 时分别改变反应的一个条件,测得容器中
时分别改变反应的一个条件,测得容器中 的浓度随时间变化情况如图所示。
的浓度随时间变化情况如图所示。
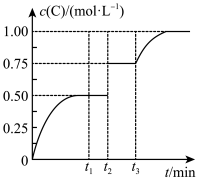
下列有关说法正确的是
 和
和 充入
充入 密闭容器中发生反应:
密闭容器中发生反应: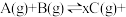
 ,在
,在 时达到平衡。在
时达到平衡。在 、
、 时分别改变反应的一个条件,测得容器中
时分别改变反应的一个条件,测得容器中 的浓度随时间变化情况如图所示。
的浓度随时间变化情况如图所示。
下列有关说法正确的是
A. |
B.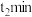 时改变的条件是使用催化剂 时改变的条件是使用催化剂 |
C. 时改变的条件是只增大生成物C的浓度 时改变的条件是只增大生成物C的浓度 |
D. 、 、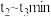 阶段反应的平衡常数均为4 阶段反应的平衡常数均为4 |
您最近一年使用:0次
2022-01-19更新
|
82次组卷
|
3卷引用:广东省肇庆市第一中学2022-2023学年高二上学期期中考试化学试题
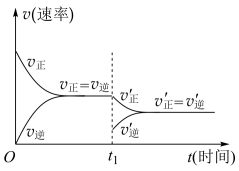
3 . 在N2(g)+3H2(g)  2NH3(g)(正反应为放热反应)的平衡体系中,在t1时刻只改变某一条件,其反应速率随时间变化的曲线如图,根据图象能得出的结论是
2NH3(g)(正反应为放热反应)的平衡体系中,在t1时刻只改变某一条件,其反应速率随时间变化的曲线如图,根据图象能得出的结论是
 2NH3(g)(正反应为放热反应)的平衡体系中,在t1时刻只改变某一条件,其反应速率随时间变化的曲线如图,根据图象能得出的结论是
2NH3(g)(正反应为放热反应)的平衡体系中,在t1时刻只改变某一条件,其反应速率随时间变化的曲线如图,根据图象能得出的结论是
| A.改变条件,平衡向逆反应方向移动 |
| B.t1时刻,改变的条件是减少了NH3的浓度 |
| C.t1时刻,改变的条件是增大了体系的压强 |
| D.达新平衡时,正反应速率增大,逆反应速率减小 |
您最近一年使用:0次
4 . 下列说法正确的是
| A.可逆反应具有的特征是正反应速率和逆反应速率相等 |
| B.在其他条件不变时,升高温度可使化学平衡向放热反应方向移动 |
| C.在其他条件不变时,增大压强一定会破坏有气体存在的反应的平衡状态 |
| D.在其他条件不变时,使用催化剂可以改变化学反应速率,但不能改变化学平衡状态 |
您最近一年使用:0次
名校
5 . 压强变化不会使下列化学反应的平衡发生移动的是( )
A.C(s)+CO2(g) 2CO(g) 2CO(g) | B.3H2(g)+N2(g) 2NH3(g) 2NH3(g) |
C.2SO2(g)+O2(g) 2SO3(g) 2SO3(g) | D.H2(g)+I2(g) 2HI(g) 2HI(g) |
您最近一年使用:0次
2019-09-28更新
|
286次组卷
|
15卷引用:广东省肇庆市实验中学2017-2018学年高二上学期期中考试化学(理)试题
广东省肇庆市实验中学2017-2018学年高二上学期期中考试化学(理)试题(已下线)2010年青海省青海师大附中高二上学期期中考试化学试卷(已下线)2011-2012学年湖南省蓝山二中高二上学期期末考试化学试卷宁夏育才中学2017-2018学年高二9月月考化学试题云南省峨山彝族自治县第一中学2017-2018学年高二12月月考(理)化学试题浙江省诸暨市牌头中学2017-2018学年高一下学期期中考试(A)化学试题黑龙江省伊春市第二中学2018-2019学年高二(理)上学期期中考试化学试题天津市静海区四校2019-2020学年高二上学期9月联考化学试题广东省广州市2019-2020学年高二上学期期中模拟测试化学试题(一)山西省阳泉市2019-2020学年高二上学期期末考试化学试题陕西省咸阳百灵中学2020-2021学年高二上学期期中考试化学试题海南省万宁市民族中学2019-2020学年度高二上学期期末考试化学试题吉林省白城市第十四中学2021-2022学年高二上学期期中考试化学试卷题2.3.1浓度 压强变化对化学平衡的影响 课前黑龙江省伊春市铁力市马永顺中学校2023-2024学年高二上学期期末考试化学试题
名校
6 . 高温下,某反应达到平衡,平衡常数K=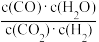 。恒容时,温度升高,H2浓度减小。下列说法正确的是( )
。恒容时,温度升高,H2浓度减小。下列说法正确的是( )
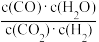 。恒容时,温度升高,H2浓度减小。下列说法正确的是( )
。恒容时,温度升高,H2浓度减小。下列说法正确的是( )| A.该反应的焓变为正值 |
| B.恒温下,增大压强,H2浓度一定减小 |
| C.升高温度,逆反应速率减小 |
| D.该反应为放热反应 |
您最近一年使用:0次
2019-06-11更新
|
529次组卷
|
6卷引用:广东省肇庆市封开县广信中学、四会中学2023-2024学年高二上学期第一次联考化学试题
广东省肇庆市封开县广信中学、四会中学2023-2024学年高二上学期第一次联考化学试题广东省中山市第一中学2018-2019学年高二上学期第一次段考化学试题(已下线)2019年9月17日 《每日一题》选修4—— 化学平衡移动的分析甘肃省武威市第六中学2019-2020学年高二上学期第一次学段考试化学试题(已下线)2021年1月浙江省普通高校招生选考科目考试化学仿真模拟试卷03浙江省台州市书生中学2020-2021学年高二下学期开学考试化学试题
7 . 已知SO3分解反应为2SO3(g)⇌2SO2(g)+O2(g)。在1.0L密闭容器中加入10mol SO3(g),在一定温度进行上述反应,反应时间(t)与容器内气体总压强(p)的数据见下表:
回答下列问题:
(1)欲提高SO3的平衡转化率,应采取的措施为_____ (填字母)。
a.增大压强 b.通入SO3 c.降低压强
(2)平衡时SO3的转化率为_____ ,该温度下的平衡常数Kw=_____
(3)研究表明,SO3(g)分解速率v=4×10﹣3×pSO3(kPa•min﹣1),t=6h时,测得体系中pO2=55kPa,则此时的pSO3=_____ kPa,v(SO3)=_____ kPa•min﹣1。
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 总压强p/kPa | 400 | 412 | 422 | 440 | 469 | 518 | 538 | 560 | 560 |
回答下列问题:
(1)欲提高SO3的平衡转化率,应采取的措施为
a.增大压强 b.通入SO3 c.降低压强
(2)平衡时SO3的转化率为
(3)研究表明,SO3(g)分解速率v=4×10﹣3×pSO3(kPa•min﹣1),t=6h时,测得体系中pO2=55kPa,则此时的pSO3=
您最近一年使用:0次
名校
8 . 在密闭容器中发生反应aX(g)+bY(g)=cZ(g)+dW(g),反应达到平衡后,保持温度不变,将容积扩大到原来的2倍,当再次达到平衡时,W的浓度为原平衡时的3/5,下列叙述正确的是( )
| A.平衡向逆反应方向移动 | B.a+b<c+d |
| C.X的体积分数增大 | D.X的转化率减小 |
您最近一年使用:0次
2019-03-04更新
|
210次组卷
|
3卷引用:【校级联考】广东省肇庆联盟校2018-2019学年高二上学期期末考试化学试题
名校
9 . 可逆反应A(g)+2B(g) 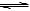 2C(g) ΔΗ<O在达到平衡时,要使C的浓度达到最大值,最适宜的条件是( )
2C(g) ΔΗ<O在达到平衡时,要使C的浓度达到最大值,最适宜的条件是( )
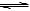 2C(g) ΔΗ<O在达到平衡时,要使C的浓度达到最大值,最适宜的条件是( )
2C(g) ΔΗ<O在达到平衡时,要使C的浓度达到最大值,最适宜的条件是( )| A.低温、高压 | B.高温、低压 |
| C.高温、高压 | D.使用合适的催化剂 |
您最近一年使用:0次
2017-12-08更新
|
125次组卷
|
4卷引用:广东省肇庆市实验中学2017-2018学年高二上学期期中考试化学(理)试题
解题方法
10 . 已知:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1。该反应可用于消除氮氧化物的污染。在130℃和180℃时,分别将0.50 molCH4和a molNO2充入1L的密闭容器中发生反应,测得有关数据如下表:
N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1。该反应可用于消除氮氧化物的污染。在130℃和180℃时,分别将0.50 molCH4和a molNO2充入1L的密闭容器中发生反应,测得有关数据如下表:
(1)开展实验1和实验2的目的是:____________________ 。
(2)180℃、反应到40min时,体系______ (填“达到”或“未达到”)平衡状态,理由是:______________ ;此时CH4的平衡转化率为:_________ 。
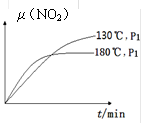
(3)在一定条件下,反应时间t与转化率μ(NO2)的关系如图所示,请在图象中画出180℃时,压强为P2(设压强P2>P1)的变化曲线,并做必要的标注_____ 。
 N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1。该反应可用于消除氮氧化物的污染。在130℃和180℃时,分别将0.50 molCH4和a molNO2充入1L的密闭容器中发生反应,测得有关数据如下表:
N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1。该反应可用于消除氮氧化物的污染。在130℃和180℃时,分别将0.50 molCH4和a molNO2充入1L的密闭容器中发生反应,测得有关数据如下表:| 实验 编号 | 温度 | 时间 min 物质 的量mol | 0 | 10 | 20 | 40 | 50 |
| 1 | 130℃ | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| 2 | 180℃ | n(CH4)/mol | 0.50 | 0.30 | 0.18 | 0.15 |
(1)开展实验1和实验2的目的是:
(2)180℃、反应到40min时,体系
(3)在一定条件下,反应时间t与转化率μ(NO2)的关系如图所示,请在图象中画出180℃时,压强为P2(设压强P2>P1)的变化曲线,并做必要的标注

您最近一年使用:0次



