名校
解题方法
1 . 以CO2、H2为原料合成CH3OH涉及的主要反应如下:
①CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H1=-49.5 kJ/mol
②CO(g)+2H2(g)⇌CH3OH(g) ∆H2=-90.4 kJ/mol
③CO2(g)+H2(g)⇌CO(g)+H2O(g) ∆H3
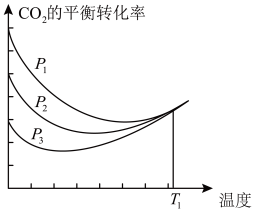
不同压强下,按照n(CO2):n(H2)=1:3投料,CO2平衡转化率随温度变化关系如图。下列说法正确的是
①CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H1=-49.5 kJ/mol
②CO(g)+2H2(g)⇌CH3OH(g) ∆H2=-90.4 kJ/mol
③CO2(g)+H2(g)⇌CO(g)+H2O(g) ∆H3
不同压强下,按照n(CO2):n(H2)=1:3投料,CO2平衡转化率随温度变化关系如图。下列说法正确的是

| A.∆H3=-40.9 kJ/mol |
| B.p1 < p2 < p3 |
| C.为同时提高CO2的平衡转化率和CH3OH的平衡产率,反应条件应选择高温、高压 |
| D.T1温度时,三条曲线几乎交于一点的原因是:该温度下,主要发生反应③ |
您最近一年使用:0次
2021-04-04更新
|
1234次组卷
|
10卷引用:北京市丰台区2021届高三一模化学试题
北京市丰台区2021届高三一模化学试题(已下线)押山东卷第14题 化学反应速率和平衡-备战2021年高考化学临考题号押题(山东卷)河北省武邑中学2021届高考七模化学试题黑龙江省大庆铁人中学2021-2022学年高二上学期开学考试化学试题湖南省武冈市第一中学2021-2022学年高三下学期5月月考化学试题湖南省邵阳市第二中学2021-2022学年高一下学期期末考试化学试题北京市顺义牛栏山第一中学2022-2023学年高二上学期期中考试化学试题北京市第一七一中学2023-2024学年高二上学期期中考试化学试题山东省烟台市龙口市2023-2024学年高二上学期10月统考化学试题云南省保山市腾冲市第八中学2020-2021学年高二下学期期中考试化学试卷
填空题
|
适中(0.65)
|
2 . 二氧化碳的捕集、利用与封存(CCUS)是我国能源领域的一个重要战略方向,CCUS或许发展成一项重要的新兴产业。
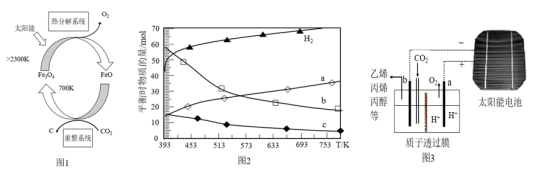
(1)国外学者提出的由CO2制取C的太阳能工艺如图1所示。
①“热分解系统”发生的反应为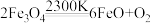 ,每分解1 mol Fe3O4转移的电子数为
,每分解1 mol Fe3O4转移的电子数为________ 。
②“重整系统”发生反应的化学方程式为________________________________ 。
(2)二氧化碳催化加氢合成低碳烯烃是目前研究的热门课题,起始时以0.1 MPa, 的投料比充入反应器中,发生反应:
的投料比充入反应器中,发生反应: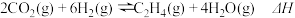 ,不同温度下平衡时的四种气态物质的物质的量如图2所示:
,不同温度下平衡时的四种气态物质的物质的量如图2所示:
①曲线b表示的物质为________ (写化学式)。②该反应的
________ 0。(填:“>”或“<”)
③为提高CO2的平衡转化率,除改变温度外,还可采取的措施是________________ (列举1项)。
(3)据报道以二氧化碳为原料采用特殊的电极电解强酸性的二氧化碳水溶液可得到多种燃料,其原理如题图3所示。
①该工艺中若选择用熔融K2CO3作介质的甲烷燃料电池替代太阳能电池,则负极反应式为________ 。
②电解时其中b极上生成乙烯的电极反应式为________________________________ 。

(1)国外学者提出的由CO2制取C的太阳能工艺如图1所示。
①“热分解系统”发生的反应为
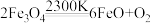 ,每分解1 mol Fe3O4转移的电子数为
,每分解1 mol Fe3O4转移的电子数为②“重整系统”发生反应的化学方程式为
(2)二氧化碳催化加氢合成低碳烯烃是目前研究的热门课题,起始时以0.1 MPa,
 的投料比充入反应器中,发生反应:
的投料比充入反应器中,发生反应: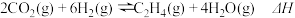 ,不同温度下平衡时的四种气态物质的物质的量如图2所示:
,不同温度下平衡时的四种气态物质的物质的量如图2所示:①曲线b表示的物质为

③为提高CO2的平衡转化率,除改变温度外,还可采取的措施是
(3)据报道以二氧化碳为原料采用特殊的电极电解强酸性的二氧化碳水溶液可得到多种燃料,其原理如题图3所示。
①该工艺中若选择用熔融K2CO3作介质的甲烷燃料电池替代太阳能电池,则负极反应式为
②电解时其中b极上生成乙烯的电极反应式为
您最近一年使用:0次
3 . 为减少碳氧化物的排放,工业上可回收 和
和 合成甲醇(
合成甲醇( )。
)。
(1)利用 和
和 反应合成甲醇时发生两个平行反应:
反应合成甲醇时发生两个平行反应:
反应Ⅰ
反应Ⅱ
控制 和
和 初始投料比为
初始投料比为 ,温度对
,温度对 平衡转化率及甲醇和
平衡转化率及甲醇和 产率的影响如图所示:
产率的影响如图所示:
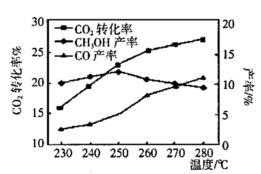
①反应Ⅰ能自发的反应条件:______ 。(填“低温”、“高温”、“任何温度”)
②由图可知温度升高 的产率上升,其主要原因可能是
的产率上升,其主要原因可能是______ 。
③由图可知获取 最适宜的温度是
最适宜的温度是______ 。
④控制 和
和 初始投料比为
初始投料比为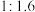 ,在
,在 时反应Ⅰ已达到平衡状态,
时反应Ⅰ已达到平衡状态, 的转化率为
的转化率为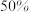 ,甲醇选择性为
,甲醇选择性为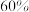 ,此时容器的体积为
,此时容器的体积为 ,若
,若 初始加入量为
初始加入量为 ,则反应Ⅰ的平衡常数是
,则反应Ⅰ的平衡常数是______ 。(甲醇的选择性:转化的 中生成甲醇的百分比)
中生成甲醇的百分比)
(2)利用 和
和 在一定条件下亦可合成甲醇,发生如下反应:
在一定条件下亦可合成甲醇,发生如下反应:
反应Ⅲ
其两种反应过程中能量的变化曲线如图中a、b所示,下列说法正确的是______ 。
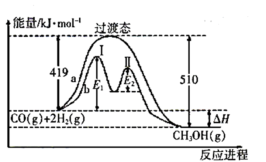
A. 上述反应的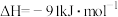
B. 反应正反应的活化能为
反应正反应的活化能为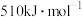
C. 过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
D. 过程使用催化剂后降低了反应的活化能和
过程使用催化剂后降低了反应的活化能和
E. 过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
(3)甲和乙两个恒容密闭容器的体积相同,向甲中加入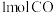 和
和 ,向乙中加入
,向乙中加入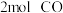 和
和 ,发生反应Ⅲ,测得不同温度下甲中
,发生反应Ⅲ,测得不同温度下甲中 的平衡转化率如图所示,请在图中画出不同温度下乙容器中
的平衡转化率如图所示,请在图中画出不同温度下乙容器中 的平衡转化率变化趋势的曲线
的平衡转化率变化趋势的曲线______ 。
(4)反应Ⅰ生成的甲醇常用作燃料电池的原料,请写出以甲醇、空气、氢氧化钾溶液为原料,石墨为电极构成的燃料电池的负极电极方程式______ 。
 和
和 合成甲醇(
合成甲醇( )。
)。(1)利用
 和
和 反应合成甲醇时发生两个平行反应:
反应合成甲醇时发生两个平行反应:反应Ⅰ

反应Ⅱ

控制
 和
和 初始投料比为
初始投料比为 ,温度对
,温度对 平衡转化率及甲醇和
平衡转化率及甲醇和 产率的影响如图所示:
产率的影响如图所示:
①反应Ⅰ能自发的反应条件:
②由图可知温度升高
 的产率上升,其主要原因可能是
的产率上升,其主要原因可能是③由图可知获取
 最适宜的温度是
最适宜的温度是④控制
 和
和 初始投料比为
初始投料比为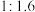 ,在
,在 时反应Ⅰ已达到平衡状态,
时反应Ⅰ已达到平衡状态, 的转化率为
的转化率为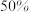 ,甲醇选择性为
,甲醇选择性为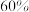 ,此时容器的体积为
,此时容器的体积为 ,若
,若 初始加入量为
初始加入量为 ,则反应Ⅰ的平衡常数是
,则反应Ⅰ的平衡常数是 中生成甲醇的百分比)
中生成甲醇的百分比)(2)利用
 和
和 在一定条件下亦可合成甲醇,发生如下反应:
在一定条件下亦可合成甲醇,发生如下反应:反应Ⅲ

其两种反应过程中能量的变化曲线如图中a、b所示,下列说法正确的是

A. 上述反应的
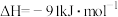
B.
 反应正反应的活化能为
反应正反应的活化能为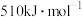
C.
 过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应D.
 过程使用催化剂后降低了反应的活化能和
过程使用催化剂后降低了反应的活化能和
E.
 过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
过程的反应速率:第Ⅱ阶段>第Ⅰ阶段(3)甲和乙两个恒容密闭容器的体积相同,向甲中加入
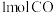 和
和 ,向乙中加入
,向乙中加入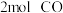 和
和 ,发生反应Ⅲ,测得不同温度下甲中
,发生反应Ⅲ,测得不同温度下甲中 的平衡转化率如图所示,请在图中画出不同温度下乙容器中
的平衡转化率如图所示,请在图中画出不同温度下乙容器中 的平衡转化率变化趋势的曲线
的平衡转化率变化趋势的曲线
(4)反应Ⅰ生成的甲醇常用作燃料电池的原料,请写出以甲醇、空气、氢氧化钾溶液为原料,石墨为电极构成的燃料电池的负极电极方程式
您最近一年使用:0次
名校
4 . 利用现代传感技术探究压强对 2NO2(g)  N2O4(g)平衡移动的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的 NO2气体后密封并保持活塞位置不变。分别在 t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。下列分析中不正确的是
N2O4(g)平衡移动的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的 NO2气体后密封并保持活塞位置不变。分别在 t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。下列分析中不正确的是
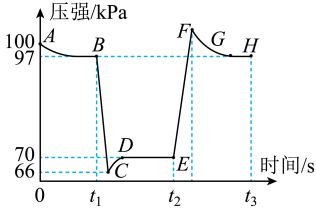
 N2O4(g)平衡移动的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的 NO2气体后密封并保持活塞位置不变。分别在 t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。下列分析中不正确的是
N2O4(g)平衡移动的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的 NO2气体后密封并保持活塞位置不变。分别在 t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。下列分析中不正确的是
| A.t1时移动活塞,使容器体积增大 |
| B.在 B、E 两点,对应的正反应速率:v(B)>v(E) |
| C.图中除 A、C、F 点外,其他点均为平衡状态 |
| D.在 E,F,H 三点中,H 点的气体平均相对分子质量最大 |
您最近一年使用:0次
2021-01-11更新
|
559次组卷
|
3卷引用:湖南省株洲市2021届高三教学质量统一检测(一)化学试题
湖南省株洲市2021届高三教学质量统一检测(一)化学试题湖南师范大学附属中学2022届高三月考(七)化学试题(已下线)专题09 化学反应速率与化学平衡(练)-2023年高考化学二轮复习讲练测(新高考专用)
名校
解题方法
5 . 某密闭容器内,可逆反应2X(?) ⇌ Y(g)+Z(s)达到平衡。则有
| A.恒容时升高温度,气体的密度增大,X一定为非气态物质 |
| B.恒温时缩小容积,气体的相对平均分子量有可能不变 |
| C.恒温恒容时,加入少量Z,则平衡向左移动 |
| D.恒温恒容时催化剂加入,Z的质量会增加 |
您最近一年使用:0次
2020-12-31更新
|
336次组卷
|
4卷引用:上海市奉贤区2021届高三一模化学试卷
上海市奉贤区2021届高三一模化学试卷(已下线)练习8 化学平衡的移动-2020-2021学年【补习教材·寒假作业】高二化学(苏教版)上海市行知中学2021届高三下学期3月月考化学试题(已下线)第七章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测
解题方法
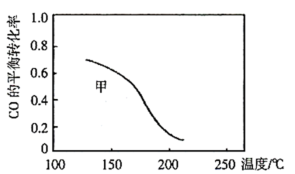
6 . CH4和CO2在催化剂作用下反应:CH4(g)+CO2(g) 2CO(g)+2H2(g)-247kJ完成下列填空:
2CO(g)+2H2(g)-247kJ完成下列填空:
(1)有利于提高CH4平衡转化率的措施是___ (任写两条)。
(2)该反应温度控制在550~750℃之间,从反应速率角度分析,选择该温度范围的可能原因:___ 。
(3)CH4和CO2各1mol充入密闭容器中,发生上述反应。
①300℃,100kPa,反应达到平衡时CO2体积分数与温度的关系如图中曲线所示。则n(平衡时气体):n(初始气体)=___ 。
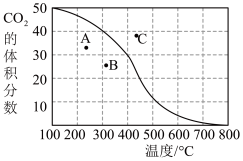
②若A、B、C三点表示不同温度和压强下已达平衡时CO2体积分数,___ 点对应的平衡常数最小,理由是:___ ;___ 点对应压强最大,理由是:___ 。
(4)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应又使积碳量减少:
积碳反应:CH4(g) C(s)+2H2(g)-75kJ
C(s)+2H2(g)-75kJ
消碳反应:CO2(g)+C(s) 2CO(g)-172kJ
2CO(g)-172kJ
一定时间内,积碳量和反应温度的关系如图所示。
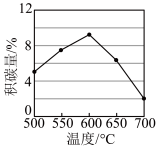
①一定温度,增大CO2的浓度有助于减少积碳,其原因是:___ 。
②温度高于600℃,积碳量减少的可能原因是:___ (任写一条)。
 2CO(g)+2H2(g)-247kJ完成下列填空:
2CO(g)+2H2(g)-247kJ完成下列填空:(1)有利于提高CH4平衡转化率的措施是
(2)该反应温度控制在550~750℃之间,从反应速率角度分析,选择该温度范围的可能原因:
(3)CH4和CO2各1mol充入密闭容器中,发生上述反应。
①300℃,100kPa,反应达到平衡时CO2体积分数与温度的关系如图中曲线所示。则n(平衡时气体):n(初始气体)=

②若A、B、C三点表示不同温度和压强下已达平衡时CO2体积分数,
(4)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应又使积碳量减少:
积碳反应:CH4(g)
 C(s)+2H2(g)-75kJ
C(s)+2H2(g)-75kJ消碳反应:CO2(g)+C(s)
 2CO(g)-172kJ
2CO(g)-172kJ一定时间内,积碳量和反应温度的关系如图所示。

①一定温度,增大CO2的浓度有助于减少积碳,其原因是:
②温度高于600℃,积碳量减少的可能原因是:
您最近一年使用:0次
2020-12-30更新
|
269次组卷
|
2卷引用:上海市杨浦区2021届高三一模化学试卷
名校
解题方法
7 . 一定条件下,可逆反应N2+3H2 2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是
2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是
 2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是
2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是 | A.加催化剂,v正、v逆都发生变化,且变化的倍数相等 |
| B.加压,v正、v逆都增大,且v正增大的倍数大于v逆增大的倍数 |
| C.降温,v正、v逆都减小,且v正减小的倍数大于v逆减小的倍数 |
| D.增大氮气的浓度,N2转化率减小,H2转化率增大 |
您最近一年使用:0次
2020-12-27更新
|
112次组卷
|
3卷引用:西藏林芝市第二高级中学2020-2021学年高二上学期期中考试理综化学试题
名校
8 . 如图所示,左室容积为右室的两倍,温度相同,现分别按照如图所示的量充入气体,同时加入少量固体催化剂使两室内气体充分反应达到平衡,打开活塞,继续反应再次达到平衡,下列说法正确的是( )
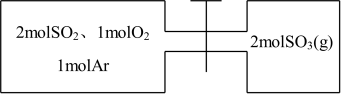

| A.第一次平衡时,SO2的物质的量左室更多 |
| B.充入气体未反应前,左室压强比右室大 |
| C.第一次平衡时,左室内压强一定小于右室 |
| D.第二次平衡时,SO2的总物质的量比第一次平衡时左室SO2的物质的量的2倍还要多 |
您最近一年使用:0次
2020-11-26更新
|
398次组卷
|
6卷引用:内蒙古赤峰市2018届高三4月模拟理科综合化学试题
19-20高二·江西南昌·阶段练习
9 . 一定温度下,向2.0L恒容密闭容器中充入1.0molPCl5反应: PCl5(g) PCl3(g)+Cl2(g),经一段时间后达到平衡。反应过程中测定的部分数据见下表。下列说法正确的是
PCl3(g)+Cl2(g),经一段时间后达到平衡。反应过程中测定的部分数据见下表。下列说法正确的是
 PCl3(g)+Cl2(g),经一段时间后达到平衡。反应过程中测定的部分数据见下表。下列说法正确的是
PCl3(g)+Cl2(g),经一段时间后达到平衡。反应过程中测定的部分数据见下表。下列说法正确的是t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A.反应在前50s的平均速率 (PCl3)=0.0032mol/(L·s) (PCl3)=0.0032mol/(L·s) |
| B.该条件下,反应的平衡常数K=0.05 |
| C.保持其它条件不变,向容器中充入PCl5(g),则PCl5的转化率增大 |
D.其它条件相同时,向空的容器中充入1.0molPCl5、0.20molPC13和0.20molCl2,此时 (正)> (正)> (逆) (逆) |
您最近一年使用:0次
名校
10 . 一定温度下,在3个容积均为1.0 L的恒容密闭容器中发生反应:PCl5 (g)  PCl3(g)+Cl2(g)。下列说法错误的是
PCl3(g)+Cl2(g)。下列说法错误的是
 PCl3(g)+Cl2(g)。下列说法错误的是
PCl3(g)+Cl2(g)。下列说法错误的是| 容器编号 | 物质的起始浓度/(mol·L-1) | 物质的平衡浓度/(mol·L-1) | ||
 | 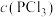 | 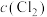 | 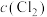 | |
| Ⅰ | 0.4 | 0 | 0 | 0.2 |
| Ⅱ | 0.6 | 0 | 0.2 | |
| Ⅲ | 0.8 | 0 | 0 | |
A.反应达到平衡时,容器I中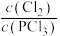 比容器Ⅱ中的小 比容器Ⅱ中的小 |
| B.反应达到平衡时,容器I与容器Ⅱ中的总压强之比为3︰4 |
C.反应达到平衡时,容器Ⅲ中 的体积分数小于 的体积分数小于 |
| D.反应达到平衡时,容器Ⅲ中0.4mol/L<c(PCl5)<0.8 mol/L |
您最近一年使用:0次
2020-09-29更新
|
716次组卷
|
6卷引用:江西省赣州市会昌县七校2021届高三联合9月月考化学试题



