名校
1 . 下列化学用语表示正确的是
A. 在水中的电离方程式: 在水中的电离方程式: |
B. 在水中的水解方程式: 在水中的水解方程式: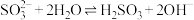 |
C.表示 燃烧热的热化学方程式: 燃烧热的热化学方程式: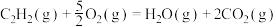  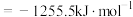 |
D.可逆反应 的平衡常数: 的平衡常数: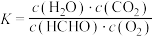 |
您最近一年使用:0次
2022-12-16更新
|
254次组卷
|
5卷引用:河南省洛阳市名校2022-2023学年高二上学期12月联考化学试题
名校
解题方法
2 . 下列相关条件下的离子方程式书写正确的是
A.侯德榜制碱法的反应之一: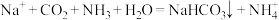 |
B.泡沫灭火器原理: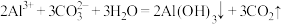 |
C.碳酸氢镁溶液中滴加过量的烧碱溶液: |
D.一定量的明矾溶液中滴加 溶液将 溶液将 完全沉淀时: 完全沉淀时: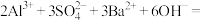 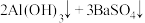 |
您最近一年使用:0次
2022-03-15更新
|
193次组卷
|
9卷引用:河南省信阳市2022-2023学年普通高中高三上学期第一次教学质量检测化学试题
河南省信阳市2022-2023学年普通高中高三上学期第一次教学质量检测化学试题湖南省五市十校教研教改共同体2021届高三上学期10月大联考化学试题山西省运城市景胜中学2020-2021学年高一10月月考化学试题黑龙江省肇东市第四中学校2020-2021学年高二上学期期中考试化学试题福建省福州市福建师范大学附属中学2021届高三上学期期中考试化学试题广东省河源中学2021届高三上学期第二次质量检测化学试题广东省佛山市第一中学2021届高三上学期期中考试化学试题广东省佛山市第一中学2021-2022学年高三上学期10月月考化学试题广东省中山市小榄中学2022-2023学年高三上学期第一次月考化学试题
解题方法
3 . 下列原理的应用及离子方程式书写均正确的是
A.用 水解制备 水解制备 (加大量水并加热): (加大量水并加热): |
B.泡沫灭火器原理: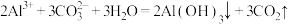 |
C.铅蓄电池放电时正极上的反应: |
D.某弱酸的酸式盐NaHB在水溶液中的水解: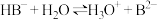 |
您最近一年使用:0次
名校
解题方法
4 . 能正确表示下列变化的离子方程式是
A.酸性高锰酸钾溶液与草酸溶液的反应:2MnO +5C2O +5C2O +16H+ =2Mn2+ + 10CO2↑+8H2O +16H+ =2Mn2+ + 10CO2↑+8H2O |
B.NaHSO3溶液的水解方程式:HSO +H2O +H2O H3O++SO H3O++SO |
C.泡沫灭火器原理:AlO +HCO +HCO +H2O=Al(OH)3↓+CO +H2O=Al(OH)3↓+CO |
D.用银作阳极电解稀盐酸:2Ag+2H++2Cl- H2↑+2AgCl H2↑+2AgCl |
您最近一年使用:0次
2022-09-06更新
|
155次组卷
|
2卷引用:河南省商丘名校2021-2022学年高二上学期期末联考化学试题
名校
5 . 按要求回答下列问题:
(1) 水解的离子方程式为
水解的离子方程式为_______
(2)25℃时,pH相同的醋酸和盐酸溶液分别用蒸馏水稀释至原来的m倍和n倍,若稀释后两溶液的pH仍相同,则m_______ n(填“>”“<”或“=”)
(3) 的电离常数依次为
的电离常数依次为 和
和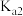 ,则
,则 的水解常数
的水解常数
_______ (用 和
和 的电离常数表示)
的电离常数表示)
(4)物质的量浓度相同的下列溶液:
① ②
② ③
③ ④
④ ⑤
⑤
按 由小到大排列的顺序是
由小到大排列的顺序是_______ (填序号)
(1)
 水解的离子方程式为
水解的离子方程式为(2)25℃时,pH相同的醋酸和盐酸溶液分别用蒸馏水稀释至原来的m倍和n倍,若稀释后两溶液的pH仍相同,则m
(3)
 的电离常数依次为
的电离常数依次为 和
和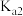 ,则
,则 的水解常数
的水解常数
 和
和 的电离常数表示)
的电离常数表示)(4)物质的量浓度相同的下列溶液:
①
 ②
② ③
③ ④
④ ⑤
⑤
按
 由小到大排列的顺序是
由小到大排列的顺序是
您最近一年使用:0次
2022-12-02更新
|
159次组卷
|
2卷引用:河南省郑州外国语学校2022-2023学年高二上学期期中考试化学试题
名校
解题方法
6 . 下列对应的方程式书写错误的是
A.盐酸中HCl的电离: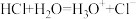 |
B.明矾用作净水剂: |
C.碳酸钠水溶液呈碱性: |
D.AgCl悬浊液中加入 溶液,沉淀逐渐变为黑色: 溶液,沉淀逐渐变为黑色: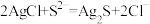 |
您最近一年使用:0次
2021-12-25更新
|
323次组卷
|
2卷引用:河南省安阳市第三十九中学2022-2023学年高二上学期第一次考试化学试题
名校
解题方法
7 . 下列解释事实的离子方程式不正确的是
A.泡沫灭火器的反应原理:Al3++3HCO =Al(OH)3↓+3CO2↑ =Al(OH)3↓+3CO2↑ |
B.用Na2S2O3做碘量法实验时,溶液pH不可太低:S2O +2H+=SO2↑+S↓+H2O +2H+=SO2↑+S↓+H2O |
C.MgCl2溶液显酸性的原因:Mg2++2H2O Mg(OH)2+2H+ Mg(OH)2+2H+ |
D.NaHSO3溶液的水解方程式:HSO +H2O +H2O H3O++SO H3O++SO |
您最近一年使用:0次
名校
8 . 氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)图1是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图(a、b均大于0),且已知:2CO(g)+2NO(g)=N2(g)+2CO2(g) △H=-ckJ·mol-1(c>0),请写出CO将NO2还原至N2时的热化学方程式____ 。

(2)图2是实验室在三个不同条件的密闭容器中合成氨时,N2的浓度随时间的变化曲线(以a、b、c表示)。已知三个条件下起始加入浓度均为:c(N2)=0.1mol·L-1,c(H2)=0.3mol·L-1;合成氨的反应:N2(g)+3H2(g) 2NH3(g) △H<0。
2NH3(g) △H<0。

①计算在曲线a达平衡时H2的转化率为____ 。
②由图2可知,b、c各有一个条件与a不同,则c的条件改变可能是____ ;写出判断b与a条件不同的理由____ 。
(3)利用图2中c条件下合成氨(容积固定)。已知化学平衡常数K与温度(T)的关系如表:
①试确定K1的相对大小,K1____ 4.1×106(填写“>”、“=”或“<”)
②恒温恒容时,下列各项能作为判断该反应达到化学平衡状态的依据的是____ 。
A.容器内NH3的浓度保持不变 B.2v(N2)正=v(H2)逆
C.容器内压强保持不变 D.混合气体的密度保持不变
(4)明矾[KAl(SO4)2·12H2O]可用作净水剂,是因为水解生成氢氧化铝胶体吸附水中的悬浮杂质。写出水解反应的离子方程式____
(1)图1是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图(a、b均大于0),且已知:2CO(g)+2NO(g)=N2(g)+2CO2(g) △H=-ckJ·mol-1(c>0),请写出CO将NO2还原至N2时的热化学方程式

(2)图2是实验室在三个不同条件的密闭容器中合成氨时,N2的浓度随时间的变化曲线(以a、b、c表示)。已知三个条件下起始加入浓度均为:c(N2)=0.1mol·L-1,c(H2)=0.3mol·L-1;合成氨的反应:N2(g)+3H2(g)
 2NH3(g) △H<0。
2NH3(g) △H<0。
①计算在曲线a达平衡时H2的转化率为
②由图2可知,b、c各有一个条件与a不同,则c的条件改变可能是
(3)利用图2中c条件下合成氨(容积固定)。已知化学平衡常数K与温度(T)的关系如表:
| T/(K) | 298 | 398 | 498 | …… |
| K | 4.1×106 | K1 | K2 | …… |
②恒温恒容时,下列各项能作为判断该反应达到化学平衡状态的依据的是
A.容器内NH3的浓度保持不变 B.2v(N2)正=v(H2)逆
C.容器内压强保持不变 D.混合气体的密度保持不变
(4)明矾[KAl(SO4)2·12H2O]可用作净水剂,是因为水解生成氢氧化铝胶体吸附水中的悬浮杂质。写出水解反应的离子方程式
您最近一年使用:0次
2022-03-18更新
|
145次组卷
|
3卷引用:河南省豫北名校联盟2021-2022学年高二下学期第二次联考化学试题
解题方法
9 . 已知常温下, 的电离常数:
的电离常数: ,HCN的电离常数
,HCN的电离常数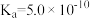 。下列方程式正确的是
。下列方程式正确的是
 的电离常数:
的电离常数: ,HCN的电离常数
,HCN的电离常数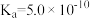 。下列方程式正确的是
。下列方程式正确的是A.HCN的电离方程式为 |
B.向 溶液中加入过量的HCN溶液: 溶液中加入过量的HCN溶液: |
C.向KCN溶液中通入少量的CO2: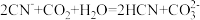 |
D. 溶液呈碱性: 溶液呈碱性: |
您最近一年使用:0次
10 . 已知:25℃时, 、
、 、
、 。
。

(1)常温下,将pH和体积均相同的 和
和 溶液分别稀释,溶液pH随加水体积的变化如图:
溶液分别稀释,溶液pH随加水体积的变化如图:
①曲线I代表___________ 溶液(填“ ”或“
”或“ ”)。
”)。
②a、b两点对应的溶液中,水的电离程度a___________ b(填“>”“<”或“=”)。
③向上述 溶液和
溶液和 溶液分别滴加等浓度的NaOH溶液,当恰好中和时,消耗NaOH溶液体积分别为
溶液分别滴加等浓度的NaOH溶液,当恰好中和时,消耗NaOH溶液体积分别为 和
和 ,则
,则
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
④酸度(AG)也可表示溶液的酸碱性, 。常温下,pH=2的硝酸溶液AG=
。常温下,pH=2的硝酸溶液AG=___________ 。
(2)25℃时,往 溶液中加入NaOH溶液。
溶液中加入NaOH溶液。
①当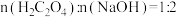 ,生成
,生成 ,
, 水解的离子方程式为
水解的离子方程式为___________ 。
②当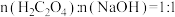 ,溶液显
,溶液显___________ 性(填“酸”、“碱”或“中”),
③等浓度等体积的 、
、 混合,溶液中
混合,溶液中
___________ 。
 、
、 、
、 。
。
(1)常温下,将pH和体积均相同的
 和
和 溶液分别稀释,溶液pH随加水体积的变化如图:
溶液分别稀释,溶液pH随加水体积的变化如图:①曲线I代表
 ”或“
”或“ ”)。
”)。②a、b两点对应的溶液中,水的电离程度a
③向上述
 溶液和
溶液和 溶液分别滴加等浓度的NaOH溶液,当恰好中和时,消耗NaOH溶液体积分别为
溶液分别滴加等浓度的NaOH溶液,当恰好中和时,消耗NaOH溶液体积分别为 和
和 ,则
,则
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。④酸度(AG)也可表示溶液的酸碱性,
 。常温下,pH=2的硝酸溶液AG=
。常温下,pH=2的硝酸溶液AG=(2)25℃时,往
 溶液中加入NaOH溶液。
溶液中加入NaOH溶液。①当
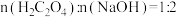 ,生成
,生成 ,
, 水解的离子方程式为
水解的离子方程式为②当
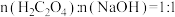 ,溶液显
,溶液显③等浓度等体积的
 、
、 混合,溶液中
混合,溶液中
您最近一年使用:0次



