名校
1 . 用相关化学反应原理解释下列问题。
(1)请用离子方程式表示热纯碱溶液除油污原理_______ 。
(2)请解释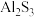 不能通过水溶液的离子反应制备,其原因是
不能通过水溶液的离子反应制备,其原因是_______ 。
(3)氯碱工业原理_______ 。
(4)难溶物ZnS作沉淀剂除去废水中 ,写出该过程的离子方程式
,写出该过程的离子方程式_______ 。
(5)将0.3mol的气态高能燃料乙硼烷( )在氧气中燃烧生成固态三氧化二硼和液态水,放出649.5kJ热量,该反应的热化学方程式为
)在氧气中燃烧生成固态三氧化二硼和液态水,放出649.5kJ热量,该反应的热化学方程式为_______ 。
(1)请用离子方程式表示热纯碱溶液除油污原理
(2)请解释
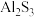 不能通过水溶液的离子反应制备,其原因是
不能通过水溶液的离子反应制备,其原因是(3)氯碱工业原理
(4)难溶物ZnS作沉淀剂除去废水中
 ,写出该过程的离子方程式
,写出该过程的离子方程式(5)将0.3mol的气态高能燃料乙硼烷(
 )在氧气中燃烧生成固态三氧化二硼和液态水,放出649.5kJ热量,该反应的热化学方程式为
)在氧气中燃烧生成固态三氧化二硼和液态水,放出649.5kJ热量,该反应的热化学方程式为
您最近一年使用:0次
2 . 下列属于水解方程式且书写正确的是
A. | B.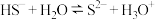 |
C.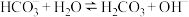 | D. |
您最近一年使用:0次
2022-11-30更新
|
94次组卷
|
2卷引用:河南省创新联盟2022-2023学年高二上学期第三次联考化学试题
3 . 请按要求用化学用语作答。
(1)已知 在氧气中燃烧完全转化为S单质放出
在氧气中燃烧完全转化为S单质放出 热量,完全转化为
热量,完全转化为 放出
放出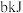 热量,写出表示
热量,写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式_______ 。
(2)明矾[化学式为 ]可以作净水剂的原因是
]可以作净水剂的原因是_______ (用离子方程式表示)。
(3)已知 是一种一元酸,写出它的正盐水解的离子方程式
是一种一元酸,写出它的正盐水解的离子方程式_______ 。
(4) 溶液可通过调节
溶液可通过调节 改变颜色,原因是
改变颜色,原因是_______ (用离子方程式表示)。
(5)将 固体放入水中,写出该反应的化学方程式
固体放入水中,写出该反应的化学方程式_______ 。
(1)已知
 在氧气中燃烧完全转化为S单质放出
在氧气中燃烧完全转化为S单质放出 热量,完全转化为
热量,完全转化为 放出
放出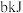 热量,写出表示
热量,写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式(2)明矾[化学式为
 ]可以作净水剂的原因是
]可以作净水剂的原因是(3)已知
 是一种一元酸,写出它的正盐水解的离子方程式
是一种一元酸,写出它的正盐水解的离子方程式(4)
 溶液可通过调节
溶液可通过调节 改变颜色,原因是
改变颜色,原因是(5)将
 固体放入水中,写出该反应的化学方程式
固体放入水中,写出该反应的化学方程式
您最近一年使用:0次
名校
4 . 下列化学用语表达正确的是
A. 的电离方程式: 的电离方程式: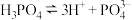 |
B.以 溶液为电解质溶液,氢氧燃料电池负极的电极反应式: 溶液为电解质溶液,氢氧燃料电池负极的电极反应式: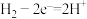 |
C. 水解的离子方程式: 水解的离子方程式: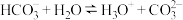 |
D. 的溶解平衡表达式: 的溶解平衡表达式: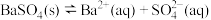 |
您最近一年使用:0次
2023-02-13更新
|
132次组卷
|
2卷引用:河南省商丘市第一高级中学2022-2023学年高二下学期3月份考试化学试题
5 . “ 还原法”制备高纯度氢碘酸和亚磷酸钠
还原法”制备高纯度氢碘酸和亚磷酸钠 的工业流程如图。
的工业流程如图。

已知:ⅰ. 为一元弱酸
为一元弱酸
ⅱ. 为二元酸,25℃时其电离常数:
为二元酸,25℃时其电离常数: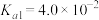 ,
,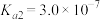
ⅲ.25℃时: ,
,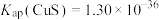
回答下列问题:
(1) 属于
属于______ (填“正盐”或“酸式盐”)。
(2)“合成”过程,主要氧化产物为 ,相应的化学方程式为
,相应的化学方程式为______ 。
(3)“除铜”过程发生的反应为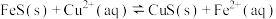 ,经过计算可得该反应的平衡常数
,经过计算可得该反应的平衡常数
______ 。
(4)常温下 的
的
______ 7(填“>”、“=”或“<”)。
(5)常温下 溶液呈碱性的原因为(用离子方程式表示)
溶液呈碱性的原因为(用离子方程式表示)______ 。
 还原法”制备高纯度氢碘酸和亚磷酸钠
还原法”制备高纯度氢碘酸和亚磷酸钠 的工业流程如图。
的工业流程如图。
已知:ⅰ.
 为一元弱酸
为一元弱酸ⅱ.
 为二元酸,25℃时其电离常数:
为二元酸,25℃时其电离常数: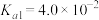 ,
,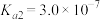
ⅲ.25℃时:
 ,
,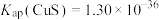
回答下列问题:
(1)
 属于
属于(2)“合成”过程,主要氧化产物为
 ,相应的化学方程式为
,相应的化学方程式为(3)“除铜”过程发生的反应为
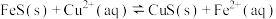 ,经过计算可得该反应的平衡常数
,经过计算可得该反应的平衡常数
(4)常温下
 的
的
(5)常温下
 溶液呈碱性的原因为(用离子方程式表示)
溶液呈碱性的原因为(用离子方程式表示)
您最近一年使用:0次
名校
解题方法
6 . 下列方程式书写正确的是
A.NaHCO3在水溶液中的电离方程式: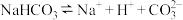 |
B.HS-的水解方程式: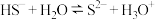 |
C. 的水解方程式: 的水解方程式: |
D.H2S的电离方程式:H2S H++HS- H++HS- |
您最近一年使用:0次
2022-01-19更新
|
193次组卷
|
3卷引用:河南省鹤壁市高中2023-2024学年高二上学期12月月考化学试题
解题方法
7 . 在下列过程中对应的离子方程式正确的是
A.银单质溶于稀硝酸:Ag+2H++ =Ag++NO↑+H2O =Ag++NO↑+H2O |
B.用标准草酸溶液滴定KMnO4:2 +16H++5 +16H++5 =2Mn2++10CO2↑+8H2O =2Mn2++10CO2↑+8H2O |
| C.醋酸钠溶液显碱性:H2O+CH3COO-=OH-+CH3COOH |
D.实验室用硫酸铜和碳酸钠溶液制备碱式碳酸铜:H2O+2Cu2++2 =Cu2(OH)2CO3↓+CO2↑ =Cu2(OH)2CO3↓+CO2↑ |
您最近一年使用:0次
解题方法
8 . 下列化学用语或图示表达不正确的是
A.砷原子的简化电子排布式为: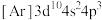 |
B. 的水解方程式: 的水解方程式: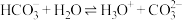 |
C.硫酸钡在水中的沉淀溶解平衡: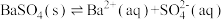 |
| D.一个电子从3p能级跃迁到3s能级,产生的原子光谱为发射光谱 |
您最近一年使用:0次
名校
解题方法
9 . 醋酸是日常生活中最常见的调味剂和重要的化工原料,醋酸钠是其常见的盐。[已知:25℃,Ka(CH3COOH)=1.69×10-5]。请回答下列问题:
(1)写出醋酸钠溶液中存在的平衡(离子方程式):___________ 。
(2)常温时,pH=3的醋酸和pH=11的NaOH溶液等体积混合后,溶液中c(Na+)___________ c(CH3COO-)(填“>”“<”或“=”),该溶液中电荷守恒表达式为___________ 。
(3)常温时,将mmol·L-1的醋酸和nmol·L-1的NaOH溶液等体积混合后,所得溶液的pH=7,则m与n的大小关系是m________ n,醋酸溶液中c(H+)_________ NaOH溶液中c(OH-)(填“>”“<”或“=”)。
(4)某小组研究25℃下CH3COOH电离平衡的影响因素。
提出假设稀释CH3COOH溶液或改变CH3COO-浓度,CH3COOH电离平衡会发生移动。
设计方案并完成实验用浓度均为0.1mol·L-1的CH3COOH和CH3COONa溶液,按下表配制总体积相同的系列溶液;测定pH,记录数据。
①根据表中信息,补充数据:a=___________ ,b=___________ 。
②由实验Ⅰ和Ⅱ可知,稀释CH3COOH溶液,电离平衡___________ (填“正”或“逆”)向移动;结合表中数据,给出判断理由:___________ 。
③由实验Ⅱ~Ⅷ可知,增大CH3COO-浓度,CH3COOH电离平衡逆向移动。
实验结论假设成立。
(1)写出醋酸钠溶液中存在的平衡(离子方程式):
(2)常温时,pH=3的醋酸和pH=11的NaOH溶液等体积混合后,溶液中c(Na+)
(3)常温时,将mmol·L-1的醋酸和nmol·L-1的NaOH溶液等体积混合后,所得溶液的pH=7,则m与n的大小关系是m
(4)某小组研究25℃下CH3COOH电离平衡的影响因素。
提出假设稀释CH3COOH溶液或改变CH3COO-浓度,CH3COOH电离平衡会发生移动。
设计方案并完成实验用浓度均为0.1mol·L-1的CH3COOH和CH3COONa溶液,按下表配制总体积相同的系列溶液;测定pH,记录数据。
| 序号 | V(CH3COOH)/mL | V(CH3COONa)/mL | V(H2O)/mL | n(CH3COONa)∶n(CH3COOH) | pH |
| Ⅰ | 40.00 | / | / | 0 | 2.86 |
| Ⅱ | 4.00 | / | 36.00 | 0 | 3.36 |
| … | |||||
| Ⅶ | 4.00 | a | b | 3∶4 | 4.53 |
| Ⅷ | 4.00 | 4.00 | 32.00 | 1∶1 | 4.65 |
②由实验Ⅰ和Ⅱ可知,稀释CH3COOH溶液,电离平衡
③由实验Ⅱ~Ⅷ可知,增大CH3COO-浓度,CH3COOH电离平衡逆向移动。
实验结论假设成立。
您最近一年使用:0次
名校
解题方法
10 . 下列解释实验现象的反应方程式不正确的是
A.向NaHSO4溶液中逐滴加入Ba(OH)2溶液,至溶液恰好呈中性:H++ +Ba2++OH-=BaSO4↓+H2O +Ba2++OH-=BaSO4↓+H2O |
| B.切开的金属Na暴露在空气中,光亮表面逐渐变暗:4Na+O2=2Na2O |
C.向Na2CO3溶液中滴入酚酞,溶液变红: +H2O⇌ +H2O⇌ +OH- +OH- |
| D.向AgCl悬浊液中滴加Na2S溶液,白色沉淀变为黑色:2AgCl(s)+S2-(aq)⇌Ag2S(s)+2Cl-(aq) |
您最近一年使用:0次



