名校
解题方法
1 . 2021年9月24日《科学》杂志发表了我国科学家的原创性重大突破,首次在实验室实现从 到淀粉的全合成。其合成路线如下:
到淀粉的全合成。其合成路线如下:
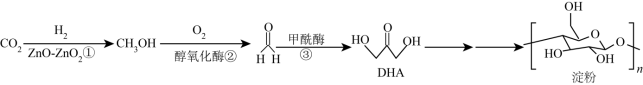
下列说法错误的是
 到淀粉的全合成。其合成路线如下:
到淀粉的全合成。其合成路线如下:
下列说法错误的是
| A.电负性:O>C>H>Zn |
| B.甲醇分子中H-C-O键角小于甲醛分子中H-C-O键角 |
| C.DHA分子间存在氢键 |
D.Zn2+溶于氨水形成配合物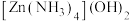 , , 的配位数为6 的配位数为6 |
您最近一年使用:0次
2022-03-20更新
|
319次组卷
|
3卷引用:河北省唐山市第一中学2022-2023学年高三上学期12月月考化学试题
2022·河北·模拟预测
2 . 硼及其化合物是用途广泛的化工原料,可以应用于新型材料的制备。回答下列问题:
(1)基态硼原子的价电子排布式为___________ ;与硼同周期且相邻的两种元素和硼的第一电离能由大到小的顺序为___________ 。
(2)碳化硼(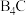 )硬度较大,可用于坦克车的装甲、避弹衣等。碳化硼的熔点为2350℃、沸点为3500℃,说明它属于
)硬度较大,可用于坦克车的装甲、避弹衣等。碳化硼的熔点为2350℃、沸点为3500℃,说明它属于___________ 晶体。原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的碳原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的碳原子,其价电子自旋磁量子数的代数和为___________ 。
(3)自然界中含硼钠盐是一种天然矿藏,其化学式为 ,实际上它的阴离子结构单元是由两个
,实际上它的阴离子结构单元是由两个 和两个
和两个 缩合而成的双六元环,应该写成
缩合而成的双六元环,应该写成 。其结构如图,它的阴离子可形成链状结构,则该晶体中不存在的作用力是
。其结构如图,它的阴离子可形成链状结构,则该晶体中不存在的作用力是___________ (填标号)。
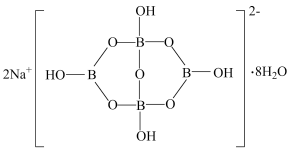
A.离子键 B.共价键 C.金属键 D.范德华力 E.氢键
(4) 的空间构型为
的空间构型为___________ , 的键角大于
的键角大于 的键角,解释其原因
的键角,解释其原因___________ 。
(5)某有机硼化物的结构简式如图2,该有机物中其他中心原子与B原子杂化类型相同的元素有___________ ,组成该有机物的第二周期元素电负性由大到小的顺序为___________ 。

(6)砷化硼的晶胞结构如图3,图4中矩形AA’C’C是沿晶胞对角面取得的截图。
①晶胞中各原子在矩形AA’C’C中的位置为___________ (填标号)。

②若晶胞的边长为apm,阿伏加德罗常数的值为 ,则晶体的密度为
,则晶体的密度为___________  (列出计算表达式)。
(列出计算表达式)。
(1)基态硼原子的价电子排布式为
(2)碳化硼(
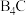 )硬度较大,可用于坦克车的装甲、避弹衣等。碳化硼的熔点为2350℃、沸点为3500℃,说明它属于
)硬度较大,可用于坦克车的装甲、避弹衣等。碳化硼的熔点为2350℃、沸点为3500℃,说明它属于 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的碳原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的碳原子,其价电子自旋磁量子数的代数和为(3)自然界中含硼钠盐是一种天然矿藏,其化学式为
 ,实际上它的阴离子结构单元是由两个
,实际上它的阴离子结构单元是由两个 和两个
和两个 缩合而成的双六元环,应该写成
缩合而成的双六元环,应该写成 。其结构如图,它的阴离子可形成链状结构,则该晶体中不存在的作用力是
。其结构如图,它的阴离子可形成链状结构,则该晶体中不存在的作用力是
A.离子键 B.共价键 C.金属键 D.范德华力 E.氢键
(4)
 的空间构型为
的空间构型为 的键角大于
的键角大于 的键角,解释其原因
的键角,解释其原因(5)某有机硼化物的结构简式如图2,该有机物中其他中心原子与B原子杂化类型相同的元素有

(6)砷化硼的晶胞结构如图3,图4中矩形AA’C’C是沿晶胞对角面取得的截图。
①晶胞中各原子在矩形AA’C’C中的位置为

②若晶胞的边长为apm,阿伏加德罗常数的值为
 ,则晶体的密度为
,则晶体的密度为 (列出计算表达式)。
(列出计算表达式)。
您最近一年使用:0次
23-24高三上·云南昆明·阶段练习
名校
3 . ZnS荧光材料的研究从1868年法国化学家Sidot发现至今已有近150年的历史。其中立方ZnS的晶胞如图所示,其晶胞参数为 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是
| A.电负性:Zn>S |
| B.S元素在元素周期表中位于s区 |
C.基态Zn原子的价层电子排布式为 |
D.立方ZnS晶体密度为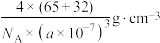 |
您最近一年使用:0次
名校
解题方法
4 . 传世名画之一的《千里江山图》中青绿山水用“绿青”[主要成分为CuCO3⋅Cu(OH)2]等矿物颜料绘制而成。下列有关说法正确的是
| A.氧元素位于元素周期表的s区 |
B. 中C原子的杂化方式为sp3 中C原子的杂化方式为sp3 |
| C.H、C、O三种元素的电负性由大到小的顺序:O>C>H |
D.“绿青”与盐酸反应的化学方程式为 |
您最近一年使用:0次
2024-03-07更新
|
232次组卷
|
3卷引用:河北省部分重点高中2023-2024学年高三上学期2月期末化学试题
名校
解题方法
5 . 下列陈述Ⅰ和陈述Ⅱ均正确,且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 三氟乙酸酸性强于三氯乙酸 | F原子电负性大于Cl原子,吸电子能力强 |
| B | 常温下,铜与稀硫酸不反应,与稀硝酸反应 | 硝酸酸性强于硫酸 |
| C | 常温下溶解度: 大于 大于 |  水解程度大于 水解程度大于 |
| D |  、 、 混合气体通入 混合气体通入 溶液中产生的白色沉淀是 溶液中产生的白色沉淀是 | 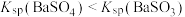 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 下列说法正确的是
| A.同一周期的元素中,第VIIA族元素的第一电离能最大 |
| B.中心原子是sp杂化的分子,其空间结构不一定为直线形 |
| C.电负性大于1.8的元素一定为非金属元素,小于1.8的一定为金属元素 |
| D.基态Mg原子失去第一个电子吸收的能量大于失去第二个电子吸收的能量 |
您最近一年使用:0次
2022-02-22更新
|
289次组卷
|
4卷引用:河北省邢台市四校联考2021-2022学年高二下学期第二次月考化学试题
解题方法
7 . 短周期主族元素W、X、Y、Z的原子序数依次增大,其中X、Y、Z同周期,X原子的电子数等于Y原子的最外层电子数。W、X、Y形成的分子的结构如图所示。下列说法正确的是
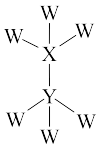

| A.电负性:W<X<Y<Z |
| B.W、Y、Z可形成离子晶体 |
| C.Y与Z形成的化合物均可被强碱溶液吸收 |
| D.W分别与Y、Z形成简单化合物的沸点:Y>Z |
您最近一年使用:0次
名校
解题方法
8 . 现有四种元素的基态原子的核外电子排布式如下:①1s22s22p3;②1s22s22p4;③1s22s22p63s23p2;④1s22s22p63s23p3。下列说法错误的是
| A.电负性:②>①>④>③ |
| B.原子半径:③>④>①>② |
| C.第一电离能:②>①>④>③ |
| D.简单气态氢化物的稳定性:②>①>④>③ |
您最近一年使用:0次
2022-01-24更新
|
517次组卷
|
3卷引用:河北省邯郸市永年区第二中学2023-2024学年高二上学期12月月考化学试题
名校
9 . 2021年9月24日《科学》杂志发表了我国科学家的原创性重大突破,首次在实验室实现从CO2到淀粉的全合成。其合成路线如下:
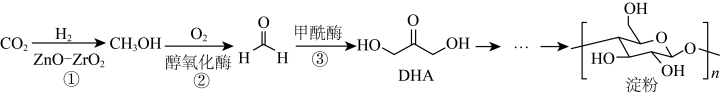
下列说法错误的是

下列说法错误的是
| A.电负性:O>C>H>Zn |
| B.Zn2+溶于氨水形成配合物[Zn(NH3)4](OH)2,Zn2+的配位数为6 |
| C.DHA分子间存在氢键 |
| D.甲醇分子中H-C-O键角小于甲醛分子中H-C-O键角 |
您最近一年使用:0次
2022-04-22更新
|
280次组卷
|
6卷引用:河北省衡水市第十四中学2022-2023学年高二下学期第一次选择性考试化学试题
10 . 氮化锗(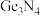 )具有耐腐蚀、硬度高等优点,应用广泛。下列说法正确的是
)具有耐腐蚀、硬度高等优点,应用广泛。下列说法正确的是
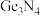 )具有耐腐蚀、硬度高等优点,应用广泛。下列说法正确的是
)具有耐腐蚀、硬度高等优点,应用广泛。下列说法正确的是| A.锗是金属,不能做半导体材料 |
| B.第4周期基态原子与锗未成对电子数相等的元素共有2种 |
C.基态锗原子的电子排布式可表示为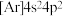 |
| D.氮化锗中氮显-3价,说明氮的电负性比锗大 |
您最近一年使用:0次
2022-10-08更新
|
278次组卷
|
2卷引用:河北省石家庄市第十七中学2022-2023高二下学期第一次月考化学试题



