名校
解题方法
1 . 化合物XYZ4ME4可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为nsn-1,X与M同周期,E在地壳中含量最多。下列说法正确的是
| A.元素电负性:E>Y>Z | B.1mol M中含有共价键数目为4NA |
| C.半径:X2+>E2- | D.YZ3和YE 的空间结构均为三角锥形 的空间结构均为三角锥形 |
您最近一年使用:0次
名校
2 . 下列有关比较正确的是
A.熔点: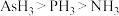 |
B.稳定性: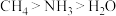 |
C.酸性: |
D.键角: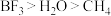 |
您最近一年使用:0次
名校
解题方法
3 . 蓝铜矿的主要成分为2CuCO3·Ca(OH)2,将它与焦炭一起加热可以生成Cu、CO2和H2O。下列说法正确的是
| A.Cu是第四周期第ⅦB族元素 |
| B.0.1mol[Cu(H2O)4]2+中所含配位键的物质的量为0.8mol |
| C.电负性:O>C>H |
| D.将0.1L0.1mol/L[Cu(NH3)4](OH)2加入足量的MgCl2溶液中,理论上可得到0.2molMg(OH)2 |
您最近一年使用:0次
名校
解题方法
4 . 黑火药的主要成分为木炭(C)、硫黄(S)和火硝 。请回答下列问题。
。请回答下列问题。
(1)基态碳原子的电子排布式为_______ 。
(2)下列轨道表示式能表示基态氮原子的核外电子排布的是_______(填标号)。
(3)C、N、O三种元素的第一电离能由大到小的顺序为_______ 。
(4)Se元素位于第4周期,与O、S同主族。
①基态Se原子中具有_______ 种运动状态不同的电子。其中能量最高的电子占据轨道的形状为_______ 。
②O、S、Se三种元素的电负性依次_______ (填“增大”或“减小”)。
(5)用铂丝蘸取 溶液,在酒精灯火焰上灼烧,透过蓝色钴玻璃观察到火焰呈紫色,从微观角度解释产生该现象的原因是
溶液,在酒精灯火焰上灼烧,透过蓝色钴玻璃观察到火焰呈紫色,从微观角度解释产生该现象的原因是_______ 。第4周期元素的基态原子中,与基态K原子具有相同最外层电子数的是_______ (填元素符号)。
 。请回答下列问题。
。请回答下列问题。(1)基态碳原子的电子排布式为
(2)下列轨道表示式能表示基态氮原子的核外电子排布的是_______(填标号)。
A.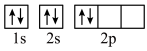 | B.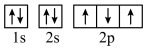 |
C.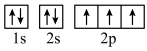 | D.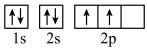 |
(3)C、N、O三种元素的第一电离能由大到小的顺序为
(4)Se元素位于第4周期,与O、S同主族。
①基态Se原子中具有
②O、S、Se三种元素的电负性依次
(5)用铂丝蘸取
 溶液,在酒精灯火焰上灼烧,透过蓝色钴玻璃观察到火焰呈紫色,从微观角度解释产生该现象的原因是
溶液,在酒精灯火焰上灼烧,透过蓝色钴玻璃观察到火焰呈紫色,从微观角度解释产生该现象的原因是
您最近一年使用:0次
名校
解题方法
5 . 物质W常用作漂白剂和氧化剂,其构成元素均为短周期主族元素,各元素原子半径与原子序数关系如下图所示,实验室常用 洗涤残留在试管壁上的Q单质。下列说法正确的是
洗涤残留在试管壁上的Q单质。下列说法正确的是
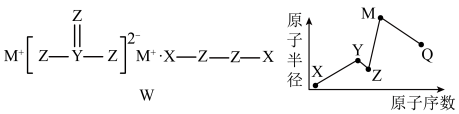
 洗涤残留在试管壁上的Q单质。下列说法正确的是
洗涤残留在试管壁上的Q单质。下列说法正确的是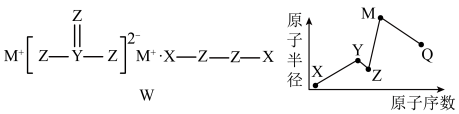
A.X可分别与Y、Z、Q形成 微粒 微粒 |
| B.Z分别与X、M形成的化合物所含化学键类型相同 |
| C.氢化物的沸点:Z>Y |
| D.电负性:M<Y<X<Z |
您最近一年使用:0次
6 . 下列说法正确的是
A. 的空间结构与其VSEPR模型相同 的空间结构与其VSEPR模型相同 |
B.氢键 中的三原子均在一条直线上 中的三原子均在一条直线上 |
| C.基态O原子核外电子的运动状态有8种 |
| D.第一电离能和电负性的大小可分别作为判断元素金属性和非金属性强弱的依据 |
您最近一年使用:0次
解题方法
7 . 卢瑟福发现质子的核反应为 ;卢瑟福的学生查德威克发现中子的核反应为
;卢瑟福的学生查德威克发现中子的核反应为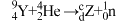 。下列说法错误的是
。下列说法错误的是
 ;卢瑟福的学生查德威克发现中子的核反应为
;卢瑟福的学生查德威克发现中子的核反应为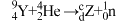 。下列说法错误的是
。下列说法错误的是| A.Y元素的第一电离能高于同周期相邻元素的 |
B.元素的电负性: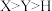 |
C. 和 和 的简单氢化物中中心原子的价层电子对数目相同 的简单氢化物中中心原子的价层电子对数目相同 |
D. 的空间结构为直线形 的空间结构为直线形 |
您最近一年使用:0次
名校
解题方法
8 . 物质的结构决定其性质。下列实例与解释不相符的是
选项 | 实例 | 解释 |
A | CO的沸点高于N2 | CO的极性大于N2 |
B | 酸性: | 羟基极性: |
C | 金刚石的熔点远高于C60 | 两种晶体中C—C键的键能不同 |
D | 室温下,将50 mL CH3COOH与50 mL苯混合,混合溶液体积为101 mL | 混合过程中削弱了CH3COOH分子间的氢键,且苯与CH3COOH分子间作用力弱于氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 在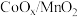 催化下醇的氧化氰化反应如图所示。下列叙述正确的是
催化下醇的氧化氰化反应如图所示。下列叙述正确的是
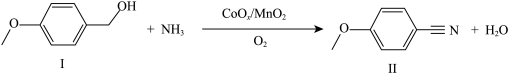
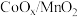 催化下醇的氧化氰化反应如图所示。下列叙述正确的是
催化下醇的氧化氰化反应如图所示。下列叙述正确的是
| A.熔点:Ⅰ>Ⅱ | B.Ⅰ所属类别为酚类 |
| C.Ⅰ和Ⅱ分子中σ键数目相同 | D.Ⅱ含有的元素中 的电负性最大 的电负性最大 |
您最近一年使用:0次
2013·河北邯郸·二模
10 . 冰晶石(Na3AlF6)是工业上冶炼铝的助熔剂,制取冰晶石(Na3AlF6)的化学方程式为2Al(OH)3+12HF+3A =2Na3AlFs+3CO2+9H2O。
(1)熔融晶体A时痛要破坏的作用力是_______ ,冰晶石中的配位体是______ 。
(2)上述反应的生成物中属于非极性分子的中心原子的杂化轨道类型为________________ ,该分子的空间构型为___________ 。
(3)上述反应的反应物中有两种元素在元素周期表中的位置相邻,用化学方程式表示二者的电负性大小:____________ ;写出含有其中电负性较小元素的原子,且形成的分子的空间构型呈“V”形的物质的化学式(单质和化合物各写一种)_______________ 、________________ 。
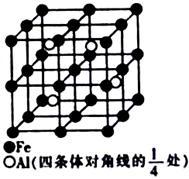
(4)某种Al—Fe合金的晶胞如图所示,该合金的化学式为_________ 。若晶胞的边长为a nm,则合金的密度为______ g• cm-3。
(1)熔融晶体A时痛要破坏的作用力是
(2)上述反应的生成物中属于非极性分子的中心原子的杂化轨道类型为
(3)上述反应的反应物中有两种元素在元素周期表中的位置相邻,用化学方程式表示二者的电负性大小:
(4)某种Al—Fe合金的晶胞如图所示,该合金的化学式为

您最近一年使用:0次

 强于
强于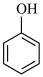
 强于
强于


