1 . 2021年9月24日《科学》杂志发表了我国科学家的原创性重大突破,首次在实验室实现从CO2到淀粉的全合成。其合成路线如下:
CO2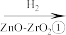 CH3OH
CH3OH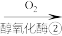
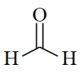
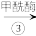
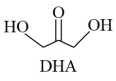
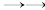
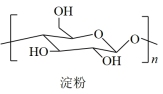
下列说法错误的是
CO2
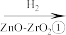 CH3OH
CH3OH



下列说法错误的是
| A.电负性:O>C>H>Zn |
| B.甲醇分子中H-C-O键角小于甲醛分子中H-C-O键角 |
| C.DHA分子间存在氢键 |
| D.Zn溶于氨水形成配合物[Zn(NH3)4](OH)2,Zn2+的配位数为6 |
您最近一年使用:0次
2022-03-04更新
|
944次组卷
|
3卷引用:山东省潍坊市2022届高三普通高等学校招生全国统一考试(一模)化学试题
山东省潍坊市2022届高三普通高等学校招生全国统一考试(一模)化学试题(已下线)回归教材重难点11 物质结构与性质-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)新疆石河子第一中学2021-2022学年高二4月月考化学试题
名校
2 . 短周期元素X、Y、Z、W、R的原子序数依次增大,Y与W同主族,Z与R同主族,它们形成的甲、乙两种物质(如图)是有机合成中常用的还原剂。下列说法正确的是
甲: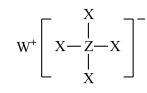 ,乙:
,乙: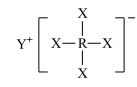
甲:
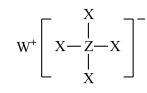 ,乙:
,乙: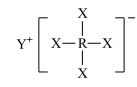
| A.电负性:X>Z>R |
| B.第一电离能:Y<Z<R |
| C.元素Z和R最高价氧化物对应的水化物都具有两性 |
| D.单质Y和W在空气中燃烧的产物所含化学键类型完全相同 |
您最近一年使用:0次
2022-03-03更新
|
722次组卷
|
6卷引用:山东省淄博市2022届高三下学期第一次模拟考试化学试题
山东省淄博市2022届高三下学期第一次模拟考试化学试题广东省佛山市第四中学2021-2022学年高二下学期3月段考化学试题(已下线)专项08 物质结构 元素周期律-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)福建省福安市第一中学2023届高三上学期第一次检测化学试题云南省富源县第一中学2021-2022学年高三下学期4月月考化学试题福建省福清虞阳中学2023-2024学年高三上学期第一次综合训练化学试题
21-22高三下·辽宁沈阳·开学考试
名校
3 . 近年来,光催化剂的研究是材料领域的热点方向。一种Ru配合物(如图所示)复合光催化剂可将CO2转化为HCOOH。下列说法错误的是
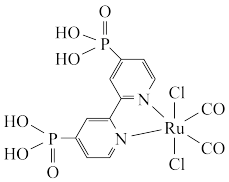

| A.Ru配合物中第二周期元素的电负性由大到小的顺序为O>N>C |
B.如图结构的吡啶环(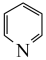 )中C、N原子的杂化方式均为sp2 )中C、N原子的杂化方式均为sp2 |
| C.该配合物中Ru的配位数是6 |
| D.HCOOH的沸点比HCHO高,主要因为HCOOH相对分子质量大于HCHO |
您最近一年使用:0次
2022-02-27更新
|
1087次组卷
|
7卷引用:化学-2022年高考考前押题密卷(山东卷)
(已下线)化学-2022年高考考前押题密卷(山东卷)辽宁省沈阳市第二中学2021-2022学年高三下学期学期初考试化学试题(已下线)押新高考卷08题 物质结构与性质-备战2022年高考化学临考题号押题(新高考通版)(已下线)第十二章 物质结构与性质(测)-2023年高考化学一轮复习讲练测(全国通用)(已下线)专题33 物质结构与性质基础-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)T9-物质结构江苏省锡东高级中学2023-2024学年高二上学期期中考试化学试卷
解题方法
4 . ⅤA族元素及其化合物在材料等方面有重要用途。根据所学知识回答下列问题:
(1)基态砷原子处于最高能级的电子云轮廓图为_______ 形。
(2) 、
、 、
、 是同主族元素的氢化物,其中键角最小的是
是同主族元素的氢化物,其中键角最小的是_______ 。
(3)叠氮化钠( )用于汽车的安全气囊中,当发生车祸时迅速分解放出氮气,使安全气囊充气。可与酸反应生成叠氮酸(
)用于汽车的安全气囊中,当发生车祸时迅速分解放出氮气,使安全气囊充气。可与酸反应生成叠氮酸( ),叠氮酸中3个氮原子的杂化类型分别为
),叠氮酸中3个氮原子的杂化类型分别为_______ (不分先后)。
(4)N原子之间可以形成π键,而 原子之间较难形成π键。从原子结构角度分析,其原因为
原子之间较难形成π键。从原子结构角度分析,其原因为_______ 。
(5)往硫酸铜溶液中加入过量氨水,可生成配离子 。已知
。已知 与
与 的空间构型都是三角锥形,但
的空间构型都是三角锥形,但 不易与
不易与 形成配离子,其原因是
形成配离子,其原因是_______ 。
(6)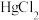 和不同浓度
和不同浓度 反应得到某种含汞化合物的晶胞结构(有四个等同的小立方体)如图所示。(部分微粒不在晶胞内,每个
反应得到某种含汞化合物的晶胞结构(有四个等同的小立方体)如图所示。(部分微粒不在晶胞内,每个 原子均处于小立方体的面心)
原子均处于小立方体的面心)
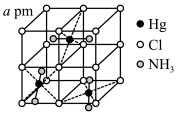
写出该含汞化合物的化学式:_______ 。则该晶体的密度
_______  (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 ,用含a、
,用含a、 的代数式表示)。
的代数式表示)。
(1)基态砷原子处于最高能级的电子云轮廓图为
(2)
 、
、 、
、 是同主族元素的氢化物,其中键角最小的是
是同主族元素的氢化物,其中键角最小的是(3)叠氮化钠(
 )用于汽车的安全气囊中,当发生车祸时迅速分解放出氮气,使安全气囊充气。可与酸反应生成叠氮酸(
)用于汽车的安全气囊中,当发生车祸时迅速分解放出氮气,使安全气囊充气。可与酸反应生成叠氮酸( ),叠氮酸中3个氮原子的杂化类型分别为
),叠氮酸中3个氮原子的杂化类型分别为(4)N原子之间可以形成π键,而
 原子之间较难形成π键。从原子结构角度分析,其原因为
原子之间较难形成π键。从原子结构角度分析,其原因为(5)往硫酸铜溶液中加入过量氨水,可生成配离子
 。已知
。已知 与
与 的空间构型都是三角锥形,但
的空间构型都是三角锥形,但 不易与
不易与 形成配离子,其原因是
形成配离子,其原因是(6)
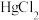 和不同浓度
和不同浓度 反应得到某种含汞化合物的晶胞结构(有四个等同的小立方体)如图所示。(部分微粒不在晶胞内,每个
反应得到某种含汞化合物的晶胞结构(有四个等同的小立方体)如图所示。(部分微粒不在晶胞内,每个 原子均处于小立方体的面心)
原子均处于小立方体的面心)
写出该含汞化合物的化学式:

 (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 ,用含a、
,用含a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
解题方法
5 . 下列对有关事实的原因分析错误的是
| 事实 | 原因 | |
| A | 白磷(P4)为正四面体分子 | 白磷分子中P−P键间的夹角是109°28′ |
| B | 分子内不同化学键之间存在一定的夹角 | 共价键具有方向性 |
| C | 键的极性H−O键>H−S键 | O的电负性大于S的电负性 |
| D | 通常状况下,1体积水溶解700体积氨气 | 氨是极性分子且有氢键的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-24更新
|
1066次组卷
|
9卷引用:山东省烟台市2021-2022学年高二上学期期末考试化学试题
山东省烟台市2021-2022学年高二上学期期末考试化学试题山东省枣庄市第三中学2021-2022学年高二3月质量检测化学试题山东省沂南第一中学2021-2022学年高二4月月考化学试题(已下线)第二章 分子结构与性质 章节过关检测-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)湖北省新高考联考协作体2021-2022学年高二3月考试化学试题广东省佛山市顺德区第一中学 2021-2022学年高二下学期期中考试化学试题福建省连城县第一中学2021-2022学年高二下学期第一次月考化学试题(已下线)专题33 物质结构与性质基础-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)广东省深圳市盐田高级中学2022-2023学年高二下学期第一次月考化学试题
名校
解题方法
6 . 现有四种元素的基态原子的核外电子排布式如下:①1s22s22p3;②1s22s22p4;③1s22s22p63s23p2;④1s22s22p63s23p3。下列说法错误的是
| A.电负性:②>①>④>③ |
| B.原子半径:③>④>①>② |
| C.第一电离能:②>①>④>③ |
| D.简单气态氢化物的稳定性:②>①>④>③ |
您最近一年使用:0次
2022-01-24更新
|
517次组卷
|
3卷引用:山东省烟台市2021-2022学年高二上学期期末考试化学试题
名校
解题方法
7 . 氨硼烷(NH3BH3) 是一种新型储氢材料,分子结构和乙烷相似。分子中与N原子相连的H呈正电性(δ+),与B原子相连的H呈负电性(δ-),它们之间存在静电作用,称双氢键,用“N−H∙∙∙H−B”表示。下列说法错误的是
| A.N和B元素均位于元素周期表的P区 |
| B.第一电离能: N> B |
| C.氨硼烷的沸点高于乙烷 |
| D.电负性:N>B>H |
您最近一年使用:0次
2022-01-22更新
|
512次组卷
|
5卷引用:山东省菏泽市2021-2022学年高二上学期期末教学质量检测化学试题
8 . 五种短周期元素X、Y、Z、L、M的某些性质如下表所示,下列判断错误的是
| 元素 | X | Y | Z | L | M |
| 最低化合价 | -4 | -2 | -1 | -2 | 0 |
| 电负性 | 2.5 | 2.5 | 3.0 | 3.5 | 1.0 |
| A.基态X原子的核外电子共占据3个原子轨道 |
| B.Z在周期表中的位置为第2周期第VIIA族 |
| C.借助电负性数值预测:YLZ2加入水中可生成YL2 |
| D.元素L、M可形成离子化合物 |
您最近一年使用:0次
2022-01-22更新
|
199次组卷
|
2卷引用:山东省滨州市2021-2022学年高二上学期期末考试化学试题
名校
解题方法
9 . 硅及其化合物广泛应用于光电材料领域,其中SiCl4与N-甲基咪唑(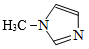 )反应可以得到M2+,其结构如图所示。下列叙述错误的是
)反应可以得到M2+,其结构如图所示。下列叙述错误的是

 )反应可以得到M2+,其结构如图所示。下列叙述错误的是
)反应可以得到M2+,其结构如图所示。下列叙述错误的是
| A.SiCl4的空间构型为正四面体 |
| B.1个M2+中含有42个σ键。 |
| C.H、C、N的电负性由大到小的顺序为N>C>H |
| D.N-甲基咪唑分子中碳原子的杂化轨道类型为sp2、sp3 |
您最近一年使用:0次
2022-01-22更新
|
891次组卷
|
6卷引用:山东省菏泽市2021~2022学年高三上学期期末考试化学(A卷 )试题
山东省菏泽市2021~2022学年高三上学期期末考试化学(A卷 )试题(已下线)提升卷03-【新高考新题型】2022年高考化学选择题标准化练习20卷(山东专用)(已下线)化学(山东A卷)-学易金卷:2023年高考第一次模拟考试卷山东省实验中学2022-2023学年高三下学期开学考试化学试题 湖北省枣阳市第一中学2021-2022学年高三下学期2月月考化学试题辽宁省沈阳市三校2023届高三下学期联合模拟考试化学试题
解题方法
10 . 已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布是 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E和D的最高能层数相同,其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E和D的最高能层数相同,其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
(1)请用元素符号完成下列空白:
①元素:C___________ 、F___________ 。
②A、B、C三种元素的电负性由大到小的顺序是:___________ 。
③B、C、D、E四种元素的第一电离能由大到小的顺序是:___________ 。
(2)下表是A~F元素中某种元素的部分电离能,由此可判断该元素是___________ (填元素符号)。
(3)F元素位于周期表的_______ 区,此区元素的价电子层结构特点是_______ 。
 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E和D的最高能层数相同,其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E和D的最高能层数相同,其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。(1)请用元素符号完成下列空白:
①元素:C
②A、B、C三种元素的电负性由大到小的顺序是:
③B、C、D、E四种元素的第一电离能由大到小的顺序是:
(2)下表是A~F元素中某种元素的部分电离能,由此可判断该元素是
| 元素 | 电离能/( | ||||
 |  |  |  |  | |
| 某种元素 | 578 | 1817 | 2745 | 11575 | 14830 |
您最近一年使用:0次

 )
)

