1 . 下列元素或化合物的性质变化顺序不正确的是
A.第一电离能: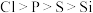 |
B.电负性: |
C.价层电子对互斥理论中, 键电子对数计入中心原子的价层电子对数 键电子对数计入中心原子的价层电子对数 |
| D.第四周期元素中,锰原子价电子层中未成对电子数最多 |
您最近一年使用:0次
名校
解题方法
2 . 物质的结构决定其性质。下列事实与解释相符的是
| 选项 | 事实 | 解释 |
| A | 一氟乙酸的 大于一溴乙酸 大于一溴乙酸 |  的电负性比 的电负性比 的大 的大 |
| B |  原子间难以形成 原子间难以形成 键 键 |  的原子半径较大,未杂化的 的原子半径较大,未杂化的 轨道很难重叠 轨道很难重叠 |
| C |  是非极性分子 是非极性分子 |  原子处在4个 原子处在4个 原子所组成的正方形中心,键的极性的向量和为零 原子所组成的正方形中心,键的极性的向量和为零 |
| D | 干冰的熔点低于 | 2个 键的键能之和小于4个 键的键能之和小于4个 键的键能之和 键的键能之和 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 优氯净(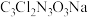 )是常用的杀菌消毒剂。下列与优氯净组成元素有关的说法正确的是
)是常用的杀菌消毒剂。下列与优氯净组成元素有关的说法正确的是
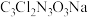 )是常用的杀菌消毒剂。下列与优氯净组成元素有关的说法正确的是
)是常用的杀菌消毒剂。下列与优氯净组成元素有关的说法正确的是| A.电负性:O>N>C | B.原子半径:Cl>Na>O |
| C.O在周期表中的位置是第2周期ⅣA族 | D.热稳定性: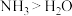 |
您最近一年使用:0次
2024-04-11更新
|
106次组卷
|
2卷引用:山东省鄄城县第一中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
4 . 某种合成医药、农药的中间体W结构如图所示,其中X、Y、Z、M、R均为短周期元素,原子序数依次增大。下列说法错误的是
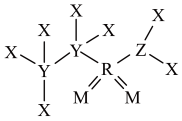
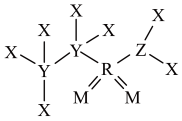
| A.简单氢化物沸点:Y<Z | B.电负性:M>Z>Y |
| C.第一电离能:Y<Z<M | D.W分子中R的杂化方式为sp3 |
您最近一年使用:0次
名校
5 . 中国科学报报道钙钛矿太阳能电池在柔性可穿戴电子设备等方面具有独特的优势和巨大的用潜力。钛酸钙晶胞俯视投影图如下:
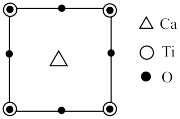
已知:晶胞中只含有一个钙原子,钙原子与钛原子之间的最近距离为xnm。
回答下列问题::
(1)基态 的核外价电子排布图为
的核外价电子排布图为___________ ,Al原子核外电子的空间运动状态有___________ 种
(2)Ti的四卤化物熔点如下表所示, 熔点高于其他三种卤化物,自
熔点高于其他三种卤化物,自 至
至 熔点依高,原因是
熔点依高,原因是___________ 。
(3)钛酸钙的组成元素的电负性大小顺序是___________ 。
(4)如图晶胞结构的化学式为___________ ; 、
、 的配位数分别为
的配位数分别为___________ 。
(5)晶体密度为___________  (列出计算式)。
(列出计算式)。

已知:晶胞中只含有一个钙原子,钙原子与钛原子之间的最近距离为xnm。
回答下列问题::
(1)基态
 的核外价电子排布图为
的核外价电子排布图为(2)Ti的四卤化物熔点如下表所示,
 熔点高于其他三种卤化物,自
熔点高于其他三种卤化物,自 至
至 熔点依高,原因是
熔点依高,原因是| 化合物 |  |  |  |  |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
(3)钛酸钙的组成元素的电负性大小顺序是
(4)如图晶胞结构的化学式为
 、
、 的配位数分别为
的配位数分别为(5)晶体密度为
 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
名校
6 . 在含铬催化剂作用下,利用二氧化碳可以合成甲醇或甲醛,化学方程式分别是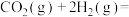
 ,
, ,下列说法正确的是
,下列说法正确的是
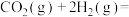
 ,
, ,下列说法正确的是
,下列说法正确的是| A.电负性:O>H>C |
B.铬原子的价电子排布式是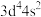 |
C.甲醛的分子结构为三角锥形,分子中碳原子采取 杂化 杂化 |
| D.水结冰时体积膨胀、密度减小的反常现象与水分子之间能形成氢键有关 |
您最近一年使用:0次
名校
7 . “点击化学”研究获得2022年诺贝尔化学奖,用该原理可制得如图含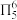 大
大 键的产物。已知杂化轨道中s成分越多,所形成的化学键越稳定。下列说法错误为是
键的产物。已知杂化轨道中s成分越多,所形成的化学键越稳定。下列说法错误为是
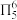 大
大 键的产物。已知杂化轨道中s成分越多,所形成的化学键越稳定。下列说法错误为是
键的产物。已知杂化轨道中s成分越多,所形成的化学键越稳定。下列说法错误为是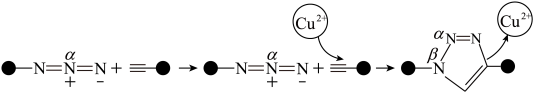
| A.铜离子增大了反应的活化能 |
| B.反应物中黑球元素的电负性强于N |
C.产物中 、 、 两位置中的N原子中, 两位置中的N原子中, 位置的N原子更容易形成配位键 位置的N原子更容易形成配位键 |
| D.反应物中氮氮键比产物中氮氮键的键长短 |
您最近一年使用:0次
名校
解题方法
8 . X、Y、Z、W是原子序数依次增大的短周期元素,X、Y可以构成 ,W的价电子排布式为
,W的价电子排布式为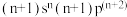 ,Z、W同主族且能构成如图所示的阴离子
,Z、W同主族且能构成如图所示的阴离子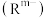 。以下说法正确的是
。以下说法正确的是

 ,W的价电子排布式为
,W的价电子排布式为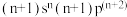 ,Z、W同主族且能构成如图所示的阴离子
,Z、W同主族且能构成如图所示的阴离子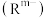 。以下说法正确的是
。以下说法正确的是
A. 中存在配位键 中存在配位键 | B. 有很好的热稳定性 有很好的热稳定性 |
| C.电负性Y>Z>W>X | D.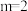 |
您最近一年使用:0次
名校
解题方法
9 . 过渡元素在现代工农业生产和科技发展方面具有重要的用途。回答下列问题:
(1)已知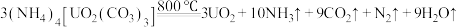 。
。
①基态U原子的外围电子排布式为 ,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是
,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是___________ (填标号)。
A. B.
B. 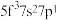 C.
C. 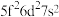 D.
D. 
②反应中断裂的化学键有___________ (填标号)。
a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
③反应所得的气态产物中属于非极性分子的是___________ (填化学式,下同);氢化物中更易与 形成配离子的是
形成配离子的是___________ 。向 溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出该反应的离子方程式
溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出该反应的离子方程式___________ 。
(2)一个配体中有两个配位原子的配体叫双齿配体,C2O 就是一种双齿配体。Fe3+的配位数是6,硫酸铁溶液中加入H2C2O4后生成配离子的化学式为
就是一种双齿配体。Fe3+的配位数是6,硫酸铁溶液中加入H2C2O4后生成配离子的化学式为___________
(3)四羰基镍 是制备铂镍合金的重要原料之一,
是制备铂镍合金的重要原料之一, 为无色有挥发性的剧毒液体,呈四面体构型。熔点25℃,沸点42℃。四羰基镍的晶体类型是
为无色有挥发性的剧毒液体,呈四面体构型。熔点25℃,沸点42℃。四羰基镍的晶体类型是___________ 。
(4)铑掺杂SrTiO3形成的催化剂,在光催化CO2还原反应中有很高的催化效率。SrTiO3的晶胞结构如图所示。其中Sr2+位于晶胞的体心,当有1%的Ti4+被Rh3+替代后,晶体中会失去部分O2-产生缺陷,此时平均每个晶胞所含O2-数目为___________ (保留三位小数)。

(1)已知
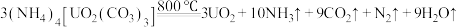 。
。①基态U原子的外围电子排布式为
 ,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是
,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是A.
 B.
B. 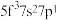 C.
C. 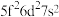 D.
D. 
②反应中断裂的化学键有
a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
③反应所得的气态产物中属于非极性分子的是
 形成配离子的是
形成配离子的是 溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出该反应的离子方程式
溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出该反应的离子方程式(2)一个配体中有两个配位原子的配体叫双齿配体,C2O
 就是一种双齿配体。Fe3+的配位数是6,硫酸铁溶液中加入H2C2O4后生成配离子的化学式为
就是一种双齿配体。Fe3+的配位数是6,硫酸铁溶液中加入H2C2O4后生成配离子的化学式为(3)四羰基镍
 是制备铂镍合金的重要原料之一,
是制备铂镍合金的重要原料之一, 为无色有挥发性的剧毒液体,呈四面体构型。熔点25℃,沸点42℃。四羰基镍的晶体类型是
为无色有挥发性的剧毒液体,呈四面体构型。熔点25℃,沸点42℃。四羰基镍的晶体类型是(4)铑掺杂SrTiO3形成的催化剂,在光催化CO2还原反应中有很高的催化效率。SrTiO3的晶胞结构如图所示。其中Sr2+位于晶胞的体心,当有1%的Ti4+被Rh3+替代后,晶体中会失去部分O2-产生缺陷,此时平均每个晶胞所含O2-数目为

您最近一年使用:0次
2024-04-03更新
|
271次组卷
|
2卷引用:山东省济宁市第一中学2023-2024学年高三下学期3月月考化学试题
名校
解题方法
10 . 化学,让生活更美好。回答下列问题:
(1)乳酸亚铁 是一种常用的补铁剂。
是一种常用的补铁剂。
①基态 核外电子的空间运动状态有
核外电子的空间运动状态有________ 种。
②乳酸分子中σ键与π键的数目比为________ 。
③乳酸亚铁中各元素的电负性由大到小的顺序为________ 。
(2)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如图:
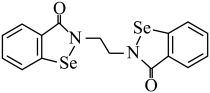
①该新药分子中有________ 种不同化学环境的C原子。
②研究发现,适量硒酸钠 可减轻重金属铊引起的中毒。
可减轻重金属铊引起的中毒。
比较键角大小:
________  (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是________ 。
③ 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为________ (填化学式)。
(3)砷化镓(GaAs)是一种优良的半导体材料,可用于制作微型激光器或太阳能电池等。
①根据元素周期律,原子半径Ga________ As(填“>”、“<”)。
② 分子的空间构型为
分子的空间构型为________ 。 的熔点高于1000℃,
的熔点高于1000℃, 的熔点为77.9℃,其原因是
的熔点为77.9℃,其原因是________ 。
(1)乳酸亚铁
 是一种常用的补铁剂。
是一种常用的补铁剂。①基态
 核外电子的空间运动状态有
核外电子的空间运动状态有②乳酸分子中σ键与π键的数目比为
③乳酸亚铁中各元素的电负性由大到小的顺序为
(2)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如图:

①该新药分子中有
②研究发现,适量硒酸钠
 可减轻重金属铊引起的中毒。
可减轻重金属铊引起的中毒。比较键角大小:

 (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是③
 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为(3)砷化镓(GaAs)是一种优良的半导体材料,可用于制作微型激光器或太阳能电池等。
①根据元素周期律,原子半径Ga
②
 分子的空间构型为
分子的空间构型为 的熔点高于1000℃,
的熔点高于1000℃, 的熔点为77.9℃,其原因是
的熔点为77.9℃,其原因是
您最近一年使用:0次



