名校
解题方法
1 . 下列各组微粒,中心原子均采用sp2杂化方式的
A.NH3,PCl3,CO ,CO2 ,CO2 | B.SO3,NO ,COCl2,BF3 ,COCl2,BF3 |
C.SO ,ClO ,ClO ,PO ,PO ,BF3 ,BF3 | D.BeCl2,NCl3,NO ,ClO ,ClO |
您最近一年使用:0次
2022-05-06更新
|
230次组卷
|
2卷引用:重庆市万州第二高级中学2021-2022学年高二下学期期末考试化学试题
名校
解题方法
2 . 下表是元素周期表的一部分。表中所列的字母分别代表一种元素。
回答下列问题:
(1)D的简单气态氢化物分子的立体构型为___________ 。
(2)第一电离能H___________ X(填“>”、“<”或“=”)。
(3)DA3的沸点比D2E的沸点高,其原因是___________ 。
(4)YE 的立体构型为
的立体构型为___________ ,YE 的键角比YE
的键角比YE 的键角小的原因是
的键角小的原因是___________ 。
| A | R | ||||||||||||||||
| B | D | E | M | T | |||||||||||||
| G | H | X | J | Y | L | ||||||||||||
| N |
(1)D的简单气态氢化物分子的立体构型为
(2)第一电离能H
(3)DA3的沸点比D2E的沸点高,其原因是
(4)YE
 的立体构型为
的立体构型为 的键角比YE
的键角比YE 的键角小的原因是
的键角小的原因是
您最近一年使用:0次
2022-05-05更新
|
101次组卷
|
2卷引用:重庆市万州纯阳中学校2021-2022学年高二下学期5月月考化学试题
3 . 下列有关说法错误的是
| A.NH3的空间构型为三角锥形 |
B.NH 中N的杂化类型为sp2 中N的杂化类型为sp2 |
C.基态N原子的轨道表示式为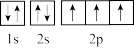 |
D.NH 中的键角比NH3中的大 中的键角比NH3中的大 |
您最近一年使用:0次
2022-05-01更新
|
208次组卷
|
3卷引用:重庆市万州纯阳中学校2021-2022学年高二下学期5月月考化学试题
名校
4 . 下列说法不正确的是
A. 的分子空间构型为V形,可推知 的分子空间构型为V形,可推知 的分子空间构型也为V形 的分子空间构型也为V形 |
B. 与 与 反应的剧烈程度弱于 反应的剧烈程度弱于 与 与 反应的剧烈程度,可知烃基为推电子基团,减小了 反应的剧烈程度,可知烃基为推电子基团,减小了 的极性 的极性 |
C. 的熔点低于 的熔点低于 ,可推知 ,可推知 的熔点低于 的熔点低于 |
D. 为两性氧化物,可推知 为两性氧化物,可推知 也为两性氧化物 也为两性氧化物 |
您最近一年使用:0次
2022-04-23更新
|
148次组卷
|
2卷引用:重庆市万州第二高级中学2021-2022学年高二下学期6月第三次质量检测化学试题
名校
解题方法
5 . 硼的化合物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态硼原子的价电子排布图为:_______ ;B、N、H的电负性由大到小的顺序为_______ 。
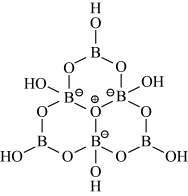
(2)科学家合成了一种含硼阴离子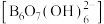 ,其结构如图所示。其中硼原子的杂化方式为
,其结构如图所示。其中硼原子的杂化方式为_______ ,该结构中共有_______ 种不同化学环境的氧原子。
(3) 与
与 结合形成固态化合物
结合形成固态化合物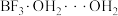 ,该物质在6.2℃时熔化电离出
,该物质在6.2℃时熔化电离出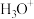 和一种含硼阴离子
和一种含硼阴离子_______ (填离子符号);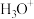 空间构型为
空间构型为_______ 。
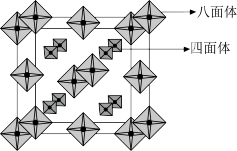
(4)金属硼氢化物可用作储氢材料。如图是一种金属硼氢化物氨合物的晶体结构示意图。图中八面体的中心代表金属M原子,顶点代表氨分子;四面体的中心代表硼原子,顶点代表氢原子。该晶体晶胞棱边夹角均为90°,棱长为apm,密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。
①该晶体的化学式为_______ 。
②金属M的相对原子质量为_______ (列出表达式)。
(1)基态硼原子的价电子排布图为:
(2)科学家合成了一种含硼阴离子
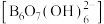 ,其结构如图所示。其中硼原子的杂化方式为
,其结构如图所示。其中硼原子的杂化方式为
(3)
 与
与 结合形成固态化合物
结合形成固态化合物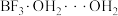 ,该物质在6.2℃时熔化电离出
,该物质在6.2℃时熔化电离出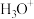 和一种含硼阴离子
和一种含硼阴离子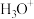 空间构型为
空间构型为(4)金属硼氢化物可用作储氢材料。如图是一种金属硼氢化物氨合物的晶体结构示意图。图中八面体的中心代表金属M原子,顶点代表氨分子;四面体的中心代表硼原子,顶点代表氢原子。该晶体晶胞棱边夹角均为90°,棱长为apm,密度为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。①该晶体的化学式为
②金属M的相对原子质量为

您最近一年使用:0次
6 . 能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力。
(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,基态镍原子最高能层的轨道形状为_______ 。
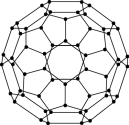
(2)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯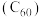 的结构如图,
的结构如图, 分子中
分子中 键的数目为
键的数目为_______ 个。
(3)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓(GaAs)、硫化镉(CdS)薄膜电池等。
①第一电离能:As_______ Ga(填“>”“<”或“=”)。
② 分子的空间结构为
分子的空间结构为_______ 。
(4)三氟化氢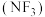 是一种无色、无味、无毒且不可燃的气体,在太阳能电池制造中得到广泛应用。它可在铜的催化作用下由
是一种无色、无味、无毒且不可燃的气体,在太阳能电池制造中得到广泛应用。它可在铜的催化作用下由 和过量的
和过量的 反应得到。往硫酸铜溶液中加入过量氨水,可生成配离子,写出该反应的离子方程式
反应得到。往硫酸铜溶液中加入过量氨水,可生成配离子,写出该反应的离子方程式_______ 。已知 与
与 的空间结构都是三角锥形,但
的空间结构都是三角锥形,但 不易与
不易与 形成配离子,其原因是
形成配离子,其原因是_______ 。
(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,基态镍原子最高能层的轨道形状为
(2)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯
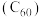 的结构如图,
的结构如图, 分子中
分子中 键的数目为
键的数目为
(3)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓(GaAs)、硫化镉(CdS)薄膜电池等。
①第一电离能:As
②
 分子的空间结构为
分子的空间结构为(4)三氟化氢
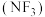 是一种无色、无味、无毒且不可燃的气体,在太阳能电池制造中得到广泛应用。它可在铜的催化作用下由
是一种无色、无味、无毒且不可燃的气体,在太阳能电池制造中得到广泛应用。它可在铜的催化作用下由 和过量的
和过量的 反应得到。往硫酸铜溶液中加入过量氨水,可生成配离子,写出该反应的离子方程式
反应得到。往硫酸铜溶液中加入过量氨水,可生成配离子,写出该反应的离子方程式 与
与 的空间结构都是三角锥形,但
的空间结构都是三角锥形,但 不易与
不易与 形成配离子,其原因是
形成配离子,其原因是
您最近一年使用:0次
名校
解题方法
7 . 铁氮化合物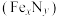 在磁记录材料领域有着广泛的应用前景。某
在磁记录材料领域有着广泛的应用前景。某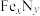 的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物
的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物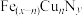 。
。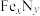 转化为两种Cu替代型产物的能量变化如图2所示,下列有关说法不正确的是
转化为两种Cu替代型产物的能量变化如图2所示,下列有关说法不正确的是

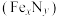 在磁记录材料领域有着广泛的应用前景。某
在磁记录材料领域有着广泛的应用前景。某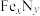 的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物
的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物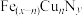 。
。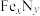 转化为两种Cu替代型产物的能量变化如图2所示,下列有关说法不正确的是
转化为两种Cu替代型产物的能量变化如图2所示,下列有关说法不正确的是 
| A.Cu元素位于元素周期表中的ds区 | B.图1中氮原子的配位数为6 |
C.更稳定的Cu替代型产物的化学式为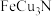 | D.当a位置Fe位于体心时,b位置Fe位于棱上 |
您最近一年使用:0次
2022-04-20更新
|
561次组卷
|
6卷引用:重庆市万州第二高级中学2021-2022学年高二下学期期中考试化学试题
名校
8 . 下列说法中不正确 的是
| A.轨道的电子云轮廓图表示的是该轨道上电子运动的全部空间 |
| B.金属的电子气理论可以很好地解释金属的导电性、导热性、延展性 |
| C.电子从3d轨道跃迁到3s轨道时,会产生发射光谱 |
D.键角: |
您最近一年使用:0次
名校
解题方法
9 . 下列有关物质结构与性质的说法正确的是
| A.金刚石与碳化硅晶体结构相似,金刚石的硬度小于碳化硅 |
B.对羟基苯甲醛(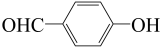 )比邻羟基苯甲醛( )比邻羟基苯甲醛(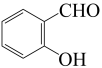 )的沸点高 )的沸点高 |
C.常温常压下,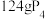 中所含P—P键数目为 中所含P—P键数目为 |
D.向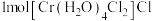 中加入足量 中加入足量 溶液,可以得到3molAgCl沉淀 溶液,可以得到3molAgCl沉淀 |
您最近一年使用:0次
10 . 下列物质中既含离子键又含配位键的是
| A. MgO | B.NaOH | C. | D.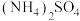 |
您最近一年使用:0次
2022-04-20更新
|
213次组卷
|
7卷引用:重庆市万州第二高级中学2021-2022学年高二下学期期中考试化学试题



