1 . 海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图所示:

(1)写出工业上由食盐制备
 的离子方程式:
的离子方程式:(2)步骤Ⅰ中已获得
 ,步骤Ⅱ中又将
,步骤Ⅱ中又将 转化为
转化为 和
和 ,其目的是
,其目的是(3)步骤Ⅱ中通入热空气吹出
 ,利用了
,利用了 的___________(填标号)。
的___________(填标号)。| A.氧化性 | B.还原性 | C.挥发性 | D.腐蚀性 |
(4)步骤Ⅱ中用纯碱溶液吸收
 ,该反应的化学方程式为
,该反应的化学方程式为(5)从理论上考虑,下列物质也能吸收
 的是___________(填标号)。
的是___________(填标号)。A. | B.NaCl溶液 | C. 溶液 溶液 | D. 溶液 溶液 |
(6)查阅资料知,
 的沸点为58.8 ℃,微溶于水,有毒性和强腐蚀性。步骤Ⅲ中对蒸馏烧瓶采取的加热方式是
的沸点为58.8 ℃,微溶于水,有毒性和强腐蚀性。步骤Ⅲ中对蒸馏烧瓶采取的加热方式是2 . 如图是中学化学中常用于混合物的分离和提纯装置,请根据装置回答问题:

(1)请将下列提纯或分离使用的装置的序号填在后面横线上。
①分离饱和食盐水与泥沙的混合物
②从食盐水中获取NaCl固体
③分离互溶的CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物
(2)在装置A和装置B中都用到玻璃棒,装置A中玻璃棒的作用是
(3)装置C中①的名称是
(4)某实验合成的乙酸异戊酯(难溶于水,密度0.867 g·mL-1) 经水洗后与水层分离的正确分液操作是
A.直接将乙酸异戊酯从分液漏斗上口倒出
B.直接将乙酸异戊酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
在分液时为使液体顺利滴下,应进行的具体操作是
(1)检验物质的常用方法有显色法、沉淀法、气体法等。下列物质检验的方法中,不合理的是
| A.酸性溶液:显色法 | B.I2:显色法 |
| C.Cl-:沉淀法 | D.Ca2+:气体法 |
| A.过滤 | B.萃取 | C.结晶 | D.蒸馏 |
| A.盐酸 | B.BaCl2溶液 | C.AgNO3溶液 | D.焰色反应 |
| A.HCl、CuCl2、NaNO3、Na2SO4 |
| B.Na2CO3、Na2SO4、HCl、H2SO4 |
| C.FeCl3、Na2SO4、NaCl、NaOH |
| D.BaCl2、Na2CO3、HCl、NaNO3 |
| A.加AgNO3溶液,生成白色沉淀,可确定有Cl-存在 |
B.加足量稀盐酸,产生无色的气体,可确定有CO 存在 存在 |
C.加足量稀盐酸,无明显现象,再加BaCl2溶液,生成白色沉淀,可确定有SO 存在 存在 |
| D.用洁净的铂丝蘸取溶液,在火焰上灼烧焰色为黄色,可确定含Na+,不含K+ |
| A.萃取剂不能溶于水,且比水更容易使碘溶解 |
| B.注入碘水和萃取剂,倒转分液漏斗反复用力振荡后即可分液 |
| C.萃取时,选用萃取剂的密度必须比水大 |
| D.若没有四氯化碳,可用酒精代替 |
 和Cl-两种负离子,使用以下操作进行检验:①滴加足量的BaCl2溶液;②滴加足量的Ba(NO3)2溶液;③过滤;④加足量的盐酸:⑤滴加AgNO3溶液。正确的操作及顺序是
和Cl-两种负离子,使用以下操作进行检验:①滴加足量的BaCl2溶液;②滴加足量的Ba(NO3)2溶液;③过滤;④加足量的盐酸:⑤滴加AgNO3溶液。正确的操作及顺序是| A.①③⑤ | B.②④③⑤ | C.②③⑤ | D.⑤③① |
| 检测次数 | 溶液中检测出的物质 |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、BaCl2、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、KCl、K2CO3、NaCl |
②在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子:
第一步:向溶液中滴加过量的
 并将其除去。
并将其除去。第二步:加入
第三步:过滤,再向滤液中加入
4 . Ⅰ.氯化钠是日常生活必需品和重要的化工原料。海水中含有大量的NaCl。
(1)下列生产过程中只发生物理变化的是__________。
| A.炼铁 | B.海带提碘 | C.氯碱工业 | D.海水晒盐 |
(2)氯化钠属于__________。
| A.酸 | B.碱 | C.盐 | D.氧化物 |
(3)
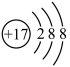 表示__________。
表示__________。| A.氯原子的结构示意图 | B.氯离子的结构示意图 |
| C.氯原子的电子式 | D.氯离子的电子式 |
Ⅱ.实验室提纯粗盐时,将粗盐溶于水后,先除去泥沙等难溶性杂质,再除去 Ca2+、 Mg2+、 等可溶性杂质。
等可溶性杂质。
(4)写出NaCl溶于水时的电离方程式
(5)为了除去可溶性杂质,依次加入稍过量的BaCl2溶液、NaOH溶液和Na2CO3液,加热至70°C左右约2分钟,冷却后过滤,得到的沉淀有BaSO4、Mg(OH)2、CaCO3和
Ⅲ.“84消毒液”是常见的消毒剂,其有效成分是NaClO。
(6)Cl2和NaOH 制备NaClO的化学方程式为
Ⅳ.如图是某品牌“84 消毒液”的使用注意事项。

(7)注意事项4“易使有色衣物脱色”,是因为 “84 消毒液”具有
A.碱性 B.强氧化性
(8)注意事项6“不可与酸性物质同时使用”,例如,若将“84 消毒液”与“洁厕灵”(含盐酸) 同时使用会产生黄绿色有毒气体。写出反应的离子方程式
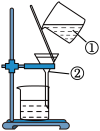
(1)写出标号仪器的名称:
①
(2)漏斗中液体的液面应该
(1)可用于分离或提纯物质的方法有:a.过滤;b.结晶;c.蒸馏;d.萃取;e.分液。请将相应分离提纯物质方法的序号填入空白处:
①从碘的氯化钾水溶液提取碘:
②分离乙酸(沸点118℃)和乙醚(沸点34℃):
③分离水和汽油的混合物:
(2)用以下物质的序号填空:①液氨;②硫酸;③熔融氯化钾;④碳酸铵溶液;⑤蔗糖。属于电解质的有
 滤液中加入稍过量KCl固体,再经处理,可将
滤液中加入稍过量KCl固体,再经处理,可将 转化为
转化为 。根据相关物质的溶解度,你认为可能的原因是
。根据相关物质的溶解度,你认为可能的原因是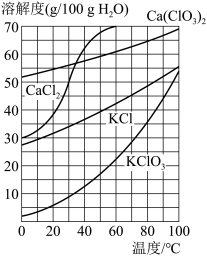
Cl2(HCl)
A.萃取 B.加热 C.结晶 D.分液 E.过滤 F.蒸馏
(1)除去食盐水中的泥沙
(2)从含有少量氯化钠的硝酸钾溶液中提取硝酸钾
(3)分离水和汽油
(4)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物
(5)有如下物质:①铁丝 ②NaOH溶液 ③Na2SO4固体 ④CO2 ⑤酒精 ⑥自来水⑦CCl4 ⑧熔融的KNO3 ⑨红褐色的氢氧化铁胶体。其中,属于电解质的是
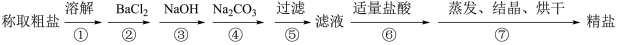
(1)判断BaCl2已过量的方法是
(2)第④步中,相关的化学方程式是
(3)过滤操作中,需要用到的玻璃仪器有



