名校
1 . 过氧化钙(CaO2)微溶于水,可作医用防腐剂、消毒剂,以下是制备CaO2的一种方法。

回答下列问题:
(1)CaO2中O元素的化合价为________ 。
(2)步骤Ⅰ中反应的离子方程式是________ 。
(3)步骤Ⅱ中反应的化学方程式是:________ =CaO2•8H2O↓+2NH4Cl,反应在冰水浴 中进行,是为了防止NH3•H2O挥发、________ (答1条即可)。
(4)待CaO2•8H2O结晶析出后通过________ (填操作名称)分离。
(5)CaO2可与水或二氧化碳缓慢反应,同时产生氧气,常用作鱼塘的供氧剂。CaO2与水反应的化学方程式是________ 。CaO2还可用于长途运输鱼苗,推测CaO2可能具有________ (填字母)性质。
a.可缓慢供氧 b.能吸收鱼苗呼出的CO2 c.可抑菌

回答下列问题:
(1)CaO2中O元素的化合价为
(2)步骤Ⅰ中反应的离子方程式是
(3)步骤Ⅱ中反应的化学方程式是:
(4)待CaO2•8H2O结晶析出后通过
(5)CaO2可与水或二氧化碳缓慢反应,同时产生氧气,常用作鱼塘的供氧剂。CaO2与水反应的化学方程式是
a.可缓慢供氧 b.能吸收鱼苗呼出的CO2 c.可抑菌
您最近一年使用:0次
名校
解题方法
2 . NaCl溶液中混有Na2SO4、Na2CO3溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如图:

(1)写出上述实验过程中所用试剂(填化学式)和基本实验操作:试剂①___________ ;试剂③___________ ;操作①___________ ;操作④___________ 。
(2)区分淀粉胶体和NaCl溶液的方法是:___________ 。
(3)沉淀A为___________ 。
(4)加入试剂②产生沉淀的化学方程式:___________ 。

(1)写出上述实验过程中所用试剂(填化学式)和基本实验操作:试剂①
(2)区分淀粉胶体和NaCl溶液的方法是:
(3)沉淀A为
(4)加入试剂②产生沉淀的化学方程式:
您最近一年使用:0次
2023-10-31更新
|
41次组卷
|
2卷引用:江西省南昌市第一中学2023-2024学年高一上学期10月月考化学试题
3 . 回答下列问题:下列可用于分离和提纯物质的方法是(填选择序号)。
a.结晶 b.蒸馏 c.过滤 d.萃取分液
(1)分离KNO3和NaCl混合物________ 。
(2)分离溴水中的溴和水________ 。
(3)除去澄清石灰水中悬浮的CaCO3颗粒:________ 。
(4)写出仪器的名称:①________ ,②________ 。
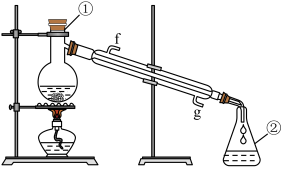
(5)若利用装置分离四氯化碳和酒精的混合物,还缺少的仪器________ ;该分离操作的名称为________ ;进行分离操作时进水口为________ (填f或g)。
a.结晶 b.蒸馏 c.过滤 d.萃取分液
(1)分离KNO3和NaCl混合物
(2)分离溴水中的溴和水
(3)除去澄清石灰水中悬浮的CaCO3颗粒:
(4)写出仪器的名称:①

(5)若利用装置分离四氯化碳和酒精的混合物,还缺少的仪器
您最近一年使用:0次
名校
解题方法
4 . 完成下列问题。
(1)下列做法中,符合“低碳”理念的是________ (填字母序号)
A.开发使用新能源汽车 B.“焚烧法”处理垃圾 C.大力发展火力发电
D.使用太阳能热水器 E.大力发展风力发电
(2)幼儿和青少年缺___________ 会患佝偻病和发育不良。
(3)如图是A、B、C三种物质的溶解度曲线图。请回答:

①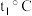 时,溶解度相等的两种物质是
时,溶解度相等的两种物质是________ 。
②B的饱和溶液中混有少量的物质A,要除去A得到较纯的B物质,可采用的结晶方法是___________ 。
③如图所示,在大烧杯中加入一定量的硝酸铵固体后,甲试管内出现的现象是___________ ,乙试管内的溶液为___________ (填“饱和”或“不饱和”)溶液。

(1)下列做法中,符合“低碳”理念的是
A.开发使用新能源汽车 B.“焚烧法”处理垃圾 C.大力发展火力发电
D.使用太阳能热水器 E.大力发展风力发电
(2)幼儿和青少年缺
(3)如图是A、B、C三种物质的溶解度曲线图。请回答:

①
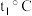 时,溶解度相等的两种物质是
时,溶解度相等的两种物质是②B的饱和溶液中混有少量的物质A,要除去A得到较纯的B物质,可采用的结晶方法是
③如图所示,在大烧杯中加入一定量的硝酸铵固体后,甲试管内出现的现象是

您最近一年使用:0次
解题方法
5 . 氮及其化合物在化学工业和环境工业中研究颇多。回答下列问题:
(1)联氨(N2H4)可用于处理锅炉水中的溶解氧,一种反应机理如图所示。

①类比NH3与HCl反应,写出H2N-NH2与足量HCl反应的化学方程式:___________ 。
②反应Ⅱ的离子方程式为___________ 。
③1molN2H4可处理水中___________ molO2。
(2)氮污染主要包括氨态氮(NH3、
 )和硝态氮(
)和硝态氮(
 、
、
 ),工业上常利用还原法处理水体中的无机氮。如普通铝粉可实现酸性污水的脱硝(硝态氮转化为N2)。
),工业上常利用还原法处理水体中的无机氮。如普通铝粉可实现酸性污水的脱硝(硝态氮转化为N2)。
①写出普通铝粉脱硝时, 反应的离子方程式:
反应的离子方程式:___________ ,酸性太强不利于脱硝,其原因是__________ 。
②等量的纳米铝粉比普通铝粉更有利于脱硝,其原因有___________ (写出一点即可)。
③研究发现纳米铁粉也有很好的脱硝效果,但水体中溶解氧(O2)过多,会大大降低脱硝效果,其原因是_________ 。
(3)氨态氮可用次氯酸钠除去,一种原理如图所示。

①NaClO除去氨态氮的总反应中,参与反应的氧化剂与还原剂的物质的量之比为___________ 。
②在较高温度下,氨态氮去除率会降低,其原因是___________ (语言叙述)。
(1)联氨(N2H4)可用于处理锅炉水中的溶解氧,一种反应机理如图所示。

①类比NH3与HCl反应,写出H2N-NH2与足量HCl反应的化学方程式:
②反应Ⅱ的离子方程式为
③1molN2H4可处理水中
(2)氮污染主要包括氨态氮(NH3、
 )和硝态氮(
)和硝态氮( 、
、 ),工业上常利用还原法处理水体中的无机氮。如普通铝粉可实现酸性污水的脱硝(硝态氮转化为N2)。
),工业上常利用还原法处理水体中的无机氮。如普通铝粉可实现酸性污水的脱硝(硝态氮转化为N2)。①写出普通铝粉脱硝时,
 反应的离子方程式:
反应的离子方程式:②等量的纳米铝粉比普通铝粉更有利于脱硝,其原因有
③研究发现纳米铁粉也有很好的脱硝效果,但水体中溶解氧(O2)过多,会大大降低脱硝效果,其原因是
(3)氨态氮可用次氯酸钠除去,一种原理如图所示。

①NaClO除去氨态氮的总反应中,参与反应的氧化剂与还原剂的物质的量之比为
②在较高温度下,氨态氮去除率会降低,其原因是
您最近一年使用:0次
6 . 现有 、
、 、
、 和
和 的混合物,选择适当的试剂除去杂质,从而得到纯净的
的混合物,选择适当的试剂除去杂质,从而得到纯净的 晶体,相应的实验流程如图所示。请回答下列问题:
晶体,相应的实验流程如图所示。请回答下列问题:
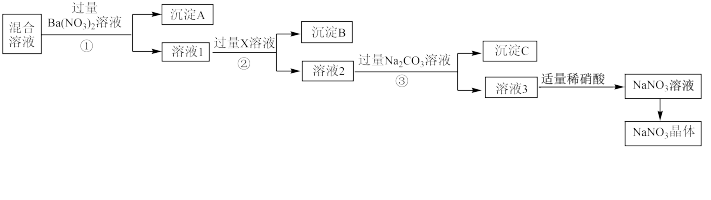
(1)沉淀 的主要成分是
的主要成分是 ___________ 。 填化学式
填化学式
(2)试剂 是
是___________ 。
(3)上述实验流程中 操作名称为
操作名称为___________ ,用到的玻璃仪器有___________ 。
(4)上述实验流程中加入过量 溶液的目的是
溶液的目的是___________ 。
(5)按此实验方案得到的溶液 中肯定含有杂质,可以向溶液
中肯定含有杂质,可以向溶液 中加入适量稀硝酸除去杂质,写出流程④除杂反应的离子方程式:
中加入适量稀硝酸除去杂质,写出流程④除杂反应的离子方程式:___________ 。
 、
、 、
、 和
和 的混合物,选择适当的试剂除去杂质,从而得到纯净的
的混合物,选择适当的试剂除去杂质,从而得到纯净的 晶体,相应的实验流程如图所示。请回答下列问题:
晶体,相应的实验流程如图所示。请回答下列问题:
(1)沉淀
 的主要成分是
的主要成分是  填化学式
填化学式
(2)试剂
 是
是(3)上述实验流程中
 操作名称为
操作名称为(4)上述实验流程中加入过量
 溶液的目的是
溶液的目的是(5)按此实验方案得到的溶液
 中肯定含有杂质,可以向溶液
中肯定含有杂质,可以向溶液 中加入适量稀硝酸除去杂质,写出流程④除杂反应的离子方程式:
中加入适量稀硝酸除去杂质,写出流程④除杂反应的离子方程式:
您最近一年使用:0次
名校
解题方法
7 . 要分离下列四组混合物,将合理答案填入空格。
①饱和食盐水与沙子 ②从KNO3和NaCl的混合溶液中获得KNO3 ③水和汽油的混合物 ④CCl4液体与甲苯液体的混合物(已知CCl4与甲苯互溶,沸点分别为76.75℃和110.6℃)
(1)分离①②的操作分别为_______ 、_______ 。
(2)分离③时所使用仪器中有一种在其他组分分离时无需使用,这种仪器是_______ 。
(3)上述四组分离过程中,需要使用酒精灯的是_______ 和_______ (填序号)。
①饱和食盐水与沙子 ②从KNO3和NaCl的混合溶液中获得KNO3 ③水和汽油的混合物 ④CCl4液体与甲苯液体的混合物(已知CCl4与甲苯互溶,沸点分别为76.75℃和110.6℃)
(1)分离①②的操作分别为
(2)分离③时所使用仪器中有一种在其他组分分离时无需使用,这种仪器是
(3)上述四组分离过程中,需要使用酒精灯的是
您最近一年使用:0次
8 . 黏土钒矿中,钒以+3价、+4价、+5价的化合物存在,还包括SiO2、Fe2O3和铝硅酸盐(Al2O3•SiO2)等。采用以下流程可由黏土钒矿制备V2O5、Fe2O3和硫酸铝铵。

已知:i.有机酸性萃取剂HR的萃取原理为:Mn+(aq)+nHR(org) MR(org)+nH+(aq)(org表示有机溶液)
MR(org)+nH+(aq)(org表示有机溶液)
ii.酸性溶液中,HR对+4价钒萃取能力强,而对+5价钒的萃取能力较弱。
iii.HR能萃取Fe3+而不能萃取Fe2+。
(1)从黏土钒矿到浸出液的流程中,加快浸出速率的措施有_______ 。
(2)浸出液中钒以+4价、+5价的形式存在,简述加入铁粉的原因:_______ 。
(3)从平衡移动原理解释加入20%H2SO4溶液的作用:_______ 。
(4)KClO3和VO2+(反应生成VO 和Cl-的离子方程式是
和Cl-的离子方程式是_______ 。
(5)测定V2O5产品的纯度
称取V2O5产品ag,先加入硫酸将V2O5转化为VO ,加入指示剂后,cmol/L(NH4)2Fe(SO4)2溶液滴定将VO
,加入指示剂后,cmol/L(NH4)2Fe(SO4)2溶液滴定将VO 转化为VO2+至终点,消耗(NH4)2Fe(SO4)2溶液的体积为VmL。假设杂质不参与反应,则V2O5产品中V2O5的质量分数是
转化为VO2+至终点,消耗(NH4)2Fe(SO4)2溶液的体积为VmL。假设杂质不参与反应,则V2O5产品中V2O5的质量分数是_______ (V2O5的摩尔质量为Mg/mol)。
(6)从无机层获得Fe(OH)3的离子方程式是_______ 。
(7)硫酸铝铵固体中含有少量硫酸铵杂质,根据如图的溶解度曲线,进一步提纯硫酸铝铵的操作是加热溶解、_______ 、洗涤、干燥。


已知:i.有机酸性萃取剂HR的萃取原理为:Mn+(aq)+nHR(org)
 MR(org)+nH+(aq)(org表示有机溶液)
MR(org)+nH+(aq)(org表示有机溶液)ii.酸性溶液中,HR对+4价钒萃取能力强,而对+5价钒的萃取能力较弱。
iii.HR能萃取Fe3+而不能萃取Fe2+。
(1)从黏土钒矿到浸出液的流程中,加快浸出速率的措施有
(2)浸出液中钒以+4价、+5价的形式存在,简述加入铁粉的原因:
(3)从平衡移动原理解释加入20%H2SO4溶液的作用:
(4)KClO3和VO2+(反应生成VO
 和Cl-的离子方程式是
和Cl-的离子方程式是(5)测定V2O5产品的纯度
称取V2O5产品ag,先加入硫酸将V2O5转化为VO
 ,加入指示剂后,cmol/L(NH4)2Fe(SO4)2溶液滴定将VO
,加入指示剂后,cmol/L(NH4)2Fe(SO4)2溶液滴定将VO 转化为VO2+至终点,消耗(NH4)2Fe(SO4)2溶液的体积为VmL。假设杂质不参与反应,则V2O5产品中V2O5的质量分数是
转化为VO2+至终点,消耗(NH4)2Fe(SO4)2溶液的体积为VmL。假设杂质不参与反应,则V2O5产品中V2O5的质量分数是(6)从无机层获得Fe(OH)3的离子方程式是
(7)硫酸铝铵固体中含有少量硫酸铵杂质,根据如图的溶解度曲线,进一步提纯硫酸铝铵的操作是加热溶解、

您最近一年使用:0次
2023-10-22更新
|
649次组卷
|
2卷引用:北京市清华大学附属中学2023-2024学年高三上学期10月月考化学试题
名校
9 . Ⅰ.黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的。爆炸时发生的反应为: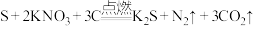 。
。
(1)该反应中,氧化剂是_____ (填化学式,下同),氧化产物是_____ 。在上述反应中若有 硫单质完全反应,被硫单质氧化的单质
硫单质完全反应,被硫单质氧化的单质 的质量是
的质量是_____ g。
Ⅱ.造纸工业是国民经济十大支柱制造业之一,在《天工开物》中记载了比较完善的造纸方法。但造纸过程会消耗大量的资源并产生污水,因此资源的回收利用以及污水的处理非常重要。某造纸厂制浆及废水处理流程如下: 。制浆废水中大部分碱性物质被回收利用,剩余的有机物在细菌池被微生物分解除去。
。制浆废水中大部分碱性物质被回收利用,剩余的有机物在细菌池被微生物分解除去。
(2)“碱液重生”过程分为以下两步反应,请补充反应ii的离子方程式:
ⅰ.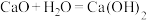 (石灰乳)
(石灰乳)
ⅱ._____ 。
(3)反应 的化学方程式为
的化学方程式为_____ 。
(4)为防止细菌失活,须先调 至中性。下列物质中,可实现该目的的有_____(填选项字母)
至中性。下列物质中,可实现该目的的有_____(填选项字母)
(5)上述过程中,循环使用的物质有_____ (写化学式)。
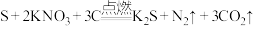 。
。(1)该反应中,氧化剂是
 硫单质完全反应,被硫单质氧化的单质
硫单质完全反应,被硫单质氧化的单质 的质量是
的质量是Ⅱ.造纸工业是国民经济十大支柱制造业之一,在《天工开物》中记载了比较完善的造纸方法。但造纸过程会消耗大量的资源并产生污水,因此资源的回收利用以及污水的处理非常重要。某造纸厂制浆及废水处理流程如下:

 。制浆废水中大部分碱性物质被回收利用,剩余的有机物在细菌池被微生物分解除去。
。制浆废水中大部分碱性物质被回收利用,剩余的有机物在细菌池被微生物分解除去。(2)“碱液重生”过程分为以下两步反应,请补充反应ii的离子方程式:
ⅰ.
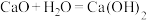 (石灰乳)
(石灰乳)ⅱ.
(3)反应
 的化学方程式为
的化学方程式为(4)为防止细菌失活,须先调
 至中性。下列物质中,可实现该目的的有_____(填选项字母)
至中性。下列物质中,可实现该目的的有_____(填选项字母)A. | B. | C. | D. |
您最近一年使用:0次
2023-10-20更新
|
89次组卷
|
2卷引用:江苏省南通市海安高级中学2023-2024学年高一上学期10月月考化学试题
名校
10 . I.某校化学一兴趣小组在社会实践活动中,考察了当地某工厂的废水(无色)处理流程,并取该厂未经处理的废水样品进行实验分析。

已知: 固体难溶于硝酸。
固体难溶于硝酸。
(1)取少量废水,向其中滴入紫色石蕊试液,溶液变红,该废水呈_______ (填“酸性”或“碱性”),说明废水中含有较大量的_______ (填离子符号),建议该厂用_______ (填化学式)处理废水。
(2)另取少量废水,滴加适量 溶液,有白色沉淀产生,说明该废水中一定含有的离子是
溶液,有白色沉淀产生,说明该废水中一定含有的离子是_______ ,其离子反应方程式为_______ 。
(3)已知该工厂废水中除含有以上离子外,还含有较多的 。该兴趣小组另取少量废水进行如图所示实验。开始时,试管中无明显现象,原因是
。该兴趣小组另取少量废水进行如图所示实验。开始时,试管中无明显现象,原因是_______ ;随试剂的滴加,试管中出现的现象是_______ ,该反应的离子方程式为_______ 。
Ⅱ.另一兴趣小组在实验室中尝试制备氢氧化铁胶体并探究它的性质。
(4)判断胶体的制备是否成功,可利用胶体的_______
(5)向 胶体中逐滴加入了稀
胶体中逐滴加入了稀 溶液,结果出现了一系列变化:
溶液,结果出现了一系列变化:
①先出现红褐色沉淀,原因是_______ 。
②随后沉淀溶解,此反应的离子方程式是_______ 。

已知:
 固体难溶于硝酸。
固体难溶于硝酸。(1)取少量废水,向其中滴入紫色石蕊试液,溶液变红,该废水呈
(2)另取少量废水,滴加适量
 溶液,有白色沉淀产生,说明该废水中一定含有的离子是
溶液,有白色沉淀产生,说明该废水中一定含有的离子是(3)已知该工厂废水中除含有以上离子外,还含有较多的
 。该兴趣小组另取少量废水进行如图所示实验。开始时,试管中无明显现象,原因是
。该兴趣小组另取少量废水进行如图所示实验。开始时,试管中无明显现象,原因是Ⅱ.另一兴趣小组在实验室中尝试制备氢氧化铁胶体并探究它的性质。
(4)判断胶体的制备是否成功,可利用胶体的
(5)向
 胶体中逐滴加入了稀
胶体中逐滴加入了稀 溶液,结果出现了一系列变化:
溶液,结果出现了一系列变化:①先出现红褐色沉淀,原因是
②随后沉淀溶解,此反应的离子方程式是
您最近一年使用:0次



