名校
1 . Na元素相关的物质有很多且具有广泛的用途。
(1)氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。粗盐中一般含有CaCl2、MgCl2、CaSO4和MgSO4杂质。从粗盐制得精盐的过程如下:

①试剂Ⅰ是_____ 。
②加入试剂Ⅱ所发生的离子方程式为:_____
③操作a中,未用到的实验仪器是_____
A.蒸发皿 B.玻璃棒 C.漏斗 D.烧杯
④用到操作c的名称为_____ ,操作b不能省略,理由是_____ 。
(2)Na2CO3、NaHCO3走进千家万户,在食品加工方面有着广泛的用途。
①下列关于Na2CO3的认识正确的是_____ 。
A.受热易分解 B.俗称纯碱、苏打 C.可用于制皂 D.可与酸反应
②传统蒸馒头常采用酵头发面,再用Na2CO3调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。等质量的碳酸钠和碳酸氢钠,消耗酸更多的是_____ 。
③若面团发得不好,面团内的气孔少,略有酸味。可不用Na2CO3而用NaHCO3,继续揉面,上锅蒸后也能蒸出松软的馒头。解释NaHCO3的作用_____ 。
(3)某品牌复合膨松剂的说明书如下图所示。其中葡萄糖酸-δ-内酯和淀粉是助剂,其作用是防止膨松剂吸潮结块而失效。焦磷酸二氢二钠的作用是_____ 。

(1)氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。粗盐中一般含有CaCl2、MgCl2、CaSO4和MgSO4杂质。从粗盐制得精盐的过程如下:

①试剂Ⅰ是
②加入试剂Ⅱ所发生的离子方程式为:
③操作a中,未用到的实验仪器是
A.蒸发皿 B.玻璃棒 C.漏斗 D.烧杯
④用到操作c的名称为
(2)Na2CO3、NaHCO3走进千家万户,在食品加工方面有着广泛的用途。
①下列关于Na2CO3的认识正确的是
A.受热易分解 B.俗称纯碱、苏打 C.可用于制皂 D.可与酸反应
②传统蒸馒头常采用酵头发面,再用Na2CO3调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。等质量的碳酸钠和碳酸氢钠,消耗酸更多的是
③若面团发得不好,面团内的气孔少,略有酸味。可不用Na2CO3而用NaHCO3,继续揉面,上锅蒸后也能蒸出松软的馒头。解释NaHCO3的作用
(3)某品牌复合膨松剂的说明书如下图所示。其中葡萄糖酸-δ-内酯和淀粉是助剂,其作用是防止膨松剂吸潮结块而失效。焦磷酸二氢二钠的作用是

您最近一年使用:0次
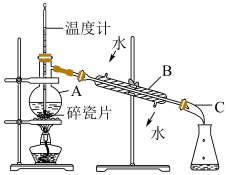
2 . 请回答实验室石油分馏的有关问题:________ ;B_____ 。
(2)图中有______ 处错误。
(3)实验室石油分馏的正确操作顺序是E→ F→____→A→______→_____→G,________ 。
A.连接接液管 B.装入碎瓷片和石油,塞上带温度计的塞子 C.检查装置气密性 D.连接B仪器及进出水管 E.在铁架台上放酒精灯,固定好铁圈,放上石棉网 F.固定好A仪器 G.加热
(4)分馏石油得到的各个馏分都是___________ (填“混合物”或“纯净物”),在A中注入原油后,加几片碎瓷片的目的是___________ 。
(2)图中有
(3)实验室石油分馏的正确操作顺序是E→ F→____→A→______→_____→G,
A.连接接液管 B.装入碎瓷片和石油,塞上带温度计的塞子 C.检查装置气密性 D.连接B仪器及进出水管 E.在铁架台上放酒精灯,固定好铁圈,放上石棉网 F.固定好A仪器 G.加热
(4)分馏石油得到的各个馏分都是
您最近一年使用:0次
名校
解题方法
3 . 碘化钾( )是实验室常用的化学试剂,用途广泛。一种利用含碘废液(碘的主要存在形式为
)是实验室常用的化学试剂,用途广泛。一种利用含碘废液(碘的主要存在形式为 和
和 )制备碘化钾的实验步骤如下:
)制备碘化钾的实验步骤如下:
步骤Ⅰ:取含碘废液,调节溶液 为
为 ,加入一定量
,加入一定量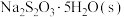 ,溶解,加热至30℃,加入稍过量
,溶解,加热至30℃,加入稍过量 粉末,搅拌,充分反应后,过滤得
粉末,搅拌,充分反应后,过滤得 沉淀;
沉淀;
步骤Ⅱ:在 圆底烧瓶中加入上述制备的
圆底烧瓶中加入上述制备的 沉淀,铁粉(过量),
沉淀,铁粉(过量), 蒸馏水,搅拌,沸水浴加热1小时,冷却,抽滤。将滤液倒入
蒸馏水,搅拌,沸水浴加热1小时,冷却,抽滤。将滤液倒入 烧杯中,加入约
烧杯中,加入约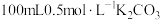 溶液,搅拌,煮沸,静置,过滤,得滤液A;
溶液,搅拌,煮沸,静置,过滤,得滤液A;
步骤Ⅲ:用氢碘酸调滤液A的 ,将滤液倒入___________(填仪器名称)中加热至___________(填现象),冷却,干燥,得到
,将滤液倒入___________(填仪器名称)中加热至___________(填现象),冷却,干燥,得到 晶体。
晶体。
回答下列问题:
(1)步骤Ⅰ中的控温方法为___________ , 与
与 转化为
转化为 的反应为①
的反应为① ,②
,② ,则反应②中氧化剂与还原剂的物质的量之比为
,则反应②中氧化剂与还原剂的物质的量之比为___________ 。
(2)步骤Ⅱ中铁粉转化为 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(3)步骤Ⅲ中,仪器的名称是___________ ,现象是___________ 。
(4)产品中KI含量的测定
称取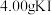 4.00样品,配成
4.00样品,配成 溶液,取
溶液,取 溶液于锥形瓶中,加入
溶液于锥形瓶中,加入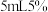 乙酸溶液及3滴曙红钠盐作指示剂,用
乙酸溶液及3滴曙红钠盐作指示剂,用 的
的 标准溶液避光滴定至沉淀呈红色(终点),平行滴定三次,消耗
标准溶液避光滴定至沉淀呈红色(终点),平行滴定三次,消耗 标准溶液分别为
标准溶液分别为 、
、 、
、 。
。
①用 标准溶液滴定时要避光的原因是
标准溶液滴定时要避光的原因是___________ ,在滴定时 溶液应盛放在
溶液应盛放在___________ (“酸式”或“碱式”)滴定管。
②样品中 的质量分数为
的质量分数为___________ 。
 )是实验室常用的化学试剂,用途广泛。一种利用含碘废液(碘的主要存在形式为
)是实验室常用的化学试剂,用途广泛。一种利用含碘废液(碘的主要存在形式为 和
和 )制备碘化钾的实验步骤如下:
)制备碘化钾的实验步骤如下:步骤Ⅰ:取含碘废液,调节溶液
 为
为 ,加入一定量
,加入一定量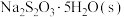 ,溶解,加热至30℃,加入稍过量
,溶解,加热至30℃,加入稍过量 粉末,搅拌,充分反应后,过滤得
粉末,搅拌,充分反应后,过滤得 沉淀;
沉淀;步骤Ⅱ:在
 圆底烧瓶中加入上述制备的
圆底烧瓶中加入上述制备的 沉淀,铁粉(过量),
沉淀,铁粉(过量), 蒸馏水,搅拌,沸水浴加热1小时,冷却,抽滤。将滤液倒入
蒸馏水,搅拌,沸水浴加热1小时,冷却,抽滤。将滤液倒入 烧杯中,加入约
烧杯中,加入约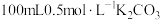 溶液,搅拌,煮沸,静置,过滤,得滤液A;
溶液,搅拌,煮沸,静置,过滤,得滤液A;步骤Ⅲ:用氢碘酸调滤液A的
 ,将滤液倒入___________(填仪器名称)中加热至___________(填现象),冷却,干燥,得到
,将滤液倒入___________(填仪器名称)中加热至___________(填现象),冷却,干燥,得到 晶体。
晶体。回答下列问题:
(1)步骤Ⅰ中的控温方法为
 与
与 转化为
转化为 的反应为①
的反应为① ,②
,② ,则反应②中氧化剂与还原剂的物质的量之比为
,则反应②中氧化剂与还原剂的物质的量之比为(2)步骤Ⅱ中铁粉转化为
 ,该反应的化学方程式为
,该反应的化学方程式为(3)步骤Ⅲ中,仪器的名称是
(4)产品中KI含量的测定
称取
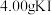 4.00样品,配成
4.00样品,配成 溶液,取
溶液,取 溶液于锥形瓶中,加入
溶液于锥形瓶中,加入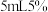 乙酸溶液及3滴曙红钠盐作指示剂,用
乙酸溶液及3滴曙红钠盐作指示剂,用 的
的 标准溶液避光滴定至沉淀呈红色(终点),平行滴定三次,消耗
标准溶液避光滴定至沉淀呈红色(终点),平行滴定三次,消耗 标准溶液分别为
标准溶液分别为 、
、 、
、 。
。①用
 标准溶液滴定时要避光的原因是
标准溶液滴定时要避光的原因是 溶液应盛放在
溶液应盛放在②样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
2024-01-02更新
|
210次组卷
|
2卷引用:贵州省贵阳市2023-2024学年高三上学期11月质量检测化学试题
名校
解题方法
4 . 选择完成下列实验的装置。
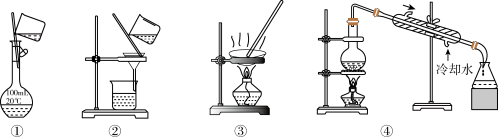
(1)除去水中的泥沙用___________ (填序号,下同)。
(2)配制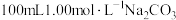 溶液,选用
溶液,选用___________ 。
(3)自来水制备蒸馏水,选用___________ 。
(4)从 溶液中获取
溶液中获取 固体,选用
固体,选用___________ 。

(1)除去水中的泥沙用
(2)配制
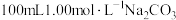 溶液,选用
溶液,选用(3)自来水制备蒸馏水,选用
(4)从
 溶液中获取
溶液中获取 固体,选用
固体,选用
您最近一年使用:0次
5 . 请选择正确的分离方法:①过滤②蒸馏③降温结晶④萃取⑤分液(请填序号)
(1)除去氯化钾中的二氧化锰___________ 。
(2)分离汽油和氯化钠溶液___________ 。
(3)除去自来水中的杂质___________ 。
(1)除去氯化钾中的二氧化锰
(2)分离汽油和氯化钠溶液
(3)除去自来水中的杂质
您最近一年使用:0次
名校
6 . Ⅰ.某研究性学习小组为了验证臭氧的氧化性强于氧气 ,设计了实验。
(1)a溶液是一种显色剂,用来检验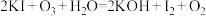 反应确有发生,a物质是
反应确有发生,a物质是___________ 。
(2)已知碘在酒精中的溶解度比在水中大得多,能否用酒精来萃取碘水中的碘___________ (填“能”或“不能”),其理由是___________ 。
(3)向碘水中加入适量的四氯化碳,充分振荡后,观察到的现象是___________。
(4)写出在臭氧消毒柜放电条件下产生 的化学方程式:
的化学方程式:___________ 。这是一个___________ (填“氧化还原”或“非氧化还原”)反应。
(5)在 氧化KI的反应中
氧化KI的反应中
①用单线桥法标出上述反应电子转移的方向和数目_________ 。
②若有9.6g 发生反应,则转移电子的物质的量为
发生反应,则转移电子的物质的量为___________ ,发生氧化反应的元素是___________ ;还原产物为___________ 。
Ⅱ.海水是巨大的资源宝库,可以进行综合利用。从海水中提取淡水、食盐和溴的过程如下:
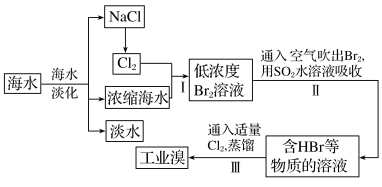
(6)步骤I获得 的反应的离子方程式为
的反应的离子方程式为___________
(7)步骤II用 水溶液吸收
水溶液吸收 ,使溴蒸气转化为氢溴酸以达到富集的目的,其反应的化学方程式为
,使溴蒸气转化为氢溴酸以达到富集的目的,其反应的化学方程式为___________ (若反应中生成2molHBr,则消耗lmol )。
)。
(8)根据上述反应可判断出 、
、 、
、 三种物质氧化性由强到弱的顺序是
三种物质氧化性由强到弱的顺序是___________ 。
(1)a溶液是一种显色剂,用来检验
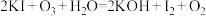 反应确有发生,a物质是
反应确有发生,a物质是(2)已知碘在酒精中的溶解度比在水中大得多,能否用酒精来萃取碘水中的碘
(3)向碘水中加入适量的四氯化碳,充分振荡后,观察到的现象是___________。
| A.溶液分层,上层紫红色,下层接近无色 |
| B.溶液不分层,溶液紫红色 |
| C.溶液分层,上层接近无色,下层紫红色 |
| D.溶液不分层,溶液黄色 |
(4)写出在臭氧消毒柜放电条件下产生
 的化学方程式:
的化学方程式:(5)在
 氧化KI的反应中
氧化KI的反应中
①用单线桥法标出上述反应电子转移的方向和数目
②若有9.6g
 发生反应,则转移电子的物质的量为
发生反应,则转移电子的物质的量为Ⅱ.海水是巨大的资源宝库,可以进行综合利用。从海水中提取淡水、食盐和溴的过程如下:

(6)步骤I获得
 的反应的离子方程式为
的反应的离子方程式为(7)步骤II用
 水溶液吸收
水溶液吸收 ,使溴蒸气转化为氢溴酸以达到富集的目的,其反应的化学方程式为
,使溴蒸气转化为氢溴酸以达到富集的目的,其反应的化学方程式为 )。
)。(8)根据上述反应可判断出
 、
、 、
、 三种物质氧化性由强到弱的顺序是
三种物质氧化性由强到弱的顺序是
您最近一年使用:0次
7 . Ⅰ.利用物质的溶解度对物质进行分离、提纯。图甲、图乙所示为一些物质的溶解度随温度变化的曲线。

(1) 固体中含少量NaCl,提纯
固体中含少量NaCl,提纯 固体的操作方法是加水溶解、
固体的操作方法是加水溶解、______ 、______ 、过滤、洗涤、干燥。
(2)图乙所示为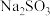 的溶解度随温度的变化曲线.常温下由
的溶解度随温度的变化曲线.常温下由 稀溶液获取
稀溶液获取 固体的方法是
固体的方法是____________ 。
Ⅱ.硫酸钠-过氧化氢加合物( )的组成可通过下列实验测定:
)的组成可通过下列实验测定:
①准确称取17.700 g样品,配制成100.00 mL溶液A
②将A两等份,取一份,加入盐酸酸化的BaCl₂溶液至沉淀完全、过滤、洗涤、干燥至恒重,得到白色固体11.65 g。
③另一份加适量稀硫酸酸化后,与50 mL 0.2 mol/L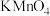 溶液恰好完全反应。
溶液恰好完全反应。
(3)已知 与
与 反应的化学方程式如下:
反应的化学方程式如下:
 ,通过计算确定样品的组成
,通过计算确定样品的组成________ (写出计算过程)。

(1)
 固体中含少量NaCl,提纯
固体中含少量NaCl,提纯 固体的操作方法是加水溶解、
固体的操作方法是加水溶解、(2)图乙所示为
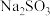 的溶解度随温度的变化曲线.常温下由
的溶解度随温度的变化曲线.常温下由 稀溶液获取
稀溶液获取 固体的方法是
固体的方法是Ⅱ.硫酸钠-过氧化氢加合物(
 )的组成可通过下列实验测定:
)的组成可通过下列实验测定:①准确称取17.700 g样品,配制成100.00 mL溶液A
②将A两等份,取一份,加入盐酸酸化的BaCl₂溶液至沉淀完全、过滤、洗涤、干燥至恒重,得到白色固体11.65 g。
③另一份加适量稀硫酸酸化后,与50 mL 0.2 mol/L
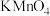 溶液恰好完全反应。
溶液恰好完全反应。(3)已知
 与
与 反应的化学方程式如下:
反应的化学方程式如下:
 ,通过计算确定样品的组成
,通过计算确定样品的组成
您最近一年使用:0次
2023-12-24更新
|
91次组卷
|
2卷引用:江苏省宿迁市沭阳县2023-2024学年高一上学期期中调研测试化学试题
名校
解题方法
8 . 物质的分离和提纯都是利用物质状态(相)的不同进行操作的,固体与液体、液体与气体、气体与固体的分离都是比较容易,相对的固固分离、液液分离、气气分离都比较困难。因此我们在进行物质的分离与提纯时经常会使用物质的状态不同进行分离。
(1)HCl中含有少量水蒸气选用的试剂为:___________ 。
(2)酒精和水分离的操作名称为:___________ 。
(3)除去CO2中的CO可采取的操作是:___________ 。
(4)氯化钠、硝酸钾的混合物中去除氯化钠的操作名称为___________ 。
(5)上述实验操作的具体操作为:___________ 。
(6)上述操作如果除不干净,可以采用的操作为___________ 。
(1)HCl中含有少量水蒸气选用的试剂为:
(2)酒精和水分离的操作名称为:
(3)除去CO2中的CO可采取的操作是:
(4)氯化钠、硝酸钾的混合物中去除氯化钠的操作名称为
(5)上述实验操作的具体操作为:
(6)上述操作如果除不干净,可以采用的操作为
您最近一年使用:0次
名校
9 . 氯化钠既是我们日常生活中不可缺少的调味品,也是一种重要的化工原料。某化学兴趣小组进行粗盐(主要含有泥沙、 、
、 、
、 、
、 、
、 )提纯实验。
)提纯实验。
I.甲同学的操作步骤如图所示:
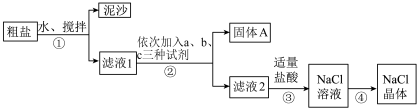
已知: 不溶于稀盐酸和稀硝酸。
不溶于稀盐酸和稀硝酸。
依据所学知识回答下列问题:
(1)操作①所用的玻璃仪器包括烧杯、___________ 。
(2)从产品纯度考虑,试剂a、b、c可以分别为___________ (填标号);加入盐酸时发生反应生成 的离子方程式为
的离子方程式为___________ 。
A. 溶液、
溶液、 溶液、
溶液、 溶液
溶液
B. 溶液、
溶液、 溶液、
溶液、 溶液
溶液
C. 溶液、
溶液、 液、
液、 溶液
溶液
II.乙同学对甲同学的实验进行评价,提出了一些猜想,并设计实验进行验证:
供选择的试剂:稀盐酸、 溶液、
溶液、 溶液。
溶液。
(3)完成上述表格中:①___________ ;②___________ ;③___________ ;④___________ 。
(4)根据乙同学的实验,请对甲同学的实验设计进行评价:___________ 。
 、
、 、
、 、
、 、
、 )提纯实验。
)提纯实验。I.甲同学的操作步骤如图所示:

已知:
 不溶于稀盐酸和稀硝酸。
不溶于稀盐酸和稀硝酸。依据所学知识回答下列问题:
(1)操作①所用的玻璃仪器包括烧杯、
(2)从产品纯度考虑,试剂a、b、c可以分别为
 的离子方程式为
的离子方程式为A.
 溶液、
溶液、 溶液、
溶液、 溶液
溶液B.
 溶液、
溶液、 溶液、
溶液、 溶液
溶液C.
 溶液、
溶液、 液、
液、 溶液
溶液II.乙同学对甲同学的实验进行评价,提出了一些猜想,并设计实验进行验证:
| 猜想 | 验证的方法 | 现象 | 结论 |
猜想1:固体A中含 | 取少量固体A于试管中,先加入足量①____________,再加入②_________。 | 有气泡产生,无白色沉淀 | ③_________ |
猜想2:最后制得的 晶体中还含有 晶体中还含有 | 取少量提纯后的 晶体于试管中,加入适量的蒸馏水溶解,滴入稀 晶体于试管中,加入适量的蒸馏水溶解,滴入稀 和 和 | ④___________ | 猜想2成立 |
 溶液、
溶液、 溶液。
溶液。(3)完成上述表格中:①
(4)根据乙同学的实验,请对甲同学的实验设计进行评价:
您最近一年使用:0次
名校
10 . 用于分离和提纯物质的方法有:A.过滤;B.蒸发结晶;C.降温结晶;D.萃取;E.分液;F.蒸馏;G.渗析。请用字母填出下列实验操作所用到的分离和提纯方法。
(1)分离苯和水__________ 。
(2)除去 胶体中的
胶体中的 杂质
杂质__________ ;
(3)用苯提取溴水中的溴单质__________ ;
(4)海水淡化__________ ;
(5)海水晒盐__________ ;
(6)除去硝酸钾固体中的少量氯化钠杂质__________ 。
(1)分离苯和水
(2)除去
 胶体中的
胶体中的 杂质
杂质(3)用苯提取溴水中的溴单质
(4)海水淡化
(5)海水晒盐
(6)除去硝酸钾固体中的少量氯化钠杂质
您最近一年使用:0次



