名校
解题方法
1 . 亚硝酰氯(NOCl)可作为有机合成试剂。
已知:①
②沸点:NOCl为-6℃, 为-34℃,NO为-152℃。
为-34℃,NO为-152℃。
③NOCl易水解,能与 反应。
反应。
某研究小组用NO和 在如图所示装置中制备NOCl,并分离回收未反应的原料。
在如图所示装置中制备NOCl,并分离回收未反应的原料。
(1)通入 和NO前先通入氩气,作用是
和NO前先通入氩气,作用是___________ ;仪器D的名称是___________ 。
(2)将催化剂负载在玻璃棉上而不是直接平铺在玻璃管中,目的是___________ 。
(3)实验所需的NO可用 和
和 溶液在稀
溶液在稀 中反应制得,离子反应方程式为
中反应制得,离子反应方程式为___________ 。
(4)为分离产物和未反应的原料,低温浴槽A的温度区间应控制在___________ ,仪器C收集的物质是___________ 。
(5)大气污染物中的氮氧化物地可用NaOH吸收,先后发生如下反应: ;
; 。若33.6mL(标况下)氮氧化物(只含NO和
。若33.6mL(标况下)氮氧化物(只含NO和 )与VmL 0.1mol/L NaOH溶液恰好完全反应,则
)与VmL 0.1mol/L NaOH溶液恰好完全反应,则
___________ 。
已知:①

②沸点:NOCl为-6℃,
 为-34℃,NO为-152℃。
为-34℃,NO为-152℃。③NOCl易水解,能与
 反应。
反应。某研究小组用NO和
 在如图所示装置中制备NOCl,并分离回收未反应的原料。
在如图所示装置中制备NOCl,并分离回收未反应的原料。
(1)通入
 和NO前先通入氩气,作用是
和NO前先通入氩气,作用是(2)将催化剂负载在玻璃棉上而不是直接平铺在玻璃管中,目的是
(3)实验所需的NO可用
 和
和 溶液在稀
溶液在稀 中反应制得,离子反应方程式为
中反应制得,离子反应方程式为(4)为分离产物和未反应的原料,低温浴槽A的温度区间应控制在
(5)大气污染物中的氮氧化物地可用NaOH吸收,先后发生如下反应:
 ;
; 。若33.6mL(标况下)氮氧化物(只含NO和
。若33.6mL(标况下)氮氧化物(只含NO和 )与VmL 0.1mol/L NaOH溶液恰好完全反应,则
)与VmL 0.1mol/L NaOH溶液恰好完全反应,则
您最近一年使用:0次
名校
2 . 利用锌灰(主要成分为ZnO,含有CuO、PbO、SiO2、FeO、Fe2O3等杂质)制备高纯ZnO的工艺流程如图:(已知PbSO4为难溶物)
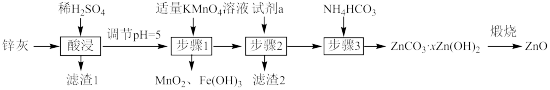
| A.滤渣1的成分只有H2SiO3和PbSO4 |
| B.加入的试剂a可为Zn,目的是除去Cu2+ |
C.步骤1中发生反应的离子方程式为MnO +3Fe3++7H2O=3Fe(OH)3↓+MnO2↓+5H+ +3Fe3++7H2O=3Fe(OH)3↓+MnO2↓+5H+ |
| D.若取步骤3后的干燥滤饼11.2g煅烧,得到产品8.1g,则x=2 |
您最近一年使用:0次
名校
3 . 除去粗盐中的杂质 、
、 和
和 ,过程如下:
,过程如下:
 、
、 和
和 ,过程如下:
,过程如下:
A.除去 的主要反应: 的主要反应: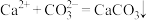 |
B.检验 是否除净的方法:取上层清液,加入足量稀盐酸溶液,无明显现象后,加 是否除净的方法:取上层清液,加入足量稀盐酸溶液,无明显现象后,加 溶液,观察是否产生沉淀 溶液,观察是否产生沉淀 |
| C.加稀盐酸调节pH后,采用蒸发结晶的方法得到NaCl固体 |
D.试剂①、②、③分别是NaOH、 、 、 |
您最近一年使用:0次
2024-04-23更新
|
188次组卷
|
2卷引用:山东省济宁市育才中学2023-2024学年高一下学期4月月考化学试题
名校
解题方法
4 . 以某铜矿石制备Cu(NO3)2晶体的工艺流程如图所示,已知铜矿石的主要成分为Cu2S和少量SiO2,滤液I中含Cu2+,滤渣I可回收单质S和SiO2。_______ 。
(2)铜矿石“氧化浸出”前需碾碎的目的是________ 。
(3)“滤液Ⅱ”中的金属阳离子为________ 。
(4)“反应”中生成Cu(NO3)2的离子方程式为________ 。
(5)“沉铁”后分离出沉淀的操作的名称为________ ,该操作在实验室进行时用到的玻璃仪器有________ 。
(6)“气体”与足量空气混合被水吸收过程中发生反应的化学方程式为________ ,其生成物可循环到上述流程中的________ (填“氧化浸出”“还原”“反应”或“沉铁”)过程中再利用。

(2)铜矿石“氧化浸出”前需碾碎的目的是
(3)“滤液Ⅱ”中的金属阳离子为
(4)“反应”中生成Cu(NO3)2的离子方程式为
(5)“沉铁”后分离出沉淀的操作的名称为
(6)“气体”与足量空气混合被水吸收过程中发生反应的化学方程式为
您最近一年使用:0次
2024-04-23更新
|
292次组卷
|
3卷引用:江西省赣州市兴国中学2023-2024学年高一下学期第一次阶段性考试化学试题
名校
5 .  是生产多晶硅的副产物。利用
是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺路线如下:
进行氯化处理以回收Li、Co等金属,工艺路线如下: 是粉红色固体,难溶于水。
是粉红色固体,难溶于水。
(1)Si在元素周期表的位置是___________ 。 的电子式为
的电子式为___________ 。
(2)烧渣是LiCl、 和
和 的混合物,“500℃焙烧”的化学方程式为
的混合物,“500℃焙烧”的化学方程式为___________ 。
(3)鉴别洗净的“滤饼3”和 中阳离子的常用方法是
中阳离子的常用方法是___________ 。
(4)实验室过滤操作时使用的玻璃仪器除玻璃棒还有___________ 。
(5)实验室检验 是否沉淀完全的操作是
是否沉淀完全的操作是___________ 。
(6)“850℃煅烧”时的化学方程式为___________ 。
 是生产多晶硅的副产物。利用
是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺路线如下:
进行氯化处理以回收Li、Co等金属,工艺路线如下: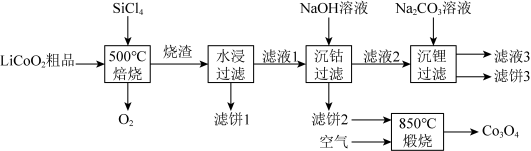
 是粉红色固体,难溶于水。
是粉红色固体,难溶于水。(1)Si在元素周期表的位置是
 的电子式为
的电子式为(2)烧渣是LiCl、
 和
和 的混合物,“500℃焙烧”的化学方程式为
的混合物,“500℃焙烧”的化学方程式为(3)鉴别洗净的“滤饼3”和
 中阳离子的常用方法是
中阳离子的常用方法是(4)实验室过滤操作时使用的玻璃仪器除玻璃棒还有
(5)实验室检验
 是否沉淀完全的操作是
是否沉淀完全的操作是(6)“850℃煅烧”时的化学方程式为
您最近一年使用:0次
名校
6 . 软锰矿的主要成分MnO2,还含有Fe2O3、MgO、Al2O3、CaO、SiO2等杂质,工业上用软锰矿制取MnSO4•H2O的流程如图
部分金属阳离子完全沉淀时的pH如下表
(1)浸出渣的主要成分为___________ (填化学式)。
(2)Mn的价层电子排布式为_________________ 。
(3)“浸出”过程中MnO2转化为Mn2+的离子方程式为_________________ 。
(4)第1步除杂加双氧水的目的是_________________ 。
(5)调pH至5~6所加的试剂,可选择__________ 。(填字母)。
a.CaO b.MgO c.Al2O3 d.氨水
(6)第2步除杂,主要是将Ca2+、Mg2+转化为相应氟化物沉淀除去,写出MnF2除去Mg2+的离子方程式:_______________ ,该反应的平衡常数为___________ (结果保留一位小数)。

部分金属阳离子完全沉淀时的pH如下表
| 金属阳离子 | Fe3+ | Al3+ | Mn2+ | Mg2+ |
| 完全沉淀时的pH | 3.2 | 5.2 | 10.4 | 12.4 |
(1)浸出渣的主要成分为
(2)Mn的价层电子排布式为
(3)“浸出”过程中MnO2转化为Mn2+的离子方程式为
(4)第1步除杂加双氧水的目的是
(5)调pH至5~6所加的试剂,可选择
a.CaO b.MgO c.Al2O3 d.氨水
(6)第2步除杂,主要是将Ca2+、Mg2+转化为相应氟化物沉淀除去,写出MnF2除去Mg2+的离子方程式:
您最近一年使用:0次
解题方法
7 . 某工厂的酸性废水中含有大量的 FeSO4和较多的 Cu2+。为了减少污染并变废为宝, 工厂计划从该废水中回收 FeSO4和金属铜。请根据以下流程图,回答下列问题。___________ ,加入试剂 b是___________ (填写试剂化学式)。
(2)为保证反应完全,流程中加入的试剂a、b均过量,溶液③中所含的阳离子有___________ (填写离子符号)。
(3)若取2mL 溶液②加入试管中,然后滴加氢氧化钠溶液,产生的现象___________ 。
(4)若取少量溶液②加入试管中,滴加一定量的 H2O2,写出反应离子方程式___________ 。
(5)产品取样研究:取 20g FeSO4·7H2O 产品加水溶解,滴加0.2mol/LBaCl2 溶液至不再产生沉淀,共消耗 BaCl2 溶液250mL,计算取样产品的纯度___________ 。
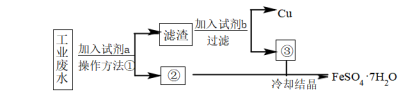
(2)为保证反应完全,流程中加入的试剂a、b均过量,溶液③中所含的阳离子有
(3)若取2mL 溶液②加入试管中,然后滴加氢氧化钠溶液,产生的现象
(4)若取少量溶液②加入试管中,滴加一定量的 H2O2,写出反应离子方程式
(5)产品取样研究:取 20g FeSO4·7H2O 产品加水溶解,滴加0.2mol/LBaCl2 溶液至不再产生沉淀,共消耗 BaCl2 溶液250mL,计算取样产品的纯度
您最近一年使用:0次
8 . 以苦卤(海水晒盐后得到的母液,显弱碱性,含 )为原料,利用空气吹出法进行“海水提溴”的工艺流程如图(已知:
)为原料,利用空气吹出法进行“海水提溴”的工艺流程如图(已知: 的沸点为58.78℃)。
的沸点为58.78℃)。
苦卤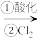 含
含 的海水
的海水 吸收液
吸收液 溴水混合物
溴水混合物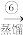 溴蒸气
溴蒸气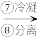 液溴
液溴
回答下列问题:
(1)①酸化的目的是防止_________________ (用离子方程式表示)。
(2)若步骤④使用 和
和 吸收吹出的
吸收吹出的 ,则反应的化学方程式为
,则反应的化学方程式为____________ ,步骤⑤再次用 氧化吸收液,重新生成
氧化吸收液,重新生成 。由此推出
。由此推出 、
、 、
、 的还原性由强到弱的顺序:
的还原性由强到弱的顺序:_________ 。空气吹出后的含溴空气中还含有 ,应选择除氯剂
,应选择除氯剂 溶液,若
溶液,若 少量,写出反应的离子方程式:
少量,写出反应的离子方程式:_____ 。
(3)步骤⑥中蒸馏的温度为80~90℃,温度过高或过低都不利于生产,请解释原因:_____________ 。
(4)该工艺流程中,不直接对“含 的海水”进行蒸馏,而是经历步骤③④⑤后才对“溴水混合物”进行蒸馏获得
的海水”进行蒸馏,而是经历步骤③④⑤后才对“溴水混合物”进行蒸馏获得 单质,“步骤③④⑤”的作用是
单质,“步骤③④⑤”的作用是____________________ 。
(5) 是一种分析试剂。向硫酸酸化的NaI溶液中逐滴加入
是一种分析试剂。向硫酸酸化的NaI溶液中逐滴加入 溶液,当加入2.6mol
溶液,当加入2.6mol  时,测得反应后溶液中溴和碘的存在形式及物质的量分别为:
时,测得反应后溶液中溴和碘的存在形式及物质的量分别为:
则原溶液中NaI的物质的量为_____________ mol。
 )为原料,利用空气吹出法进行“海水提溴”的工艺流程如图(已知:
)为原料,利用空气吹出法进行“海水提溴”的工艺流程如图(已知: 的沸点为58.78℃)。
的沸点为58.78℃)。苦卤
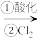 含
含 的海水
的海水 吸收液
吸收液 溴水混合物
溴水混合物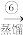 溴蒸气
溴蒸气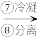 液溴
液溴回答下列问题:
(1)①酸化的目的是防止
(2)若步骤④使用
 和
和 吸收吹出的
吸收吹出的 ,则反应的化学方程式为
,则反应的化学方程式为 氧化吸收液,重新生成
氧化吸收液,重新生成 。由此推出
。由此推出 、
、 、
、 的还原性由强到弱的顺序:
的还原性由强到弱的顺序: ,应选择除氯剂
,应选择除氯剂 溶液,若
溶液,若 少量,写出反应的离子方程式:
少量,写出反应的离子方程式:(3)步骤⑥中蒸馏的温度为80~90℃,温度过高或过低都不利于生产,请解释原因:
(4)该工艺流程中,不直接对“含
 的海水”进行蒸馏,而是经历步骤③④⑤后才对“溴水混合物”进行蒸馏获得
的海水”进行蒸馏,而是经历步骤③④⑤后才对“溴水混合物”进行蒸馏获得 单质,“步骤③④⑤”的作用是
单质,“步骤③④⑤”的作用是(5)
 是一种分析试剂。向硫酸酸化的NaI溶液中逐滴加入
是一种分析试剂。向硫酸酸化的NaI溶液中逐滴加入 溶液,当加入2.6mol
溶液,当加入2.6mol  时,测得反应后溶液中溴和碘的存在形式及物质的量分别为:
时,测得反应后溶液中溴和碘的存在形式及物质的量分别为:粒子 |
|
|
|
物质的量/mol | 1.3 | 2 |
您最近一年使用:0次
名校
解题方法
9 . 晾晒海水获得的粗盐中含有可溶性杂质 、
、 、
、 等。粗盐提纯的工艺流程如下,下列说法正确的是
等。粗盐提纯的工艺流程如下,下列说法正确的是
 、
、 、
、 等。粗盐提纯的工艺流程如下,下列说法正确的是
等。粗盐提纯的工艺流程如下,下列说法正确的是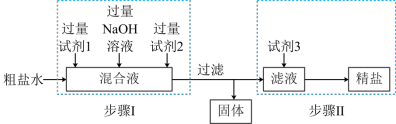
A.“步骤I”中试剂1为 溶液,试剂2为 溶液,试剂2为 溶液 溶液 |
| B.实验室分离“步骤I”生成的沉淀所需的玻璃仪器有烧杯、分液漏斗、玻璃棒 |
| C.“步骤II”中试剂3可以用稀硫酸代替稀盐酸 |
| D.“步骤II”从滤液中获得精盐的方法是蒸发结晶 |
您最近一年使用:0次
10 . 某中学研究性学习小组的以黄铁矿 (杂质为石英)为原料,设计了如下工艺流程:
(杂质为石英)为原料,设计了如下工艺流程:
(1)在空气中焙烧黄铁矿的化学方程式为:__________________________ 。
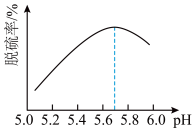
(2)研究发现,pH和温度对石灰石浆液的脱硫效率有一定影响。当烟气通入速度一定时,石灰石浆液的脱硫率与浆液pH的关系如图所示( )。
)。__________ 。
a.烟气通入石灰石浆液时的温度越高,吸收越快,吸收率越高
b.反应时需鼓入足量的空气以保证 被充分氧化生成
被充分氧化生成
c.将脱硫后的气体通入 溶液,可粗略判断烟气脱硫效率
溶液,可粗略判断烟气脱硫效率
d.石灰石浆液pH>5.7烟气脱硫效果降低,是因为石灰石的溶解程度增大
(3)写出反应Ⅱ的化学反应方程式_____________________ 。检验反应Ⅱ所得的滤液中所含阴离子的方法是____________________________ 。
(4)向红渣酸浸得到的滤液中加入适量铁粉还原,再由还原后的滤液制得 的操作为:
的操作为:__________ 、__________ 、过滤、洗涤、干燥。
(5)反应①反应方程式是______________ 。从反应①至④制取高纯多晶硅的过程中可以循环利用的物质有____________________ 。
 (杂质为石英)为原料,设计了如下工艺流程:
(杂质为石英)为原料,设计了如下工艺流程: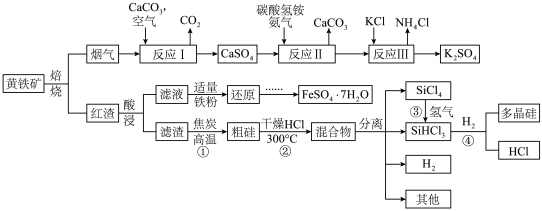
(1)在空气中焙烧黄铁矿的化学方程式为:
(2)研究发现,pH和温度对石灰石浆液的脱硫效率有一定影响。当烟气通入速度一定时,石灰石浆液的脱硫率与浆液pH的关系如图所示(
 )。
)。
a.烟气通入石灰石浆液时的温度越高,吸收越快,吸收率越高
b.反应时需鼓入足量的空气以保证
 被充分氧化生成
被充分氧化生成
c.将脱硫后的气体通入
 溶液,可粗略判断烟气脱硫效率
溶液,可粗略判断烟气脱硫效率d.石灰石浆液pH>5.7烟气脱硫效果降低,是因为石灰石的溶解程度增大
(3)写出反应Ⅱ的化学反应方程式
(4)向红渣酸浸得到的滤液中加入适量铁粉还原,再由还原后的滤液制得
 的操作为:
的操作为:(5)反应①反应方程式是
您最近一年使用:0次