重庆市2021届高三二诊康德卷(二模) 化学试题
重庆
高三
二模
2022-04-08
492次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、物质结构与性质、常见无机物及其应用、有机化学基础、化学实验基础、化学反应原理
重庆市2021届高三二诊康德卷(二模) 化学试题
重庆
高三
二模
2022-04-08
492次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、物质结构与性质、常见无机物及其应用、有机化学基础、化学实验基础、化学反应原理
一、单选题 添加题型下试题
单选题
|
适中(0.65)
解题方法
1. 化学与材料、生活密切相关,下列说法正确的是
| A.可溶性铜盐有毒,故人体内不存在铜元素 |
| B.新冠病毒疫苗冷藏存放的目的是避免蛋白质变性 |
C.“歼 ”飞机上大量使用的碳纤维是一种新型有机高分子材料 ”飞机上大量使用的碳纤维是一种新型有机高分子材料 |
| D.“蛟龙”号潜水器上的钛合金材料具有强度大、密度大、耐腐蚀等特性 |
【知识点】 化学科学对人类文明发展的意义解读 高分子材料 金属材料的性质及利用
您最近一年使用:0次
2021-04-19更新
|
315次组卷
|
2卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
单选题
|
适中(0.65)
解题方法
2. 下列化学用语的表述不正确 的是
A. 的结构式: 的结构式: | B.氯化铵的电子式: |
C.联氨 的球棍模型为 的球棍模型为 | D. 离子的结构示意图为 离子的结构示意图为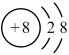 |
【知识点】 化学用语综合判断 化学键与物质类别关系的判断解读
您最近一年使用:0次
2022-04-08更新
|
367次组卷
|
3卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
单选题
|
容易(0.94)
3. 下列变化中,符合图示电子转移的是
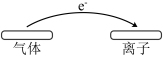

A. 溶液在空气中变质 溶液在空气中变质 | B. 气体使酸性高锰酸钾溶液褪色 气体使酸性高锰酸钾溶液褪色 |
| C.将氨气通入水中 | D.用 溶液吸收制取氯气的尾气 溶液吸收制取氯气的尾气 |
您最近一年使用:0次
2021-04-19更新
|
427次组卷
|
3卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题(已下线)专题05 氧化还原反应(限时精练)-2022届高考化学一轮复习热点题型归纳与变式训练 重庆市2021届高三二诊康德卷(二模) 化学试题
单选题
|
适中(0.65)
4. 一种食用香料的结构简式如图所示。下列有关说法不正确 的是
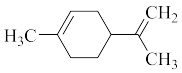

| A.它的一氯代物有8种 |
| B.它的分子中所有的碳原子不可能在同一平面上 |
C.它和丁基苯(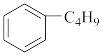 )互为同分异构体 )互为同分异构体 |
| D.一定条件下,它分别可以发生取代、氧化、还原等反应 |
您最近一年使用:0次
2021-04-19更新
|
331次组卷
|
2卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
单选题
|
适中(0.65)
5. 下列说法正确的是
| A.金属氧化物均为碱性氧化物 |
B.用饱和 溶液可鉴别乙酸乙酯、乙醇、乙酸 溶液可鉴别乙酸乙酯、乙醇、乙酸 |
| C.用红色石蕊试纸检测氨气时,试纸不能润湿 |
D.食醋清洗水垢的离子方程式为: |
您最近一年使用:0次
2021-04-19更新
|
187次组卷
|
2卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
单选题
|
适中(0.65)
6. 我国科研人员研究了在 催化剂上
催化剂上 加氢制甲醇过程中水的作用机理,其主反应历程如图所示(其中
加氢制甲醇过程中水的作用机理,其主反应历程如图所示(其中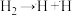 )。下列说法正确的是
)。下列说法正确的是

 催化剂上
催化剂上 加氢制甲醇过程中水的作用机理,其主反应历程如图所示(其中
加氢制甲醇过程中水的作用机理,其主反应历程如图所示(其中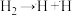 )。下列说法正确的是
)。下列说法正确的是
A.二氧化碳加氢制甲醇的反应原子利用率为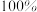 |
| B.该反应过程中,涉及了极性共价键和非极性共价键的断裂和生成 |
| C.使用催化剂可提高二氧化碳和氢气的平衡转化率 |
D.第④步变化的反应式为: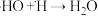 |
【知识点】 催化剂对化学反应速率的影响解读 共价键概念及判断解读
您最近一年使用:0次
2021-04-19更新
|
244次组卷
|
2卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
7. 下列实验操作或现象能用平衡移动原理解释的是
A.低温下食品不易变质 | B.用 与 与 制氧气 制氧气 |
C.淀粉在不同条件下水解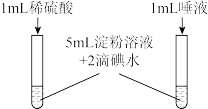 | D.卤化银沉淀的转化 |
| A.A | B.B | C.C | D.D |
【知识点】 催化剂对化学反应速率的影响解读 沉淀转化解读 淀粉、纤维素的水解
您最近一年使用:0次
2021-04-19更新
|
131次组卷
|
2卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
单选题
|
较难(0.4)
名校
8. 有 四种短周期主族元素,它们的原子序数依次增大,由这四种元素组成的化合物如图所示,下列说法正确的是
四种短周期主族元素,它们的原子序数依次增大,由这四种元素组成的化合物如图所示,下列说法正确的是

 四种短周期主族元素,它们的原子序数依次增大,由这四种元素组成的化合物如图所示,下列说法正确的是
四种短周期主族元素,它们的原子序数依次增大,由这四种元素组成的化合物如图所示,下列说法正确的是
A.原子半径大小: |
| B.Z和Y只能形成含有离子键的化合物 |
C. 三种元素能形成一种使高锰酸钾褪色的二元酸 三种元素能形成一种使高锰酸钾褪色的二元酸 |
| D.Y和W形成的化合物沸点高于X和W形成的化合物的沸点 |
您最近一年使用:0次
2021-04-19更新
|
1351次组卷
|
6卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题(已下线)化学-学科网2021年高三5月大联考考后强化卷(广东卷)(已下线)专题五 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)湖南省岳阳县一中2022届高三年级入学考试化学试题重庆市2021届高三二诊康德卷(二模) 化学试题福建省福州市福建师范大学附属中学2021-2022学年高二下学期期中考试化学试题
单选题
|
适中(0.65)
名校
9. 设 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是
 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是A.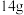 聚丙烯中含 聚丙烯中含 键总数目为 键总数目为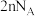 |
B.常温下, 的 的 溶液中含有的 溶液中含有的 数目为 数目为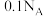 |
C.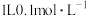 的 的 溶液中,阴离子总数大于 溶液中,阴离子总数大于 |
D.含有 个 个 胶粒的氢氧化铁胶体中,铁元素的质量为 胶粒的氢氧化铁胶体中,铁元素的质量为 |
您最近一年使用:0次
2021-04-19更新
|
671次组卷
|
4卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题(已下线)专题02 NA及其应用—2022年高考化学二轮复习讲练测(全国版)-讲义重庆市2021届高三二诊康德卷(二模) 化学试题湖南省怀化市沅陵县第一中学2021-2022学年高三下学期第二次模拟考试化学试题
单选题
|
较易(0.85)
名校
解题方法
您最近一年使用:0次
2021-04-19更新
|
318次组卷
|
3卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
单选题
|
适中(0.65)
解题方法
11. 微生物燃料电池是利用微生物作为催化剂降解污水中的有机物(以对苯二甲酸为例),其原理如图装置所示。下列判断错误 的是
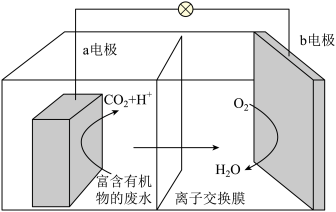

A.该微生物电池工作时 向负极移动 向负极移动 |
| B.该微生物电池工作时,电流由b极经负载流向a极 |
| C.微生物电池在处理废水时的能量转化为化学能变为电能 |
D.该微生物电池的负极电极反应式为: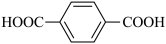 +12H2O-30e- +12H2O-30e- 8CO2+30H+ 8CO2+30H+ |
【知识点】 原电池电子流向判断及应用解读 原电池电极反应式书写解读 燃料电池
您最近一年使用:0次
2021-04-19更新
|
325次组卷
|
4卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题(已下线)第18讲 原电池 化学电源(精练)-2022年高考化学一轮复习讲练测重庆市2021届高三二诊康德卷(二模) 化学试题 四川省成都市石室天府中学2023-2024学年高三上学期入学考试化学试题
单选题
|
适中(0.65)
12. 下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将铁块放入浓硝酸中 | 无明显现象 | 二者在常温下不反应 |
| B | 将氯水滴入含有 的 的 溶液中 溶液中 | 产生红色沉淀 | 实验中发生的离子反应: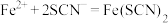 |
| C | 向碘水中加入等体积的 ,振荡、静置 ,振荡、静置 | 上层接近无色 下层显紫红色 |  在 在 中的溶解度大于在水中的溶解度 中的溶解度大于在水中的溶解度 |
| D | 在某溶液中先加入 溶液,再滴入盐酸 溶液,再滴入盐酸 | 先有白色沉淀,加入盐酸,沉淀不溶解 | 原溶液中一定有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-04-19更新
|
329次组卷
|
2卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
单选题
|
适中(0.65)
13. 室温下,用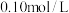 的盐酸滴定
的盐酸滴定 ,滴定过程中
,滴定过程中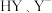 的物质的量分数与溶液
的物质的量分数与溶液 变化关系如图所示[已知:
变化关系如图所示[已知: ]。下列说法正确的是
]。下列说法正确的是

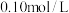 的盐酸滴定
的盐酸滴定 ,滴定过程中
,滴定过程中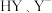 的物质的量分数与溶液
的物质的量分数与溶液 变化关系如图所示[已知:
变化关系如图所示[已知: ]。下列说法正确的是
]。下列说法正确的是
A. 是弱酸,其电离平衡常数为 是弱酸,其电离平衡常数为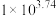 |
B.a代表的是 的物质的量分数随 的物质的量分数随 的变化关系 的变化关系 |
C.溶液中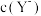 与 与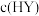 之和始终为定值 之和始终为定值 |
D.X点所在溶液中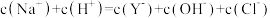 |
您最近一年使用:0次
2021-04-19更新
|
229次组卷
|
3卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题(已下线)难点8 水溶液中的四大平衡常数-2021年高考化学【热点·重点·难点】专练(山东专用)重庆市2021届高三二诊康德卷(二模) 化学试题
单选题
|
适中(0.65)
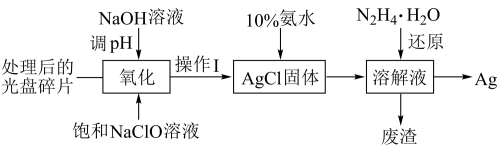
14. 实验室从光盘金属层中提取 (其他金属微量忽略不计)的流程如下图所示,已知“氧化”与“还原”过程中分别生成了
(其他金属微量忽略不计)的流程如下图所示,已知“氧化”与“还原”过程中分别生成了 和
和 。下列说法
。下列说法不正确 的是
 (其他金属微量忽略不计)的流程如下图所示,已知“氧化”与“还原”过程中分别生成了
(其他金属微量忽略不计)的流程如下图所示,已知“氧化”与“还原”过程中分别生成了 和
和 。下列说法
。下列说法
| A.操作I的名称是过滤 |
| B.“氧化”过程可适当加热提高反应速率 |
C.“氧化”过程发生的反应为 |
D.理论上每消耗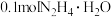 能提取的 能提取的 的质量为 的质量为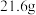 |
您最近一年使用:0次
2021-04-19更新
|
359次组卷
|
3卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题(已下线)专题05 氧化还原反应 (热点讲义)-2022届高考化学一轮复习热点题型归纳与变式训练重庆市2021届高三二诊康德卷(二模) 化学试题
二、解答题 添加题型下试题
解答题-工业流程题
|
较难(0.4)
解题方法
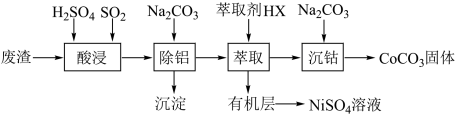
15. 金属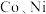 性质相似,在电子工业以及金属材料上应用十分广泛。现以含钴、镍、铝的废渣(主要成分为
性质相似,在电子工业以及金属材料上应用十分广泛。现以含钴、镍、铝的废渣(主要成分为 、少量杂质
、少量杂质 )提取钴、镍化合物的工艺如下:
)提取钴、镍化合物的工艺如下:
已知: 时,
时,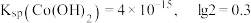
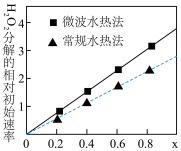
(1)酸浸时得到一种气体,其化学式为___________ ,酸浸时 参与的离子反应方程式为
参与的离子反应方程式为___________ ,能提高钴、镍元素浸出率的措施有___________ (写出两条即可)。
(2)除铝时加入碳酸钠产生沉淀的离子反应方程式为___________ , 时,若“沉钴”开始时
时,若“沉钴”开始时 ,则控制
,则控制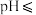
___________ 时不会产生 。
。
(3)用 为原料采用微波水热法和常规水热法均可制得使
为原料采用微波水热法和常规水热法均可制得使 分解的高效催化剂
分解的高效催化剂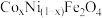 ,(其中
,(其中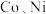 均为
均为 价)。如图是用两种不同方法制得的
价)。如图是用两种不同方法制得的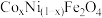 在
在 时催化分解
时催化分解 的
的 溶液的相对初始速率随x变化曲线。
溶液的相对初始速率随x变化曲线。
①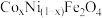 中
中 的价态为
的价态为___________ 。
②由图中信息可知:___________ 法制取的催化剂活性更高。
③ 两种离子中催化效果更好的是
两种离子中催化效果更好的是___________ 。
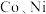 性质相似,在电子工业以及金属材料上应用十分广泛。现以含钴、镍、铝的废渣(主要成分为
性质相似,在电子工业以及金属材料上应用十分广泛。现以含钴、镍、铝的废渣(主要成分为 、少量杂质
、少量杂质 )提取钴、镍化合物的工艺如下:
)提取钴、镍化合物的工艺如下:
已知:
 时,
时,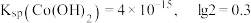

(1)酸浸时得到一种气体,其化学式为
 参与的离子反应方程式为
参与的离子反应方程式为(2)除铝时加入碳酸钠产生沉淀的离子反应方程式为
 时,若“沉钴”开始时
时,若“沉钴”开始时 ,则控制
,则控制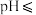
 。
。(3)用
 为原料采用微波水热法和常规水热法均可制得使
为原料采用微波水热法和常规水热法均可制得使 分解的高效催化剂
分解的高效催化剂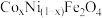 ,(其中
,(其中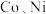 均为
均为 价)。如图是用两种不同方法制得的
价)。如图是用两种不同方法制得的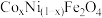 在
在 时催化分解
时催化分解 的
的 溶液的相对初始速率随x变化曲线。
溶液的相对初始速率随x变化曲线。①
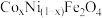 中
中 的价态为
的价态为②由图中信息可知:
③
 两种离子中催化效果更好的是
两种离子中催化效果更好的是
您最近一年使用:0次
2021-04-19更新
|
251次组卷
|
2卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
解答题-原理综合题
|
较难(0.4)
解题方法
16. 硫及硫的化合物在生产、生活以及国防上都有广泛的用途,如 主要作为制造黏胶纤维、玻璃纸的原材料。请回答下列有关问题。
主要作为制造黏胶纤维、玻璃纸的原材料。请回答下列有关问题。

(1)已知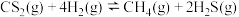 。在体积为
。在体积为 的恒容密闭容器中,起始加入
的恒容密闭容器中,起始加入 和
和 的物质的量分别为
的物质的量分别为 和
和 ,测得不同温度下平衡体系中
,测得不同温度下平衡体系中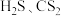 的物质的量分数与温度的关系如图所示:
的物质的量分数与温度的关系如图所示:
①上述反应的正反应是___________ 反应(填“放热”或“吸热”),理由是___________ 。
②下列图象正确且一定能说明 时刻反应处于平衡状态的是
时刻反应处于平衡状态的是___________ (填标号)。
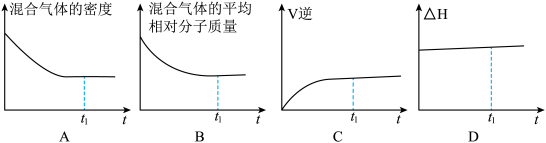
③A点时混合气体的平均相对分子质量为___________ (保留一位小数);若此时测得容器内 的压强为p,则该反应的平衡常数
的压强为p,则该反应的平衡常数
___________ 。
(2)工业生产中利用原电池可将 转化为
转化为 ,装置如图
,装置如图 所示:
所示:
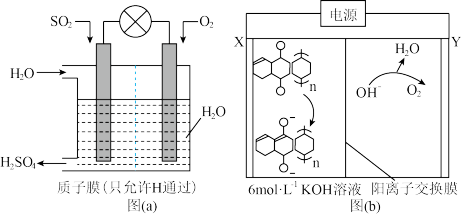
①则正极的电极反应式为___________ 。
②用该电池给一种可充电的新型水系聚合物空气电池充电,其装置如图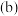 所示,
所示, 往
往___________ (填“X”或“Y”)区移动;电解的总反应式为___________ 。
 主要作为制造黏胶纤维、玻璃纸的原材料。请回答下列有关问题。
主要作为制造黏胶纤维、玻璃纸的原材料。请回答下列有关问题。
(1)已知
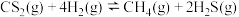 。在体积为
。在体积为 的恒容密闭容器中,起始加入
的恒容密闭容器中,起始加入 和
和 的物质的量分别为
的物质的量分别为 和
和 ,测得不同温度下平衡体系中
,测得不同温度下平衡体系中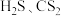 的物质的量分数与温度的关系如图所示:
的物质的量分数与温度的关系如图所示:①上述反应的正反应是
②下列图象正确且一定能说明
 时刻反应处于平衡状态的是
时刻反应处于平衡状态的是
③A点时混合气体的平均相对分子质量为
 的压强为p,则该反应的平衡常数
的压强为p,则该反应的平衡常数
(2)工业生产中利用原电池可将
 转化为
转化为 ,装置如图
,装置如图 所示:
所示:
①则正极的电极反应式为
②用该电池给一种可充电的新型水系聚合物空气电池充电,其装置如图
 所示,
所示, 往
往【知识点】 化学平衡的有关计算 化学平衡状态的判断方法解读 原电池原理理解解读
您最近一年使用:0次
2021-04-19更新
|
198次组卷
|
2卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
解答题-实验探究题
|
适中(0.65)
17. 富马酸亚铁(结构简式 ,相对分子质量170)是治疗贫血药物的一种。实验制备富马酸亚铁并测其产品中富马酸亚铁的质量分数。
,相对分子质量170)是治疗贫血药物的一种。实验制备富马酸亚铁并测其产品中富马酸亚铁的质量分数。
Ⅰ.富马酸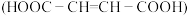 的制备。制取装置如图所示(夹持仪器已略去),按如图装置打开分液漏斗活塞,滴加糠醛(
的制备。制取装置如图所示(夹持仪器已略去),按如图装置打开分液漏斗活塞,滴加糠醛(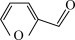 ),在
),在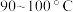 条件下持续加热
条件下持续加热 。
。
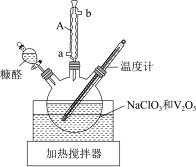
(1)仪器A的名称是___________ ,仪器A的作用是___________ 。
Ⅱ.富马酸亚铁的制备
步骤1:将 富马酸置于
富马酸置于 烧杯中,加水
烧杯中,加水 在热沸搅拌下,加入
在热沸搅拌下,加入 溶液
溶液 ,使其
,使其 为
为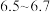 ;
;
步骤2:将上述溶液转移至如图所示的装置中,缓慢加入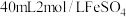 溶液,维持温度
溶液,维持温度 ,充分搅拌
,充分搅拌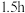 ;
;

步骤3:冷却、过滤,洗涤沉淀,然后水浴干燥,得到粗产品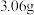
(2)在回流过程中一直通入氮气的目的是___________ 。
(3)步骤1控制溶液 为
为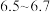 ;若反应后溶液的
;若反应后溶液的 太小,则引起的后果是
太小,则引起的后果是___________ ,若反应后溶液的 太大,则引起的后果是
太大,则引起的后果是___________ 。
Ⅲ.产品纯度测定
步骤①:准确称取粗产品 ,加煮沸过的
,加煮沸过的 ,溶液
,溶液 ,待样品完全溶解后,加煮沸过的冷水
,待样品完全溶解后,加煮沸过的冷水 和4滴邻二氮菲-亚铁指示剂,立即用
和4滴邻二氮菲-亚铁指示剂,立即用 (硫酸高铈铵)
(硫酸高铈铵)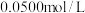 标准溶液进行滴定。用去标准液的体积为
标准溶液进行滴定。用去标准液的体积为 (反应式为
(反应式为 )。
)。
步骤②:不加产品,重复步骤①操作,滴定终点用去标准液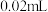 。
。
(4)___________ (填“能”或“否”)直接用酸性高锰酸钾滴定来测定产品的纯度。
(5)产品中富马酸亚铁的质量分数为___________ 。
 ,相对分子质量170)是治疗贫血药物的一种。实验制备富马酸亚铁并测其产品中富马酸亚铁的质量分数。
,相对分子质量170)是治疗贫血药物的一种。实验制备富马酸亚铁并测其产品中富马酸亚铁的质量分数。Ⅰ.富马酸
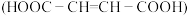 的制备。制取装置如图所示(夹持仪器已略去),按如图装置打开分液漏斗活塞,滴加糠醛(
的制备。制取装置如图所示(夹持仪器已略去),按如图装置打开分液漏斗活塞,滴加糠醛( ),在
),在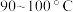 条件下持续加热
条件下持续加热 。
。
(1)仪器A的名称是
Ⅱ.富马酸亚铁的制备
步骤1:将
 富马酸置于
富马酸置于 烧杯中,加水
烧杯中,加水 在热沸搅拌下,加入
在热沸搅拌下,加入 溶液
溶液 ,使其
,使其 为
为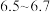 ;
;步骤2:将上述溶液转移至如图所示的装置中,缓慢加入
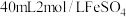 溶液,维持温度
溶液,维持温度 ,充分搅拌
,充分搅拌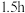 ;
;
步骤3:冷却、过滤,洗涤沉淀,然后水浴干燥,得到粗产品
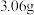
(2)在回流过程中一直通入氮气的目的是
(3)步骤1控制溶液
 为
为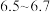 ;若反应后溶液的
;若反应后溶液的 太小,则引起的后果是
太小,则引起的后果是 太大,则引起的后果是
太大,则引起的后果是Ⅲ.产品纯度测定
步骤①:准确称取粗产品
 ,加煮沸过的
,加煮沸过的 ,溶液
,溶液 ,待样品完全溶解后,加煮沸过的冷水
,待样品完全溶解后,加煮沸过的冷水 和4滴邻二氮菲-亚铁指示剂,立即用
和4滴邻二氮菲-亚铁指示剂,立即用 (硫酸高铈铵)
(硫酸高铈铵)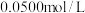 标准溶液进行滴定。用去标准液的体积为
标准溶液进行滴定。用去标准液的体积为 (反应式为
(反应式为 )。
)。步骤②:不加产品,重复步骤①操作,滴定终点用去标准液
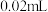 。
。(4)
(5)产品中富马酸亚铁的质量分数为
您最近一年使用:0次
2021-04-19更新
|
451次组卷
|
4卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题(已下线)化学-学科网2021年高三5月大联考考后强化卷(广东卷)重庆市2021届高三二诊康德卷(二模) 化学试题(已下线)易错点33 物质的制备-备战2023年高考化学考试易错题
解答题-结构与性质
|
较难(0.4)
解题方法
18. 离子液体被认为是21世纪理想的绿色溶剂,是指室温或者接近室温时呈液态,而本身由阴、阳离子构成的化合物。氯代 丁基
丁基 甲基咪唑离子液
甲基咪唑离子液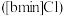 可以与
可以与 混合形成离子液体;
混合形成离子液体; 也可以转化成其他离子液体,下图是
也可以转化成其他离子液体,下图是 与
与 离子交换反应合成离子液体
离子交换反应合成离子液体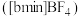 的流程:
的流程:

(1)请画出基态 原子的价电子排布图
原子的价电子排布图___________ ;同周期元素中基态原子未成对电子数与硼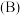 原子相同的有
原子相同的有___________ (填元素符号)。
(2)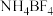 中N原子的杂化方式为
中N原子的杂化方式为___________ ,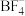 的空间构型为
的空间构型为___________ , 中几种元素电负性由大到小的顺序为
中几种元素电负性由大到小的顺序为___________ 。
(3)已知分子中的大 键可以用
键可以用 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表大
键的原子数,n代表大 键中的电子数,则
键中的电子数,则 中大
中大 键可以表示为
键可以表示为___________ 。
(4) 熔点为
熔点为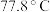 ,则
,则 的晶体类型为
的晶体类型为___________ , 和
和 混合形成离子液体的过程中会存在以下转化:
混合形成离子液体的过程中会存在以下转化: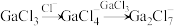 ,请画出
,请画出 的结构式
的结构式___________ 。
(5)某种 的晶胞结构如图所示,
的晶胞结构如图所示, 以六方最密方式堆积,
以六方最密方式堆积, 在其八面体空隙中(注:未全部标出,如:
在其八面体空隙中(注:未全部标出,如: 在
在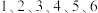 构成的八面体体心)。
构成的八面体体心)。
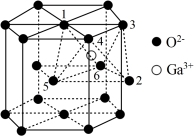
①该晶胞中 的配位数为
的配位数为___________ 。
②该晶胞有___________  (保留一位小数)八面体空隙未填充阳离子。
(保留一位小数)八面体空隙未填充阳离子。
③已知氧离子半径为 ,晶胞的高为
,晶胞的高为 代表阿伏加德罗常数的值,该晶体的密度为
代表阿伏加德罗常数的值,该晶体的密度为___________  (用含
(用含 和
和 的代数式表示)。
的代数式表示)。
 丁基
丁基 甲基咪唑离子液
甲基咪唑离子液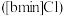 可以与
可以与 混合形成离子液体;
混合形成离子液体; 也可以转化成其他离子液体,下图是
也可以转化成其他离子液体,下图是 与
与 离子交换反应合成离子液体
离子交换反应合成离子液体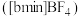 的流程:
的流程:
(1)请画出基态
 原子的价电子排布图
原子的价电子排布图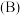 原子相同的有
原子相同的有(2)
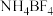 中N原子的杂化方式为
中N原子的杂化方式为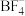 的空间构型为
的空间构型为 中几种元素电负性由大到小的顺序为
中几种元素电负性由大到小的顺序为(3)已知分子中的大
 键可以用
键可以用 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表大
键的原子数,n代表大 键中的电子数,则
键中的电子数,则 中大
中大 键可以表示为
键可以表示为(4)
 熔点为
熔点为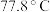 ,则
,则 的晶体类型为
的晶体类型为 和
和 混合形成离子液体的过程中会存在以下转化:
混合形成离子液体的过程中会存在以下转化: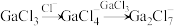 ,请画出
,请画出 的结构式
的结构式(5)某种
 的晶胞结构如图所示,
的晶胞结构如图所示, 以六方最密方式堆积,
以六方最密方式堆积, 在其八面体空隙中(注:未全部标出,如:
在其八面体空隙中(注:未全部标出,如: 在
在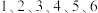 构成的八面体体心)。
构成的八面体体心)。
①该晶胞中
 的配位数为
的配位数为②该晶胞有
 (保留一位小数)八面体空隙未填充阳离子。
(保留一位小数)八面体空隙未填充阳离子。③已知氧离子半径为
 ,晶胞的高为
,晶胞的高为 代表阿伏加德罗常数的值,该晶体的密度为
代表阿伏加德罗常数的值,该晶体的密度为 (用含
(用含 和
和 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2021-04-19更新
|
298次组卷
|
2卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
解答题-有机推断题
|
适中(0.65)
19. 合成化学在新药发现的多个阶段至关重要。下图为合成药物中间体F和高分子化合物M的合成路线。

已知:
(1)B的化学名称是___________ 。
(2)C中的官能团名称是___________ 。
(3)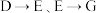 的反应类型分别是
的反应类型分别是___________ 、___________ 。
(4)A和B在路易斯酸作用下,除生成C外,还可生成与C互为同分异构体的有机物,其结构简式为___________ 。
(5)H生成M的化学方程式为___________ 。
(6)芳香族化合物X是F的同分异构体,苯环上的一氯代物有2种, 发生水解反应消耗
发生水解反应消耗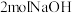 ,符合要求的同分异构体有
,符合要求的同分异构体有___________ 种。
(7)根据本题信息和已学知识,写出以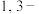 丁二烯和
丁二烯和 溴丙烷为原料制备苯甲酸,且不超过四步的合成路线:
溴丙烷为原料制备苯甲酸,且不超过四步的合成路线:___________ (乙醇及其它无机试剂任选)。

已知:

(1)B的化学名称是
(2)C中的官能团名称是
(3)
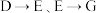 的反应类型分别是
的反应类型分别是(4)A和B在路易斯酸作用下,除生成C外,还可生成与C互为同分异构体的有机物,其结构简式为
(5)H生成M的化学方程式为
(6)芳香族化合物X是F的同分异构体,苯环上的一氯代物有2种,
 发生水解反应消耗
发生水解反应消耗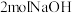 ,符合要求的同分异构体有
,符合要求的同分异构体有(7)根据本题信息和已学知识,写出以
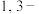 丁二烯和
丁二烯和 溴丙烷为原料制备苯甲酸,且不超过四步的合成路线:
溴丙烷为原料制备苯甲酸,且不超过四步的合成路线:
您最近一年使用:0次
2021-04-19更新
|
203次组卷
|
2卷引用:重庆市普通高中学业水平选择性考试2021届高三第二次联合诊断检测化学试题
试卷分析
整体难度:适中
考查范围:化学与STSE、认识化学科学、物质结构与性质、常见无机物及其应用、有机化学基础、化学实验基础、化学反应原理
试卷题型(共 19题)
题型
数量
单选题
14
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 化学科学对人类文明发展的意义 高分子材料 金属材料的性质及利用 | |
| 2 | 0.65 | 化学用语综合判断 化学键与物质类别关系的判断 | |
| 3 | 0.94 | 氧化还原反应的几组概念 氯气与碱溶液反应 二氧化硫与其他强氧化剂的反应 Fe2+的还原性 | |
| 4 | 0.65 | 同分异构体的数目的确定 含碳碳双键物质的性质的推断 有机分子中原子共面的判断 | |
| 5 | 0.65 | 酸、碱、盐、氧化物的概念及其相互联系 离子方程式的正误判断 有机物的检验 化学实验方案的设计与评价 | |
| 6 | 0.65 | 催化剂对化学反应速率的影响 共价键概念及判断 | |
| 7 | 0.65 | 催化剂对化学反应速率的影响 沉淀转化 淀粉、纤维素的水解 | |
| 8 | 0.4 | 元素周期律、元素周期表的推断 根据原子结构进行元素种类推断 | |
| 9 | 0.65 | 胶体的定义及分类 物质的量有关计算 结合物质结构基础知识与NA相关推算 依据物质的量浓度公式的基础计算 | |
| 10 | 0.85 | 化学反应热的计算 盖斯定律的应用 | |
| 11 | 0.65 | 原电池电子流向判断及应用 原电池电极反应式书写 燃料电池 | |
| 12 | 0.65 | 硝酸的强氧化性 硫酸根离子的检验 铁盐的检验 萃取和分液 | |
| 13 | 0.65 | 电离平衡常数及影响因素 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 | |
| 14 | 0.65 | 氧化还原反应方程式的配平 物质分离、提纯综合应用 电子转移计算 | |
| 二、解答题 | |||
| 15 | 0.4 | 氧化还原反应方程式的配平 盐类双水解反应 溶度积常数相关计算 | 工业流程题 |
| 16 | 0.4 | 化学平衡的有关计算 化学平衡状态的判断方法 原电池原理理解 | 原理综合题 |
| 17 | 0.65 | Fe2+的还原性 常用仪器及使用 物质含量的测定 物质制备的探究 | 实验探究题 |
| 18 | 0.4 | 元素性质与电负性的关系 利用杂化轨道理论判断分子的空间构型 简单配合物的成键 离子晶体 | 结构与性质 |
| 19 | 0.65 | 有机合成综合考查 有机推断综合考查 | 有机推断题 |

 和
和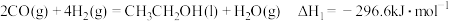

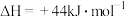
 和
和 反应生成
反应生成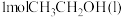 和
和 的
的 为
为