名校
1 . 宏观辨识与微观探析是化学学科核心素养之一、下列物质性质实验对应的离子方程式书写正确的是
A.铁片插入稀硫酸中: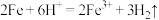 |
B. 放入水中: 放入水中: |
C.用 溶液腐蚀铜电路板: 溶液腐蚀铜电路板: |
D.向氢氧化钠溶液中通入过量 : : |
您最近一年使用:0次
2022-01-24更新
|
205次组卷
|
3卷引用:湖南省长沙市明德中学2023-2024学年高一上学期期末考试化学试题
解题方法
2 . 根据实验目的,设计相关实验,下列实验操作、现象解释及结论都正确的是
| 序号 | 操作 | 现象 | 解释或结论 |
A | 在含0.1mol的AgNO3溶液中依次加入NaCl溶液和KI溶液 | 溶液中先有白色沉淀生成,后来又变成黄色 | Ksp(AgCl)>Ksp(AgI) |
B | 在Ca(ClO)2溶液中通入SO2气体 | 有沉淀生成 | 酸性:H2SO3>HClO |
C | 向酸性KMnO4溶液中滴加乙醇 | 溶液紫色褪去 | 乙醇具有还原性 |
D | 向溴水中加入苯,充分振荡,静置 | 水层几乎无色 | 苯与溴发生了反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-09-21更新
|
337次组卷
|
2卷引用:湖南省邵阳市武冈市2023-2024学年高三上学期期中考试化学试题
3 . 某无色溶液中只含有 、
、 、
、 、
、 、
、 、
、 、
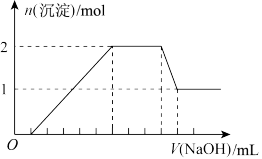
、 等离子中的几种,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示。下列说法错误的是
等离子中的几种,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示。下列说法错误的是
 、
、 、
、 、
、 、
、 、
、 、
、 等离子中的几种,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示。下列说法错误的是
等离子中的几种,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示。下列说法错误的是
A.溶液中一定存在 、 、 | B.溶液中一定不存在 、 、 |
C.溶液中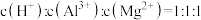 | D.溶液中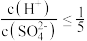 |
您最近一年使用:0次
解题方法
4 . 某铝土矿中主要含有Al2O3、Al(OH)3还含有Fe2O3等杂质。利用拜耳法生产氧化铝的流程如图所示:

请回答下列问题:
(1)粉碎后的铝土矿碱浸时应在较高温度下进行,其目的是____________________ 。滤渣1的主要成分为________________ 。
(2)Al2O3与NaOH溶液反应的离子方程式为____________________________________ 。
(3)加Al(OH)3晶核的目的是促进Al(OH)3的析出。上述“稀释、结晶”工艺,也可用通入足量的_________ 气体的方法来代替。(已知:通入该气体后,其产物之一可用来做发酵粉)。
(4)焙烧过程中发生的化学方程式为_________________________________ 。
(5)浓缩所得的NaOH溶液由于吸收了空气中的CO2而含有杂质,该杂质可通过苛化(即与少量熟石灰反应)反应除去,写出苛化反应的化学方程式:_________________________________________________ 。
(6)该生产流程能实现____________________ (填化学式)的循环利用。

请回答下列问题:
(1)粉碎后的铝土矿碱浸时应在较高温度下进行,其目的是
(2)Al2O3与NaOH溶液反应的离子方程式为
(3)加Al(OH)3晶核的目的是促进Al(OH)3的析出。上述“稀释、结晶”工艺,也可用通入足量的
(4)焙烧过程中发生的化学方程式为
(5)浓缩所得的NaOH溶液由于吸收了空气中的CO2而含有杂质,该杂质可通过苛化(即与少量熟石灰反应)反应除去,写出苛化反应的化学方程式:
(6)该生产流程能实现
您最近一年使用:0次
2020-01-17更新
|
301次组卷
|
2卷引用:湖南省娄底市娄星区2020-2021学年高二下学期期中考试化学试题
5 . 如图所示实验装置用于验证某些物质的性质。在A试管中装入足量的固体NaHCO3。试回答下列问题:
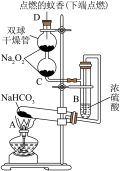
(1)在A试管内发生反应的化学方程式是_____________ ;
(2)B装置的作用是_____________________ ;
(3)在双球干燥管内发生反应的化学方程式为_________ ;
(4)实验时在C装置中观察到的现象是_______________ ;
(5)若将双球干燥管内的Na2O2换成Na2O,则实验时观察到的现象是___________________________________ 。

(1)在A试管内发生反应的化学方程式是
(2)B装置的作用是
(3)在双球干燥管内发生反应的化学方程式为
(4)实验时在C装置中观察到的现象是
(5)若将双球干燥管内的Na2O2换成Na2O,则实验时观察到的现象是
您最近一年使用:0次
2019-12-18更新
|
357次组卷
|
17卷引用:湖南省醴陵市第一中学2017-2018学年高一上学期第二次月考(12月)化学试题
湖南省醴陵市第一中学2017-2018学年高一上学期第二次月考(12月)化学试题湖南省邵东县第一中学2019-2020学年高一上学期第三次月考化学试题2015-2016学年贵州省遵义航天中学高一上期末化学试卷2015-2016学年内蒙古集宁一中高一上第二次月考化学试卷2016-2017学年广西桂林中学高一上学期段考化学卷2018版化学(苏教版)高考总复习课时跟踪训练:钠、镁及其重要化合物内蒙古通辽实验中学2017-2018学年高一上学期期末考试化学试题云南省中央民大附中芒市国际学校2017-2018学年高一上学期末考试化学试卷广西桂梧高中2017-2018学年高一下学期第一次月考化学试题(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第1讲 钠及其氧化物【押题专练】(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第1讲 钠及化合物 (题型专练)内蒙古自治区乌兰察布市北京八中乌兰察布分校2019-2020学年高一上学期期末考试化学试题山东省泰安市宁阳一中2020-2021学年高一上学期第一次阶段性考试化学试题(已下线)【镇江新东方】高一上期中考试河北省唐山市十县一中联盟2022-2023学年高一上学期期中考试化学试题河北省唐山市2022—2023学年高一上学期期中考试化学试题北京市通州区2022-2023学年高一上学期期中考试化学试题
名校
解题方法
6 . 某同学为了测定实验中一瓶因保存不善而部分变质的氢氧化钠和碳酸钠的质量分数,设计了如图所示的装置(图中的铁架台已略去),实验步骤如下:①按图连接好装置;②称取氧氧化钠样品2g,放入A中试管内,向B中集气瓶内倒入饱和二氧化碳水溶液至瓶颈处;③向分液漏斗中倒入稀硫酸,打开活塞,让稀硫酸滴入试管中(过量),关闭活塞。反应结束后,量筒中收集到饱和二氧化碳水溶液220 mL。请回答下列问题:

(1)判断氢氧化钠变质的实验现象是__ ,氢氧化钠变质的原因是____ 。因此,实验室中氢氧化钠必须__ 保存。
(2)在实验步骤①和②之间,还缺少一个实验步骤,该实验步骤是__ 。
(3) B中集气瓶装的饱和二氧化碳水溶液不能用水代替,其理由是___ 。
(4)判断步骤③中滴入的稀硫酸已过量的标志是___ 。
(5)氧氧化钠样品碳酸钠的质量分数为__ (CO2的密度约为2.0g/L,二氧化碳的体积等于排出的饱和二氧化碳水溶液的体积)。
(6)用上述装置不能测定已部分变质的氢氧化钠样品中氢氧化钠的质量分数,理由是___ 。

(1)判断氢氧化钠变质的实验现象是
(2)在实验步骤①和②之间,还缺少一个实验步骤,该实验步骤是
(3) B中集气瓶装的饱和二氧化碳水溶液不能用水代替,其理由是
(4)判断步骤③中滴入的稀硫酸已过量的标志是
(5)氧氧化钠样品碳酸钠的质量分数为
(6)用上述装置不能测定已部分变质的氢氧化钠样品中氢氧化钠的质量分数,理由是
您最近一年使用:0次
名校
解题方法
7 . 碳酸镧咀嚼片是一种不含钙和铝的磷酸盐结合剂,常用于治疗慢性肾衰患者的高磷血症。实验室模拟用LaCl3为原料来制备碳酸镧。为避免生成碱式碳酸镧[La(OH)CO3],整个反应在较低的pH条件下进行。
(1)某化学兴趣小组利用下列装置在实验室中用碳酸氢铵制备碳酸镧。

①在实验室用装置甲还可以制取下列中的气体:________ (填字母代号)。
A.O2 B.Cl2 C.H2 D.NO E.SO2 F.C2H2 G.C2H4
②仪器X的作用是__________ 。
③实验中应先开K2再开K1,原因是_________ 。
④为保证碳酸镧的纯度,实验过程中需要注意的问题有_______ (答一条即可)。
(2)碳酸钠或碳酸氢钠与氯化镧反应均可生成碳酸镧。
①为了高磷血症患者的安全,通常选用碳酸氢钠溶液,优点是________ (答一条即可)。
②NaHCO3与LaCl3反应过程中会发生两个平行反应,其离子方程式为A.____ 和B.H++ =CO2↑+H2O。
=CO2↑+H2O。
③T℃时,碳酸镧的溶解度为1.0×10-7mol/L, 的电离平衡常数为6.0×10-11。请计算反应A的平衡常数K=
的电离平衡常数为6.0×10-11。请计算反应A的平衡常数K=______ 。
(1)某化学兴趣小组利用下列装置在实验室中用碳酸氢铵制备碳酸镧。

①在实验室用装置甲还可以制取下列中的气体:
A.O2 B.Cl2 C.H2 D.NO E.SO2 F.C2H2 G.C2H4
②仪器X的作用是
③实验中应先开K2再开K1,原因是
④为保证碳酸镧的纯度,实验过程中需要注意的问题有
(2)碳酸钠或碳酸氢钠与氯化镧反应均可生成碳酸镧。
①为了高磷血症患者的安全,通常选用碳酸氢钠溶液,优点是
②NaHCO3与LaCl3反应过程中会发生两个平行反应,其离子方程式为A.
 =CO2↑+H2O。
=CO2↑+H2O。③T℃时,碳酸镧的溶解度为1.0×10-7mol/L,
 的电离平衡常数为6.0×10-11。请计算反应A的平衡常数K=
的电离平衡常数为6.0×10-11。请计算反应A的平衡常数K=
您最近一年使用:0次
解题方法
8 . 我国食盐可分为原盐、精盐、特种食盐以及营养盐等,其中特种食盐又分为低钠盐、加碘盐、加硒盐、加锌盐、加铁盐等。低钠盐是以加碘食盐为基础,添加一定量 ,适用于中老年人和患有高血压病患者长期食用。加铁盐中添加一定量亚铁盐,如
,适用于中老年人和患有高血压病患者长期食用。加铁盐中添加一定量亚铁盐,如 ,适用于铁缺乏人群。
,适用于铁缺乏人群。
I.某一实验小组对低钠盐进行研究。
(1) 检验:用洁净的铂丝蘸取低钠盐固体,灼烧,直接观察火焰呈黄色,甲同学认为含
检验:用洁净的铂丝蘸取低钠盐固体,灼烧,直接观察火焰呈黄色,甲同学认为含 ,无
,无 。但乙同学进行实验,透过蓝色钴玻璃观察到火焰呈
。但乙同学进行实验,透过蓝色钴玻璃观察到火焰呈_______ 色,否定了甲同学的观点。
(2) 的含量测定:取
的含量测定:取 的低钠盐溶于水配成溶液,加足量稀硝酸和硝酸银溶液,充分反应后,得到干燥的白色沉淀质量为
的低钠盐溶于水配成溶液,加足量稀硝酸和硝酸银溶液,充分反应后,得到干燥的白色沉淀质量为 ,便可以计算低钠盐中
,便可以计算低钠盐中 的含量。你认为该方案是否可行?
的含量。你认为该方案是否可行?_______ (若可行,请写出含量表达式:若不可行,请写出不可行理由)。
Ⅱ.另一实验小组对加铁盐进行研究。
(3)配制溶液:准确称量 该加铁盐,配制
该加铁盐,配制 加铁盐溶液。需要使用的玻璃仪器:烧杯、量筒、玻璃棒、
加铁盐溶液。需要使用的玻璃仪器:烧杯、量筒、玻璃棒、 容量瓶、
容量瓶、_______ 。
(4)定性检验:检验该加铁盐中是否添加有 ,并检验其是否变质。实验小组设计了以下实验,请完成表格。
,并检验其是否变质。实验小组设计了以下实验,请完成表格。
(5)定量测定:加铁盐国标是含铁量为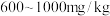 。取
。取 所配溶液,加入足量
所配溶液,加入足量 溶液,充分反应后过滤,加热固体至质量不再变化,称得剩余红棕色固体为
溶液,充分反应后过滤,加热固体至质量不再变化,称得剩余红棕色固体为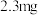 ,计算该盐含铁量为
,计算该盐含铁量为_______ 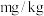 。
。
 ,适用于中老年人和患有高血压病患者长期食用。加铁盐中添加一定量亚铁盐,如
,适用于中老年人和患有高血压病患者长期食用。加铁盐中添加一定量亚铁盐,如 ,适用于铁缺乏人群。
,适用于铁缺乏人群。I.某一实验小组对低钠盐进行研究。
(1)
 检验:用洁净的铂丝蘸取低钠盐固体,灼烧,直接观察火焰呈黄色,甲同学认为含
检验:用洁净的铂丝蘸取低钠盐固体,灼烧,直接观察火焰呈黄色,甲同学认为含 ,无
,无 。但乙同学进行实验,透过蓝色钴玻璃观察到火焰呈
。但乙同学进行实验,透过蓝色钴玻璃观察到火焰呈(2)
 的含量测定:取
的含量测定:取 的低钠盐溶于水配成溶液,加足量稀硝酸和硝酸银溶液,充分反应后,得到干燥的白色沉淀质量为
的低钠盐溶于水配成溶液,加足量稀硝酸和硝酸银溶液,充分反应后,得到干燥的白色沉淀质量为 ,便可以计算低钠盐中
,便可以计算低钠盐中 的含量。你认为该方案是否可行?
的含量。你认为该方案是否可行?Ⅱ.另一实验小组对加铁盐进行研究。
(3)配制溶液:准确称量
 该加铁盐,配制
该加铁盐,配制 加铁盐溶液。需要使用的玻璃仪器:烧杯、量筒、玻璃棒、
加铁盐溶液。需要使用的玻璃仪器:烧杯、量筒、玻璃棒、 容量瓶、
容量瓶、(4)定性检验:检验该加铁盐中是否添加有
 ,并检验其是否变质。实验小组设计了以下实验,请完成表格。
,并检验其是否变质。实验小组设计了以下实验,请完成表格。| 步骤 | 操作 | 现象 | 结论 |
| 步骤1 | 取所配溶液,加入① | 无明显现象该 | 加铁盐中添加 且未变质 且未变质 |
| 步骤2 | 向步骤1所得溶液中加入② | ③ |
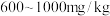 。取
。取 所配溶液,加入足量
所配溶液,加入足量 溶液,充分反应后过滤,加热固体至质量不再变化,称得剩余红棕色固体为
溶液,充分反应后过滤,加热固体至质量不再变化,称得剩余红棕色固体为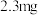 ,计算该盐含铁量为
,计算该盐含铁量为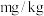 。
。
您最近一年使用:0次
名校
解题方法
9 . 2015年8月12日,天津滨海新区爆炸事故确认有氰化钠(NaCN)、亚硝酸钠等,氰化钠毒性很强,遇水、酸会产生有毒易燃氰化氢(HCN)气体。氰化氢的沸点只有26 ℃,因此相当容易挥发进入空气,这就大大增加了中毒的风险。同时氰化钠遇到亚硝酸钠会发生爆炸。回答下列问题:
(1)写出氰化钠遇水产生氰化氢气体的离子方程式_________________________
(2)爆炸现场约700吨的氰化钠大约需要900吨的双氧水来处理。氰化钠与双氧水相遇后,会释放出氨气同时析出白色晶体,使得氰化钠的毒性大大降低,写出氰化钠与双氧水反应的化学方程式________________________________ 。
(3)爆炸残留在废水中的CN-可以用Cr2O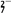 处理,拟定下列流程进行废水处理,
处理,拟定下列流程进行废水处理,
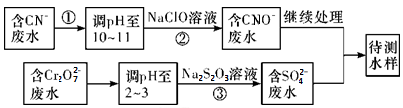
①上述处理废水流程中主要使用的方法是____________
a.混凝法 b.中和法 c.沉淀法 d.氧化还原法
②②中反应后无气体放出,该反应的离子方程式为_________________ ;
③步骤③中,每处理0.4 mol Cr2O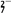 时转移电子2.4 mol,该反应的离子方程式
时转移电子2.4 mol,该反应的离子方程式_________ ;
(1)写出氰化钠遇水产生氰化氢气体的离子方程式
(2)爆炸现场约700吨的氰化钠大约需要900吨的双氧水来处理。氰化钠与双氧水相遇后,会释放出氨气同时析出白色晶体,使得氰化钠的毒性大大降低,写出氰化钠与双氧水反应的化学方程式
(3)爆炸残留在废水中的CN-可以用Cr2O
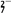 处理,拟定下列流程进行废水处理,
处理,拟定下列流程进行废水处理,
①上述处理废水流程中主要使用的方法是
a.混凝法 b.中和法 c.沉淀法 d.氧化还原法
②②中反应后无气体放出,该反应的离子方程式为
③步骤③中,每处理0.4 mol Cr2O
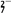 时转移电子2.4 mol,该反应的离子方程式
时转移电子2.4 mol,该反应的离子方程式
您最近一年使用:0次
2017-12-13更新
|
624次组卷
|
2卷引用:湖南省浏阳一中、醴陵一中、南方中学2017-2018学年高二12月联考化学试题
名校
解题方法
10 . 电子工业上使用的印刷电路板,是在敷有铜膜的塑料板上以涂层保护所要的线路,然后用三氯化铁浓溶液作用掉(腐蚀)未受保护的铜膜后形成的。某工程师为了从使用过的腐蚀废液(含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费)中回收铜,并将铁的化合物全部转化为FeCl3溶液作为腐蚀液原料循环使用,准备采用下列步骤:
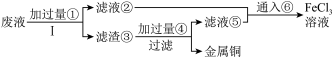
(1)写出FeCl3溶液与铜箔发生反应的离子方程式:____________ 。
(2)检验废腐蚀液中是否含有Fe3+所需试剂名称:________ ,实验现象:______________ 。
(3)向②中加入NaOH溶液并长时间暴露在空气中,此过程的现象:___________ ,此转化的化学方程式为:______________ 。
(4)写出③中所含物质:________ ,⑥发生反应的离子方程式:_______ 。

(1)写出FeCl3溶液与铜箔发生反应的离子方程式:
(2)检验废腐蚀液中是否含有Fe3+所需试剂名称:
(3)向②中加入NaOH溶液并长时间暴露在空气中,此过程的现象:
(4)写出③中所含物质:
您最近一年使用:0次
2020-09-04更新
|
242次组卷
|
2卷引用:湖南省长沙市雨花区2019-2020学年高一上学期期末考试化学试题



