9-10高一下·湖南·期末
解题方法
1 . 已知A、B、C、D、E是短周期中的5种非金属元素,它们的原子序数依次增大。A元素原子形成的阳离子核外电子数为零,B原子的最外层电子数是内层电子数的2倍。C、D在元素周期表中处于左右相邻的位置,它们的单质是空气的主要成分, E元素与D元素同主族。
(1) 请写出元素符号:A_______ , E______ 。
(2) C的气态氢化物的水溶液呈_______ 性(填“酸”、“碱”或“中”),写出C的气态氢化物的电子式_____________ ,以及与HCl形成的盐的化学式______________ 。
⑶A、B两元素形成的相对分子质量最小的有机物的分子式____ ,空间构型是___ 。
(1) 请写出元素符号:A
(2) C的气态氢化物的水溶液呈
⑶A、B两元素形成的相对分子质量最小的有机物的分子式
您最近一年使用:0次
名校
2 . 由铝硅两种物质组成的试样11 g,均匀地分成等质量的两份,一份与足量的盐酸接触可产生气体a L,一份与足量的NaOH溶液接触产生同样的气体b L,则此试样中铝与硅的质量比为
| A.4a /3(b-a) | B.9a/7(b-a) | C.a/(b-a) | D.无法计算 |
您最近一年使用:0次
2016-12-09更新
|
161次组卷
|
3卷引用:湖南省衡阳市第八中学2017届高三上学期第四次月考化学(实验班)试题
解题方法
3 . 铝是重要的金属材料,铝土矿(主要成分A12O3另含少量的SiO2、Fe2O3等)是工业上制铝的原料。实验室模拟工业上以铝土矿为原料制取铵明矾晶体 [NH4Al(SO4)2·12H2O]的工艺流程如下图所示:

请回答下列问题:
(1)为提高铝土矿与盐酸的反应速率,可采取的措施有______________________________ (写两条)。
(2)固体a的主要成分为__________________ (写化学式)。
(3)II中烧碱过量的原因是________________________________________ 。
(4)写出III中主要反应的离子方程式__________________________________________ 。
(5)制取铵明矾溶液的化学方程式为_________________________________________ ;由铵明矾溶液制取铵明矾晶体的实验操作依次为(填操作名称)______________________ 、____________ 、过滤、洗涤。
(6)设计实验证明铵明矾溶液中含有NH4+_______________________________________ 。

请回答下列问题:
(1)为提高铝土矿与盐酸的反应速率,可采取的措施有
(2)固体a的主要成分为
(3)II中烧碱过量的原因是
(4)写出III中主要反应的离子方程式
(5)制取铵明矾溶液的化学方程式为
(6)设计实验证明铵明矾溶液中含有NH4+
您最近一年使用:0次
解题方法
4 . 下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。

(1)写出单质B与强碱溶液反应的离子方程式___________________________ ,写出由沉淀J生成H溶液的离子方程式_______________________________ 。
(2)溶液E中加入氨水时,先生成白色沉淀L,白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式______________________________ 。
(3) K是一种集消毒与净水为一体的新型净水剂,试写出G→K的化学方程式:_______________
(4)溶液I中所含金属离子是__________________ 。

(1)写出单质B与强碱溶液反应的离子方程式
(2)溶液E中加入氨水时,先生成白色沉淀L,白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式
(3) K是一种集消毒与净水为一体的新型净水剂,试写出G→K的化学方程式:
(4)溶液I中所含金属离子是
您最近一年使用:0次
11-12高三上·湖南常德·阶段练习
解题方法
5 . 物质A~G均由短周期元素组成,A、B为非金属气体单质,B原子最外层电子数比次外层电子数的2倍还多1.甲、乙均为金属单质,且甲的原子半径在第三周期最大。各物质间的转化关系如下(部分生成物未给出,且未注明反应条件):
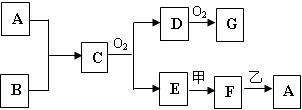
请回答:
(1)物质D的化学式_______ ;
(2)物质A的电子式是_______ ;
(3)实验室制取C的化学方程式_______ ;
(4)物质F和乙反应生成A的离子方程式_______ 。

请回答:
(1)物质D的化学式
(2)物质A的电子式是
(3)实验室制取C的化学方程式
(4)物质F和乙反应生成A的离子方程式
您最近一年使用:0次
名校
解题方法
6 . Ⅰ.历史会被尘封,但不会被掩盖,更不会被忘记。1939年4月,日寇在侵略晋城时使用了生化武器氯气弹,犯下了滔天之罪。某化学兴趣小组同学利用以下装置制备和收集少量干燥、纯净的氯气,选用如图所示仪器及药品:

(1)上述实验中,用来盛放浓盐酸的仪器的名称是___________ 。
(2)选择上述仪器并按顺序连接(填各接口处的字母):___________ 。
(3)制得的 通过盛有饱和食盐水的装置,目的是
通过盛有饱和食盐水的装置,目的是___________ 。
(4)氢氧化钠溶液的作用是___________ (用化学方程式表示)。
(5)若需要制取 ,需要
,需要 的质量为
的质量为___________ g。
Ⅱ.亚氯酸钠 是一种高效的漂白剂和消毒剂,它在酸性条件下生成
是一种高效的漂白剂和消毒剂,它在酸性条件下生成 并放出
并放出 ,
, 有类似
有类似 的性质。某兴趣小组探究亚氯酸钠的制备与性质。
的性质。某兴趣小组探究亚氯酸钠的制备与性质。
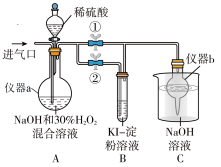
i.制备亚氯酸钠
关闭止水夹②,打开止水夹①,从进气口通入足量 ,充分反应。
,充分反应。
(6)装置A中生成 的离子方程式为
的离子方程式为___________ 。
ii.探究亚氯酸钠的性质
停止通 气体,再通入空气一段时间后,关闭止水夹①,打开止水夹②,向A中滴入稀硫酸。
气体,再通入空气一段时间后,关闭止水夹①,打开止水夹②,向A中滴入稀硫酸。
(7)开始时A中反应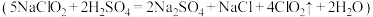 缓慢,稍后产生气体的速率急剧加快,请解释可能的原因
缓慢,稍后产生气体的速率急剧加快,请解释可能的原因___________ 。
(8)实验完成后,为防止装置中滞留的有毒气体污染空气,可以进行的操作是:再次打开止水夹①,___________ 。

(1)上述实验中,用来盛放浓盐酸的仪器的名称是
(2)选择上述仪器并按顺序连接(填各接口处的字母):
(3)制得的
 通过盛有饱和食盐水的装置,目的是
通过盛有饱和食盐水的装置,目的是(4)氢氧化钠溶液的作用是
(5)若需要制取
 ,需要
,需要 的质量为
的质量为Ⅱ.亚氯酸钠
 是一种高效的漂白剂和消毒剂,它在酸性条件下生成
是一种高效的漂白剂和消毒剂,它在酸性条件下生成 并放出
并放出 ,
, 有类似
有类似 的性质。某兴趣小组探究亚氯酸钠的制备与性质。
的性质。某兴趣小组探究亚氯酸钠的制备与性质。
i.制备亚氯酸钠
关闭止水夹②,打开止水夹①,从进气口通入足量
 ,充分反应。
,充分反应。(6)装置A中生成
 的离子方程式为
的离子方程式为ii.探究亚氯酸钠的性质
停止通
 气体,再通入空气一段时间后,关闭止水夹①,打开止水夹②,向A中滴入稀硫酸。
气体,再通入空气一段时间后,关闭止水夹①,打开止水夹②,向A中滴入稀硫酸。(7)开始时A中反应
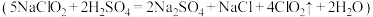 缓慢,稍后产生气体的速率急剧加快,请解释可能的原因
缓慢,稍后产生气体的速率急剧加快,请解释可能的原因(8)实验完成后,为防止装置中滞留的有毒气体污染空气,可以进行的操作是:再次打开止水夹①,
您最近一年使用:0次



