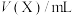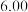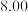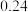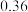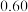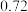1 . 已知某炔烃与卤化氢按物质的量为1:2发生加成反应后,生成的有机物至少需6mol的卤素单质才能把其分子中的氢原子全部取代,则该炔烃可能是
| A.丙炔 | B.1-丁炔 | C.3-己炔 | D.2-庚炔 |
您最近一年使用:0次
2024-03-29更新
|
266次组卷
|
3卷引用:吉林省延吉市延边第二中学2023-2024学年高二下学期5月期中化学试题
名校
解题方法
2 . 下列离子方程式中,错误的是
A. 与 与 反应: 反应: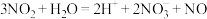 |
B. 溶液与过量 溶液与过量 溶液反应: 溶液反应: |
C.将少量铜屑放入浓硝酸中: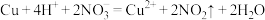 |
D.硫酸亚铁溶液中加入稀硝酸: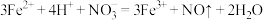 |
您最近一年使用:0次
2024-03-22更新
|
336次组卷
|
3卷引用:吉林省延吉市延边第二中学2023-2024学年高一下学期5月期中化学试题
名校
解题方法
3 . 硫酸亚铁在高温条件下分解可生成 、
、 、
、 ,反应方程式为:
,反应方程式为: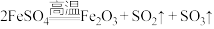 ,为探究硫酸亚铁的分解产物,将硫酸亚铁装入如图所示的装置a中,打开
,为探究硫酸亚铁的分解产物,将硫酸亚铁装入如图所示的装置a中,打开 和
和 ,缓缓通入
,缓缓通入 ,加热。实验后反应管中残留固体为红色粉末。下列说法中正确的是
,加热。实验后反应管中残留固体为红色粉末。下列说法中正确的是
 、
、 、
、 ,反应方程式为:
,反应方程式为: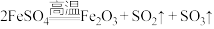 ,为探究硫酸亚铁的分解产物,将硫酸亚铁装入如图所示的装置a中,打开
,为探究硫酸亚铁的分解产物,将硫酸亚铁装入如图所示的装置a中,打开 和
和 ,缓缓通入
,缓缓通入 ,加热。实验后反应管中残留固体为红色粉末。下列说法中正确的是
,加热。实验后反应管中残留固体为红色粉末。下列说法中正确的是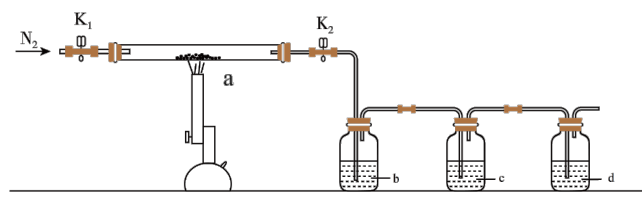
A.反应管中残留固体红色粉末是 |
B.装置b中的试剂为 溶液,反应后有白色沉淀生成 溶液,反应后有白色沉淀生成 |
C.装置c中的试剂为酸性 溶液,作用是除去混合气体中的 溶液,作用是除去混合气体中的 |
D.分解的气体产物中有 、 、 ,应该先检验 ,应该先检验 |
您最近一年使用:0次
2024-03-11更新
|
297次组卷
|
2卷引用:吉林省延吉市延边第二中学2023-2024学年高一下学期5月期中化学试题
4 . 某新型有机物M的结构如图所示。有关M的说法错误的是
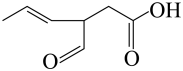
A.M的分子式为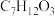 | B.M中含有三种官能团 |
| C.M分子中含有手性碳原子 | D.M中的碳原子杂化方式有两种 |
您最近一年使用:0次
2024-03-01更新
|
1141次组卷
|
4卷引用: 吉林省梅河口市第五中学2023-2024学年高二下学期第一次月考化学试题
名校
解题方法
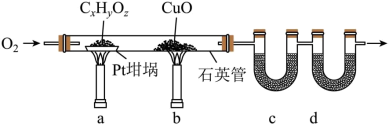
5 . 元素分析是有机化合物的表征手段之一,按下图实验装置(部分装置略)对有机化合物进行C、H元素分析。
(1)将装有样品的Pt坩埚和CuO放入石英管中,先通入一定的O2,而后将已称重的U型管c、d与石英管连接,检查装置气密性。依次点燃煤气灯___________ (排a、b顺序),进行实验。
(2)O2的作用有为实验提供氧化剂、提供气流保证反应产物完全进入到U型管中。CuO的作用是___________ (举1例,用化学方程式表示)。
(3)c和d中的试剂分别是___________ 、___________ (填标号)。c和d中的试剂不可调换,理由是___________ 。
A.CaCl2 B.NaCl C.碱石灰(CaO+NaOH) D.Na2SO3
(4)Pt坩埚中样品CxHyOz反应完全后,应进行操作:___________ 。取下c和d管称重。
(5)若样品CxHyOz为0.0236g,实验结束后,c管增重0.0108g,d管增重0.0352g。质谱测得该有机物的相对分子量为118,其分子式为___________ 。
(1)将装有样品的Pt坩埚和CuO放入石英管中,先通入一定的O2,而后将已称重的U型管c、d与石英管连接,检查装置气密性。依次点燃煤气灯
(2)O2的作用有为实验提供氧化剂、提供气流保证反应产物完全进入到U型管中。CuO的作用是
(3)c和d中的试剂分别是
A.CaCl2 B.NaCl C.碱石灰(CaO+NaOH) D.Na2SO3
(4)Pt坩埚中样品CxHyOz反应完全后,应进行操作:
(5)若样品CxHyOz为0.0236g,实验结束后,c管增重0.0108g,d管增重0.0352g。质谱测得该有机物的相对分子量为118,其分子式为
您最近一年使用:0次
2024-02-26更新
|
401次组卷
|
2卷引用:吉林省通化市梅河口市博文学校2022-2023学年高二下学期期末考试化学试题
名校
解题方法
6 . 铁元素广泛存在于自然界中,铁及其化合物有着丰富的化学性质。
(1) 铁粉与
铁粉与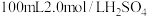 溶液反应,产生
溶液反应,产生 的体积(标准状况下)随时间变化如图。
的体积(标准状况下)随时间变化如图。 反应平均速率
反应平均速率
_______ 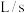 ;
;
② 、
、 、
、 三点反应速率从大到小顺序是:
三点反应速率从大到小顺序是:_______ 。
(2)常温下, 溶液与
溶液与 溶液反应生成血红色配合物,反应方程式可表示为
溶液反应生成血红色配合物,反应方程式可表示为 ,下列说法正确的是_______。(填标号)
,下列说法正确的是_______。(填标号)
(3)反应 在加入
在加入 催化后,反应进程中的能量变化如下图所示。已知反应机理中有
催化后,反应进程中的能量变化如下图所示。已知反应机理中有 出现。
出现。__________________________________________ ;
②反应过程中由于 浓度较低而不容易被检测到,请回答
浓度较低而不容易被检测到,请回答 浓度较低的原因:
浓度较低的原因:____________________________________ 。
(4)某些有色物质会吸收特定波长的光,吸光度与有色物质的浓度呈正比,这是分光光度法的基本原理,用公式表示为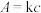 。溶液中
。溶液中 与邻二氮菲(
与邻二氮菲( ,一种双齿配体,其结构见下图)会生成橘黄色的配合物
,一种双齿配体,其结构见下图)会生成橘黄色的配合物 ,反应为:
,反应为: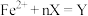 ;取
;取 的溶液,加入不同体积浓度均为
的溶液,加入不同体积浓度均为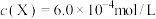 的
的 溶液,充分反应后加水定容至
溶液,充分反应后加水定容至 ,得到系列溶液,测其吸光度,结果如下表:
,得到系列溶液,测其吸光度,结果如下表:
根据此数据,可以推断反应计量数 ,并计算
,并计算 值,且可利用分光光度法测定未知溶液中
值,且可利用分光光度法测定未知溶液中 的浓度。
的浓度。
已知:1. 为吸光度,无单位;
为吸光度,无单位; 为常数,单位为
为常数,单位为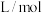 ;
; 为有色物质的物质的量浓度,单位为
为有色物质的物质的量浓度,单位为 (
( 和
和 吸光度近似为0)。
吸光度近似为0)。
①使用该方法时,需要控制 在2~9之间,其原因为:
在2~9之间,其原因为:____________________ 。
② 中
中 的配位数为
的配位数为_______ 。(填标号)
A.2 B.3 C.6 D.8
③该实验条件下 值为
值为______________ 。
(1)
 铁粉与
铁粉与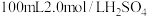 溶液反应,产生
溶液反应,产生 的体积(标准状况下)随时间变化如图。
的体积(标准状况下)随时间变化如图。
 反应平均速率
反应平均速率
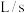 ;
;②
 、
、 、
、 三点反应速率从大到小顺序是:
三点反应速率从大到小顺序是:(2)常温下,
 溶液与
溶液与 溶液反应生成血红色配合物,反应方程式可表示为
溶液反应生成血红色配合物,反应方程式可表示为 ,下列说法正确的是_______。(填标号)
,下列说法正确的是_______。(填标号)A.增大 溶液的浓度,平衡常数增大 溶液的浓度,平衡常数增大 |
B.向上述平衡体系中加入适量 固体,平衡不移动 固体,平衡不移动 |
| C.加水稀释,平衡向左移动,且溶液的红色变浅 |
D.加入少量铁粉,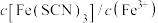 减小 减小 |
(3)反应
 在加入
在加入 催化后,反应进程中的能量变化如下图所示。已知反应机理中有
催化后,反应进程中的能量变化如下图所示。已知反应机理中有 出现。
出现。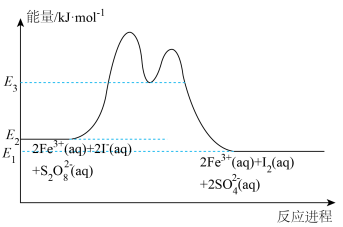
②反应过程中由于
 浓度较低而不容易被检测到,请回答
浓度较低而不容易被检测到,请回答 浓度较低的原因:
浓度较低的原因:(4)某些有色物质会吸收特定波长的光,吸光度与有色物质的浓度呈正比,这是分光光度法的基本原理,用公式表示为
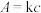 。溶液中
。溶液中 与邻二氮菲(
与邻二氮菲( ,一种双齿配体,其结构见下图)会生成橘黄色的配合物
,一种双齿配体,其结构见下图)会生成橘黄色的配合物 ,反应为:
,反应为: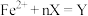 ;取
;取 的溶液,加入不同体积浓度均为
的溶液,加入不同体积浓度均为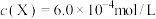 的
的 溶液,充分反应后加水定容至
溶液,充分反应后加水定容至 ,得到系列溶液,测其吸光度,结果如下表:
,得到系列溶液,测其吸光度,结果如下表:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
 ,并计算
,并计算 值,且可利用分光光度法测定未知溶液中
值,且可利用分光光度法测定未知溶液中 的浓度。
的浓度。已知:1.
 为吸光度,无单位;
为吸光度,无单位; 为常数,单位为
为常数,单位为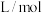 ;
; 为有色物质的物质的量浓度,单位为
为有色物质的物质的量浓度,单位为 (
( 和
和 吸光度近似为0)。
吸光度近似为0)。2.邻二氮菲的结构如图所示: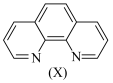
①使用该方法时,需要控制
 在2~9之间,其原因为:
在2~9之间,其原因为:②
 中
中 的配位数为
的配位数为A.2 B.3 C.6 D.8
③该实验条件下
 值为
值为
您最近一年使用:0次
13-14高二下·宁夏银川·期末
7 . 下列说法或有关化学用语的表达正确的是
| A.在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量 |
B.基态Fe原子的外围电子排布图为: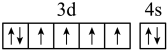 |
| C.因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 |
| D.根据原子核外电子排布的特点,Cu在周期表中属于s区元素 |
您最近一年使用:0次
2024-02-04更新
|
226次组卷
|
62卷引用:2014-2015吉林省吉林市第五十五中学高二下学期期中考试化学试卷
2014-2015吉林省吉林市第五十五中学高二下学期期中考试化学试卷吉林省辽源五中2017-2018学年高二下学期第一次月考化学试题吉林省扶余市第一中学2018-2019学年高二下学期第一次月考化学试题吉林省长春市第二十九中学2019-2020学年高二下学期期中考试化学试题吉林地区普通高中友好学校联合体2021-2022学年高二下学期期末考试化学试题吉林省普通高中友好学校联合体2023-2024学年高二上学期第三十七届基础年段期末联考化学试题(已下线)2013-2014宁夏银川一中高二下学期期末考试化学试卷2014-2015学年宁夏宁大附中高二上学期期中考试化学试卷2015-2016学年山西省大同一中高二下3月月考化学试卷2015-2016学年贵州省思南中学高二下期中化学试卷2015-2016学年辽宁省五校协作体高二下学期期中考试化学试卷2015-2016学年云南省德宏州芒一中高二下学期期末化学试卷山西省大同市第一中学2016-2017学年高二5月月考化学试题新疆呼图壁县第一中学2016-2017学年高二下学期期末考试化学试题贵州省思南中学2016-2017学年高二下学期期末考试化学试题2017-2018学年人教版高中化学选修三 模块综合质量检测四川省广安市第二中学校2017-2018学年高二下学期第二次月考化学试题山西省沁县中学2018-2019学年高二下学期第一次月考化学试题内蒙古自治区第一机械制造(集团)有限公司第一中学2018-2019学年高二下学期期中考试化学试题山东省聊城市2019-2020学年高三化学一轮复习《物质结构与性质(》模拟测试四川省广安第二中学校2017-2018学年高二下学期第一次月考化学试题辽宁省丹东市2017-2018学年高二下学期期末质量监测化学试题广西靖西市第二中学2019-2020学年高二下学期开学考试化学试题陕西省榆林市第十二中学2019-2020学年高二下学期期中考试化学试题江苏省如东高级中学2019-2020学年高一下学期第二次阶段测试化学试题安徽省安庆市太湖县2019-2020学年高二下学期期中质量调研考试化学试题福建省莆田市仙游县第二中学2019-2020学年高二下学期期中考试化学试题四川省南充市阆中中学2020-2021学年高二上学期期中考试化学试题安徽省蚌埠第三中学2019-2020学年高二下学期期末考试化学试题(已下线)模块同步卷12 综合检测卷(提升卷)-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)(已下线)专题11 物质结构与性质——备战2021年高考化学纠错笔记山东省济南市济阳区闻韶中学2020-2021学年高三(3班)12月第一次模拟考试化学试题宁夏青铜峡市高级中学2020-2021学年高二下学期第一次月考化学试题宁夏青铜峡市高级中学2020-2021学年高二下学期期中考试化学试题辽宁省沈阳市辽中区第一高级中学2020-2021学年高二下学期开学考试化学试题天津市实验中学滨海学校2020-2021学年高二下学期期中化学试题甘肃省武威第十八中学2020-2021学年高二下学期期中考试化学试题(已下线)作业02 原子结构与元素的性质-2021年高二化学暑假作业(人教版2019)新疆昌吉教育共同体2020-2021学年高二下学期期末质量检测化学试题福建省漳州市正兴学校2020-2021学年高二下学期期末考试化学试题宁夏银川市第六中学2020-2021学年高二下学期期末考试化学试题四川省遂宁市第二中学校2021-2022学年高二上学期期中考试化学试题辽宁省本溪市第二高级中学2021-2022学年高二上学期期末考试化学试题山西省长治市沁源县第一中学等名校2021-2022学年高二下学期5月联考化学试题第一章 本章复习提升1云南省石屏县第一中学2021-2022学年高二下学期3月份考试化学试题福建省莆田市第一中学2021-2022学年高二下学期期末考试化学试题安徽省合肥市肥东县综合高中2021-2022学年高二下学期期中考试化学试题四川省广安市邻水县二中 2022-2023学年高三上学期9月考化学试题甘肃省庆阳市第六中学2021-2022学年高二下学期期末考试化学试题福建省泉州科技中学2021-2022学年高二下学期期中考试化学试题新疆克拉玛依市高级中学2021-2022学年高二下学期期末考试化学试题重庆市荣昌永荣中学校2021-2022学年高二下学期期末考试化学试题山东省新泰市第一中学2022-2023学年高二下学期第一次大单元考试化学试题山东省青岛第十九中学2022-2023学年高二下学期4月月考化学试题宁夏青铜峡市宁朔中学2022-2023学年高二下学期期中考试化学试题四川省广元中学2022-2023学年高二下学期5月期中考试化学试题安徽省安庆市第二中学2022-2023学年高二下学期期中考试化学试题河北省唐山市开滦一中2022-2023学年高二下学期期末考试化学试题湖南省长郡中学2023-2024学年高二下学期寒假检测(开学考试)化学试题湖北省武汉西藏中学2023-2024学年高二下学期4月月考化学试题(已下线)猜想01 原子结构与性质 【考题猜想】(8大题型)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)
名校
解题方法
8 . 硼氢化钠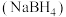 是一种潜在储氢剂,在有机合成中也被称为“万能还原剂”。实验室制备、提纯、分析
是一种潜在储氢剂,在有机合成中也被称为“万能还原剂”。实验室制备、提纯、分析 纯度的步骤如下,请结合信息回答问题。
纯度的步骤如下,请结合信息回答问题。
Ⅰ. 的制备
的制备
先打开 ,向装置中鼓入
,向装置中鼓入 ,然后升温到110℃左右,打开搅拌器快速搅拌,将融化的Na快速分散到石蜡油中,然后升温到200℃,关闭
,然后升温到110℃左右,打开搅拌器快速搅拌,将融化的Na快速分散到石蜡油中,然后升温到200℃,关闭 ,打开
,打开 通入
通入 ,充分反应后制得
,充分反应后制得 。然后升温到240℃,持续搅拌下通入
。然后升温到240℃,持续搅拌下通入 ,打开
,打开 ,向三颈瓶中滴入硼酸三甲酯[分子式为
,向三颈瓶中滴入硼酸三甲酯[分子式为 ,沸点为68℃],充分反应后,降温后离心分离得到
,沸点为68℃],充分反应后,降温后离心分离得到 和
和 的固体混合物。
的固体混合物。
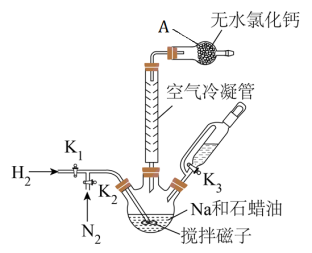
(1)仪器A的名称是__________ 。
(2)写出 与
与 的化学反应方程式
的化学反应方程式__________ 。
(3)将Na分散到石蜡油中的目的是__________ 。
Ⅱ. 的提纯
的提纯
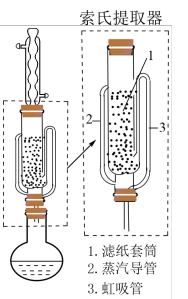
(4) 可采用索氏提取法提纯,其装置如图所示。实验时将
可采用索氏提取法提纯,其装置如图所示。实验时将 和
和 的固体混合物放入滤纸套筒1中,烧瓶中异丙胺(熔点:
的固体混合物放入滤纸套筒1中,烧瓶中异丙胺(熔点: ℃,沸点:33℃)受热蒸发,蒸汽沿导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,再经导管3返回烧瓶,从而实现连续萃取。当萃取完全后,
℃,沸点:33℃)受热蒸发,蒸汽沿导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,再经导管3返回烧瓶,从而实现连续萃取。当萃取完全后, 在
在__________ (填“圆底烧瓶”或“索氏提取器”)中。
(5)分离异丙胺和 并回收溶剂的方法是
并回收溶剂的方法是__________ 。
Ⅲ. 的纯度分析[已知
的纯度分析[已知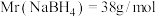 ]
]
步骤1:取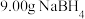 产品(杂质不参与反应),将产品溶于X溶液后配成
产品(杂质不参与反应),将产品溶于X溶液后配成 溶液,取
溶液,取 置于碘量瓶中,加入
置于碘量瓶中,加入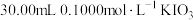 溶液充分反应。(反应为
溶液充分反应。(反应为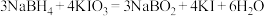 )
)
步骤2:向步骤1所得溶液中加入过量的KI溶液,用稀硫酸溶液调节pH,使过量 转化为
转化为 ,冷却后暗处放置数分钟。(反应为
,冷却后暗处放置数分钟。(反应为 )
)
步骤3:向步骤2所得溶液中加 和
和 缓冲溶液调pH约为5.0,加入几滴淀粉指示剂,用
缓冲溶液调pH约为5.0,加入几滴淀粉指示剂,用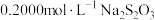 标准溶液滴定至终点,消耗标准溶液的体积为
标准溶液滴定至终点,消耗标准溶液的体积为 。(反应为
。(反应为 )
)
(6)X溶液为__________ (写化学式)。
(7)产品中 的纯度为
的纯度为__________ %。
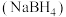 是一种潜在储氢剂,在有机合成中也被称为“万能还原剂”。实验室制备、提纯、分析
是一种潜在储氢剂,在有机合成中也被称为“万能还原剂”。实验室制备、提纯、分析 纯度的步骤如下,请结合信息回答问题。
纯度的步骤如下,请结合信息回答问题。
|
|
| |
性质 | 固体,可溶于异丙胺或水,常温下与水缓慢反应,与酸剧烈反应,强碱环境下能稳定存在 | 固体,强还原性,与水剧烈反应产生 | 固体,难溶于异丙胺,常温下与水剧烈反应 |
 的制备
的制备先打开
 ,向装置中鼓入
,向装置中鼓入 ,然后升温到110℃左右,打开搅拌器快速搅拌,将融化的Na快速分散到石蜡油中,然后升温到200℃,关闭
,然后升温到110℃左右,打开搅拌器快速搅拌,将融化的Na快速分散到石蜡油中,然后升温到200℃,关闭 ,打开
,打开 通入
通入 ,充分反应后制得
,充分反应后制得 。然后升温到240℃,持续搅拌下通入
。然后升温到240℃,持续搅拌下通入 ,打开
,打开 ,向三颈瓶中滴入硼酸三甲酯[分子式为
,向三颈瓶中滴入硼酸三甲酯[分子式为 ,沸点为68℃],充分反应后,降温后离心分离得到
,沸点为68℃],充分反应后,降温后离心分离得到 和
和 的固体混合物。
的固体混合物。
(1)仪器A的名称是
(2)写出
 与
与 的化学反应方程式
的化学反应方程式(3)将Na分散到石蜡油中的目的是
Ⅱ.
 的提纯
的提纯(4)
 可采用索氏提取法提纯,其装置如图所示。实验时将
可采用索氏提取法提纯,其装置如图所示。实验时将 和
和 的固体混合物放入滤纸套筒1中,烧瓶中异丙胺(熔点:
的固体混合物放入滤纸套筒1中,烧瓶中异丙胺(熔点: ℃,沸点:33℃)受热蒸发,蒸汽沿导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,再经导管3返回烧瓶,从而实现连续萃取。当萃取完全后,
℃,沸点:33℃)受热蒸发,蒸汽沿导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,再经导管3返回烧瓶,从而实现连续萃取。当萃取完全后, 在
在
(5)分离异丙胺和
 并回收溶剂的方法是
并回收溶剂的方法是Ⅲ.
 的纯度分析[已知
的纯度分析[已知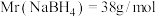 ]
]步骤1:取
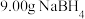 产品(杂质不参与反应),将产品溶于X溶液后配成
产品(杂质不参与反应),将产品溶于X溶液后配成 溶液,取
溶液,取 置于碘量瓶中,加入
置于碘量瓶中,加入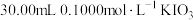 溶液充分反应。(反应为
溶液充分反应。(反应为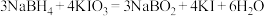 )
)步骤2:向步骤1所得溶液中加入过量的KI溶液,用稀硫酸溶液调节pH,使过量
 转化为
转化为 ,冷却后暗处放置数分钟。(反应为
,冷却后暗处放置数分钟。(反应为 )
)步骤3:向步骤2所得溶液中加
 和
和 缓冲溶液调pH约为5.0,加入几滴淀粉指示剂,用
缓冲溶液调pH约为5.0,加入几滴淀粉指示剂,用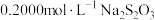 标准溶液滴定至终点,消耗标准溶液的体积为
标准溶液滴定至终点,消耗标准溶液的体积为 。(反应为
。(反应为 )
)(6)X溶液为
(7)产品中
 的纯度为
的纯度为
您最近一年使用:0次
2024-02-02更新
|
278次组卷
|
2卷引用:吉林省通化市梅河口市第五中学2023-2024学年高三上学期1月期末化学试题
名校
解题方法
9 . 某无色溶液可能由Na+、Ba2+、Cu2+、 、
、 、
、 、Cl-中的一种或几种。为了确定该溶液的成分,进行如下实验:
、Cl-中的一种或几种。为了确定该溶液的成分,进行如下实验:
①取少量该溶液加入足量氯水,有气体产生,得到甲溶液;
②取少量甲溶液,向其中加入硝酸酸化的硝酸银溶液,产生白色沉淀甲;
③取少量原溶液,向其中加入Ba(OH)2溶液,产生白色沉淀乙,加足量稀盐酸,沉淀部分溶解。
下列关于原溶液说法正确的是
 、
、 、
、 、Cl-中的一种或几种。为了确定该溶液的成分,进行如下实验:
、Cl-中的一种或几种。为了确定该溶液的成分,进行如下实验:①取少量该溶液加入足量氯水,有气体产生,得到甲溶液;
②取少量甲溶液,向其中加入硝酸酸化的硝酸银溶液,产生白色沉淀甲;
③取少量原溶液,向其中加入Ba(OH)2溶液,产生白色沉淀乙,加足量稀盐酸,沉淀部分溶解。
下列关于原溶液说法正确的是
A.肯定存在 |
| B.肯定不存在 Ba2+,可能存在Cu2+ |
C. 、 、 均不存在 均不存在 |
| D.是否存在Na+需要通过焰色试验来确定 |
您最近一年使用:0次
2024-02-02更新
|
127次组卷
|
3卷引用:吉林省“BEST合作体”2023-2024学年高一上学期期末考试化学试题
名校
10 . 环丙沙星是喹诺酮类抗菌药物,具有广谱抗菌活性,杀菌效果好,某研究小组按下列路线合成环丙沙星(H)。
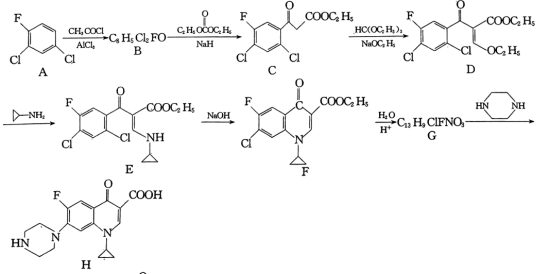
已知:RCOCH3

回答下列问题:
(1)B的结构简式是___________ 。
(2)C中含氧官能团名称是___________ 。
(3)写出D→E的化学方程式:___________ 。
(4)E→F的反应类型为___________ 。
(5)A的芳香族同分异构体有___________ 种(本身除外);写出符合下列要求的G的同分异构体的结构简式:___________ 。
①分子中含有2个苯环;
②lH-NMR谱表明:分子中共有5种不同化学环境的氢原子且数目之比为2:2:2:2:1;
③能与FeCl3溶液发生显色反应,且两种水解产物同样可以与FeCl3溶液发生显色反应。
(6)以 和
和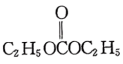 为原料合成
为原料合成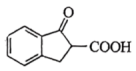 的路线图为:
的路线图为:
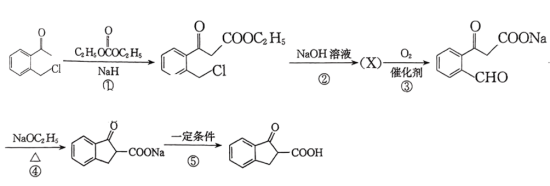
则X的结构简式为___________ ;反应⑤中的一定条件是指___________ 。

已知:RCOCH3


回答下列问题:
(1)B的结构简式是
(2)C中含氧官能团名称是
(3)写出D→E的化学方程式:
(4)E→F的反应类型为
(5)A的芳香族同分异构体有
①分子中含有2个苯环;
②lH-NMR谱表明:分子中共有5种不同化学环境的氢原子且数目之比为2:2:2:2:1;
③能与FeCl3溶液发生显色反应,且两种水解产物同样可以与FeCl3溶液发生显色反应。
(6)以
 和
和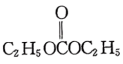 为原料合成
为原料合成 的路线图为:
的路线图为:
则X的结构简式为
您最近一年使用:0次