1 . 如图,某液态金属储能电池放电时产生金属化合物Li3Bi,下列说法正确的是
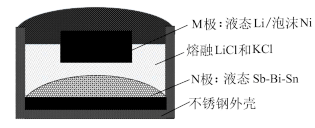

| A.放电时,电子流向为M电极→熔融LiCl和KCl→N电极 |
| B.放电时,N电极反应为3Li++Bi-3e-=Li3B |
| C.充电时,M电极的质量增加 |
| D.充电时,N极与外接电源的负极相连 |
您最近一年使用:0次
名校
2 . 化学实验是进行科学实验的基础。某实验小组在用NaOH标准溶液满定未知浓度的稀盐酸的实验中,下列操作符合规范的是
|
|
|
|
| A.试剂分类存放 | B.量取稀盐酸 | C.碱式滴定管排气泡 | D.滴加酚酞 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-24更新
|
151次组卷
|
4卷引用:2024届广西普通高中学业水平选择性考试第二次调研考试化学试题
2024届广西普通高中学业水平选择性考试第二次调研考试化学试题河南省安阳市2023-2024学年高三上学期第一次调研考试化学试题陕西省商洛市部分学校联考2023-2024学年高三上学期10月月考化学试题(已下线)专题03 化学实验基础-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
名校
解题方法
3 . 甲醇是重要的化工原料之一,也可用作燃料,利用合成气(主要成分为CO、CO2和H2)可以合成甲醇,涉及的反应如下:
反应ⅰ:CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
反应ii:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2=-49.9kJ∙mol-1
CH3OH(g)+H2O(g) △H2=-49.9kJ∙mol-1
反应iii:CO2(g)+H2(g) CO(g)+H2O(g) △H3=+41.6kJ∙mol-1
CO(g)+H2O(g) △H3=+41.6kJ∙mol-1
请回答下列问题:
(1)在某催化剂作用下,反应ⅰ的反应历程如图所示(图中数据表示微粒数目以及微粒的相对总能量,*表示吸附在催化剂上):

①反应ⅰ在______ (填“较低”或“较高”)温度下才能自发进行。
②结合反应历程,写出反应ⅰ中生成甲醇的决速步骤的反应方程式:_______ 。
③m=_______ (计算结果保留两位有效数字,已知1cV=1.6×10-22kJ)。
(2)反应ⅰ的Arrhenius经验公式Rlnk=- +C(Ea为活化能,k为速率常数,R和C均为常数,T为温度),实验数据如图中曲线M所示。当改变外界条件时,实验数据如图中曲线N所示,则实验可能改变的外界条件是
+C(Ea为活化能,k为速率常数,R和C均为常数,T为温度),实验数据如图中曲线M所示。当改变外界条件时,实验数据如图中曲线N所示,则实验可能改变的外界条件是______ 。

(3)将一定量的CO2(g)和H2(g)充入密闭容器中并加入合适的催化剂,只发生反应ii和iii。相同温度下,在不同压强下测得CO2的平衡转化率、CH3OH(g)的选择性[ ×100%]和CO的选择[
×100%]和CO的选择[ ×100%]随压强的变化曲线如图所示。
×100%]随压强的变化曲线如图所示。

图中表示CO2的平衡转化率的曲线是______ (填“m”“n”或“p”),简述判断方法:______ 。
(4)有研究认为,在某催化剂作用下反应ⅱ先后通过反应ⅲ、ⅰ来实现。保持温度T不变向一恒容密闭容器中充入4molCO2和8molH2,在该催化剂作用下发生反应,经5min达到平衡,测得H2O(g)的物质的量为3mol,起始及达平衡时容器的总压强分别为1.5akPa、akPa,则从开始到平衡用H2分压表示的平均反应速率为_______ kPa∙min-1(用含a的式子表示,下同,分压=总压×物质的量分数);反应ⅱ的压强平衡常数Kp=______ (kPa)-2(Kp为用分压代替浓度计算的平衡常数)。
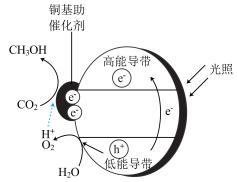
(5)光催化CO2制甲醇技术也是研究热点。铜基纳米光催化材料还原CO2的机理如图所示,光照时,低能价带失去电子并产生空穴(h+,具有强氧化性)。光催化原理与电解原理类似,则高能导带相当于电解池的______ 极;在低能价带上,H2O直接转化为O2的电极反应式为______ 。
反应ⅰ:CO(g)+2H2(g)
 CH3OH(g) △H1
CH3OH(g) △H1反应ii:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H2=-49.9kJ∙mol-1
CH3OH(g)+H2O(g) △H2=-49.9kJ∙mol-1反应iii:CO2(g)+H2(g)
 CO(g)+H2O(g) △H3=+41.6kJ∙mol-1
CO(g)+H2O(g) △H3=+41.6kJ∙mol-1请回答下列问题:
(1)在某催化剂作用下,反应ⅰ的反应历程如图所示(图中数据表示微粒数目以及微粒的相对总能量,*表示吸附在催化剂上):

①反应ⅰ在
②结合反应历程,写出反应ⅰ中生成甲醇的决速步骤的反应方程式:
③m=
(2)反应ⅰ的Arrhenius经验公式Rlnk=-
 +C(Ea为活化能,k为速率常数,R和C均为常数,T为温度),实验数据如图中曲线M所示。当改变外界条件时,实验数据如图中曲线N所示,则实验可能改变的外界条件是
+C(Ea为活化能,k为速率常数,R和C均为常数,T为温度),实验数据如图中曲线M所示。当改变外界条件时,实验数据如图中曲线N所示,则实验可能改变的外界条件是
(3)将一定量的CO2(g)和H2(g)充入密闭容器中并加入合适的催化剂,只发生反应ii和iii。相同温度下,在不同压强下测得CO2的平衡转化率、CH3OH(g)的选择性[
 ×100%]和CO的选择[
×100%]和CO的选择[ ×100%]随压强的变化曲线如图所示。
×100%]随压强的变化曲线如图所示。
图中表示CO2的平衡转化率的曲线是
(4)有研究认为,在某催化剂作用下反应ⅱ先后通过反应ⅲ、ⅰ来实现。保持温度T不变向一恒容密闭容器中充入4molCO2和8molH2,在该催化剂作用下发生反应,经5min达到平衡,测得H2O(g)的物质的量为3mol,起始及达平衡时容器的总压强分别为1.5akPa、akPa,则从开始到平衡用H2分压表示的平均反应速率为
(5)光催化CO2制甲醇技术也是研究热点。铜基纳米光催化材料还原CO2的机理如图所示,光照时,低能价带失去电子并产生空穴(h+,具有强氧化性)。光催化原理与电解原理类似,则高能导带相当于电解池的

您最近一年使用:0次
解题方法
4 . 常温下,几种弱酸的电离常数如表所示。
下列离子方程式正确的是
| 酸 | HClO | H2CO3 | H2SO3 | HCN |
| Ka | 3.0×10-8 | K1=4.3×10-7,K2=5.6×10-11 | K1=1.5×10-2,K2=1.0×10-7 | 4.9×10-10 |
A.向“84”消毒液中通入少量CO2:2ClO—+CO2+H2O= +2HClO +2HClO |
| B.向漂粉精溶液中通入少量SO2:Ca2++2ClO—+SO2+H2O=CaSO3↓+2HClO |
C.向KCN溶液中通入少量SO2:CN—+SO2+H2O=HCN+ |
D.向Na2SO3溶液中通入少量CO2: +CO2+H2O= +CO2+H2O= + + |
您最近一年使用:0次
2023-12-23更新
|
208次组卷
|
2卷引用:广西钦州市第四中学2023-2024学年高三上学期12月考试化学试卷
解题方法
5 . 如图为实验室利用浓盐酸和 制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条,F中为红色的铜网,其右端出气管口放有脱脂棉。
制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条,F中为红色的铜网,其右端出气管口放有脱脂棉。_______ ,写出实验室制取氯气的化学方程式:_______ 。
(2)C中盛装的溶液作用是_______ ,装置D中试剂是_______ 。
(3)E中红色布条是否褪色(填“是”或“否”)_______ ,由此可以得出的结论是_______ 。
(4)F中发生的化学方程式为_______ ,若有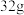 铜被氧化,则参与反应的
铜被氧化,则参与反应的 的质量为
的质量为_______ g。
(5)若H中加入的是氢氧化钠溶液,则该装置的作用是_______ 。
 制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条,F中为红色的铜网,其右端出气管口放有脱脂棉。
制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条,F中为红色的铜网,其右端出气管口放有脱脂棉。
(2)C中盛装的溶液作用是
(3)E中红色布条是否褪色(填“是”或“否”)
(4)F中发生的化学方程式为
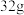 铜被氧化,则参与反应的
铜被氧化,则参与反应的 的质量为
的质量为(5)若H中加入的是氢氧化钠溶液,则该装置的作用是
您最近一年使用:0次
6 . 下列各组离子在指定溶液中一定能大量共存的是
A.无色透明溶液中: |
B.氯水中: |
C.常温下 的溶液中: 的溶液中: |
D. 溶液中: 溶液中: |
您最近一年使用:0次
10-11高一上·辽宁沈阳·期中
名校
解题方法
7 . 在一定条件下, 和
和 可发生如下反应:
可发生如下反应: ,从而可知在
,从而可知在 中,元素R的化合价是
中,元素R的化合价是
 和
和 可发生如下反应:
可发生如下反应: ,从而可知在
,从而可知在 中,元素R的化合价是
中,元素R的化合价是| A.+7价 | B.+4价 | C.+5价 | D.+6价 |
您最近一年使用:0次
2023-12-23更新
|
452次组卷
|
153卷引用:2013-2014学年广西北海市合浦县高一上学期期中考试化学试卷
(已下线)2013-2014学年广西北海市合浦县高一上学期期中考试化学试卷广西壮族自治区百色市田阳高中2019-2020学年高一上学期期中考试化学试题广西玉林师院附中、玉林市育才中学、玉林十一中、玉林市田家炳中学2019-2020学年高一上学期期中考试化学试题广西桂林市第十八中学2021-2022学年高一上学期开学考试化学试题广西贵港市名校2023-2024学年高一上学期入学联考化学试题(已下线)2010年辽宁省沈阳四校联合体高一上学期期中考试化学卷(已下线)2010年黑龙江牡丹江一中高一上学期期中考试化学试卷(已下线)2010年江苏省海安县南莫中学高一上学期期中考试化学试卷(已下线)2011-2012年浙江省金华一中高一上学期期中考试化学试卷(已下线)2011-2012年黑龙江哈九中高一上学期期中考试化学试卷(已下线)2011-2012学年辽宁省沈阳同泽女中高一上学期期中考试化学试卷(已下线)2011-2012学年山东省微山一中高一上学期期中考试化学试卷(已下线)2011-2012学年山东济宁梁山二中高一12月月考化学试卷(已下线)2011-2012学年武汉二中高一上学期期中考试化学试卷(已下线)2012届陕西省西安市第一中学高三上学期期中考试化学试卷(已下线)2011-2012学年黑龙江省绥棱县第一中学高一上学期期末考试化学试卷(已下线)2011-2012学年河北省衡水中学高一下学期期末考试化学试卷(已下线)2012-2013学年江西省白鹭洲中学高一第一次月考化学试卷(已下线)2012-2013学年安徽六安新安中学高一上学期期中考试化学试卷(已下线)2012-2013学年河北省石家庄市第一中学高一上学期期中考试化学试卷(已下线)2013-2014学年安徽省合肥一中高一上学期期中考试化学试卷(已下线)2013-2014学年重庆市重庆一中高一上学期期中考试化学试卷(已下线)2013-2014安徽省合肥一中高一上学期期中考试化学试卷(已下线)2014-2015河北保定某重点中学同步作业(必修1苏教版)2.2.3离子反应(已下线)2014-2015学年度河南省许昌市五校高一上期第一次联考化学试卷2014-2015辽宁省大连市高一上学期期末考试化学试卷2014-2015学年山东济南外国语学校高一上期中化学试卷2015-2016学年广东省广州培正中学高一上学期期中测试化学试卷2015-2016学年福建厦门双十中学高一上期中考试化学试卷2015-2016学年浙江省杭州二中高一上期末化学试卷2015-2016学年福建省莆田八中高一上学期第二次月考化学试卷2016-2017学年云南省云天化中学高一9月月考化学卷2016-2017学年黑龙江哈尔滨六中高一上期中化学试卷2016-2017学年江西省上高二中高一上月考二化学卷2016-2017学年新疆生产建设兵团二中高一上期中化学卷2017届陕西省黄陵中学高三上学期第三次质检化学试卷2016-2017学年辽宁省六校协作体高一下学期期初化学试卷辽宁省葫芦岛市六校协作体2016-2017学年高一下学期期初考试化学试题安徽省蚌埠市第二中学2017-2018学年高二上学期开学考试化学试题山西省运城中学、芮城中学2017-2018学年高一上学期期中联考化学试题河北省阜城中学2017-2018学年高一上学期第四次月考化学试题江西省抚州市临川实验学校2017-2018学年高一上学期期中考试化学试题高中化学人教版 必修1 第二章 化学物质及其变化 3.氧化还原反应 氧化还原反应安徽省濉溪县临涣中学2017-2018学年高一上学期第二次月考化学试题浙江省定海一中2017-2018学年高一第一学期期中考试化学试卷贵州省六盘水盘县四中2017-2018学年高一下学期期末考试化学试题【全国百强校】云南省云天化中学2018-2019学年高一上学期期中考试化学试题贵州省正安县一中2018-2019学年高一上学期期中考试化学试题【全国百强校】山东省菏泽第一中学八一路校区2018-2019学年高一上学期12月月考化学试题【全国百强校】山西省山西大学附属中学2018-2019学年高一下学期2月模块诊断化学试题江西省南康中学2017-2018学年高一上学期期中考试化学试题吉林省乾安县七中2017-2018学年高一上学期期中考试化学试卷吉林省吉林地区普通高中友好学校联合体第三十一届2019-2020学年高一上学期期中考试化学试题内蒙古自治区乌兰察布市集宁一中2019-2020学年高一上学期期中考试化学试题广东省北大附中深圳南山分校2020届高三上学期期中考试化学试题四川省雅安中学2019-2020学年高一上学期期中考试化学试题河南省漯河市实验高中2019-2020学年高一上学期期中考试化学试题宁夏青铜峡市高级中学2019-2020学年高一上学期期中考试化学试题北京市第二十二中学2019-2020学年高一上学期期中考试化学试题江西省南昌市新建县第一中学2020届高三上学期第一次月考化学试题(共建部)黑龙江省大庆市第四中学2019-2020学年高一上学期第二次月考化学试题河南省驻马店市正阳县高级中学2019-2020学年高一上学期第三次素质检测化学试题云南省马关县第二中学2019-2020学年高一上学期期末考试化学试题2020年春季人教版高中化学必修1第二章《化学物质及其变化》测试卷青海省西宁市第十四中学2019-2020学年高二上学期期末考试化学试题贵州省黔南布依族苗族自治州瓮安第二中学2019-2020学年高三上学期期末考试化学试题福建省福州市福建师范大学附属中学2017-2018学年高一下学期期中考试化学试题河北省石家庄市第二中学2018-2019学年高一上学期期末考试化学试题辽宁省营口市第二高级中学2019-2020学年高一上学期第一次月考化学试题(已下线)衔接点09 氧化还原反应的表示-2020年【衔接教材·暑假作业】初高中衔接化学(已下线)衔接点08 氧化还原反应的一般规律-2020年【衔接教材·暑假作业】初高中衔接化学山西省朔州市怀仁市第一中学云东校区2019-2020学年高一期末考试化学试题(已下线)3.2.3 离子反应练习(2)——《高中新教材同步备课》(苏教版 必修第一册)(已下线)第2章 总结与检测(2)——《高中新教材同步备课》(鲁科版 必修第一册)河南省平顶山市舞钢市第一高级中学2021届高三9月月考化学试题吉林省白城市洮南市第一中学2021届高三上学期第一次月考化学试题江苏省南京外国语学校2018-2019学年高一上学期期中考试化学试题黑龙江省绥化市安达市第七中学2020-2021学年高一上学期9月月考化学试题河南省新乡市2020-2021学年高一阶段测试化学试题山西省运城市新绛中学、河津中学等校2020-2021学年高一上学期10月联考化学试题(已下线)【浙江新东方】21(已下线)【浙江新东方】14(已下线)【浙江新东方】15江苏省南京师范大学附属中学2020-2021学年高一上学期期中考试化学试题湖南省长沙市南雅中学2020—2021学年高一上学期第一次月考化学试题湖北省荆门市沙洋县沙洋中学2020-2021学年高一上学期10月月考化学试题湖南省常德市第一中学2020-2021学年高一上学期期中考试化学试题安徽省合肥瑶海区合肥市第十一中学2020-2021学年高一上学期期中考试化学试题吉林省榆树市第一高级中学2021届高三上学期第三次模拟考试化学试题吉林省大安市第六中学2020-2021学年高一上学期第二次月考化学试题甘肃省张掖市2020-2021学年高一上学期期末学业水平质量检测化学试题甘肃省镇原县第二中学2020-2021学年高一上学期期中考试化学试题陕西省宝鸡市渭滨区2020-2021学年高一上学期期末考试化学试题江苏省苏州市西安交通大学苏州附属中学2020-2021学年高一上学期期中考试化学试卷黑龙江省伊春市伊美区第二中学2020-2021学年高一上学期第三次月考化学试题吉林省长春市第一五一中学2020-2021学年高一上学期期中考试化学试题(已下线)衔接点08 氧化还原反应的一般规律-2021年初升高化学无忧衔接(已下线)衔接点09 氧化还原反应的表示-2021年初升高化学无忧衔接河北师范大学附属实验中学2020~2021学年高一上学期10月月考化学试题山西省运城市稷山中学2022届高三上学期月考(一)化学试题吉林省白城市第一中学2021-2022学年高一上学期第一次阶段考试化学试题陕西省榆林市绥德中学2020-2021学年高一下学期第一次阶段性测试化学试卷黑龙江省双鸭山市第一中学2021-2022学年高一上学期第一次月考化学试题广东省名校2021-2022学年高一上学期第一次月考化学试卷河北省石家庄市师范大学附属实验中学2021-2022高一上学期10月月考化学试卷宁夏银川唐徕回民中学2021-2022学年高一11月月考化学试题陕西省西安市第一中学2022届高三上学期期中考试化学试题北京师范大学附属中学2021-2022学年高一上学期期中考试化学试题湖北省巴东一中2020-2021学年高一上学期第三次月考化学试题江西省吉安市遂川中学2021-2022学年高一上学期第一次月考化学(B卷)试题湖南省长郡中学2021-2022学年高一上学期期末考试化学试题(已下线)衔接点13 氧化还原反应的规律和表示方法-2022年初升高化学无忧衔接?吉林省长春市东北师范大学附属中学2022-2023学年高一上学期阶段考试化学试题北京市丰台区丰台第二中学2022-2023学年上学期高三10月月考化学试题新疆生产建设兵团第一师高级中学2022-2023学年高一上学期第一次月考化学试题黑龙江省鸡西市英桥高级中学2021-2022学年高二下学期期末考试化学试题湖北省襄阳四中2021-2022学年高一上学期10月考试化学试题陕西省西安市铁一中2022-2023学年高一上学期第一次月考化学试题湖南省邵阳市武冈市2020-2021学年高一上学期期中考试化学试题北京市第一七一中学2022-2023学年高一上学期期中考试化学试题辽宁省锦州市渤海大学附属高级中学2022-2023学年高一上学期期中考试化学试题安徽省六安中学2021-2022学年高一上学期期中考试化学试题云南省昆明市禄劝彝族苗族自治县第一中学2021-2022学年高一网络班10月月考化学试题安徽省阜阳第一中学2022-2023学年高一上学期第三次月考化学试题河北省唐山市乐亭第二中学2022-2023学年高一上学期期末考试化学试题重庆实验外国语学校2022-2023学年高一上学期1月期末考试化学试题(已下线)第二章 物质的量化学实验基本技能 第8练 化学计算的常用方法福建省莆田锦江中学2022-2023学年高一上学期期末质检化学试题广东省河源市龙川县第一中学2022-2023学年高一上学期期末考试化学试题云南省玉溪第一中学2022-2023学年高一上学期第一月考化学试题 微专题(四) 氧化还原反应的简单规律及应用甘肃省天水市甘谷县2023-2024学年高三上学期第一次检测化学试题河南省河南中原名校联考2023-2024学年高一上学期9月月考化学试题陕西省西安高新第一中学2023-2024学年高一上学期第一次月考化学试题辽宁省鞍山市普通高中2023-2024学年高一上学期10月月考化学(A卷)试题新疆乌鲁木齐第八中学2023-2024学年高一上学期第一次月考化学试题云南省昆明市第八中学2023-2024学年高一上学期9月月考化学试卷题吉林省长春市新解放学校2022-2023学年高一上学期11月期中化学试题湖南省株洲市第二中学2023-2024学年高一上学期第一次适应性检测化学试题 天津市双菱中学2023-2024学年高一上学期期中考试化学试卷湖南省洞口县第九中学2023-2024学年高一上学期第一次月考化学试题辽宁省大连保税区第一高级中学2023-2024学年高一上学期10月月考化学(A)试题江西省景德镇市乐平市第三中学2023-2024学年高一上学期10月月考化学试题湖南省岳阳县第一中学2023-2024学年高一上学期第一次月考化学试题 辽宁省阜新市第二高级中学2023-2024学年高一上学期第一次考试化学试卷河南省濮阳市第一高级中学2023-2024学年高一上学期第一次质量检测化学试题四川省内江市威远中学2023-2024学年高一上学期期中考试化学试题黑龙江省实验中学2023-2024学年高一上学期期中测试化学试题河南省开封市五县联考2023-2024学年高一上学期12月月考化学试题北京市第三十五中学2021-2022学年高一上学期期中考试化学试题湖南省永州市祁阳县第四中学2023-2024学年高一上学期期中考试化学试题北京市第一六一中学2023-2024学年高一上学期期中考试化学试题四川省泸州市泸县第五中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
8 . 某校化学兴趣小组为探究 性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
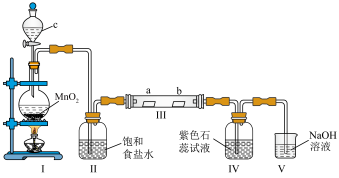
(1)装置Ⅰ中仪器c的名称是___________ ,实验室以二氧化锰和浓盐酸共热制备氯气的离子方程式为___________ 。
(2)装置Ⅱ的作用是___________ 。
(3)若产生的 足量,实验过程中装置Ⅳ中的实验现象是
足量,实验过程中装置Ⅳ中的实验现象是___________ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。
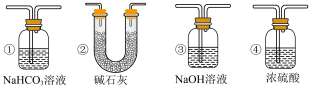
通过装置Ⅲ观察到预期现象,得出的结论是___________ 。
(5)实验结束后为了检验溶液中含有 ,请写出实验方案:
,请写出实验方案:___________ 。
(6)装置Ⅴ中可用饱和 溶液,反应的生成物有3种,其中有
溶液,反应的生成物有3种,其中有 、NaClO。试写出该反应的化学方程式:
、NaClO。试写出该反应的化学方程式:___________ 。
(7)整个实验应在通风厨中进行,并开启通风设备,原因是___________ 。
 性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生的
 足量,实验过程中装置Ⅳ中的实验现象是
足量,实验过程中装置Ⅳ中的实验现象是(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

通过装置Ⅲ观察到预期现象,得出的结论是
(5)实验结束后为了检验溶液中含有
 ,请写出实验方案:
,请写出实验方案:(6)装置Ⅴ中可用饱和
 溶液,反应的生成物有3种,其中有
溶液,反应的生成物有3种,其中有 、NaClO。试写出该反应的化学方程式:
、NaClO。试写出该反应的化学方程式:(7)整个实验应在通风厨中进行,并开启通风设备,原因是
您最近一年使用:0次
名校
9 . 常温下,某实验人员在两个相同的容器中分别加入20 mL 0.2 mol⋅L-1  溶液和40 mL 0.1 mol⋅L-1 NaHA溶液,再分别用0.2 mol⋅L-1盐酸滴定,利用pH计和压力传感器检测,绘制曲线如图所示。(已知
溶液和40 mL 0.1 mol⋅L-1 NaHA溶液,再分别用0.2 mol⋅L-1盐酸滴定,利用pH计和压力传感器检测,绘制曲线如图所示。(已知 溶液达到某浓度后,会放出一定量气体,溶液体积变化可忽略不计)
溶液达到某浓度后,会放出一定量气体,溶液体积变化可忽略不计)
 溶液和40 mL 0.1 mol⋅L-1 NaHA溶液,再分别用0.2 mol⋅L-1盐酸滴定,利用pH计和压力传感器检测,绘制曲线如图所示。(已知
溶液和40 mL 0.1 mol⋅L-1 NaHA溶液,再分别用0.2 mol⋅L-1盐酸滴定,利用pH计和压力传感器检测,绘制曲线如图所示。(已知 溶液达到某浓度后,会放出一定量气体,溶液体积变化可忽略不计)
溶液达到某浓度后,会放出一定量气体,溶液体积变化可忽略不计)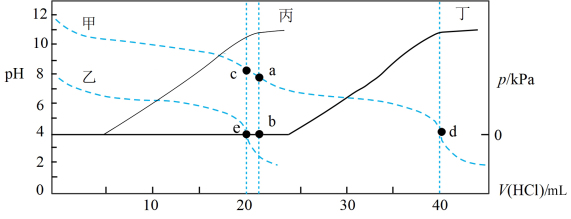
| A.图中曲线乙和丙代表向NaHA溶液中滴加盐酸 |
B.由图可知,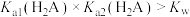 |
C.a点溶液中存在: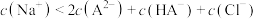 |
| D.根据pH-V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂 |
您最近一年使用:0次
2023-12-22更新
|
141次组卷
|
2卷引用:广西钦州市第四中学2023-2024学年高二上学期11月考试化学试卷
10 . 用NA表示阿伏加德罗常数的值,下列说法正确的是
A. 的 的 中含 中含 数为NA 数为NA | B.常温常压下,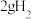 中含有的氢原子数为2NA 中含有的氢原子数为2NA |
C. 镁原子中含有的电子数为2NA 镁原子中含有的电子数为2NA | D.常温常压下, 含有的分子数为2NA 含有的分子数为2NA |
您最近一年使用:0次
2023-12-22更新
|
62次组卷
|
2卷引用:广西钦州市第四中学2023-2024学年高三上学期10月考试化学试卷