真题
解题方法
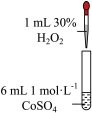
1 . 学习小组为探究 、
、 能否催化
能否催化 的分解及相关性质,室温下进行了实验I~Ⅳ。
的分解及相关性质,室温下进行了实验I~Ⅳ。
已知: 为粉红色、
为粉红色、 为蓝色、
为蓝色、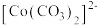 为红色、
为红色、 为墨绿色。回答下列问题:
为墨绿色。回答下列问题:
(1)配制 的
的 溶液,需要用到下列仪器中的
溶液,需要用到下列仪器中的_______ (填标号)。
_______ (填“能”或“不能”)催化 的分解。实验Ⅱ中
的分解。实验Ⅱ中 大大过量的原因是
大大过量的原因是_______ 。实验Ⅲ初步表明 能催化
能催化 的分解,写出
的分解,写出 在实验Ⅲ中所发生反应的离子方程式
在实验Ⅲ中所发生反应的离子方程式_______ 、_______ 。
(3)实验I表明,反应 难以正向进行,利用化学平衡移动原理,分析
难以正向进行,利用化学平衡移动原理,分析 、
、 分别与
分别与 配位后,正向反应能够进行的原因
配位后,正向反应能够进行的原因_______ 。_______ 、_______ 。
 、
、 能否催化
能否催化 的分解及相关性质,室温下进行了实验I~Ⅳ。
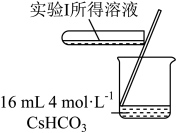
的分解及相关性质,室温下进行了实验I~Ⅳ。| 实验I | 实验Ⅱ | 实验Ⅲ |
|
|
|
| 无明显变化 | 溶液变为红色,伴有气泡产生 | 溶液变为墨绿色,并持续产生能使带火星木条复燃的气体 |
 为粉红色、
为粉红色、 为蓝色、
为蓝色、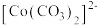 为红色、
为红色、 为墨绿色。回答下列问题:
为墨绿色。回答下列问题:(1)配制
 的
的 溶液,需要用到下列仪器中的
溶液,需要用到下列仪器中的a.  b.
b. 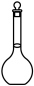 c.
c.  d.
d.

 的分解。实验Ⅱ中
的分解。实验Ⅱ中 大大过量的原因是
大大过量的原因是 能催化
能催化 的分解,写出
的分解,写出 在实验Ⅲ中所发生反应的离子方程式
在实验Ⅲ中所发生反应的离子方程式(3)实验I表明,反应
 难以正向进行,利用化学平衡移动原理,分析
难以正向进行,利用化学平衡移动原理,分析 、
、 分别与
分别与 配位后,正向反应能够进行的原因
配位后,正向反应能够进行的原因实验Ⅳ:
您最近一年使用:0次
名校
解题方法
2 . 光催化剂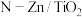 可用于含硫废液的氧化处理,光生电子
可用于含硫废液的氧化处理,光生电子 与水电离出的
与水电离出的 、
、 作用生成过氧羟基自由基
作用生成过氧羟基自由基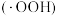 ,空穴
,空穴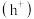 与水电离出的
与水电离出的 作用生成羟基自由基
作用生成羟基自由基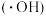 ,
, 分别与
分别与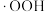 和
和 反应生成
反应生成 ,变化过程如图所示。下列说法错误的是
,变化过程如图所示。下列说法错误的是
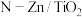 可用于含硫废液的氧化处理,光生电子
可用于含硫废液的氧化处理,光生电子 与水电离出的
与水电离出的 、
、 作用生成过氧羟基自由基
作用生成过氧羟基自由基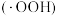 ,空穴
,空穴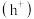 与水电离出的
与水电离出的 作用生成羟基自由基
作用生成羟基自由基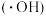 ,
, 分别与
分别与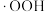 和
和 反应生成
反应生成 ,变化过程如图所示。下列说法错误的是
,变化过程如图所示。下列说法错误的是
A.通过①②过程和③④过程产生的 之比为1∶1 之比为1∶1 |
B. 氧化 氧化 的反应为 的反应为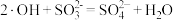 |
C. 过低或过高均会影响催化剂的催化效果 过低或过高均会影响催化剂的催化效果 |
D.氧化含硫废液的总反应为 |
您最近一年使用:0次
名校
3 . 请回答下列问题:
(1)冷敷袋俗称冰袋,在日常生活中有降温、保鲜和镇痛等多种用途。
①制作冷敷袋常利用吸热的化学变化来实现,以下组合最能满足的是___________ 。(填字母)
A.冰 B.硝酸铵+水 C.硝酸铵+水合碳酸钠
②下列过程中的热量变化与冰袋一致的有___________ 。(填字母)
a. b.盐酸和镁条
b.盐酸和镁条
c.盐酸和碳酸氢钠 d. 和氯化铵
和氯化铵
e. 分解
分解
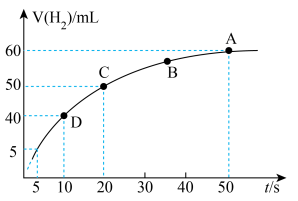
③某课外实验小组利用压强传感器、温度传感器、数据采集器和计算机等数字化实验设备,探究镁与一定量盐酸的反应速率,测得产生 的体积与反应时间的关系曲线如图所示,结合所学知识分析速率变化的原因为
的体积与反应时间的关系曲线如图所示,结合所学知识分析速率变化的原因为___________ ;在20s内用H+浓度表示的平均反应速率
___________ (20s时溶液体积为50mL,气体摩尔体积为25L/mol)。 ,是一个常见的放热反应。回答下列问题。
,是一个常见的放热反应。回答下列问题。
t℃时,向填充有催化剂、体积为2L的刚性容器中充入一定量的 和
和 合成氨,实验中测得
合成氨,实验中测得 随时间的变化如表所示:
随时间的变化如表所示:
①4-6min内 的平均反应速率
的平均反应速率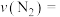
___________ 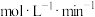
②下列情况能说明反应达到平衡状态的是___________ (填标号)。
A.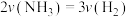 B.混合气体的平均相对分子质量不再变化
B.混合气体的平均相对分子质量不再变化
C. 体积分数不再变化 D.混合气体的密度保持不变
体积分数不再变化 D.混合气体的密度保持不变
③如表列出了在不同温度和压强下,反应达到平衡时 的百分含量
的百分含量 。
。
从表中数据得出,合成氨最优的条件是___________ 。
(1)冷敷袋俗称冰袋,在日常生活中有降温、保鲜和镇痛等多种用途。
①制作冷敷袋常利用吸热的化学变化来实现,以下组合最能满足的是
A.冰 B.硝酸铵+水 C.硝酸铵+水合碳酸钠
②下列过程中的热量变化与冰袋一致的有
a.
 b.盐酸和镁条
b.盐酸和镁条c.盐酸和碳酸氢钠 d.
 和氯化铵
和氯化铵e.
 分解
分解③某课外实验小组利用压强传感器、温度传感器、数据采集器和计算机等数字化实验设备,探究镁与一定量盐酸的反应速率,测得产生
 的体积与反应时间的关系曲线如图所示,结合所学知识分析速率变化的原因为
的体积与反应时间的关系曲线如图所示,结合所学知识分析速率变化的原因为
 ,是一个常见的放热反应。回答下列问题。
,是一个常见的放热反应。回答下列问题。t℃时,向填充有催化剂、体积为2L的刚性容器中充入一定量的
 和
和 合成氨,实验中测得
合成氨,实验中测得 随时间的变化如表所示:
随时间的变化如表所示:①4-6min内
 的平均反应速率
的平均反应速率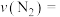
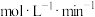
| 时间/min | 2 | 4 | 6 | 8 | 10 | 12 |
 / / | 0.04 | 0.10 | 0.14 | 0.16 | 0.16 | 0.16 |
A.
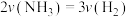 B.混合气体的平均相对分子质量不再变化
B.混合气体的平均相对分子质量不再变化C.
 体积分数不再变化 D.混合气体的密度保持不变
体积分数不再变化 D.混合气体的密度保持不变③如表列出了在不同温度和压强下,反应达到平衡时
 的百分含量
的百分含量 。
。压强/MPa % %温度/℃ | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.5 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
您最近一年使用:0次
名校
4 . 羟基自由基( )是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为
)是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为 和
和 的原电池—电解池组合装置如下图,实现发电、环保二位一体。下列说法不正确的是
的原电池—电解池组合装置如下图,实现发电、环保二位一体。下列说法不正确的是
 )是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为
)是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为 和
和 的原电池—电解池组合装置如下图,实现发电、环保二位一体。下列说法不正确的是
的原电池—电解池组合装置如下图,实现发电、环保二位一体。下列说法不正确的是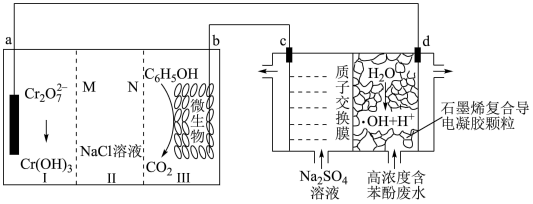
| A.c电极的电势低于d电极的电势 |
B.b极区发生的反应为 |
C.系统工作时,每转移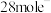 消耗 消耗 苯酚 苯酚 |
D.相同条件下,c、d两极产生气体的体积比为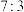 |
您最近一年使用:0次
名校
5 .  是三元弱酸。室温下,向
是三元弱酸。室温下,向 的
的 溶液中滴加
溶液中滴加 溶液调节pH。混合溶液中
溶液调节pH。混合溶液中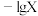 [表示
[表示 、
、 、
、 ]随溶液
]随溶液 的变化如图所示。下列说法不正确的是
的变化如图所示。下列说法不正确的是
 是三元弱酸。室温下,向
是三元弱酸。室温下,向 的
的 溶液中滴加
溶液中滴加 溶液调节pH。混合溶液中
溶液调节pH。混合溶液中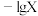 [表示
[表示 、
、 、
、 ]随溶液
]随溶液 的变化如图所示。下列说法不正确的是
的变化如图所示。下列说法不正确的是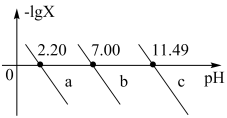
A.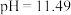 时, 时,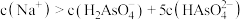 |
B.溶液中存在关系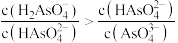 |
C.随着 的增大, 的增大, 保持不变 保持不变 |
D.常温下, 的 的 的数量级为 的数量级为 |
您最近一年使用:0次
名校
解题方法
6 . 碲(Te)常用于冶金工业,也是石油裂解的催化剂。工业上常以碲铜废料(主要成分是 )为原料提取碲,其工艺流程如下:
)为原料提取碲,其工艺流程如下: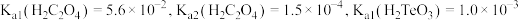 ,
,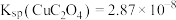 。
。
(1) 中碲元素的化合价为
中碲元素的化合价为_______ 。碲在元素周期表中的位置为_______ 。
(2)“氧化酸浸”得到 和
和 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(3) 可溶于
可溶于 ,反应
,反应 的平衡常数为
的平衡常数为_______ 。(保留两位有效数字){已知:反应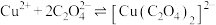 的平衡常数
的平衡常数 }
}
(4)“还原”在 50 ℃条件下进行: ,反应中还原产物和氧化产物的物质的量之比为
,反应中还原产物和氧化产物的物质的量之比为_______ 。
(5)“还原”时, 的实际投入量大于理论量,其可能原因有
的实际投入量大于理论量,其可能原因有_______ 。
(6)将一定质量的 置于
置于 气中热解,测得剩余固体的质量与原始固体的质量的比值约为
气中热解,测得剩余固体的质量与原始固体的质量的比值约为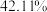 ,则剩余固体的化学式为
,则剩余固体的化学式为_______ 。
 )为原料提取碲,其工艺流程如下:
)为原料提取碲,其工艺流程如下:
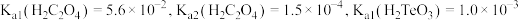 ,
,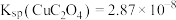 。
。(1)
 中碲元素的化合价为
中碲元素的化合价为(2)“氧化酸浸”得到
 和
和 ,该反应的化学方程式为
,该反应的化学方程式为(3)
 可溶于
可溶于 ,反应
,反应 的平衡常数为
的平衡常数为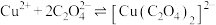 的平衡常数
的平衡常数 }
}(4)“还原”在 50 ℃条件下进行:
 ,反应中还原产物和氧化产物的物质的量之比为
,反应中还原产物和氧化产物的物质的量之比为(5)“还原”时,
 的实际投入量大于理论量,其可能原因有
的实际投入量大于理论量,其可能原因有(6)将一定质量的
 置于
置于 气中热解,测得剩余固体的质量与原始固体的质量的比值约为
气中热解,测得剩余固体的质量与原始固体的质量的比值约为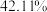 ,则剩余固体的化学式为
,则剩余固体的化学式为
您最近一年使用:0次
名校
7 . 在恒温恒压下,向 密闭容器中充入
密闭容器中充入 和
和 ,发生如下反应:
,发生如下反应: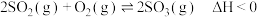 ,
, 后,反应达到平衡,生成
后,反应达到平衡,生成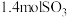 ,同时放出热量
,同时放出热量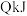 。则下列分析正确的是
。则下列分析正确的是
 密闭容器中充入
密闭容器中充入 和
和 ,发生如下反应:
,发生如下反应: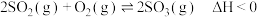 ,
, 后,反应达到平衡,生成
后,反应达到平衡,生成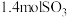 ,同时放出热量
,同时放出热量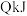 。则下列分析正确的是
。则下列分析正确的是A.若把条件“恒温恒压”改为“恒温恒容”,平衡时 的浓度前者大于后者 的浓度前者大于后者 |
B. 后,如果保持温度不变,将容器的容积扩大到原来的两倍,再达到平衡时 后,如果保持温度不变,将容器的容积扩大到原来的两倍,再达到平衡时 的浓度等于 的浓度等于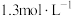 |
C.若把条件“恒温恒压”改为“恒压绝热”,则平衡后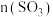 大于 大于 |
D.在该条件下,反应前后的压强之比为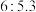 |
您最近一年使用:0次
名校
8 . 以浓差电池(因电解质溶液浓度不同而形成的电池)为电源。以石墨为电极,将 转化为高纯度
转化为高纯度 的装置如图所示,下列说法错误的是
的装置如图所示,下列说法错误的是
 转化为高纯度
转化为高纯度 的装置如图所示,下列说法错误的是
的装置如图所示,下列说法错误的是
A.停止工作后,若要使电池恢复原状态,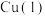 与电源正极相连 与电源正极相连 |
B.转移 电子时,甲室电解质溶液质量增加 电子时,甲室电解质溶液质量增加 |
C.电解过程中,丁室溶液的 会增大 会增大 |
D. 为阳极,电极方程式为 为阳极,电极方程式为 |
您最近一年使用:0次
9 . 从“钛磁铁矿”冶炼金属铁后的“含钛高炉渣”中提取金属钛的工艺流程如下:
②“水浸”溶液的 。
。
请回答下列问题:
(1)“熔融”时,为了使反应物充分受热融化反应,可以采取的措施有___________ 。
(2)某实验小组模拟“熔融”过程的反应,将固体 与
与 按物质的量1:2混合反应生成
按物质的量1:2混合反应生成 反应过程的热重曲线如图所示。
反应过程的热重曲线如图所示。 的方程式为
的方程式为___________ 。
②“水浸”后滤渣主要有___________ 。
(3)整合剂EDTA(乙二胺四乙酸三钠, )能够与金属阳离子按1:1反应形成非常稳定的整合物(
)能够与金属阳离子按1:1反应形成非常稳定的整合物(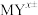 )。已知
)。已知 ,
,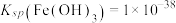
①“水解”步骤加入EDTA的目的是___________ 。
②常温下,某溶液中 和Fe3+浓度均为:
和Fe3+浓度均为: 的溶液中,用氨水调pH至4时溶液中的
的溶液中,用氨水调pH至4时溶液中的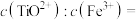
___________ 。
(4)一种 晶体结构如图(黑球表示
晶体结构如图(黑球表示 ,白球表示
,白球表示 ),其熔点为1850℃。
),其熔点为1850℃。 的配位数为
的配位数为___________ 。
②“电解”时,以覆盖氮化硼的石墨电极为阳极,电解 的共熔物得到金属钛,
的共熔物得到金属钛,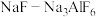 的作用是
的作用是___________ 。
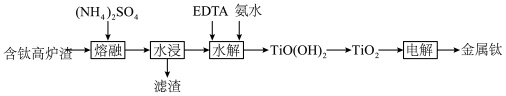
| 组分 |  |  |  |  |  |  | 其他 |
| 质量分数% | 34 | 6~16 | 17~19 | 14~16 | 8.0~9.0 | 3.0~4.2 | 0.8 |
 。
。请回答下列问题:
(1)“熔融”时,为了使反应物充分受热融化反应,可以采取的措施有
(2)某实验小组模拟“熔融”过程的反应,将固体
 与
与 按物质的量1:2混合反应生成
按物质的量1:2混合反应生成 反应过程的热重曲线如图所示。
反应过程的热重曲线如图所示。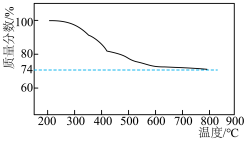
 的方程式为
的方程式为②“水浸”后滤渣主要有
(3)整合剂EDTA(乙二胺四乙酸三钠,
 )能够与金属阳离子按1:1反应形成非常稳定的整合物(
)能够与金属阳离子按1:1反应形成非常稳定的整合物(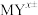 )。已知
)。已知 ,
,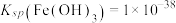
①“水解”步骤加入EDTA的目的是
②常温下,某溶液中
 和Fe3+浓度均为:
和Fe3+浓度均为: 的溶液中,用氨水调pH至4时溶液中的
的溶液中,用氨水调pH至4时溶液中的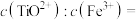
(4)一种
 晶体结构如图(黑球表示
晶体结构如图(黑球表示 ,白球表示
,白球表示 ),其熔点为1850℃。
),其熔点为1850℃。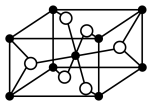
 的配位数为
的配位数为②“电解”时,以覆盖氮化硼的石墨电极为阳极,电解
 的共熔物得到金属钛,
的共熔物得到金属钛,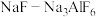 的作用是
的作用是
您最近一年使用:0次
名校
解题方法
10 . 非金属的卤化物水解可以分为亲电水解和亲核水解,实例及部分机理示意如下:发生亲电水解的条件是中心原子具有孤电子对,能接受H2O的H+的进攻,如: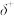 和空的价层轨道,接受H2O的孤电子对进攻,如:
和空的价层轨道,接受H2O的孤电子对进攻,如:

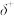 和空的价层轨道,接受H2O的孤电子对进攻,如:
和空的价层轨道,接受H2O的孤电子对进攻,如:
| A.NCl3和SiCl4水解过程中中心原子的杂化方式不变 |
| B.推测CCl4比SiCl4难发生亲核水解 |
| C.推测NF3比NCl3难发生亲电水解: |
| D.已知AsCl3的水解产物为H3AsO3和HCl,推测其水解类型为亲核水解 |
您最近一年使用:0次
2024-06-11更新
|
143次组卷
|
2卷引用:湖北省武昌区2024届高三下学期5月质量检测(二模)化学试题