名校
解题方法
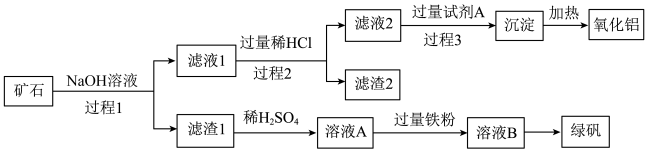
1 . 铝、铁、硅的单质及化合物在工业生产中具有广泛应用,工业上常用某矿石(主要成分有Al2O3、Fe2O3、FeO、SiO2等)来制备绿矾(FeSO4•7H2O)和氧化铝,其工艺流程如图:
回答下列问题:
(1)滤渣1的成分是_______ ,举例说明滤渣2的用途 _______ 。
(2)用离子方程式表示溶液A加入过量铁粉的目的是_______ 。
(3)写出由滤液1生成滤液2的离子方程式_______ 。
(4)过程1、2、3均涉及分离操作,所需玻璃仪器有_______ 。
(5)过程3需要加入的试剂A是_______ ,写出此过程的离子方程式 _______ 。

回答下列问题:
(1)滤渣1的成分是
(2)用离子方程式表示溶液A加入过量铁粉的目的是
(3)写出由滤液1生成滤液2的离子方程式
(4)过程1、2、3均涉及分离操作,所需玻璃仪器有
(5)过程3需要加入的试剂A是
您最近一年使用:0次
名校
解题方法
2 . 铝和氟的化合物在制造、化工等领域都有广泛应用。回答下列问题:
(1)基态铝原子的核外电子排布式为___________ ,占据最高能级的电子云轮廓图形状为___________ 。
(2)通常情况下, 可由六氟铝酸铵
可由六氟铝酸铵 受热分解制得,请写出该反应的化学方程式:
受热分解制得,请写出该反应的化学方程式:___________ 。
(3) 具有较高的熔点(1040℃),属于
具有较高的熔点(1040℃),属于___________ (填晶体类型)晶体; 在178℃时升华,写出
在178℃时升华,写出 、
、 晶体类型不同的原因
晶体类型不同的原因___________ (从原子结构与元素性质的角度作答)。
(4) 在水溶液中实际上是以
在水溶液中实际上是以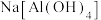 的形式存在。其中
的形式存在。其中 为配离子,Al原子的杂化方式为
为配离子,Al原子的杂化方式为___________ ,该阴离子中存在的化学键有___________ (填字母)。
A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
(5)萤石( )晶体的晶胞如图所示,已知立方体边长为
)晶体的晶胞如图所示,已知立方体边长为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 晶体的密度为
晶体的密度为___________  (列出计算式)。
(列出计算式)。
(1)基态铝原子的核外电子排布式为
(2)通常情况下,
 可由六氟铝酸铵
可由六氟铝酸铵 受热分解制得,请写出该反应的化学方程式:
受热分解制得,请写出该反应的化学方程式:(3)
 具有较高的熔点(1040℃),属于
具有较高的熔点(1040℃),属于 在178℃时升华,写出
在178℃时升华,写出 、
、 晶体类型不同的原因
晶体类型不同的原因(4)
 在水溶液中实际上是以
在水溶液中实际上是以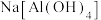 的形式存在。其中
的形式存在。其中 为配离子,Al原子的杂化方式为
为配离子,Al原子的杂化方式为A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
(5)萤石(
 )晶体的晶胞如图所示,已知立方体边长为
)晶体的晶胞如图所示,已知立方体边长为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 晶体的密度为
晶体的密度为 (列出计算式)。
(列出计算式)。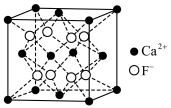
您最近一年使用:0次
2024-03-05更新
|
573次组卷
|
3卷引用:新疆阿克苏市实验中学2022-2023学年高二下学期第三次月考化学试题
名校
3 . A、B、C是三种常见短周期元素的单质,常温下D为无色液体,E是一种常见的温室气体,F是化合物.其转化关系如图(反应条件和部分产物略去)。试回答:

(1)E的结构式是______ 。
(2)单质X和B或D均能反应生成黑色晶体Y,Y的化学式是;______ ;
(3)E的大量排放会引起很多环境问题.有科学家提出,用E和 合成
合成 和
和 ,对E进行综合利用。25℃,101kPa时该反应的热化学方程式是
,对E进行综合利用。25℃,101kPa时该反应的热化学方程式是______ 。
已知
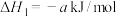
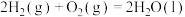
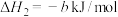
(4)已知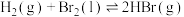
 ;蒸发1mol
;蒸发1mol 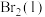 需要吸收的能量为30kJ,其它相关数据如下表。则表中a为
需要吸收的能量为30kJ,其它相关数据如下表。则表中a为______ 。
(5)以NaCl等为原料制备 的过程如下:
的过程如下:
①在无隔膜、微酸性条件下电解,发生反应: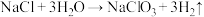 (未配平)。
(未配平)。
②在电解后溶液中加入KCl发生复分解反应,降温结晶,得
③一定条件下反应: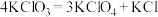 ,将产物分离得到
,将产物分离得到 。
。
该过程制得的 样品中含少量KCl杂质,为测定产品纯度进行如下实验:准确称取m g样品溶于水中,配成250mL溶液,从中取出25.00mL于锥形瓶中,加入适量葡萄糖,加热使
样品中含少量KCl杂质,为测定产品纯度进行如下实验:准确称取m g样品溶于水中,配成250mL溶液,从中取出25.00mL于锥形瓶中,加入适量葡萄糖,加热使 全部转化为
全部转化为 ,反应为:
,反应为: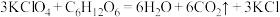 ,加入少量
,加入少量 溶液作指示剂,用
溶液作指示剂,用
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液体积V mL。滴定达到终点时,产生砖红色
溶液体积V mL。滴定达到终点时,产生砖红色 沉淀。计算
沉淀。计算 样品的纯度
样品的纯度______ (用含c、V的代数式表示)。

(1)E的结构式是
(2)单质X和B或D均能反应生成黑色晶体Y,Y的化学式是;
(3)E的大量排放会引起很多环境问题.有科学家提出,用E和
 合成
合成 和
和 ,对E进行综合利用。25℃,101kPa时该反应的热化学方程式是
,对E进行综合利用。25℃,101kPa时该反应的热化学方程式是已知

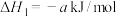
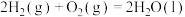
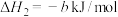
(4)已知
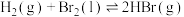
 ;蒸发1mol
;蒸发1mol 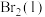 需要吸收的能量为30kJ,其它相关数据如下表。则表中a为
需要吸收的能量为30kJ,其它相关数据如下表。则表中a为物质 |
|
|
|
1mol分子中的化学键断裂时需要吸收的能量(kJ) | 436 | a | 369 |
(5)以NaCl等为原料制备
 的过程如下:
的过程如下:①在无隔膜、微酸性条件下电解,发生反应:
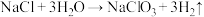 (未配平)。
(未配平)。②在电解后溶液中加入KCl发生复分解反应,降温结晶,得

③一定条件下反应:
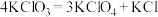 ,将产物分离得到
,将产物分离得到 。
。该过程制得的
 样品中含少量KCl杂质,为测定产品纯度进行如下实验:准确称取m g样品溶于水中,配成250mL溶液,从中取出25.00mL于锥形瓶中,加入适量葡萄糖,加热使
样品中含少量KCl杂质,为测定产品纯度进行如下实验:准确称取m g样品溶于水中,配成250mL溶液,从中取出25.00mL于锥形瓶中,加入适量葡萄糖,加热使 全部转化为
全部转化为 ,反应为:
,反应为: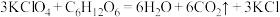 ,加入少量
,加入少量 溶液作指示剂,用
溶液作指示剂,用
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液体积V mL。滴定达到终点时,产生砖红色
溶液体积V mL。滴定达到终点时,产生砖红色 沉淀。计算
沉淀。计算 样品的纯度
样品的纯度
您最近一年使用:0次
2024-01-21更新
|
65次组卷
|
2卷引用:新疆乌鲁木齐市第九中学2023-2024学年高三上学期11月月考化学试题
名校
解题方法
4 . 已知:pKa=-lgKa,25℃时,H2XO3的pKa1=10-1.85,pKa2=10-7.19,常温下,用0.1mol/LNaOH溶液滴定20mL0.1mol/LH2XO3溶液的滴定曲线如图所示下列说法不正确的是
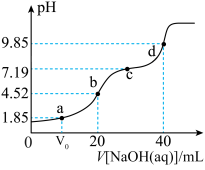

A.a点溶液中:c(H2XO3)=c(HXO ) ) |
B.b点溶液中:c(H2XO3)+c(H+)=c(XO )+c(OH-) )+c(OH-) |
C.c点溶液中:c(Na+)=3c(HXO ) ) |
D.d点溶液中:c(Na+)>c(XO )>c(OH-)>c(HXO )>c(OH-)>c(HXO )>c(H+) )>c(H+) |
您最近一年使用:0次
2023-11-17更新
|
164次组卷
|
2卷引用:新疆奎屯市第一高级中学2023-2024学年高二上学期期中考试化学试题
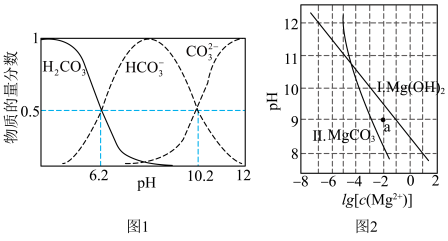
5 . 25℃下,图1表示 溶液中,各含碳粒子的物质的量分数与pH的关系。在图2中,曲线Ⅰ满足关系
溶液中,各含碳粒子的物质的量分数与pH的关系。在图2中,曲线Ⅰ满足关系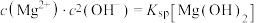 ,曲线Ⅱ满足关系
,曲线Ⅱ满足关系 。[注:起始
。[注:起始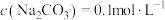 ,不同pH下
,不同pH下 由图1得到]。下列说法不正确的是
由图1得到]。下列说法不正确的是
 溶液中,各含碳粒子的物质的量分数与pH的关系。在图2中,曲线Ⅰ满足关系
溶液中,各含碳粒子的物质的量分数与pH的关系。在图2中,曲线Ⅰ满足关系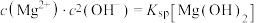 ,曲线Ⅱ满足关系
,曲线Ⅱ满足关系 。[注:起始
。[注:起始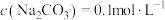 ,不同pH下
,不同pH下 由图1得到]。下列说法不正确的是
由图1得到]。下列说法不正确的是
A.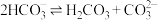 的平衡常数 的平衡常数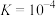 |
B.当一半的 发生水解时,溶液 发生水解时,溶液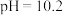 |
C.图2的a点,平衡后的溶液中,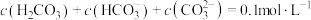 |
D.25℃时,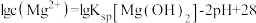 |
您最近一年使用:0次
2023-11-11更新
|
868次组卷
|
4卷引用:新疆维吾尔自治区乌鲁木齐八一中学2023-2024学年高二上学期1月期末化学试题
新疆维吾尔自治区乌鲁木齐八一中学2023-2024学年高二上学期1月期末化学试题浙江省金华市十校2024届高三上学期11月模拟考试化学试题湖北省黄冈市蕲春县实验高级中学2024届高三一轮复习10月月考化学试题(已下线)专题07 水溶液中的离子反应与平衡(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)
6 . 常温下,一种解释乙酰水杨酸(用HA表示, )药物在人体吸收模式如下:
)药物在人体吸收模式如下:

假设离子不会穿过组织薄膜,而未电离的HA则可自由穿过该膜且达到平衡。下列说法错误的是
 )药物在人体吸收模式如下:
)药物在人体吸收模式如下:
假设离子不会穿过组织薄膜,而未电离的HA则可自由穿过该膜且达到平衡。下列说法错误的是
| A.血浆中HA电离程度比胃中大 | B.在胃中,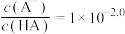 |
C.在血浆中,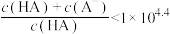 | D.总药量之比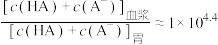 |
您最近一年使用:0次
2023-10-25更新
|
1033次组卷
|
10卷引用:新疆乌鲁木齐八一中学2023-2024学年高二上学期11月期中化学试题
新疆乌鲁木齐八一中学2023-2024学年高二上学期11月期中化学试题湖北省腾云联盟2023-2024学年高三上学期10月联考化学试题湖北省部分高中2024届高三上学期10月联考化学试题辽宁省沈阳市东北育才学校2023-2024学年高二上学期期中考试化学试题【定心卷】3.1.3 电离平衡常数随堂练习-人教版2023-2024学年选择性必修1湖北省襄阳市第六中学2023-2024学年高二上学期10月月考化学试题江西省南昌市第一中学2023-2024学年高二上学期11月期中考试化学试题黑龙江省大庆实验中学实验三部2023-2024学年高三上学期阶段考试(二)化学试题河南省南阳市第一中学校2023-2024学年高二上学期12月月考化学试题四川省攀枝花市2023-2024学年高二上学期普通高中教学质量监测化学试题
名校
解题方法
7 . 向 饱和溶液(有足量
饱和溶液(有足量 固体)中滴加氨水,发生反应
固体)中滴加氨水,发生反应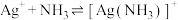 和
和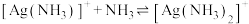 ,
,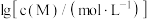 与
与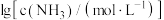 的关系如图所示{其中
的关系如图所示{其中 代表
代表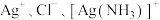 或
或 }。
}。
 饱和溶液(有足量
饱和溶液(有足量 固体)中滴加氨水,发生反应
固体)中滴加氨水,发生反应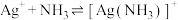 和
和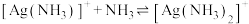 ,
,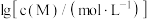 与
与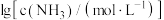 的关系如图所示{其中
的关系如图所示{其中 代表
代表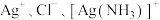 或
或 }。
}。
A.曲线Ⅲ表示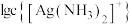 随 随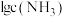 的变化曲线 的变化曲线 |
B.随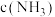 增大, 增大, 先增大后减小 先增大后减小 |
C.反应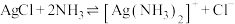 的平衡常数为 的平衡常数为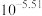 |
D.完全溶解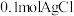 ,至少需要含有 ,至少需要含有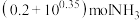 的氨水 的氨水 |
您最近一年使用:0次
2023-10-06更新
|
900次组卷
|
8卷引用:新疆维吾尔自治区塔城地区2024届高三第二次模拟考试理综-化学试题
名校
8 . 帕比司他是治疗某些恶性肿瘤的药物,其中间体E的合成路线如下:
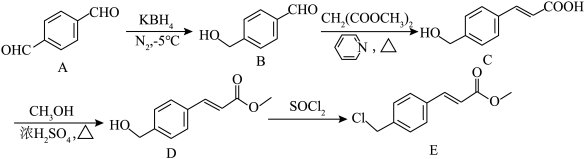
(1)A→B的反应类型为___________ 。
(2)B分子中碳原子的杂化轨道类型为___________ 。
(3)B→C的反应需经历B→M→…→C的过程,中间体M的分子式为C13H16O6,该中间体的结构简式为___________ 。
(4)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:___________ 。
①分子中含有4种不同化学环境的氢原子;②碱性条件水解,酸化后得2种产物,其中一种产物含苯环和2种含氧官能团,且能发生银镜反应。
(5)设计以 和丙二酸二甲酯[CH2(COOCH3)2]为原料制备
和丙二酸二甲酯[CH2(COOCH3)2]为原料制备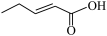 的合成路线流程图(无机试剂和有机溶剂任用,合成路线示例见本题题干)
的合成路线流程图(无机试剂和有机溶剂任用,合成路线示例见本题题干)___________ 。

(1)A→B的反应类型为
(2)B分子中碳原子的杂化轨道类型为
(3)B→C的反应需经历B→M→…→C的过程,中间体M的分子式为C13H16O6,该中间体的结构简式为
(4)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:
①分子中含有4种不同化学环境的氢原子;②碱性条件水解,酸化后得2种产物,其中一种产物含苯环和2种含氧官能团,且能发生银镜反应。
(5)设计以
 和丙二酸二甲酯[CH2(COOCH3)2]为原料制备
和丙二酸二甲酯[CH2(COOCH3)2]为原料制备 的合成路线流程图(无机试剂和有机溶剂任用,合成路线示例见本题题干)
的合成路线流程图(无机试剂和有机溶剂任用,合成路线示例见本题题干)
您最近一年使用:0次
2023-09-09更新
|
206次组卷
|
3卷引用:新疆乌鲁木齐市第六十八中学2023-2024学年高三下学期2月月考化学试题
名校
解题方法
9 . 短周期主族元素 原子序数依次增大,
原子序数依次增大, 为地壳中含量最高的元素,
为地壳中含量最高的元素, 与
与 元素不同周期且
元素不同周期且 原子的核外未成对电子数为1,由
原子的核外未成对电子数为1,由 组成的物质结构式如图所示。下列说法错误的是
组成的物质结构式如图所示。下列说法错误的是
 原子序数依次增大,
原子序数依次增大, 为地壳中含量最高的元素,
为地壳中含量最高的元素, 与
与 元素不同周期且
元素不同周期且 原子的核外未成对电子数为1,由
原子的核外未成对电子数为1,由 组成的物质结构式如图所示。下列说法错误的是
组成的物质结构式如图所示。下列说法错误的是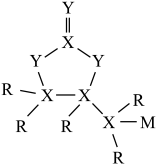
A.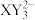 的VSEPR模型名称为平面三角形 的VSEPR模型名称为平面三角形 |
B. 的最高价氧化物对应的水化物为强酸 的最高价氧化物对应的水化物为强酸 |
C.该化合物中 原子最外层均满足 原子最外层均满足 结构 结构 |
D. 元素所在周期中,第一电离能大于 元素所在周期中,第一电离能大于 的元素有2种 的元素有2种 |
您最近一年使用:0次
2023-07-11更新
|
1143次组卷
|
17卷引用:新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高三上学期12月月考化学试卷
新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高三上学期12月月考化学试卷湖南省邵阳市2023届高三下学期第二次联考(二模)化学试题山东省曹县第一中学2022-2023学年高三下学期2月月考化学试题(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(选择题6-10)(已下线)山东省青岛市2023届高三下学期一模化学试题变式题(选择题1-5)河南省焦作市博爱县第一中学2022-2023学年高二下学期6月期末考试化学试题安徽省合肥市合肥第一中学2022-2023学年高二下学期期末考试化学试题湖南省邵阳市邵东市2022-2023学年高三下学期3月月考化学试题河南省焦作市博爱县第一中学2023届高三下学期三模化学试题(已下线)选择题6-10江西省抚州市乐安县第二中学2023-2024学年高三上学期11月期中化学试题(已下线)选择题6-10(已下线)选择题6-102023届山西省太原市第五中学高三下学期5月二模理综试题重庆市万州第二高级中学2023-2024学年高二下学期3月月考化学试题四川省南充市仪陇中学校2023-2024学年高二下学期4月月考化学试题青海省西宁市第十四中学2023-2024学年高二下学期期中化学试卷
10 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:

已知:最高价铬酸根在酸性介质中以Cr2O 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。
存在。
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为___________ (填化学式)。
(2)水浸渣中主要有SiO2和___________ 。
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是___________ 。
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO3和MgNH4PO4的形式沉淀,该步需要控制溶液的pH≈9以达到最好的除杂效果,若pH<9时,会导致___________ ;pH>9时,会导致___________ 。
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到V2O5沉淀,V2O5在pH<1时,溶解为VO 或VO3+在碱性条件下,溶解为VO
或VO3+在碱性条件下,溶解为VO 或VO
或VO ,上述性质说明V2O5具有
,上述性质说明V2O5具有___________ (填标号)。
A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na2S2O5)溶液,反应的离子方程式为___________ 。

已知:最高价铬酸根在酸性介质中以Cr2O
 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。
存在。回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为
(2)水浸渣中主要有SiO2和
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO3和MgNH4PO4的形式沉淀,该步需要控制溶液的pH≈9以达到最好的除杂效果,若pH<9时,会导致
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到V2O5沉淀,V2O5在pH<1时,溶解为VO
 或VO3+在碱性条件下,溶解为VO
或VO3+在碱性条件下,溶解为VO 或VO
或VO ,上述性质说明V2O5具有
,上述性质说明V2O5具有A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na2S2O5)溶液,反应的离子方程式为
您最近一年使用:0次
2023-06-10更新
|
19013次组卷
|
18卷引用:新疆维吾尔自治区阿克苏地区第二中学2023-2024学年高三上学期第二次月考化学试题
新疆维吾尔自治区阿克苏地区第二中学2023-2024学年高三上学期第二次月考化学试题2023年高考新课标理综化学真题(已下线)T26-工业流程题(已下线)2023年高考化学真题完全解读(新课标卷:适用安徽、云南、山西、吉林、黑龙江五省)(PPT+Word)(已下线)专题18 工艺流程题(已下线)2023年高考山东卷化学真题变式题(工业流程题)(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题(已下线)第19练 化学工艺流程题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)四川省绵阳市高中理科突击班2023-2024学年高三上学期第零次诊断性考试理综化学试题(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)四川省遂宁市第二中学校2023-2024学年高三上学期第一次诊断性考试理综试题(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)山东省滨州市2023-2024学年高三上学期11月期中考试化学试题(已下线)题型06 化工微流程-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型16 无机化工流程综合分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型三 工艺流程中的答题规范-备战2024年高考化学答题技巧与模板构建