名校
解题方法
1 .  是主要的大气污染物,必须脱除才能排放。一定条件下,
是主要的大气污染物,必须脱除才能排放。一定条件下, 与
与 反应可转化为无污染物质,某小组在实验室模拟了该过程。
反应可转化为无污染物质,某小组在实验室模拟了该过程。
(1)氨气的制备:___________ 。
②实验室制氨气的化学方程式为___________ 。
③若要制备和收集纯净、干燥的氨气,应该选择如图装置___________ (填序号),其中C中试剂为___________ (填试剂名称)。
(2)氨气与氮氧化物的反应(已知: 。)
。) 中加入少量催化剂,将
中加入少量催化剂,将 和
和 的混合气体注入
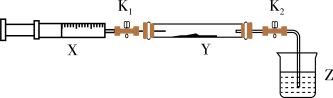
的混合气体注入 管中,关闭
管中,关闭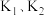 。
。
②打开 ,将注射器
,将注射器 中的
中的 缓慢注入
缓慢注入 中,此时观察到的现象为
中,此时观察到的现象为___________ ,写出其中一个化学反应方程式___________
③待装置恢复到室温,打开 ,同时向
,同时向 中注入适量空气,试分析注入适量空气的原因
中注入适量空气,试分析注入适量空气的原因___________ 。
④若 氨气恰好能将
氨气恰好能将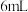 混合气体进行无毒化处理,则混合气体中
混合气体进行无毒化处理,则混合气体中 和
和 的物质的量之比为
的物质的量之比为___________ 。
 是主要的大气污染物,必须脱除才能排放。一定条件下,
是主要的大气污染物,必须脱除才能排放。一定条件下, 与
与 反应可转化为无污染物质,某小组在实验室模拟了该过程。
反应可转化为无污染物质,某小组在实验室模拟了该过程。(1)氨气的制备:
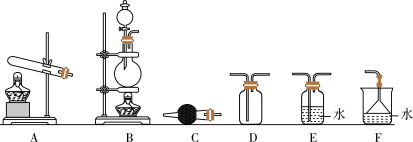
②实验室制氨气的化学方程式为
③若要制备和收集纯净、干燥的氨气,应该选择如图装置
(2)氨气与氮氧化物的反应(已知:
 。)
。)
 中加入少量催化剂,将
中加入少量催化剂,将 和
和 的混合气体注入
的混合气体注入 管中,关闭
管中,关闭 。
。②打开
 ,将注射器
,将注射器 中的
中的 缓慢注入
缓慢注入 中,此时观察到的现象为
中,此时观察到的现象为③待装置恢复到室温,打开
 ,同时向
,同时向 中注入适量空气,试分析注入适量空气的原因
中注入适量空气,试分析注入适量空气的原因④若
 氨气恰好能将
氨气恰好能将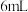 混合气体进行无毒化处理,则混合气体中
混合气体进行无毒化处理,则混合气体中 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
名校
解题方法
2 . 碱性锌锰电池是日常生活中消耗量最大的电池,其构造如图所示。放电时总反应为: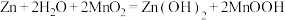 ,从废旧碱性锌锰电池中回收
,从废旧碱性锌锰电池中回收 和
和 的工艺如图:
的工艺如图: 中,
中, 元素的化合价为
元素的化合价为___________ 。
(2)碱性锌锰电池放电时正极的电极反应为___________ 。
(3)“还原焙烧”过程中,高价金属化合物被还原为低价氧化物或金属单质(其中 、
、 被还原成
被还原成 ),能发生这样反应的主要原因是“粉料”中含有
),能发生这样反应的主要原因是“粉料”中含有___________ (填化学式)。
(4)“浸出”后的溶液中含有的金属阳离子有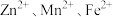 ,写出该过程生成
,写出该过程生成 的离子反应方程式
的离子反应方程式___________ 。
(5) “净化”是为了除去浸出液中的 ,方法为:加入试剂A,再调节
,方法为:加入试剂A,再调节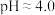 使
使 完全沉淀。则该步骤中试剂A的主要作用为
完全沉淀。则该步骤中试剂A的主要作用为___________ 。
A.作催化剂 B.作还原剂 C.作氧化剂
(6)“电解”时,控制溶液 值,使电解过程不产生任何气体,写出阳极的电极反应式为
值,使电解过程不产生任何气体,写出阳极的电极反应式为___________ ,当电解回收 的质量为
的质量为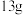 ,理论上能回收
,理论上能回收 的质量为
的质量为___________ 。
(7)本工艺中应循环利用的物质是___________ (填化学式)。
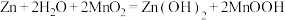 ,从废旧碱性锌锰电池中回收
,从废旧碱性锌锰电池中回收 和
和 的工艺如图:
的工艺如图: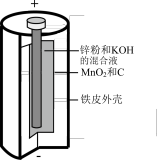
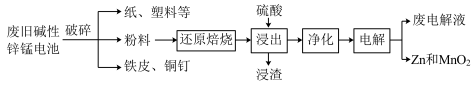
 中,
中, 元素的化合价为
元素的化合价为(2)碱性锌锰电池放电时正极的电极反应为
(3)“还原焙烧”过程中,高价金属化合物被还原为低价氧化物或金属单质(其中
 、
、 被还原成
被还原成 ),能发生这样反应的主要原因是“粉料”中含有
),能发生这样反应的主要原因是“粉料”中含有(4)“浸出”后的溶液中含有的金属阳离子有
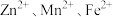 ,写出该过程生成
,写出该过程生成 的离子反应方程式
的离子反应方程式(5) “净化”是为了除去浸出液中的
 ,方法为:加入试剂A,再调节
,方法为:加入试剂A,再调节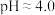 使
使 完全沉淀。则该步骤中试剂A的主要作用为
完全沉淀。则该步骤中试剂A的主要作用为A.作催化剂 B.作还原剂 C.作氧化剂
(6)“电解”时,控制溶液
 值,使电解过程不产生任何气体,写出阳极的电极反应式为
值,使电解过程不产生任何气体,写出阳极的电极反应式为 的质量为
的质量为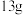 ,理论上能回收
,理论上能回收 的质量为
的质量为(7)本工艺中应循环利用的物质是
您最近一年使用:0次
名校
解题方法
3 . 在一定容积的密闭容器中,进行如下化学反应: ,其化学平衡常数K和温度t的关系如表:
,其化学平衡常数K和温度t的关系如表:
回答下列问题:
(1)该反应的化学平衡常数表达式为
_______ 。
(2)某温度下,各物质的平衡浓度符合关系式: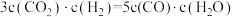 ,试判断此时的温度为
,试判断此时的温度为_______ 。
(3)若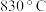 时,向容器中充入
时,向容器中充入 、
、 ,反应达到平衡后,其化学平衡常数K
,反应达到平衡后,其化学平衡常数K_______ 1.0(填“大于”“小于”或“等于”)。
(4)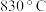 时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的容积,平衡
时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的容积,平衡_______ 移动(填“向正反应方向”“向逆反应方向”或“不”)。
(5)若 时,在某时刻反应体系中
时,在某时刻反应体系中 的浓度分别为
的浓度分别为 ,则此时上述反应
,则此时上述反应_______ (填“向正反应方向进行”“向逆反应方向进行”或“处于平衡状态”)。
(6)甲醇( )燃料电池具有很多优点,引起了人们的研究兴趣,现有以下三种甲醇燃料电池:碱性甲醇燃料电池、酸性甲醇燃料电池、熔融碳酸盐甲醇燃料电池,熔融碳酸盐甲醇燃料电池中正极电极反应式为
)燃料电池具有很多优点,引起了人们的研究兴趣,现有以下三种甲醇燃料电池:碱性甲醇燃料电池、酸性甲醇燃料电池、熔融碳酸盐甲醇燃料电池,熔融碳酸盐甲醇燃料电池中正极电极反应式为_______ ;碱性甲醇燃料电池中,负极的电极反应式为_______ 。
 ,其化学平衡常数K和温度t的关系如表:
,其化学平衡常数K和温度t的关系如表:t/ | 700 | 800 | 830 | 1000 | 12000 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为

(2)某温度下,各物质的平衡浓度符合关系式:
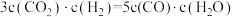 ,试判断此时的温度为
,试判断此时的温度为(3)若
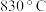 时,向容器中充入
时,向容器中充入 、
、 ,反应达到平衡后,其化学平衡常数K
,反应达到平衡后,其化学平衡常数K(4)
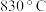 时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的容积,平衡
时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的容积,平衡(5)若
 时,在某时刻反应体系中
时,在某时刻反应体系中 的浓度分别为
的浓度分别为 ,则此时上述反应
,则此时上述反应(6)甲醇(
 )燃料电池具有很多优点,引起了人们的研究兴趣,现有以下三种甲醇燃料电池:碱性甲醇燃料电池、酸性甲醇燃料电池、熔融碳酸盐甲醇燃料电池,熔融碳酸盐甲醇燃料电池中正极电极反应式为
)燃料电池具有很多优点,引起了人们的研究兴趣,现有以下三种甲醇燃料电池:碱性甲醇燃料电池、酸性甲醇燃料电池、熔融碳酸盐甲醇燃料电池,熔融碳酸盐甲醇燃料电池中正极电极反应式为
您最近一年使用:0次
名校
4 . Ⅰ 重庆奉节的脐橙闻名遐迩,从脐橙果皮中提取的橙油具有抗菌抑菌、抗氧化、祛痰平喘等多种作用,常用于医药、食品加工、日化等多个领域。橙油的主要成分是柠檬烯,其结构简式如下。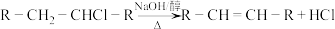 R为烃基或H
R为烃基或H
(1)柠檬烯的分子式______ ,官能团名称______ 。
(2)柠檬烯的一氯代物:______ 种。
(3)写出A→B的化学方程式:______ 。
(4)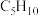 不属于烯烃的同分异构体有
不属于烯烃的同分异构体有______ 种。
(5)E的结构简式:______ 。
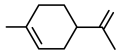
Ⅱ 高分子的循环利用过程如下图所示。______ 。
(7)b与 发生加成反应最多可生成
发生加成反应最多可生成______ 种二溴代物。

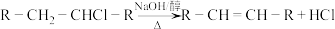 R为烃基或H
R为烃基或H(2)
(1)柠檬烯的分子式
(2)柠檬烯的一氯代物:
(3)写出A→B的化学方程式:
(4)
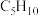 不属于烯烃的同分异构体有
不属于烯烃的同分异构体有(5)E的结构简式:
Ⅱ 高分子的循环利用过程如下图所示。
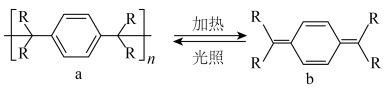 (R为
(R为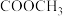 )
)
(7)b与
 发生加成反应最多可生成
发生加成反应最多可生成
您最近一年使用:0次
名校
5 . 肼( )是一种强还原性的高能物质,在航天、能源等领域有广泛应用。
)是一种强还原性的高能物质,在航天、能源等领域有广泛应用。
(1)火箭发射可以用肼(液态)作燃料, 作氧化剂,两者反应生成
作氧化剂,两者反应生成 和水蒸气。
和水蒸气。
已知:
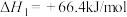
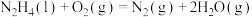
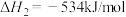
请写出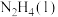 与
与 反应的热化学方程式
反应的热化学方程式______ 。
(2)向恒容密闭容器内加入一定量 ,一定条件下体系中存在以下平衡:
,一定条件下体系中存在以下平衡:
Ⅰ.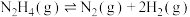
Ⅱ.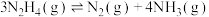
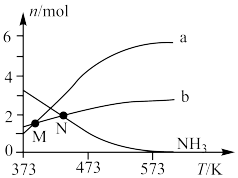
在较高温度肼几乎分解完全,分解产物的物质的量随温度变化如图:______ 。
②在较高温度肼几乎分解完全的原因可能是______ 。
③N点时,体系内 为
为______ 。
(3) 是二元弱碱,
是二元弱碱, 在水溶液中存在如下两步电离:
在水溶液中存在如下两步电离:
①
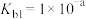 ;
;
②__________________________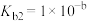 。
。
①写出 在水溶液中的第②步电离方程式:
在水溶液中的第②步电离方程式:______ 。
②25℃时,向 的水溶液中加入稀硫酸,欲使
的水溶液中加入稀硫酸,欲使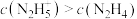 ,同时
,同时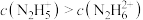 ,应控制溶液的
,应控制溶液的 范围为
范围为______ (用含a、b的式子表示)。
(4)利用 燃料电池电解
燃料电池电解 溶液并制备
溶液并制备 ,装置如图所示(
,装置如图所示(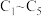 均为石墨电极,假设各装置在工作过程中溶液体积不变)。
均为石墨电极,假设各装置在工作过程中溶液体积不变)。 电极反应式为
电极反应式为______ 。
②若甲装置 电极上消耗标准状况下1.12L的
电极上消耗标准状况下1.12L的 ,理论上丙装置阳极室溶液质量减少
,理论上丙装置阳极室溶液质量减少______ g。
 )是一种强还原性的高能物质,在航天、能源等领域有广泛应用。
)是一种强还原性的高能物质,在航天、能源等领域有广泛应用。(1)火箭发射可以用肼(液态)作燃料,
 作氧化剂,两者反应生成
作氧化剂,两者反应生成 和水蒸气。
和水蒸气。已知:

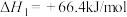
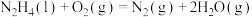
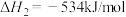
请写出
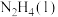 与
与 反应的热化学方程式
反应的热化学方程式(2)向恒容密闭容器内加入一定量
 ,一定条件下体系中存在以下平衡:
,一定条件下体系中存在以下平衡:Ⅰ.
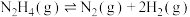
Ⅱ.
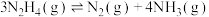
在较高温度肼几乎分解完全,分解产物的物质的量随温度变化如图:
②在较高温度肼几乎分解完全的原因可能是
③N点时,体系内
 为
为(3)
 是二元弱碱,
是二元弱碱, 在水溶液中存在如下两步电离:
在水溶液中存在如下两步电离:①

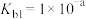 ;
;②__________________________
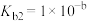 。
。①写出
 在水溶液中的第②步电离方程式:
在水溶液中的第②步电离方程式:②25℃时,向
 的水溶液中加入稀硫酸,欲使
的水溶液中加入稀硫酸,欲使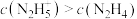 ,同时
,同时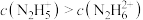 ,应控制溶液的
,应控制溶液的 范围为
范围为(4)利用
 燃料电池电解
燃料电池电解 溶液并制备
溶液并制备 ,装置如图所示(
,装置如图所示(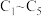 均为石墨电极,假设各装置在工作过程中溶液体积不变)。
均为石墨电极,假设各装置在工作过程中溶液体积不变)。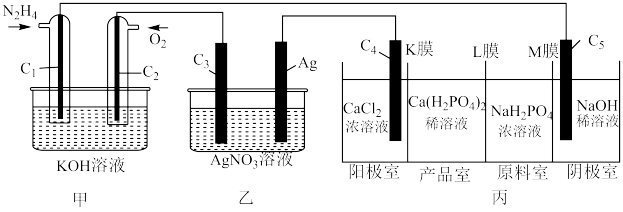
 电极反应式为
电极反应式为②若甲装置
 电极上消耗标准状况下1.12L的
电极上消耗标准状况下1.12L的 ,理论上丙装置阳极室溶液质量减少
,理论上丙装置阳极室溶液质量减少
您最近一年使用:0次
名校
6 . 下列事实的解释不正确 的是
事实 | 解释 | |
A | 气态 再失去一个电子比气态 再失去一个电子比气态 再失去一个电子更难 再失去一个电子更难 |  的价层电子排布为 的价层电子排布为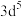 ,3d轨道为半充满比较稳定; ,3d轨道为半充满比较稳定; 的价层电子排布为 的价层电子排布为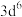 ,再失去一个电子可达到3d轨道半充满的比较稳定状态 ,再失去一个电子可达到3d轨道半充满的比较稳定状态 |
B | 晶体中每个分子紧邻的分子数:干冰晶体(12个)>冰(4个) | 冰中水分子间主要以氢键结合,干冰晶体中二氧化碳分子间主要以范德华力结合 |
C | 分子的极性: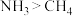 |  键的极性大于 键的极性大于 键的极性 键的极性 |
D | 酸性: | 氟的电负性大于氯的电负性,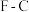 的极性大于 的极性大于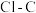 的极性,使 的极性,使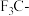 的极性大于 的极性大于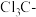 的极性,导致 的极性,导致 的羧基中的羟基的极性更大,更易电离出 的羧基中的羟基的极性更大,更易电离出 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 一种新型漂白剂(见下图)可用于漂白羊毛等,其中W、Y、Z为不同周期不同主族的短周期元素,Y的最外层p能级上只有一个单电子,X是地壳中含量最多的元素。W、Y、Z的最外层电子数之和等于X的最外层电子数,W、X对应的简单离子核外电子排布相同。下列叙述不正确的是
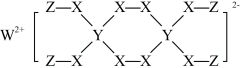
A.该化合物中每个原子都达到 稳定结构 稳定结构 |
B.原子序数: ,对应的简单离子半径顺序: ,对应的简单离子半径顺序: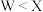 |
| C.基态Y原子中有3种能量不同的电子,这些电子的运动状态共5种 |
D.电负性: |
您最近一年使用:0次
名校
8 . 有机物数量众多,不仅构成了生机勃勃的生命世界,也是燃料、材料、食品和药物的主要来源。请按要求回答下列问题:
(1)相对分子质量为114,其一氯代物只有一种的链状烷烃的结构简式为___________ ,该物质的名称为___________ 。
(2)一种有机物X的键线式如图所示___________ ;
②有机物Y是X的同分异构体,且属于芳香族化合物,Y在一定条件下可发生反应生成高分子化合物,该反应的化学方程式为___________ 。
(3) 中官能团名称为
中官能团名称为___________ ,其同分异构体中,满足下列条件(①属于酚类;②含有2个甲基,且连在同一个碳原子上)的结构有___________ 种;其中,核磁共振氢谱有四组峰,且峰面积之比为6:2:2:1的结构简式为___________ 。
(4)已知烯烃能发生如下的反应: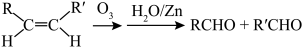 ,请写出下列反应产物的结构简式:
,请写出下列反应产物的结构简式:
___________ 。
(1)相对分子质量为114,其一氯代物只有一种的链状烷烃的结构简式为
(2)一种有机物X的键线式如图所示
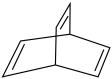
②有机物Y是X的同分异构体,且属于芳香族化合物,Y在一定条件下可发生反应生成高分子化合物,该反应的化学方程式为
(3)
 中官能团名称为
中官能团名称为(4)已知烯烃能发生如下的反应:
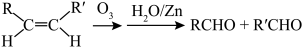 ,请写出下列反应产物的结构简式:
,请写出下列反应产物的结构简式:
您最近一年使用:0次
名校
9 . 中学教材对Cu与 的反应进行了讲解,但深入研究时用到了控制变量法(即有多个变量时,应该控制其他变量不变,只允许一个变量发生变化的研究方法),设计了如下的实验装置,并探讨了一些值得思考的问题.
的反应进行了讲解,但深入研究时用到了控制变量法(即有多个变量时,应该控制其他变量不变,只允许一个变量发生变化的研究方法),设计了如下的实验装置,并探讨了一些值得思考的问题.
Ⅰ.利用如图装置完成Cu与 制取氮氧化物的反应.实验过程中可观察到装置B中液面上方为无色气体,C中液面上方为红棕色气体.
制取氮氧化物的反应.实验过程中可观察到装置B中液面上方为无色气体,C中液面上方为红棕色气体.___________ ;
(2)用化学方程式解释C中液面上方为红棕色气体的原理___________ ;
(3)将分液漏斗中液体换为稀硫酸和硝酸钠混合液也出现了溶解现象。此时烧瓶中发生反应的离子方程式为___________ ;
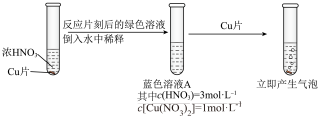
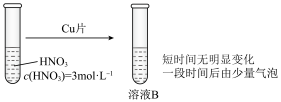
Ⅱ.深入研究时,有同学观察到了以下现象:实验1中蓝色溶液A遇铜片立即产生气泡;而相同条件下实验2中3mol/L硝酸遇铜片短时间内无明显变化,一段时间后才有少量气泡产生。实验操作如下:
分析蓝色溶液A的成分后,学习小组探究蓝色溶液A与铜片能够立即发生反应的原因。
实验验证:
(4)将少量硫酸铜固体加入到 硝酸中,溶液呈蓝色,放入铜片,无明显变化。该同学这样做是为了验证
硝酸中,溶液呈蓝色,放入铜片,无明显变化。该同学这样做是为了验证___________ (填化学式)对该反应是否有催化作用。该同学这样做不能得出该物质不是催化剂的正确结论,还应该考虑___________ 和___________ 的影响;
(5)某同学又提出可能是 对该反应有催化作用。为了得出该结论,应该补充的实验为
对该反应有催化作用。为了得出该结论,应该补充的实验为___________ (写实验操作及现象)。
 的反应进行了讲解,但深入研究时用到了控制变量法(即有多个变量时,应该控制其他变量不变,只允许一个变量发生变化的研究方法),设计了如下的实验装置,并探讨了一些值得思考的问题.
的反应进行了讲解,但深入研究时用到了控制变量法(即有多个变量时,应该控制其他变量不变,只允许一个变量发生变化的研究方法),设计了如下的实验装置,并探讨了一些值得思考的问题.Ⅰ.利用如图装置完成Cu与
 制取氮氧化物的反应.实验过程中可观察到装置B中液面上方为无色气体,C中液面上方为红棕色气体.
制取氮氧化物的反应.实验过程中可观察到装置B中液面上方为无色气体,C中液面上方为红棕色气体.
(2)用化学方程式解释C中液面上方为红棕色气体的原理
(3)将分液漏斗中液体换为稀硫酸和硝酸钠混合液也出现了溶解现象。此时烧瓶中发生反应的离子方程式为
Ⅱ.深入研究时,有同学观察到了以下现象:实验1中蓝色溶液A遇铜片立即产生气泡;而相同条件下实验2中3mol/L硝酸遇铜片短时间内无明显变化,一段时间后才有少量气泡产生。实验操作如下:
| 实验1 |
|
| 实验2 |
|
实验验证:
(4)将少量硫酸铜固体加入到
 硝酸中,溶液呈蓝色,放入铜片,无明显变化。该同学这样做是为了验证
硝酸中,溶液呈蓝色,放入铜片,无明显变化。该同学这样做是为了验证(5)某同学又提出可能是
 对该反应有催化作用。为了得出该结论,应该补充的实验为
对该反应有催化作用。为了得出该结论,应该补充的实验为
您最近一年使用:0次
名校
10 . 将7.6g铜和铁的混合物投入200mL稀硝酸中,充分反应后得到标准状况下1.12LNO,有部分金属未溶解;继续加入400mL等浓度的稀硝酸,金属完全溶解,并得到标准状况下1.12LNO,此时溶液中不含 ,则下列说法正确的是
,则下列说法正确的是
 ,则下列说法正确的是
,则下列说法正确的是| A.原混合物中铜和铁的物质的量之比为1:1 |
B.稀硝酸的物质的量浓度为 |
| C.第一次剩余的金属重量为4.8g |
| D.向反应后的溶液中加入铁粉,最多可以溶解9.8g |
您最近一年使用:0次