1 . 下列物质一定互为同系物的是
| A.C5H10和CH2=CHCH3 | B.2-甲基丁烷和CH3CH2CH2CH2CH3 |
C.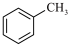 和 和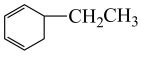 | D.C7H16和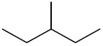 |
您最近一年使用:0次
名校
解题方法
2 . 利用化学反应原理分析指导工业生产具有重要的现实意义,回答下列问题。___________ 。
(2)合成氨的反应,T1℃时在容积为2L的恒容密闭容器中通入2molN2和5molH2发生反应。5min时反应达到平衡状态,达平衡时N2(g)的转化率为50%,求:
①0~5min内该反应的平均速率v(H2)=___________ mol/(L•min);平衡常数K=___________ 。___________ (填序号)。
a.升高温度 b.将平衡体系中的NH3(g)分离出来
c.减小容器的体积增大体系压强 d.加入合适的催化剂
(3)泡沫灭火器中通常装有NaHCO3溶液和Al2(SO4)3溶液,请写出这两种溶液混合时的离子反应方程式___________ 。
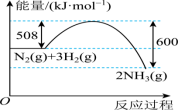
(2)合成氨的反应,T1℃时在容积为2L的恒容密闭容器中通入2molN2和5molH2发生反应。5min时反应达到平衡状态,达平衡时N2(g)的转化率为50%,求:
①0~5min内该反应的平均速率v(H2)=
②相同条件下,改变反应物的起始通入量,某时刻测得N2、H2、NH3的物质的量分别为2mol、4mol、2mol,则此时反应达到平衡状态 ),v正
),v正
a.升高温度 b.将平衡体系中的NH3(g)分离出来
c.减小容器的体积增大体系压强 d.加入合适的催化剂
(3)泡沫灭火器中通常装有NaHCO3溶液和Al2(SO4)3溶液,请写出这两种溶液混合时的离子反应方程式
您最近一年使用:0次
名校
3 . I、按要求写出下列方程式:
(1)FeCl3水解的离子方程式:___________ 。
(2)NaHCO3水解的离子方程式:___________ 。
(3)NH3•H2O的电离方程式:___________ 。
(4)Mg(OH)2在水中的沉淀溶解平衡用离子方程式表示:___________ 。
Ⅱ、回答下列问题。
(5)25℃时,0.01mol/L的NaOH溶液的pH=___________ ;由水电离出c(H+)=___________ mol/L。
(6)25℃时,将10mLpH=2醋酸溶液稀释到1000mL后溶液的pH___________ 4(填“大于”“小于”或“等于”)。
(7)某温度时,Ksp[AgI]=9.0×10-16,求AgI饱和溶液中c(Ag+)=___________ mol/L
(1)FeCl3水解的离子方程式:
(2)NaHCO3水解的离子方程式:
(3)NH3•H2O的电离方程式:
(4)Mg(OH)2在水中的沉淀溶解平衡用离子方程式表示:
Ⅱ、回答下列问题。
(5)25℃时,0.01mol/L的NaOH溶液的pH=
(6)25℃时,将10mLpH=2醋酸溶液稀释到1000mL后溶液的pH
(7)某温度时,Ksp[AgI]=9.0×10-16,求AgI饱和溶液中c(Ag+)=
您最近一年使用:0次
4 . 在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是___________ (用字母表示,下同)。
(2)同体积、同物质的量浓度的三种酸,中和NaOH 的能力由大到小的顺序是___________ 。
(3)若三者pH相同时,物质的量浓度由大到小的顺序是___________ 。
(4)将pH相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液的体积大小关系为___________ 。
(5)将pH相同的三种酸均加水稀释至原来的100倍后,pH由大到小的顺序是___________ 。
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是
(2)同体积、同物质的量浓度的三种酸,中和NaOH 的能力由大到小的顺序是
(3)若三者pH相同时,物质的量浓度由大到小的顺序是
(4)将pH相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液的体积大小关系为
(5)将pH相同的三种酸均加水稀释至原来的100倍后,pH由大到小的顺序是
您最近一年使用:0次
名校
解题方法
5 . 下列关于胶体的叙述错误的是
| A.病毒蛋白质分子的直径约为80 nm,在空气中可以形成气溶胶 |
| B.胶体和溶液的分散质均能透过滤纸 |
| C.纳米材料粒子直径在1~100 nm,因此纳米材料属于胶体 |
| D.自然界中云、雾、烟都是胶体 |
您最近一年使用:0次
2024-05-11更新
|
176次组卷
|
2卷引用:湖北省武汉西藏中学2023-2024学年高一下学期5月期中考试化学试题
6 . 下列分散系中分散质直径最小的是
| A.氢氧化铁悬浊液 | B.氢氧化铝胶体 |
| C.淀粉溶液 | D.硫酸铜溶液 |
您最近一年使用:0次
7 . 黑火药是中国古代四大发明之一,其爆炸反应为2KNO3+S+3C=K2S+N2↑+3CO2↑。下列说法正确的是
| A.黑火药中含有两种单质 | B.反应中C作为氧化剂 |
| C.反应中S作还原剂 | D.反应为置换反应 |
您最近一年使用:0次
8 . 下列各组离子在指定溶液中能大量共存的是
A.食盐水中:Fe2+、 、Cl-、 、Cl-、 | B.氯化铁溶液中:Mg2+、K+、Cl-、OH-- |
C.苏打溶液(Na2CO3)中:Ca2+、Al3+、Cl-、 | D.白醋中:K+、Na+、 、 、 |
您最近一年使用:0次
解题方法
9 . 在氧气中燃烧0.22g硫和铁组成的混合物,使其中的硫全部转化为二氧化硫,把这些二氧化硫全部氧化成三氧化硫并转变为硫酸,这些硫酸可用10mL 氢氧化钠溶液完全中和,则原混合物中硫的百分含量为
氢氧化钠溶液完全中和,则原混合物中硫的百分含量为______ ?
 氢氧化钠溶液完全中和,则原混合物中硫的百分含量为
氢氧化钠溶液完全中和,则原混合物中硫的百分含量为
您最近一年使用:0次
解题方法
10 . 从1L NaOH溶液取出100mL,若将取出的这100mL NaOH溶液加水稀释至500mL,所得溶液中溶质的物质的量浓度是
NaOH溶液取出100mL,若将取出的这100mL NaOH溶液加水稀释至500mL,所得溶液中溶质的物质的量浓度是______  ?含NaOH的质量
?含NaOH的质量______ 克?
 NaOH溶液取出100mL,若将取出的这100mL NaOH溶液加水稀释至500mL,所得溶液中溶质的物质的量浓度是
NaOH溶液取出100mL,若将取出的这100mL NaOH溶液加水稀释至500mL,所得溶液中溶质的物质的量浓度是 ?含NaOH的质量
?含NaOH的质量
您最近一年使用:0次



