名校
1 . 化学贯穿古今,下列对古诗词所涉及化学知识的解读不正确的是
| A.“错把陈醋当成墨,写尽半生纸上酸”,陈醋是混合物 |
| B.“熬胆矾铁斧,久之亦化为铜”,其中铜能导电,所以铜是电解质 |
| C.“墨滴无声入水惊,如烟袅袅幻形生”中的“墨滴”能产生丁达尔效应 |
| D.“松叶堪为酒,春来酿几多”,清香的美酒在酿制过程中发生的变化涉及电子转移 |
您最近一年使用:0次
2 . 已知反应: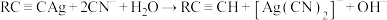 ,该反应可用于提纯炔烃。下列说法错误的是
,该反应可用于提纯炔烃。下列说法错误的是
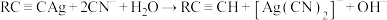 ,该反应可用于提纯炔烃。下列说法错误的是
,该反应可用于提纯炔烃。下列说法错误的是A. 的电子式为 的电子式为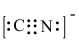 |
B.基态O原子的价电子排布图为 |
C. 的空间填充模型为 的空间填充模型为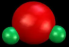 |
D.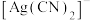 中 中 键与 键与 键的个数比为1:2 键的个数比为1:2 |
您最近一年使用:0次
2024-06-16更新
|
318次组卷
|
7卷引用:江西省吉安市第一中学2023-2024学年高三上学期11月期中考试化学试题
名校
解题方法
3 . 一种制备 的工艺路线如图所示,反应
的工艺路线如图所示,反应 所得溶液pH在3~4之间,反应
所得溶液pH在3~4之间,反应 需及时补加
需及时补加 以保持反应在
以保持反应在 条件下进行。常温下,
条件下进行。常温下, 的电离平衡常数
的电离平衡常数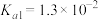 ,
,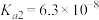 。下列说法正确的是
。下列说法正确的是
 的工艺路线如图所示,反应
的工艺路线如图所示,反应 所得溶液pH在3~4之间,反应
所得溶液pH在3~4之间,反应 需及时补加
需及时补加 以保持反应在
以保持反应在 条件下进行。常温下,
条件下进行。常温下, 的电离平衡常数
的电离平衡常数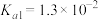 ,
,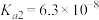 。下列说法正确的是
。下列说法正确的是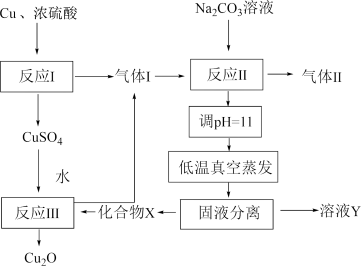
A.反应 、 、 、 、 均为氧化还原反应 均为氧化还原反应 |
B.低温真空蒸发主要目的是防止 被氧化 被氧化 |
C.溶液Y可循环用于反应 所在操作单元吸收气体 所在操作单元吸收气体 |
D.若 产量不变,参与反应 产量不变,参与反应 的X与 的X与 物质的量之比 物质的量之比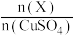 增大时,需补加 增大时,需补加 的量增多 的量增多 |
您最近一年使用:0次
2024-06-10更新
|
103次组卷
|
4卷引用:湖南师大附中2023-2024学年高二下学期期中考试化学试题
4 . 在溶液中能与 反应产生气泡的离子是
反应产生气泡的离子是
 反应产生气泡的离子是
反应产生气泡的离子是| A.K+ | B.Ca2+ | C.H+ | D.Na+ |
您最近一年使用:0次
5 . 回答下列问题
(1)0.5molCO2的质量是___________ g;分子数为___________ 。在标准状况下,体积为___________ 。
(2)0.5molNa2SO4含有___________ molSO ,含
,含___________ molO,含___________ 个O,Na2SO4摩尔质量为___________ 。
(1)0.5molCO2的质量是
(2)0.5molNa2SO4含有
 ,含
,含
您最近一年使用:0次
6 . “84”消毒液是常用的消毒用品,由Cl2与NaOH溶液制得,其有效成分次氯酸钠(NaClO)中氯元素化合价为
| A.-1 | B.+1 | C.+3 | D.+5 |
您最近一年使用:0次
名校
解题方法
7 . 标准状况下,1.5mol 的体积为
的体积为
 的体积为
的体积为| A.11.2L | B.22.4L | C.33.6L | D.67.2L |
您最近一年使用:0次
2024-05-22更新
|
79次组卷
|
5卷引用:广西桂林市第十八中学2019-2020学年高二上学期期中考试化学(文)试题
广西桂林市第十八中学2019-2020学年高二上学期期中考试化学(文)试题贵州省长顺文博高级中学2020-2021学年高二上学期期中考试化学试题湖南省普通高中2024届高三学业水平合格性考试模拟试卷(二)化学试题(已下线)山东省青岛市2023-2024学年高三下学期第三次模拟考试化学试题(已下线)江苏省南京市第十三中学2024届高三下学期适应性考试化学试题
名校
8 . 回答下列问题:
(1)在 和
和 溶液中存在如下平衡:
溶液中存在如下平衡: (黄色)
(黄色) (无色)
(无色)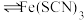 (红色)。将上述溶液均分置于两支试管中;向其中一支试管中加入饱和
(红色)。将上述溶液均分置于两支试管中;向其中一支试管中加入饱和 溶液,溶液颜色变
溶液,溶液颜色变___________ (填“深”或“浅”);向另一支试管中滴加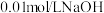 溶液,平衡向
溶液,平衡向___________ (填“正”或“逆”)方向移动。
(2)已知: (
( ,橙色)
,橙色) (
( ,黄色)
,黄色)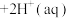
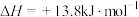 某同学利用以上可逆反应研究浓度对化学平衡的影响,现象如下:
某同学利用以上可逆反应研究浓度对化学平衡的影响,现象如下: 中颜色不变后与试管
中颜色不变后与试管 比较,溶液颜色变浅;②快速滴入浓硫酸,试管
比较,溶液颜色变浅;②快速滴入浓硫酸,试管 温度略有升高,溶液颜色与试管
温度略有升高,溶液颜色与试管 相比溶液颜色变深。下列说法正确的是___________。
相比溶液颜色变深。下列说法正确的是___________。
(3)某同学进行了硫代硫酸钠与硫酸反应的有关实验,实验过程的数据记录如表(见表格),请结合表中信息,回答有关问题:
已知:该反应的化学方程式:
①写出上述反应的离子方程式___________ 。
②根据你所掌握的知识判断,在上述实验中,反应速率最快的可能是___________ (填实验序号)。
③在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件,其中:1和2、1和3的组合比较,所研究的问题是___________ 。找出哪种组合是温度对化学反应速率的影响___________ 。
④教材中利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用排水法测量单位时间内气体体积的大小进行比较:___________ 。
(1)在
 和
和 溶液中存在如下平衡:
溶液中存在如下平衡: (黄色)
(黄色) (无色)
(无色)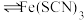 (红色)。将上述溶液均分置于两支试管中;向其中一支试管中加入饱和
(红色)。将上述溶液均分置于两支试管中;向其中一支试管中加入饱和 溶液,溶液颜色变
溶液,溶液颜色变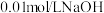 溶液,平衡向
溶液,平衡向(2)已知:
 (
( ,橙色)
,橙色) (
( ,黄色)
,黄色)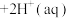
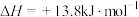 某同学利用以上可逆反应研究浓度对化学平衡的影响,现象如下:
某同学利用以上可逆反应研究浓度对化学平衡的影响,现象如下: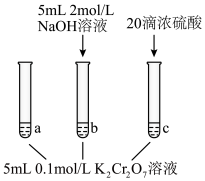
 中颜色不变后与试管
中颜色不变后与试管 比较,溶液颜色变浅;②快速滴入浓硫酸,试管
比较,溶液颜色变浅;②快速滴入浓硫酸,试管 温度略有升高,溶液颜色与试管
温度略有升高,溶液颜色与试管 相比溶液颜色变深。下列说法正确的是___________。
相比溶液颜色变深。下列说法正确的是___________。| A.该反应为氧化还原反应 |
B.待试管 中溶液颜色不变的目的是使 中溶液颜色不变的目的是使 完全反应 完全反应 |
C.试管 中的现象说明影响平衡的主要因素是温度 中的现象说明影响平衡的主要因素是温度 |
| D.该实验不能证明减小生成物浓度,平衡正向移动 |
(3)某同学进行了硫代硫酸钠与硫酸反应的有关实验,实验过程的数据记录如表(见表格),请结合表中信息,回答有关问题:
| 实验编号 | 实验温度 | 参加反应的物质 | ||||
 |  |  | ||||
 |  |  |  |  | ||
| 1 | 20 | 10 | 0.1 | 10 | 0.1 | 0 |
| 2 | 20 | 5 | 0.1 | 10 | 0.1 | 5 |
| 3 | 20 | 10 | 0.1 | 5 | 0.1 | 5 |
| 4 | 40 | 5 | 0.1 | 10 | 0.1 | 5 |

①写出上述反应的离子方程式
②根据你所掌握的知识判断,在上述实验中,反应速率最快的可能是
③在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件,其中:1和2、1和3的组合比较,所研究的问题是
④教材中利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用排水法测量单位时间内气体体积的大小进行比较:
您最近一年使用:0次
9 . 某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂。请填写下列空白:
(1)某学生的操作步骤如下:
A.移取20.00mL待测溶液注入洁净的锥形瓶中,并加入2~3滴酚酞试液。
B.用标准溶液润洗滴定管2~3次。
C.调节滴定管旋塞使尖嘴充满溶液,把盛有标准溶液的酸式滴定管固定好。
D.取标准盐酸溶液注入酸式滴定管至零刻度以上2~3cm。
E.调节液面至零刻度(或以下),记下读数V1。
F.用标准溶液滴定至终点,记下滴定管液面的刻度V2。
请写出操作步骤的正确顺序___________ 。
→___________→___________→___________→A→F。
(2)滴定终点的判断方法:___________ 。
(3)滴定结束时,酸式滴定管中的液面如图所示,则读数为___________ mL。
(5)某学生根据三次实验分别记录有关数据如表:
请选用其中合理数据求出该氢氧化钠溶液物质的量浓度:c(NaOH)=___________ mol/L。(计算结果保留4位有效数字)
(6)由于错误操作,使得上述所测氢氧化钠溶液的浓度偏高的是___________(填字母)。
(1)某学生的操作步骤如下:
A.移取20.00mL待测溶液注入洁净的锥形瓶中,并加入2~3滴酚酞试液。
B.用标准溶液润洗滴定管2~3次。
C.调节滴定管旋塞使尖嘴充满溶液,把盛有标准溶液的酸式滴定管固定好。
D.取标准盐酸溶液注入酸式滴定管至零刻度以上2~3cm。
E.调节液面至零刻度(或以下),记下读数V1。
F.用标准溶液滴定至终点,记下滴定管液面的刻度V2。
请写出操作步骤的正确顺序
→___________→___________→___________→A→F。
(2)滴定终点的判断方法:
(3)滴定结束时,酸式滴定管中的液面如图所示,则读数为

A. | B. | C. | D. |
(5)某学生根据三次实验分别记录有关数据如表:
| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol•L-1盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积 | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
(6)由于错误操作,使得上述所测氢氧化钠溶液的浓度偏高的是___________(填字母)。
| A.中和滴定到达终点时俯视滴定管内液面读数 |
| B.碱式滴定管用蒸馏水洗净后立即取用25.00mL待测碱溶液注入锥形瓶进行滴定 |
| C.酸式滴定管用蒸馏水洗净后立即装标准溶液来滴定 |
| D.锥形瓶用待测液润洗 |
您最近一年使用:0次
10 . 下列物质一定互为同系物的是
| A.C5H10和CH2=CHCH3 | B.2-甲基丁烷和CH3CH2CH2CH2CH3 |
C.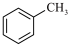 和 和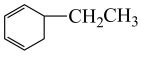 | D.C7H16和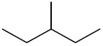 |
您最近一年使用:0次



