名校
1 . 按要求填写下列空白:
(1) 个
个 的质量为
的质量为___________ g。
(2)标况下, 的摩尔质量为
的摩尔质量为___________ ,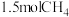 质量为
质量为___________ 。
(3)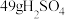 含有
含有___________ 个氢原子,共含有___________ 个原子。
(4)已知标准状况下 的密度为
的密度为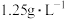 ,X原子最外层有
,X原子最外层有___________ 个电子。
(5)现有下列物质:① 晶体,②石墨,③无水乙醇,④小苏打,⑤熔融
晶体,②石墨,③无水乙醇,④小苏打,⑤熔融 ,⑥醋(乙)酸,⑦液氨,⑧稀硫酸,⑨
,⑥醋(乙)酸,⑦液氨,⑧稀硫酸,⑨ 固体,⑩
固体,⑩ 红褐色胶体其中属于电解质的是:
红褐色胶体其中属于电解质的是:___________ ,能导电的物质是:___________ 。(填序号)
(1)
 个
个 的质量为
的质量为(2)标况下,
 的摩尔质量为
的摩尔质量为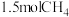 质量为
质量为(3)
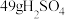 含有
含有(4)已知标准状况下
 的密度为
的密度为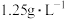 ,X原子最外层有
,X原子最外层有(5)现有下列物质:①
 晶体,②石墨,③无水乙醇,④小苏打,⑤熔融
晶体,②石墨,③无水乙醇,④小苏打,⑤熔融 ,⑥醋(乙)酸,⑦液氨,⑧稀硫酸,⑨
,⑥醋(乙)酸,⑦液氨,⑧稀硫酸,⑨ 固体,⑩
固体,⑩ 红褐色胶体其中属于电解质的是:
红褐色胶体其中属于电解质的是:
您最近一年使用:0次
2 . 请回答下列问题:
(1)已知实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为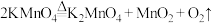 ,氧化产物是
,氧化产物是___________ (填化学式)。
(2)查阅资料可知,铜和浓 共热,发生反应
共热,发生反应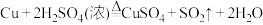 ,该反应中还原剂与氧化剂的物质的量之比为
,该反应中还原剂与氧化剂的物质的量之比为___________ ,其中 在反应中表现的性质为
在反应中表现的性质为___________ 。
(3)已知反应
① ;
;
②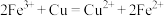 ;
;
③ ;
;
④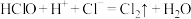 。
。
微粒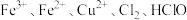 氧化性由强到弱的顺序为
氧化性由强到弱的顺序为___________
(4)请配平下列反应方程式:___________
___________ ___________
___________ (浓)=___________
(浓)=___________ ___________
___________ ___________
___________ ___________
___________
若反应中发生氧化反应的 物质的量为
物质的量为 ,则反应中转移的电子数为
,则反应中转移的电子数为___________ 。
(1)已知实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为
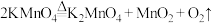 ,氧化产物是
,氧化产物是(2)查阅资料可知,铜和浓
 共热,发生反应
共热,发生反应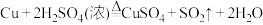 ,该反应中还原剂与氧化剂的物质的量之比为
,该反应中还原剂与氧化剂的物质的量之比为 在反应中表现的性质为
在反应中表现的性质为(3)已知反应
①
 ;
;②
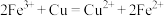 ;
;③
 ;
;④
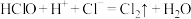 。
。微粒
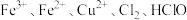 氧化性由强到弱的顺序为
氧化性由强到弱的顺序为(4)请配平下列反应方程式:
___________
 ___________
___________ (浓)=___________
(浓)=___________ ___________
___________ ___________
___________ ___________
___________
若反应中发生氧化反应的
 物质的量为
物质的量为 ,则反应中转移的电子数为
,则反应中转移的电子数为
您最近一年使用:0次
3 . Ⅰ、把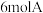 气体和
气体和 气体混合放入
气体混合放入 密闭容器中,在一定条件下发生反应:
密闭容器中,在一定条件下发生反应: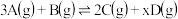 ,经
,经 达到平衡,此时生成
达到平衡,此时生成 为
为 ,测定
,测定 的平均反应速率为
的平均反应速率为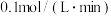 ,计算:
,计算:
(1)B的转化率___________ ,
(2)恒温达平衡时容器内的压强与开始时压强比___________ 。
Ⅱ、将等物质的量的 、
、 混合于
混合于 的密闭容器中,发生如下反应:
的密闭容器中,发生如下反应: ,经
,经 后,测得
后,测得 的浓度为
的浓度为 的平均反应速率为
的平均反应速率为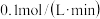 。求:
。求:
(3)此时 的浓度
的浓度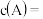
___________  ,
,
(4)B的平均反应速率: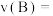
___________ 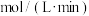 ,
,
(5)x的值为___________ 。
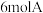 气体和
气体和 气体混合放入
气体混合放入 密闭容器中,在一定条件下发生反应:
密闭容器中,在一定条件下发生反应: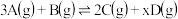 ,经
,经 达到平衡,此时生成
达到平衡,此时生成 为
为 ,测定
,测定 的平均反应速率为
的平均反应速率为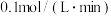 ,计算:
,计算:(1)B的转化率
(2)恒温达平衡时容器内的压强与开始时压强比
Ⅱ、将等物质的量的
 、
、 混合于
混合于 的密闭容器中,发生如下反应:
的密闭容器中,发生如下反应: ,经
,经 后,测得
后,测得 的浓度为
的浓度为 的平均反应速率为
的平均反应速率为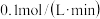 。求:
。求:(3)此时
 的浓度
的浓度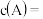
 ,
,(4)B的平均反应速率:
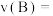
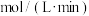 ,
,(5)x的值为
您最近一年使用:0次
2022-09-27更新
|
627次组卷
|
4卷引用:湖北省襄阳市第三中学2021-2022学年高一下学期期中考试化学试题
4 . 回答下列问题:
(1)一定量的乙醇和O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g)。产物分别经过浓硫酸和碱石灰,浓硫酸增重10.8g,碱石灰增重13.2g。求乙醇和氧气物质的量分别是_______ 、_______ 。
(2)若将0.5mol乙醇与9.2g金属钠充分反应,则标况下生成气体的体积是_______ 。
(1)一定量的乙醇和O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g)。产物分别经过浓硫酸和碱石灰,浓硫酸增重10.8g,碱石灰增重13.2g。求乙醇和氧气物质的量分别是
(2)若将0.5mol乙醇与9.2g金属钠充分反应,则标况下生成气体的体积是
您最近一年使用:0次
解题方法
5 . 在某温度下,将H2和I2各0.10 mol的气态混合物充入10L的密闭容器中,充分反应达到平衡后,测得c(H2)=0.005 0mol/L。
(1)通过计算求该反应的平衡常数__________ 。
(2)在上述温度下,该容器中若通入H2和I2蒸气各0.20 mol,通过计算求达到化学平衡状态时各物质的浓度___________ 。
(1)通过计算求该反应的平衡常数
(2)在上述温度下,该容器中若通入H2和I2蒸气各0.20 mol,通过计算求达到化学平衡状态时各物质的浓度
您最近一年使用:0次
6 . (1)若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热量。其热化学方程式为_ 。
(2)甲醇(CH3OH)的燃烧热为725.8kJ/mol,写出甲醇的燃烧热的热化学方程式_____ 。
(3)已知H-H键的键能为436kJ·mol-1,Cl-Cl键的键能为243 kJ·mol-1,H-Cl键的键能为431kJ·mol-1,则H2(g)+Cl2(g)=2HCl(g)的反应热(ΔH)等于_____ kJ·mol-1
(4)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s)⇌NaNO3(s)+ClNO(g) K1 ΔH1
2NO(g)+Cl2(g)⇌2ClNO(g) K2 ΔH2
则4NO2(g)+2NaCl(s)⇌2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=___ (用含有K1、K2的式子表示);其反应热为______ (用含有ΔH1、ΔH2的式子表示)。
(2)甲醇(CH3OH)的燃烧热为725.8kJ/mol,写出甲醇的燃烧热的热化学方程式
(3)已知H-H键的键能为436kJ·mol-1,Cl-Cl键的键能为243 kJ·mol-1,H-Cl键的键能为431kJ·mol-1,则H2(g)+Cl2(g)=2HCl(g)的反应热(ΔH)等于
(4)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s)⇌NaNO3(s)+ClNO(g) K1 ΔH1
2NO(g)+Cl2(g)⇌2ClNO(g) K2 ΔH2
则4NO2(g)+2NaCl(s)⇌2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=
您最近一年使用:0次
7 . 某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。请回答下列问题:
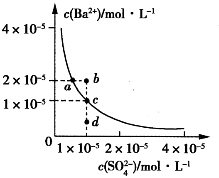
(1)下列说法正确的是__ (填序号)。
A.向BaSO4饱和溶液中加入固体Na2SO4可以由a点变到b点
B.通过蒸发可以由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
(2)将100mL1mol•L-1H2SO4溶液加入100mL含Ba2+0.137g的溶液中充分反应后,过滤,滤液中残留的Ba2+的物质的量浓度约为___ 。
(3)若沉淀分别用100mL纯水和100mL0.01mol•L-1的H2SO4溶液洗涤,两种情况下损失的BaSO4的质量之比为__ 。

(1)下列说法正确的是
A.向BaSO4饱和溶液中加入固体Na2SO4可以由a点变到b点
B.通过蒸发可以由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
(2)将100mL1mol•L-1H2SO4溶液加入100mL含Ba2+0.137g的溶液中充分反应后,过滤,滤液中残留的Ba2+的物质的量浓度约为
(3)若沉淀分别用100mL纯水和100mL0.01mol•L-1的H2SO4溶液洗涤,两种情况下损失的BaSO4的质量之比为
您最近一年使用:0次
2020-06-14更新
|
154次组卷
|
4卷引用:2016-2017学年湖北省襄阳五中高二上10月月考化学试卷
2016-2017学年湖北省襄阳五中高二上10月月考化学试卷【全国百强校】黑龙江省双鸭山市第一中学2018-2019学年高二下学期开学考试化学试题(已下线)【南昌新东方】江西省九江一中2014-2015学年高二上学期期中化学试卷(已下线)专题3 溶液中的离子反应 综合评价(1)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)
10-11高一下·河北邯郸·期末
名校
8 . 将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g) 2C(g)+2D(g),反应进行到10 s末,测得A的物质的量为1.8 mol, B的物质的量为0.6 mol,C的物质的量为0.8 mol,则:
2C(g)+2D(g),反应进行到10 s末,测得A的物质的量为1.8 mol, B的物质的量为0.6 mol,C的物质的量为0.8 mol,则:
(1)用C表示10 s内反应的平均反应速率为__________ ;
(2)反应前A的物质的量浓度是__________ ;
(3)10 s末,生成物D的浓度为________ ;
(4)若改变下列条件,生成D的速率如何变化(用“增大”“减小”或“不变”填空)。
 2C(g)+2D(g),反应进行到10 s末,测得A的物质的量为1.8 mol, B的物质的量为0.6 mol,C的物质的量为0.8 mol,则:
2C(g)+2D(g),反应进行到10 s末,测得A的物质的量为1.8 mol, B的物质的量为0.6 mol,C的物质的量为0.8 mol,则:(1)用C表示10 s内反应的平均反应速率为
(2)反应前A的物质的量浓度是
(3)10 s末,生成物D的浓度为
(4)若改变下列条件,生成D的速率如何变化(用“增大”“减小”或“不变”填空)。
| 编号 | 改变的条件 | 生成D的速率 |
| ① | 降低温度 | |
| ② | 增大A的浓度 | |
| ③ | 使用催化剂 | |
| ④ | 恒容下充入Ne(不参与体系反应) |
您最近一年使用:0次
2020-04-18更新
|
333次组卷
|
8卷引用:2017届湖北省老河口市江山中学高三10月月考化学卷
2017届湖北省老河口市江山中学高三10月月考化学卷(已下线)2010-2011学年河北省邯郸市高一下学期期末考试化学试卷(已下线)2010—2011学年山东省微山一中高一下学期期末考试化学试卷(已下线)2019年3月31日 《每日一题》 必修2 每周一测【全国百强校】山西省晋中市平遥中学2018-2019学年高一下学期期中考试化学试题广东省郁南县连滩中学2019-2020学年高一下学期期中考试化学试题甘肃省靖远县第四中学2019-2020学年高一下学期期中考试化学(普通班)试题山东省济宁市泗水县2020-2021学年高一下学期期中考试化学试题
11-12高三上·湖北襄阳·期中
名校
解题方法
9 . 取等物质的量浓度的 溶液两份A和B,每份10mL,分别向A、B中通入不等量的
溶液两份A和B,每份10mL,分别向A、B中通入不等量的 ,再继续向两溶液中逐滴加入
,再继续向两溶液中逐滴加入 的盐酸,标准状况下产生的
的盐酸,标准状况下产生的 气体体积与所加的盐酸溶液体积之的关系如下图所示,试回答下列问题:
气体体积与所加的盐酸溶液体积之的关系如下图所示,试回答下列问题:
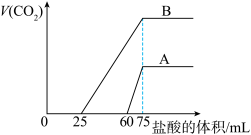
(1)原 溶液的物质的量浓度为
溶液的物质的量浓度为________ 
(2)曲线A表明,原 溶液中通入
溶液中通入 后,所得溶液中的溶质为(写化学式)
后,所得溶液中的溶质为(写化学式)________ ;其物质的量之比为________ ;
(3)曲线B表明,原 溶液中通入
溶液中通入 后,所得溶液加盐酸后产生
后,所得溶液加盐酸后产生 气体体积(标准状况)的最大值为
气体体积(标准状况)的最大值为________ mL。
 溶液两份A和B,每份10mL,分别向A、B中通入不等量的
溶液两份A和B,每份10mL,分别向A、B中通入不等量的 ,再继续向两溶液中逐滴加入
,再继续向两溶液中逐滴加入 的盐酸,标准状况下产生的
的盐酸,标准状况下产生的 气体体积与所加的盐酸溶液体积之的关系如下图所示,试回答下列问题:
气体体积与所加的盐酸溶液体积之的关系如下图所示,试回答下列问题:
(1)原
 溶液的物质的量浓度为
溶液的物质的量浓度为
(2)曲线A表明,原
 溶液中通入
溶液中通入 后,所得溶液中的溶质为(写化学式)
后,所得溶液中的溶质为(写化学式)(3)曲线B表明,原
 溶液中通入
溶液中通入 后,所得溶液加盐酸后产生
后,所得溶液加盐酸后产生 气体体积(标准状况)的最大值为
气体体积(标准状况)的最大值为
您最近一年使用:0次
2020-02-27更新
|
399次组卷
|
10卷引用:2012届湖北省襄阳市四校高三上学期期中联考化学试卷
(已下线)2012届湖北省襄阳市四校高三上学期期中联考化学试卷2016届山东省乳山市第一中学高三上学期10月月考化学试卷2015-2016学年广东省汕头金山中学高一上期末化学试卷2016-2017学年江西省南昌二中高一上第二次考试化学卷黑龙江省齐齐哈尔市第八中学2019届高三9月月考化学试题湖北省武汉市汉阳一中2018-2019学年高一上学期12月月考化学试题江西省新余市分宜中学2020届高三上学期第一次段考化学试题(已下线)【新东方】2020-44(已下线)专题3.1 金属钠及其化合物 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》天津市耀华中学2021-2022学年高一上学期期中考试化学试题
10 . 某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
(1)该反应的化学方程式为_______________________________ ;
(2)反应开始至2min,以气体Z表示的平均反应速率为________________ ;
(3)混合气体的平均相对分子质量比起始时___________ ;(填“大”,“小”或“相等”)
平衡时容器内混合气体密度比起始时______ (填“大”,“小”或“相等”)
(4)将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中a:b=___________ .

(1)该反应的化学方程式为
(2)反应开始至2min,以气体Z表示的平均反应速率为
(3)混合气体的平均相对分子质量比起始时
平衡时容器内混合气体密度比起始时
(4)将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中a:b=

您最近一年使用:0次
2019-05-16更新
|
397次组卷
|
5卷引用:【全国校级联考】湖北省襄阳市四校(襄州一中、枣阳一中、宜城一中、曾都一中)2017-2018学年高一下学期期中联考化学试题



