解题方法
1 . 下列有关反应的离子方程式正确的是
A.将铁粉加入 溶液中: 溶液中: |
B.将氧化亚铁加入稀盐酸中: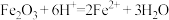 |
| C.四氧化三铁与稀硫酸反应:Fe3O4+8H+=3Fe2++4H2O |
| D.向氢氧化铁中加入足量稀盐酸:H++OH-=H2O |
您最近一年使用:0次
解题方法
2 . 学好化学让生活更美好,下列相关说法错误的是
| A.碳酸氢钠可以用于制药或焙制糕点 |
| B.“火树银花”中的焰火实质上是金属元素的焰色试验 |
| C.漂白粉、漂粉精、漂白液均用作消毒剂,其主要成分均为NaClO |
| D.葡萄酒中的花青素在碱性环境下显蓝色,故可用苏打粉检验假红酒 |
您最近一年使用:0次
3 . 已知: △H=-14.9 kJ·mol-1。某温度下在甲、乙两个恒容密闭容器中充入反应物,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)=0.008 mol·L-1。下列判断正确的是
△H=-14.9 kJ·mol-1。某温度下在甲、乙两个恒容密闭容器中充入反应物,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)=0.008 mol·L-1。下列判断正确的是
 △H=-14.9 kJ·mol-1。某温度下在甲、乙两个恒容密闭容器中充入反应物,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)=0.008 mol·L-1。下列判断正确的是
△H=-14.9 kJ·mol-1。某温度下在甲、乙两个恒容密闭容器中充入反应物,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)=0.008 mol·L-1。下列判断正确的是起始浓度 | c(H2)/(mol·L-1) | c(I2)/(mol·L-1) | c(HI)/(mol·L-1) |
甲 | 0.01 | 0.01 | 0 |
乙 | 0.02 | 0.02 | 0 |
| A.平衡时,乙中H2的转化率与甲中的相等 |
| B.平衡时,甲中混合物的颜色比乙中深 |
| C.平衡时,甲、乙中热量的变化值相等 |
| D.该温度下,反应的平衡常数K=4 |
您最近一年使用:0次
4 . 醋酸是常见的一元弱酸。请运用化学反应原理回答下列问题:
(1)室温下,pH=2的醋酸中,水电离出的c(H+)=_________ mol·L-1;该醋酸和pH=2的盐酸溶液相比,导电性_________ (填“相同”“不同”或“无法判断”)。
(2)pH相同的盐酸和醋酸分别与足量的锌粒反应,生成等量的H2时所需时间较短的是_________ 。
(3)向100 mL0.1mol·L-1醋酸溶液中滴入NaOH溶液,下列浓度大小顺序不可能出现的是_________ (填字母)。
a.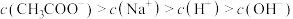
b.
c.
d.
(4)常温下,将10mLpH=2的醋酸溶液稀释至1000 mL,溶液的pH (填“>”“<”或“=”)4;在醋酸稀释过程中下列数值变大的是 。
(5)醋酸中存在平衡:CH3COOH CH3COO-+H+,下列措施可使醋酸的pH增大,并且电离平衡向右移动的是 。
CH3COO-+H+,下列措施可使醋酸的pH增大,并且电离平衡向右移动的是 。
(1)室温下,pH=2的醋酸中,水电离出的c(H+)=
(2)pH相同的盐酸和醋酸分别与足量的锌粒反应,生成等量的H2时所需时间较短的是
(3)向100 mL0.1mol·L-1醋酸溶液中滴入NaOH溶液,下列浓度大小顺序不可能出现的是
a.
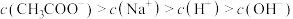
b.

c.

d.

(4)常温下,将10mLpH=2的醋酸溶液稀释至1000 mL,溶液的pH (填“>”“<”或“=”)4;在醋酸稀释过程中下列数值变大的是 。
| A.c(H+) | B.c(OH-)/c(CH2COO-) | C.c(H+)·c(OH-) | D. |
 CH3COO-+H+,下列措施可使醋酸的pH增大,并且电离平衡向右移动的是 。
CH3COO-+H+,下列措施可使醋酸的pH增大,并且电离平衡向右移动的是 。| A.加入Na2CO3溶液 | B.加入盐酸 |
| C.加水稀释 | D.对醋酸溶液加热 |
您最近一年使用:0次
解题方法
5 . 向盛有氯气的集气瓶中,注入约五分之一容器体积的下列液体并轻轻振荡,观察到的现象记录如图所示。判断瓶中注入的液体是
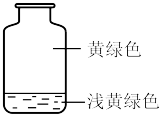

| A.AgNO3溶液 | B.NaOH溶液 | C.水 | D.FeCl2溶液 |
您最近一年使用:0次
6 . 化学与社会、生活密切相关。下列叙述正确的是
| A.二氧化硅可用于制作光感电池 |
| B.漂白粉在空气中久置变质,是因为漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
| C.绿色化学要求从源头上消除或减少生产活动对环境的污染 |
| D.燃煤中加入CaO可以减少酸雨的形成及温室气体的排放 |
您最近一年使用:0次
7 . 实验室以含钴废料(主要成分是CoO、Co2O3,含少量Fe2O3、Al2O3等杂质)为原料制备CoCO3的流程如图所示。
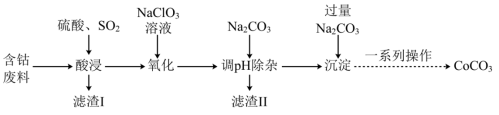
已知:①“酸浸”后过滤得到的滤液中含有Co2+、Fe2+、Al3+等。
②有关沉淀数据如表(完全沉淀时金属离子浓度≤1×10-5mol/L):
回答下列问题:
(1)基态钴原子的价层电子排布式为_______ ,在“酸浸”之前,先要对含钴废料进行粉碎处理,其目的是_______ 。
(2)“酸浸”时需通入SO2,其中SO2作______ (填“氧化剂”或“还原剂”),由于“酸浸”时,溶液中会产生Fe3+,写出SO2与Fe3+反应的离子方程式:______ 。
(3)“氧化”流程中,氧化剂与还原剂的物质的量之比为______ 。
(4)常温下,若浸取液中c(Co2+)=0.1mol/L,则“调pH除杂”时需调节溶液pH的范围为______ 至______ 。(加入NaClO3和Na2CO3时,溶液的体积变化忽略)
(5)“滤渣II”的主要成分为______ 。
(6)“一系列操作”为过滤、洗涤、干燥,其中过滤所需要的硅酸盐材质的仪器有_______ 。
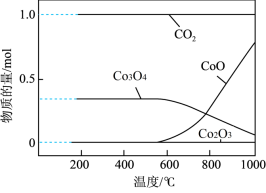
(7)将得到的CoCO3固体在空气中加热,反应温度对反应产物的影响如图所示,则500~1000℃时,发生主要反应的化学方程式为_______ 。

已知:①“酸浸”后过滤得到的滤液中含有Co2+、Fe2+、Al3+等。
②有关沉淀数据如表(完全沉淀时金属离子浓度≤1×10-5mol/L):
| 沉淀 | Al(OH)3 | Fe(OH)3 | Co(OH)2 |
| 恰好完全沉淀时的pH | 5.2 | 2.8 | 9.4 |
(1)基态钴原子的价层电子排布式为
(2)“酸浸”时需通入SO2,其中SO2作
(3)“氧化”流程中,氧化剂与还原剂的物质的量之比为
(4)常温下,若浸取液中c(Co2+)=0.1mol/L,则“调pH除杂”时需调节溶液pH的范围为
(5)“滤渣II”的主要成分为
(6)“一系列操作”为过滤、洗涤、干燥,其中过滤所需要的硅酸盐材质的仪器有
(7)将得到的CoCO3固体在空气中加热,反应温度对反应产物的影响如图所示,则500~1000℃时,发生主要反应的化学方程式为

您最近一年使用:0次
8 . 下列实验设计不能达到实验目的的是
| 实验目的 | 实验设计 | |
| A | 证明氧化性Cl2>Br2>I2 | 向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液 |
| B | 比较水和乙醇中氢的活泼性 | 分别将少量钠投入到盛有水和乙醇的烧杯中 |
| C | 检验溶液中FeSO4是否被氧化 | 取少量待测液,滴加KSCN溶液,观察溶液颜色变化 |
| D | 工业酒精制备无水乙醇 | 工业酒精中加生石灰,蒸馏 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 能正确表示下列反应的离子方程式为
A.过量铁粉加入稀硝酸中:Fe+4H++NO =Fe3++NO↑+2H2O =Fe3++NO↑+2H2O |
| B.氯化铜溶液中通入硫化氢:Cu2++S2-=CuS↓ |
C.用Na2SO3溶液吸收少量Cl2:3SO +Cl2+H2O=2HSO +Cl2+H2O=2HSO +2Cl-+SO +2Cl-+SO |
D.同浓度同体积NH4HSO4溶液与NaOH溶液混合:NH +OH-=NH3•H2O +OH-=NH3•H2O |
您最近一年使用:0次
10 . 设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.2L0.5mol/L亚硫酸溶液中含有的H+数为2NA |
| B.23gNa与足量O2反应,生成Na2O和Na2O2的混合物,转移的电子数为NA |
| C.标准状况下,22.4LCHCl3中含有氯原子数目为3NA |
| D.28gC2H4分子中含有的σ键数目为4NA |
您最近一年使用:0次



