解题方法
1 . 某澄清透明溶液中可能含Na+、K+、Mg2+、Cu2+、OH-、Cl-、 、
、 中的一种或几种(不考虑离子水解),现进行如下实验:并回答下列问题:
中的一种或几种(不考虑离子水解),现进行如下实验:并回答下列问题:
①用玻璃棒蘸取少量溶液滴在红色石蕊试纸上,试纸变蓝;
②取少量原溶液于试管中,逐滴滴加盐酸至过量,有气体放出;
③再向②所得溶液中加入BaCl2溶液,没有沉淀生成;
④再向③所得溶液中滴加足量硝酸酸化后,加入AgNO3液,有白色沉淀生成。
(1)根据步骤①可以推断溶液中一定含有___________ ,一定不含有___________ 。
(2)根据步骤②、③可以推断出溶液中一定含有___________ ,一定不含有___________ 。
(3)步骤④中产生的白色沉淀为___________ (填化学式)。
(4)通过步骡④不能确定溶液中含有 ,其原因是
,其原因是___________ 。
 、
、 中的一种或几种(不考虑离子水解),现进行如下实验:并回答下列问题:
中的一种或几种(不考虑离子水解),现进行如下实验:并回答下列问题:①用玻璃棒蘸取少量溶液滴在红色石蕊试纸上,试纸变蓝;
②取少量原溶液于试管中,逐滴滴加盐酸至过量,有气体放出;
③再向②所得溶液中加入BaCl2溶液,没有沉淀生成;
④再向③所得溶液中滴加足量硝酸酸化后,加入AgNO3液,有白色沉淀生成。
(1)根据步骤①可以推断溶液中一定含有
(2)根据步骤②、③可以推断出溶液中一定含有
(3)步骤④中产生的白色沉淀为
(4)通过步骡④不能确定溶液中含有
 ,其原因是
,其原因是
您最近一年使用:0次
解题方法
2 . 金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制钠的工业方法,其反应原理是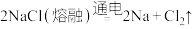 。请完成下列有关单质钠的问题。
。请完成下列有关单质钠的问题。
(1)保存金属钠的正确方法是___________ (填字母)。
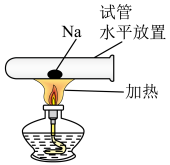
(2)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应(如图所示),生成淡黄色固体,请写出该反应的化学方程式:___________ 。___________ 。
(4)将一小块金属钠投入 溶液中,发生反应的总化学方程式为
溶液中,发生反应的总化学方程式为___________ 。
(5)常温常压下,CO2和过氧化钠反应后,若固体质量增加了28g,反应中消耗的CO2的质量是___________ g。
(6)根据上述实验小组同学猜测过氧化钠可用作呼吸面具、潜水艇等中的供氧剂。请选择适当的化学试剂和实验仪器,用如图所示的实验装置进行实验,以证明过氧化钠可作供氧剂。请回答下列问题。___________ 。
②装置B中盛有饱和NaHCO3溶液,其作用是___________ 。
③装置D中盛放的试剂是___________ ,其目的是___________ 。
④当观察到试管F中收集满气体,为证明收集的气体是O2,还需要进行哪些实验操作?___________ 。
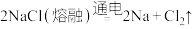 。请完成下列有关单质钠的问题。
。请完成下列有关单质钠的问题。(1)保存金属钠的正确方法是
| A.放在棕色瓶中 | B.放在石蜡油中 | C.放在水中 | D.放在煤油中 |
(2)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应(如图所示),生成淡黄色固体,请写出该反应的化学方程式:
(4)将一小块金属钠投入
 溶液中,发生反应的总化学方程式为
溶液中,发生反应的总化学方程式为(5)常温常压下,CO2和过氧化钠反应后,若固体质量增加了28g,反应中消耗的CO2的质量是
(6)根据上述实验小组同学猜测过氧化钠可用作呼吸面具、潜水艇等中的供氧剂。请选择适当的化学试剂和实验仪器,用如图所示的实验装置进行实验,以证明过氧化钠可作供氧剂。请回答下列问题。
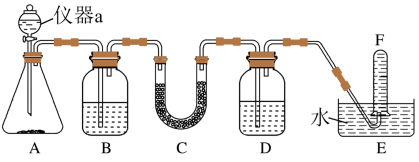
②装置B中盛有饱和NaHCO3溶液,其作用是
③装置D中盛放的试剂是
④当观察到试管F中收集满气体,为证明收集的气体是O2,还需要进行哪些实验操作?
您最近一年使用:0次
解题方法
3 . 将Cl2通入70℃的氢氧化钠水溶液中,发生以下反应(未配平):
 ,反应完成后测得溶液中NaClO与NaClO3的物质的量浓度之比为5:2,则该溶液中NaClO与NaCl的物质的量之比为
,反应完成后测得溶液中NaClO与NaClO3的物质的量浓度之比为5:2,则该溶液中NaClO与NaCl的物质的量之比为
 ,反应完成后测得溶液中NaClO与NaClO3的物质的量浓度之比为5:2,则该溶液中NaClO与NaCl的物质的量之比为
,反应完成后测得溶液中NaClO与NaClO3的物质的量浓度之比为5:2,则该溶液中NaClO与NaCl的物质的量之比为| A.5:2 | B.2:5 | C.5:16 | D.1:3 |
您最近一年使用:0次
解题方法
4 . 已知下列反应:
①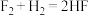 (冷暗处剧烈反应)
(冷暗处剧烈反应)
②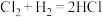 (常温下剧烈反应)
(常温下剧烈反应)
③
则F2、Cl2、Br2氧化性由强到弱的顺序是
①
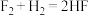 (冷暗处剧烈反应)
(冷暗处剧烈反应)②
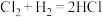 (常温下剧烈反应)
(常温下剧烈反应)③

则F2、Cl2、Br2氧化性由强到弱的顺序是
A.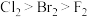 | B. | C.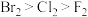 | D.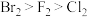 |
您最近一年使用:0次
解题方法
5 . 已知几种阴离子还原性顺序为Cl-<Br-<I-<S2-,若某溶液含有相同数目的Cl-、Br-、I-、S2-,当向其中通入过量的Cl2,最后被氧化的离子是
| A.Br- | B.Cl- | C.I- | D.S2- |
您最近一年使用:0次
解题方法
6 . 下列氧化还原反应方程式中,电子转移方向和数目正确的是
A.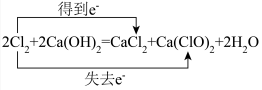 | B.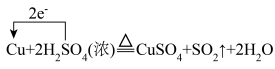 |
C.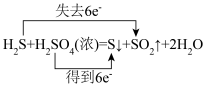 | D.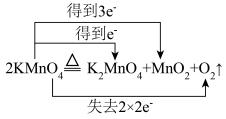 |
您最近一年使用:0次
解题方法
7 . 研究化学反应中的能量变化可以为提高工业生产效率提供指导性的理论依据。请结合所学化学反应原理相关知识回答下列问题:
(1)计算化学反应中的能量变化有多种途径。
①通过化学键的键能计算。已知:
计算可得:

_______ 
②通过盖斯定律计算。已知:
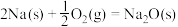
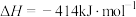

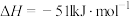
写出Na2O2与Na反应生成Na2O的热化学方程式:_______ 。
(2)实现“节能减排”和“低碳经济”的一项重要课题就是将CO2转化为可利用的资源,工业上有一种方法是用CO2来生产燃料甲醇。
已知:
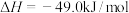 ,在一定条件下,向体积固定为1L的密闭容器中充入1molCO2和3molH2,测得CO2气体和CH3OH(g))的浓度随时间变化曲线如图所示。
,在一定条件下,向体积固定为1L的密闭容器中充入1molCO2和3molH2,测得CO2气体和CH3OH(g))的浓度随时间变化曲线如图所示。
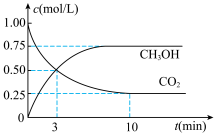
①甲醇中的官能团名称为_______ 。
②反应开始至平衡时,反应速率
_______ mol/(L⋅min)。CO2的平衡转化率为_______ 。
③为了加快化学反应速率,只改变下列某一条件,可采取的措施有_______ (填序号)。
A.升高温度 B.扩大容器体积 C.再充入CO2气体 D.使用合适的催化剂
(1)计算化学反应中的能量变化有多种途径。
①通过化学键的键能计算。已知:
| 化学键 | H—H | Cl—Cl | H—Cl |
| 键能(kJ/mol) | 436 | 247 | 434 |



②通过盖斯定律计算。已知:
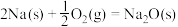
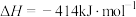

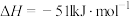
写出Na2O2与Na反应生成Na2O的热化学方程式:
(2)实现“节能减排”和“低碳经济”的一项重要课题就是将CO2转化为可利用的资源,工业上有一种方法是用CO2来生产燃料甲醇。
已知:

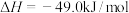 ,在一定条件下,向体积固定为1L的密闭容器中充入1molCO2和3molH2,测得CO2气体和CH3OH(g))的浓度随时间变化曲线如图所示。
,在一定条件下,向体积固定为1L的密闭容器中充入1molCO2和3molH2,测得CO2气体和CH3OH(g))的浓度随时间变化曲线如图所示。
①甲醇中的官能团名称为
②反应开始至平衡时,反应速率

③为了加快化学反应速率,只改变下列某一条件,可采取的措施有
A.升高温度 B.扩大容器体积 C.再充入CO2气体 D.使用合适的催化剂
您最近一年使用:0次
解题方法
8 . 在标准状况下,实验甲、乙、丙各取30.0mL相同浓度的盐酸,然后分别慢慢加入组成相同的镁铝合金粉末,得下表中有关数据(假设反应前后溶液体积不变)。
下列说法不正确的是
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 255 | 385 | 459 |
| 气体体积/mL | 280 | 336 | 336 |
| A.实验甲中盐酸过量 |
| B.实验乙中盐酸不足 |
| C.实验中c(HCl)=1.0mol/L |
| D.该镁铝合金粉末中Mg、Al的物质的量之比为2:1 |
您最近一年使用:0次
解题方法
9 . 医院给患者输液用的葡萄糖注射液是葡萄糖(化学式为C6H12O6)的水溶液,其标签上的部分内容如图所示。利用标签所提供的信息,回答下列问题:
(1)该注射液中葡萄糖的物质的量浓度是___________ (计算结果精确到小数点后2位) 。
。
(2)某同学进行某项实验时需要480mL上述葡萄糖溶液,配制过程如下。
①该同学需称取___________ g葡萄糖在烧杯中溶解。
②配制时正确的操作顺序是___________ (用字母表示,每个字母只能用一次)。
A.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,将洗涤液均注入容量瓶中,振荡
B.用托盘天平准确称取葡萄糖并加入盛有少量蒸馏水(约50mL)的烧杯中,用玻璃棒慢慢搅拌,使其完全溶解
C.将溶解完全的葡萄糖溶液沿玻璃棒注入一定规格的容量瓶中
D.将容量瓶盖紧,摇匀
E.改用胶头滴管滴加蒸馏水,使溶液凹液面的最低处恰好与刻度线相切
F.继续往容量瓶内加蒸馏水至液面离容量瓶颈刻度线下1~2cm处
③在配制过程中,下列操作会使所配溶液的浓度偏高的是___________ (填字母)。
A.用托盘天平称取葡萄糖时“左物右码”
B.溶解时使用的烧杯和玻璃棒未洗涤
C.洗净的容量瓶未经干燥就用于配制溶液
D.定容时俯视刻度线
E.加蒸馏水超过刻度线后,用胶头滴管吸出多余的液体
(3)已知溶液中某溶质的物质的量除以溶剂的质量称为该溶质的质量摩尔浓度,单位为mol/kg。
①已知上述所配葡萄糖溶液的密度为 ,则其质量摩尔浓度为
,则其质量摩尔浓度为___________ (计算结果精确到小数点后2位)mol/kg。
②若将标准状况下aLHCl气体完全溶于bg水中,所得盐酸中HCl的质量摩尔浓度为___________ (用含a、b的代数式表示)mol/kg。
5%葡萄糖注射器 【性状】本品为无色或几乎无色的的透明液体,味甜【规格】500mL 【密度】1g/mL 【贮藏】密闭保存 |
 。
。(2)某同学进行某项实验时需要480mL上述葡萄糖溶液,配制过程如下。
①该同学需称取
②配制时正确的操作顺序是
A.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,将洗涤液均注入容量瓶中,振荡
B.用托盘天平准确称取葡萄糖并加入盛有少量蒸馏水(约50mL)的烧杯中,用玻璃棒慢慢搅拌,使其完全溶解
C.将溶解完全的葡萄糖溶液沿玻璃棒注入一定规格的容量瓶中
D.将容量瓶盖紧,摇匀
E.改用胶头滴管滴加蒸馏水,使溶液凹液面的最低处恰好与刻度线相切
F.继续往容量瓶内加蒸馏水至液面离容量瓶颈刻度线下1~2cm处
③在配制过程中,下列操作会使所配溶液的浓度偏高的是
A.用托盘天平称取葡萄糖时“左物右码”
B.溶解时使用的烧杯和玻璃棒未洗涤
C.洗净的容量瓶未经干燥就用于配制溶液
D.定容时俯视刻度线
E.加蒸馏水超过刻度线后,用胶头滴管吸出多余的液体
(3)已知溶液中某溶质的物质的量除以溶剂的质量称为该溶质的质量摩尔浓度,单位为mol/kg。
①已知上述所配葡萄糖溶液的密度为
 ,则其质量摩尔浓度为
,则其质量摩尔浓度为②若将标准状况下aLHCl气体完全溶于bg水中,所得盐酸中HCl的质量摩尔浓度为
您最近一年使用:0次
10 .  是一种高效、安全的消毒剂。实验室制备
是一种高效、安全的消毒剂。实验室制备 的原理是用亚氯酸钠固体与纯净、干燥的氯气反应:
的原理是用亚氯酸钠固体与纯净、干燥的氯气反应: 。如图1是实验室用于制备和收集一定量纯净的
。如图1是实验室用于制备和收集一定量纯净的 的装置(部分夹持装置已省略)。
的装置(部分夹持装置已省略)。
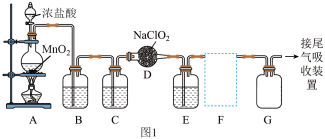
(1)圆底烧瓶中发生反应的化学方程式为___________ ,在该反应中浓盐酸表现的性质是___________ (填序号)。
a.只有还原性 b.还原性和酸性 c.只有氧化性 d.氧化性和酸性
(2)实验中相关气体在不同溶剂中的溶解性如表所示。
B、C、E装置中的试剂依次是___________ (填序号,下同)、___________ 、___________ 。
a.NaOH溶液 b.浓硫酸 c.饱和食盐水 d.CCl4 e.饱和石灰水
(3)如图2是一些常用的气体收集装置,F处应选用的收集装置是___________ (填序号),其中与E装置导管相连的导管口是___________ (填接口字母)。

(4) 泡腾片由
泡腾片由 、固体酸及辅助剂混合制得,是一种家用消毒用品。使用时只需将泡腾片放入水中,5~10分钟即可完全溶解并释放出
、固体酸及辅助剂混合制得,是一种家用消毒用品。使用时只需将泡腾片放入水中,5~10分钟即可完全溶解并释放出 。
。
① 泡腾片使用时需要加水,水的作用是
泡腾片使用时需要加水,水的作用是___________ 。
②补全泡腾片在水中发生反应的离子方程式:_______ ;
___________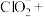 ___________
___________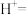 ___________
___________ ___________+___________
___________+___________ 。
。
 是一种高效、安全的消毒剂。实验室制备
是一种高效、安全的消毒剂。实验室制备 的原理是用亚氯酸钠固体与纯净、干燥的氯气反应:
的原理是用亚氯酸钠固体与纯净、干燥的氯气反应: 。如图1是实验室用于制备和收集一定量纯净的
。如图1是实验室用于制备和收集一定量纯净的 的装置(部分夹持装置已省略)。
的装置(部分夹持装置已省略)。
(1)圆底烧瓶中发生反应的化学方程式为
a.只有还原性 b.还原性和酸性 c.只有氧化性 d.氧化性和酸性
(2)实验中相关气体在不同溶剂中的溶解性如表所示。
| ClO2 | Cl2 | HCl | |
| 水 | 极易溶 | 可溶 | 极易溶 |
| CCl4 | 难溶 | 易溶 | 难溶 |
a.NaOH溶液 b.浓硫酸 c.饱和食盐水 d.CCl4 e.饱和石灰水
(3)如图2是一些常用的气体收集装置,F处应选用的收集装置是

(4)
 泡腾片由
泡腾片由 、固体酸及辅助剂混合制得,是一种家用消毒用品。使用时只需将泡腾片放入水中,5~10分钟即可完全溶解并释放出
、固体酸及辅助剂混合制得,是一种家用消毒用品。使用时只需将泡腾片放入水中,5~10分钟即可完全溶解并释放出 。
。①
 泡腾片使用时需要加水,水的作用是
泡腾片使用时需要加水,水的作用是②补全泡腾片在水中发生反应的离子方程式:
___________
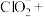 ___________
___________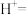 ___________
___________ ___________+___________
___________+___________ 。
。
您最近一年使用:0次



