解题方法
1 . 如图是某校化学实验室中硫酸试剂标签上的部分内容。据此下列说法正确的是
| 硫酸 化学纯(CP)(500mL) 品名:硫酸 化学式:  相对分子质量:98 密度: 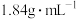 质量分数:98% |
A.硫酸的物质的量浓度为 |
B.配制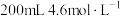 的稀硫酸需量取该硫酸50mL 的稀硫酸需量取该硫酸50mL |
| C.该瓶硫酸的质量是920g |
D.等质量的水与该硫酸混合所得溶液的物质的量浓度大于 |
您最近一年使用:0次
名校
2 . 设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A.1mol NaOH中含有的阴、阳离子总数是 |
B.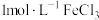 溶液中所含 溶液中所含 的数目为 的数目为 |
C.标准状况下,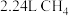 中含有氢原子的数目为 中含有氢原子的数目为 |
D.常温常压下,9.6g由 和 和 组成的混合气体中所含氧原子总数为 组成的混合气体中所含氧原子总数为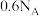 |
您最近一年使用:0次
名校
3 . 实验室需要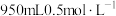 的稀硫酸和
的稀硫酸和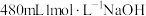 溶液进行实验,请你用98%的浓硫酸(
溶液进行实验,请你用98%的浓硫酸(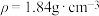 )和NaOH固体进行配制。回答下列问题:
)和NaOH固体进行配制。回答下列问题:
(1)配制稀硫酸时,需要使用的玻璃仪器有量筒、烧杯、胶头滴管、玻璃棒、_______ (填仪器名称)。
(2)配制稀硫酸时,需要量取98%的浓硫酸_______ (精确到0.1)mL。
(3)对所配制的稀硫酸进行测定,发现其浓度为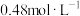 ,下列各项操作可能引起该误差的是
,下列各项操作可能引起该误差的是_______ (填字母)。
A.用量筒量取浓硫酸时仰视
B.转移稀释的硫酸溶液后未洗涤烧杯和玻璃棒
C.浓硫酸稀释后未经冷却即转移到容量瓶中
D.容量瓶未干燥就用来配制溶液
E.定容后摇匀溶液,发现液面低于刻度线,再加入少量蒸馏水使液面与刻度线相平
(4)配制NaOH溶液时,应称量的NaOH固体质量为_______ g。
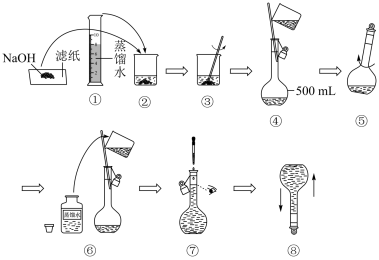
(5)某同学在实验室配制NaOH溶液的过程如图所示,其中有错误的操作是_______ (填序号)。
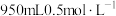 的稀硫酸和
的稀硫酸和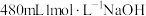 溶液进行实验,请你用98%的浓硫酸(
溶液进行实验,请你用98%的浓硫酸(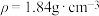 )和NaOH固体进行配制。回答下列问题:
)和NaOH固体进行配制。回答下列问题:(1)配制稀硫酸时,需要使用的玻璃仪器有量筒、烧杯、胶头滴管、玻璃棒、
(2)配制稀硫酸时,需要量取98%的浓硫酸
(3)对所配制的稀硫酸进行测定,发现其浓度为
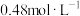 ,下列各项操作可能引起该误差的是
,下列各项操作可能引起该误差的是A.用量筒量取浓硫酸时仰视
B.转移稀释的硫酸溶液后未洗涤烧杯和玻璃棒
C.浓硫酸稀释后未经冷却即转移到容量瓶中
D.容量瓶未干燥就用来配制溶液
E.定容后摇匀溶液,发现液面低于刻度线,再加入少量蒸馏水使液面与刻度线相平
(4)配制NaOH溶液时,应称量的NaOH固体质量为
(5)某同学在实验室配制NaOH溶液的过程如图所示,其中有错误的操作是

您最近一年使用:0次
名校
4 . 下列溶液中 的浓度最小的是
的浓度最小的是
 的浓度最小的是
的浓度最小的是A. 的 的 溶液 溶液 | B.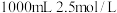 的 的 溶液 溶液 |
C.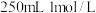 的 的 溶液 溶液 | D.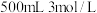 的 的 溶液 溶液 |
您最近一年使用:0次
名校
5 . 某食品经检测含 浓度为
浓度为 ,则
,则 的物质的量浓度为
的物质的量浓度为
 浓度为
浓度为 ,则
,则 的物质的量浓度为
的物质的量浓度为A.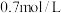 | B.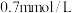 | C. | D.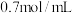 |
您最近一年使用:0次
名校
6 . 下列关于物质的量浓度表述正确的是
A.将7.8g  溶于水,配成100g溶液,所得溶液质量分数为7.8% 溶于水,配成100g溶液,所得溶液质量分数为7.8% |
B.质量分数为3.65%的200g盐酸溶液中,含 分子的数目为 分子的数目为 |
C.将25g胆矾( )溶于75克水中,可得到质量分数为16% )溶于75克水中,可得到质量分数为16% 的溶液 的溶液 |
D.将7.1g  通入水中,完全溶于水得到100g溶液,理论上可获得3.65%的盐酸溶液 通入水中,完全溶于水得到100g溶液,理论上可获得3.65%的盐酸溶液 |
您最近一年使用:0次
名校
解题方法
7 . 计算题
(1)一定量的质量分数为10%的氢氧化钠溶液,若将其蒸发掉100g水,其质量分数恰好变为20%,溶液体积变为80mL,则浓缩后的氢氧化钠溶液物质的量浓度为___________ mol/L。
(2)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是___________ L。(用含字母的式子表示,NA表示阿伏伽德罗常数)
(3)有8gNa2O、Na2O2、Na2CO3、NaOH的混合物与200g质量分数为3.65%的盐酸恰好反应,最终得NaCl固体质量为___________ g。
(4)在VL硫酸铁溶液中,含有agFe3+,取出 L溶液,则取出的
L溶液,则取出的 L溶液中,SO
L溶液中,SO 的物质的量浓度为
的物质的量浓度为___________ mol/L。
(1)一定量的质量分数为10%的氢氧化钠溶液,若将其蒸发掉100g水,其质量分数恰好变为20%,溶液体积变为80mL,则浓缩后的氢氧化钠溶液物质的量浓度为
(2)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是
(3)有8gNa2O、Na2O2、Na2CO3、NaOH的混合物与200g质量分数为3.65%的盐酸恰好反应,最终得NaCl固体质量为
(4)在VL硫酸铁溶液中,含有agFe3+,取出
 L溶液,则取出的
L溶液,则取出的 L溶液中,SO
L溶液中,SO 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
名校
解题方法
8 . 某市售盐酸的质量分数为36.5%,密度为1.2g·cm-3,该盐酸中溶质的物质的量浓度是
| A.0.5mol·L-1 | B.3mol·L-1 | C.8.4mol·L-1 | D.12.0mol·L-1 |
您最近一年使用:0次
名校
解题方法
9 . 将物质的量浓度为2cmol/L、质量分数为a%的硫酸溶液,加水稀释至物质的量浓度为cmol/L,质量分数变为b%。则a、b之间的大小关系为(已知:硫酸溶液的浓度越大密度越大)
| A.a=2b | B.2b>a | C.a>2b | D.不能比较 |
您最近一年使用:0次
10 . 完成下列计算
(1)标况下,将4.48 L的氯化氢气体溶于水中配制成2 L溶液,所得溶液浓度为______ 。
(2)2 L硫酸铝溶液中含2.7 g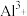 ,则该溶液中
,则该溶液中 的物质的量浓度是
的物质的量浓度是______ 。
(3)将10 mL 1.0 mol/L 溶液加水稀释至100 mL,所得的溶液中Na+物质的量浓度为
溶液加水稀释至100 mL,所得的溶液中Na+物质的量浓度为______ 。
(4)100 mL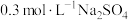 溶液和50 mL
溶液和50 mL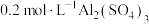 溶液混合后,溶液中
溶液混合后,溶液中 的物质的量浓度为
的物质的量浓度为______ 。
(5)某同学配制的植物营养液中有4种离子,其中所含的 、
、 、
、 的物质的量浓度分别为
的物质的量浓度分别为 、
、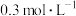 、
、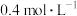 ,则
,则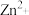 的物质的量浓度是
的物质的量浓度是______ 。
(1)标况下,将4.48 L的氯化氢气体溶于水中配制成2 L溶液,所得溶液浓度为
(2)2 L硫酸铝溶液中含2.7 g
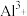 ,则该溶液中
,则该溶液中 的物质的量浓度是
的物质的量浓度是(3)将10 mL 1.0 mol/L
 溶液加水稀释至100 mL,所得的溶液中Na+物质的量浓度为
溶液加水稀释至100 mL,所得的溶液中Na+物质的量浓度为(4)100 mL
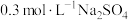 溶液和50 mL
溶液和50 mL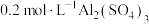 溶液混合后,溶液中
溶液混合后,溶液中 的物质的量浓度为
的物质的量浓度为(5)某同学配制的植物营养液中有4种离子,其中所含的
 、
、 、
、 的物质的量浓度分别为
的物质的量浓度分别为 、
、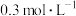 、
、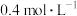 ,则
,则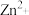 的物质的量浓度是
的物质的量浓度是
您最近一年使用:0次



