名校
1 . 回答下列问题:
(1)在标准状况下,1.7g氨气所占的体积约为_______ L,它与_______ 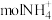 含有相同数目的电子。
含有相同数目的电子。
(2)某气态氧化物化学式为 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物中R的相对原子质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物中R的相对原子质量为_______ 。
(3)同温同压下, 与氦气的密度之比为
与氦气的密度之比为_______ ,若质量相同,两种气体的体积比为_______ 。
(4)在标准状况下,将A气体VL(摩尔质量是 )溶于0.5L水中,所得溶液的密度为
)溶于0.5L水中,所得溶液的密度为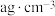 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为_______ 。
(5)现有含 和
和 的混合溶液200mL,其中
的混合溶液200mL,其中 物质的量浓度为
物质的量浓度为 ,
, 物质的量浓度为
物质的量浓度为 ,若向此溶液中加入一定量浓硫酸,使其配成
,若向此溶液中加入一定量浓硫酸,使其配成 和
和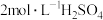 的混合溶液。请问最终所得混合溶液的体积是
的混合溶液。请问最终所得混合溶液的体积是_______ mL,需加入密度为 、质量分数为98%的浓硫酸
、质量分数为98%的浓硫酸_______ mL(保留到小数点后1位)。
(1)在标准状况下,1.7g氨气所占的体积约为
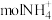 含有相同数目的电子。
含有相同数目的电子。(2)某气态氧化物化学式为
 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物中R的相对原子质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物中R的相对原子质量为(3)同温同压下,
 与氦气的密度之比为
与氦气的密度之比为(4)在标准状况下,将A气体VL(摩尔质量是
 )溶于0.5L水中,所得溶液的密度为
)溶于0.5L水中,所得溶液的密度为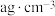 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为(5)现有含
 和
和 的混合溶液200mL,其中
的混合溶液200mL,其中 物质的量浓度为
物质的量浓度为 ,
, 物质的量浓度为
物质的量浓度为 ,若向此溶液中加入一定量浓硫酸,使其配成
,若向此溶液中加入一定量浓硫酸,使其配成 和
和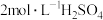 的混合溶液。请问最终所得混合溶液的体积是
的混合溶液。请问最终所得混合溶液的体积是 、质量分数为98%的浓硫酸
、质量分数为98%的浓硫酸
您最近一年使用:0次
解答题-实验探究题
|
较易(0.85)
|
名校
解题方法
2 . 实验室用固体KCl配制0.5mol/L的KCl溶液450mL,有以下仪器:①烧杯②胶头滴管③1000mL容量瓶④500mL容量瓶⑤玻璃棒⑥托盘天平(带砝码)⑦酒精灯⑧药匙
(1)配制时时使用的仪器有_______ (填代号)。
(2)该实验两次用到玻璃棒,其作用分别是_______ 、_______ 。
(3)配制时一般可分为以下几个步骤:①称量②计算③转移④溶解⑤摇匀⑥定容⑦洗涤⑧冷却。其正确的操作顺序为_______
(4)试计算应称取的KCl固体的质量为_______  。取出配制后的该KCl溶液10mL加水稀释到100mL,稀释后溶液中KCl的物质的量浓度是
。取出配制后的该KCl溶液10mL加水稀释到100mL,稀释后溶液中KCl的物质的量浓度是_______ 。
(5)下列操作对KCl溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“不变”)。
①摇匀后发现液面低于刻度线再加水_______ ;
②定容时俯视观察液面_______ 。
(1)配制时时使用的仪器有
(2)该实验两次用到玻璃棒,其作用分别是
(3)配制时一般可分为以下几个步骤:①称量②计算③转移④溶解⑤摇匀⑥定容⑦洗涤⑧冷却。其正确的操作顺序为
(4)试计算应称取的KCl固体的质量为
 。取出配制后的该KCl溶液10mL加水稀释到100mL,稀释后溶液中KCl的物质的量浓度是
。取出配制后的该KCl溶液10mL加水稀释到100mL,稀释后溶液中KCl的物质的量浓度是(5)下列操作对KCl溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“不变”)。
①摇匀后发现液面低于刻度线再加水
②定容时俯视观察液面
您最近一年使用:0次
名校
3 . 回答下列问题:
(1)已知 与浓盐酸室温下可发生如下反应:
与浓盐酸室温下可发生如下反应: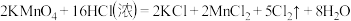 ,氧化剂和还原剂的物质的量之比为
,氧化剂和还原剂的物质的量之比为_______ ,生成标准状况下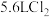 ,时消耗的
,时消耗的 的物质的量为
的物质的量为_______ 。
(2)质量比为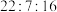 的
的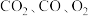 ,其物质的量之比为
,其物质的量之比为_______ 。
(3)某盐混合溶液中含有离子: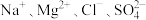 ,测得
,测得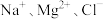 的物质的量浓度依次为:
的物质的量浓度依次为: ,则
,则
_______ 。
(1)已知
 与浓盐酸室温下可发生如下反应:
与浓盐酸室温下可发生如下反应: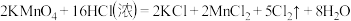 ,氧化剂和还原剂的物质的量之比为
,氧化剂和还原剂的物质的量之比为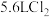 ,时消耗的
,时消耗的 的物质的量为
的物质的量为(2)质量比为
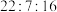 的
的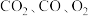 ,其物质的量之比为
,其物质的量之比为(3)某盐混合溶液中含有离子:
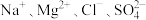 ,测得
,测得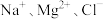 的物质的量浓度依次为:
的物质的量浓度依次为: ,则
,则
您最近一年使用:0次
名校
4 . 下列说法正确的是
A.同浓度的 、 、 、 、 溶液体积之比为 溶液体积之比为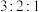 ,则 ,则 浓度之比为 浓度之比为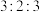 |
B.将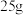 胆矾( 胆矾( )溶于水配成 )溶于水配成 溶液,该溶液的物质的量浓度为 溶液,该溶液的物质的量浓度为 |
C.欲将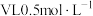 的盐酸浓度增大1倍,可将溶液加热浓缩到原体积的一半 的盐酸浓度增大1倍,可将溶液加热浓缩到原体积的一半 |
D.将 的 的 溶液和 溶液和 的 的 溶液等体积混合后,若忽略溶液体积变化, 溶液等体积混合后,若忽略溶液体积变化,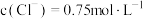 |
您最近一年使用:0次
2023-12-19更新
|
166次组卷
|
3卷引用:陕西省宝鸡市渭滨区2023-2024学年高一上学期期末考试化学试题
5 . 回答下列问题
(1)①石墨 ②苛性钠 ③石灰乳 ④熔融氯化钾 ⑤盐酸 ⑥氨气 ⑦蔗糖 ⑧铁⑨液态氯化氢 ⑩硫酸溶液,上述物质中能导电且属于电解质的是___________ ,属于混合物的是___________ (填编号)
(2)按要求进行化学计算:
①在同温、同压、同体积的条件下, 与某气体A的质量之比是1:16,则A的摩尔质量为
与某气体A的质量之比是1:16,则A的摩尔质量为___________ 。
②一定量的Al、Mg混合物加入一定物质的量浓度、一定体积的盐酸溶液中恰好完全反应,放出标况下11.2L气体,再向溶液中加入 氢氧化钠溶液恰好使溶液中金属阳离子完全沉淀,则需要氢氧化钠溶液的体积为
氢氧化钠溶液恰好使溶液中金属阳离子完全沉淀,则需要氢氧化钠溶液的体积为___________ mL。
③相同体积的 、
、 、
、 溶液,分别与足量的
溶液,分别与足量的 溶液反应,当生成的
溶液反应,当生成的 质量相同时,则三种溶液的物质的量浓度之比为
质量相同时,则三种溶液的物质的量浓度之比为___________ 。
(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为
①配平该反应:_______

②当有32g硫单质完全反应时,生成氧化产物的物质的量是___________ mol。
(1)①石墨 ②苛性钠 ③石灰乳 ④熔融氯化钾 ⑤盐酸 ⑥氨气 ⑦蔗糖 ⑧铁⑨液态氯化氢 ⑩硫酸溶液,上述物质中能导电且属于电解质的是
(2)按要求进行化学计算:
①在同温、同压、同体积的条件下,
 与某气体A的质量之比是1:16,则A的摩尔质量为
与某气体A的质量之比是1:16,则A的摩尔质量为②一定量的Al、Mg混合物加入一定物质的量浓度、一定体积的盐酸溶液中恰好完全反应,放出标况下11.2L气体,再向溶液中加入
 氢氧化钠溶液恰好使溶液中金属阳离子完全沉淀,则需要氢氧化钠溶液的体积为
氢氧化钠溶液恰好使溶液中金属阳离子完全沉淀,则需要氢氧化钠溶液的体积为③相同体积的
 、
、 、
、 溶液,分别与足量的
溶液,分别与足量的 溶液反应,当生成的
溶液反应,当生成的 质量相同时,则三种溶液的物质的量浓度之比为
质量相同时,则三种溶液的物质的量浓度之比为(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为

①配平该反应:

②当有32g硫单质完全反应时,生成氧化产物的物质的量是
您最近一年使用:0次
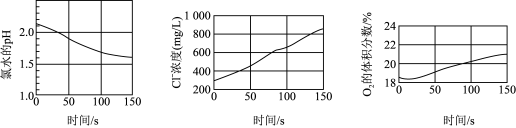
6 . 某兴趣小组利用数字化实验测定光照过程中氯水的 、氯水中氯离子的浓度、广口瓶中氧气的体积分数三者的变化,实验结果如图所示。下列说法正确的是
、氯水中氯离子的浓度、广口瓶中氧气的体积分数三者的变化,实验结果如图所示。下列说法正确的是
 、氯水中氯离子的浓度、广口瓶中氧气的体积分数三者的变化,实验结果如图所示。下列说法正确的是
、氯水中氯离子的浓度、广口瓶中氧气的体积分数三者的变化,实验结果如图所示。下列说法正确的是
A.氯水中存在自由移动的离子,能导电,但 属于非电解质 属于非电解质 |
B.氯水的 值随光照时间增加而减少,是因为次氯酸见光分解为酸性更强的酸 值随光照时间增加而减少,是因为次氯酸见光分解为酸性更强的酸 |
C.光照过程中 体积分数逐渐增加,说明发生了氧化还原反应,其中 体积分数逐渐增加,说明发生了氧化还原反应,其中 为还原产物 为还原产物 |
D.由图可知,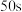 时 时 浓度约为 浓度约为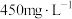 ,计算可知氯水中 ,计算可知氯水中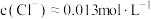 |
您最近一年使用:0次
名校
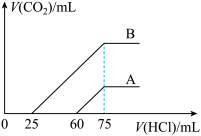
7 . 取A、B两份物质的量浓度相等的NaOH溶液,体积均为50mL,分别向其中通入一定量的 后,再分别稀释到100mL,在稀释后的溶液中分别滴加0.1mol/L的盐酸,产生的
后,再分别稀释到100mL,在稀释后的溶液中分别滴加0.1mol/L的盐酸,产生的 体积(标准状况)与所加盐酸的体积关系如图,下列说法正确的是
体积(标准状况)与所加盐酸的体积关系如图,下列说法正确的是
 后,再分别稀释到100mL,在稀释后的溶液中分别滴加0.1mol/L的盐酸,产生的
后,再分别稀释到100mL,在稀释后的溶液中分别滴加0.1mol/L的盐酸,产生的 体积(标准状况)与所加盐酸的体积关系如图,下列说法正确的是
体积(标准状况)与所加盐酸的体积关系如图,下列说法正确的是
A.原NaOH溶液的物质的量浓度 |
B.A曲线表明原溶液通入 后,所得溶质为 后,所得溶质为 和 和 且物质的量之比为1∶3 且物质的量之比为1∶3 |
C.B曲线表明原溶液通入 后,所得溶质为 后,所得溶质为 和 和 且物质的量之比为1∶l 且物质的量之比为1∶l |
D.B曲线表明原溶液通入 后,所得溶质与盐酸反应产生气体的最大体积为33.6mL标准状况) 后,所得溶质与盐酸反应产生气体的最大体积为33.6mL标准状况) |
您最近一年使用:0次
8 . 下列说法中正确的是
A.将 加入水中配成1L溶液,则所得溶液中溶质的物质的量浓度是 加入水中配成1L溶液,则所得溶液中溶质的物质的量浓度是 |
| B.用小刀切下一小块金属钠,将剩余的钠再放回原试剂瓶 |
C.标准状况下,将 气体溶于1L水中,所得溶液中溶质的物质的量浓度是 气体溶于1L水中,所得溶液中溶质的物质的量浓度是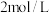 |
D.向某溶液中加入 溶液产生白色沉淀,再加稀盐酸沉淀不溶解,说明原溶液中一定含有 溶液产生白色沉淀,再加稀盐酸沉淀不溶解,说明原溶液中一定含有 |
您最近一年使用:0次
名校
解题方法
9 . 在相同体积、相同物质的量浓度的酸中,一定相等的是
| A.溶质的质量分数 | B.溶质的质量 |
| C.氢离子的物质的量 | D.溶质的物质的量 |
您最近一年使用:0次
2023-12-07更新
|
141次组卷
|
24卷引用:陕西省蓝田县城关中学大学区联考2022-2023学年高一下学期6月期末考试化学试题
陕西省蓝田县城关中学大学区联考2022-2023学年高一下学期6月期末考试化学试题辽宁省大连市2019-2020学年高一上学期期中考试化学试题湖北省荆州市沙市区沙市中学2019-2020学年高一化学过关训练9《化学计量在实验中的应用》山东省沂水县第四中学2020~2021学年高一上学期阶段检测化学试题浙江省台州市书生中学2020-2021学年高一上学期第三次月考化学试题(已下线)【浙江新东方】在线化学 (15)山东省济宁市2020-2021学年高一下学期期末联考化学试题湖南省怀化市第五中学2019-2020学年高一下学期期中考试化学试题人教2019版必修第一册第二章 海中的重要元素——钠和氯复习与提高云南省丽江市2021-2022学年高一上学期期末质量监测化学试题浙江省宁波市六校联盟2021-2022学年高一上学期期中考试化学试题天津市河东区普通高中2022年高二学业水平合格考试模拟化学试题辽宁省大连市2021-2022学年高一上学期期末考试化学试题黑龙江省密山市第四中学2021-2022学年高一上学期期中考试化学试题浙江省湖州市三贤联盟2022-2023学年高一上学期期中联考化学试题湖南省长沙市明德中学2022-2023学年高一上学期期中考试化学试题第4课时 物质的量浓度的有关计算(已下线)课时3 物质的量浓度贵州省贵阳市2023-2024学年清镇市博雅实验学校高一第三次月考化学贵州省清镇市博雅实验学校2023-2024学年高一上学期第四次月考化学试卷河北省石家庄市第二中学西校区2023-2024学年高一上学期12月月考化学试题广东省惠州市2023-2024学年高一上学期期末质量检测化学试题山东省济南市2023-2024学年高一上学期1月期末考试化学试题青海省西宁市大通回族土族自治县第二完全中学2022-2023学年高一下学期开学检测化学试卷
解题方法
10 . 实验室用密度为1.84g/mL,质量分数为98%浓硫酸配制250mL0.1mol/L的硫酸溶液,填空并请回答下列问题:
(1)配制250mL0.1mol/L的硫酸溶液,需要量取浓硫酸的体积是_____ mL(精确到0.1);
(2)配制时,正确的操作顺序是(请按字母排序表示,每个字母只用一次)_____ ;
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓硫酸,沿玻璃棒倒入加入少量水(约30mL)的烧杯中,并用玻璃棒慢慢搅动,使其混合均匀,静置冷却
C.将已冷却的硫酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(3)若溶液注入容量瓶前未恢复到室温,则所配溶液浓度将_____ (填“偏高”、“偏低”或“无影响”,下同),若定容时俯视刻度线则所配溶液浓度将_____ 。
(1)配制250mL0.1mol/L的硫酸溶液,需要量取浓硫酸的体积是
(2)配制时,正确的操作顺序是(请按字母排序表示,每个字母只用一次)
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓硫酸,沿玻璃棒倒入加入少量水(约30mL)的烧杯中,并用玻璃棒慢慢搅动,使其混合均匀,静置冷却
C.将已冷却的硫酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(3)若溶液注入容量瓶前未恢复到室温,则所配溶液浓度将
您最近一年使用:0次



