1 . 根据所学知识,回答下列问题:
(1)分类在化学学习中起着非常重要的作用,下列分类标准合理的是___ (填标号)。
(2)现有以下六种物质:①NaCl溶液,②Cl2,③HClO,④蔗糖,⑤NaOH固体,⑥稀硫酸。其中属于电解质的是___ (填序号)。
(3)化学计量是化学定量研究的基础。
①3.01×1023个CH4分子的物质的量为___ mol,质量为___ g。
②将30mL0.5mol•L-1NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为___ mol•L-1。
③等质量的H2S和NH3,其分子个数比N(H2S):N(NH3)=___ ,标准状况下气体的体积比V(H2S):V(NH3)= ___ 。
(4)食品干燥剂的作用是降低食品包装袋中的温度,防止食品变质腐败。CaO、CaCl2均可用作食品干燥剂。
①CaO吸水能力强的原理为____ (填化学方程式),CaO的保存方法为___ 。
②检验CaCl2溶液中Cl-存在的具体操作及现象为___ 。
(1)分类在化学学习中起着非常重要的作用,下列分类标准合理的是
| A.根据物质溶于水后形成的溶液呈碱性,可将此类物质归类为碱 |
| B.根据物质能否导电,将物质分为电解质和非电解质 |
| C.根据反应中是否有电子的转移,将化学反应分为氧化还原反应和非氧化还原反应 |
| D.根据分散系中分散质粒子的直径大小,将分散系分为溶液,胶体和浊液 |
(3)化学计量是化学定量研究的基础。
①3.01×1023个CH4分子的物质的量为
②将30mL0.5mol•L-1NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为
③等质量的H2S和NH3,其分子个数比N(H2S):N(NH3)=
(4)食品干燥剂的作用是降低食品包装袋中的温度,防止食品变质腐败。CaO、CaCl2均可用作食品干燥剂。
①CaO吸水能力强的原理为
②检验CaCl2溶液中Cl-存在的具体操作及现象为
您最近一年使用:0次
解题方法
2 . 现有由硝酸钾、硝酸铵、硝酸镁组成的无土栽培液 ,部分离子的浓度如下表所示:
,部分离子的浓度如下表所示:
(1)混合液中,硝酸铵的物质的量为___________ ,硝酸钾的质量为___________ 。
(2)该混合溶液中硝酸镁的物质的量浓度为___________ ,将该混合溶液加水稀释至体积为 ,稀释后溶液中
,稀释后溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
(3)向该稀释后的溶液中通入标准状况下的
___________ L可使 沉淀完全,写出
沉淀完全,写出 沉淀过程中的离子方程式
沉淀过程中的离子方程式___________ 。
 ,部分离子的浓度如下表所示:
,部分离子的浓度如下表所示:| 离子种类 |  |  |  |
离子的物质的量浓度( ) ) | 0.2 | 0.1 | 0.6 |
(1)混合液中,硝酸铵的物质的量为
(2)该混合溶液中硝酸镁的物质的量浓度为
 ,稀释后溶液中
,稀释后溶液中 的物质的量浓度为
的物质的量浓度为(3)向该稀释后的溶液中通入标准状况下的

 沉淀完全,写出
沉淀完全,写出 沉淀过程中的离子方程式
沉淀过程中的离子方程式
您最近一年使用:0次
名校
3 . 将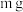 某二价金属氯化物溶于水中配成
某二价金属氯化物溶于水中配成 溶液,从中取出一半,再加水稀释到
溶液,从中取出一半,再加水稀释到 ,此时
,此时 的物质的量浓度为
的物质的量浓度为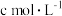 ,则此氯化物中金属原子的相对原子质量为
,则此氯化物中金属原子的相对原子质量为
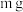 某二价金属氯化物溶于水中配成
某二价金属氯化物溶于水中配成 溶液,从中取出一半,再加水稀释到
溶液,从中取出一半,再加水稀释到 ,此时
,此时 的物质的量浓度为
的物质的量浓度为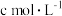 ,则此氯化物中金属原子的相对原子质量为
,则此氯化物中金属原子的相对原子质量为A.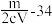 | B.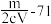 | C.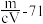 | D.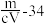 |
您最近一年使用:0次
2021-11-06更新
|
648次组卷
|
4卷引用:四川省成都市蓉城名校联盟2021-2022学年高一上学期期中联考化学试题
4 . 实验室有质量分数为98%,密度为 的浓硫酸,现需配制浓度为
的浓硫酸,现需配制浓度为 ,体积为
,体积为 的稀硫酸,则所需浓硫酸的体积为
的稀硫酸,则所需浓硫酸的体积为
 的浓硫酸,现需配制浓度为
的浓硫酸,现需配制浓度为 ,体积为
,体积为 的稀硫酸,则所需浓硫酸的体积为
的稀硫酸,则所需浓硫酸的体积为
A.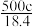 | B.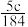 | C.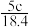 | D.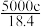 |
您最近一年使用:0次
2021-11-06更新
|
272次组卷
|
3卷引用:四川省成都市蓉城名校联盟2021-2022学年高一上学期期中联考化学试题
名校
解题方法
5 . 根据所学知识,按要求填写下列空格。
(1)约含 个氧原子的
个氧原子的 的物质的量为
的物质的量为___________  ,与上述
,与上述 中所含原子总数相同的
中所含原子总数相同的 标准状况下体积是
标准状况下体积是___________ L;
(2) 硫酸铝溶液中,
硫酸铝溶液中,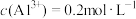 ,则
,则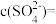
___________  ;将该溶液稀释至
;将该溶液稀释至 ,稀释后溶液中的
,稀释后溶液中的 的物质的量为
的物质的量为___________  。
。
(3) 某金属硝酸盐
某金属硝酸盐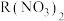 中含有
中含有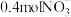 ,则
,则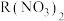 的摩尔质量为
的摩尔质量为___________ , 的相对原子质量为
的相对原子质量为___________ 。
(4)现有标准状况下 和
和 混合气体为
混合气体为 ,其质量为
,其质量为 ,则此混合气体中,
,则此混合气体中, 和
和 的物质的量之比为
的物质的量之比为___________ ,C和O原子个数比为___________ 。
(1)约含
 个氧原子的
个氧原子的 的物质的量为
的物质的量为 ,与上述
,与上述 中所含原子总数相同的
中所含原子总数相同的 标准状况下体积是
标准状况下体积是(2)
 硫酸铝溶液中,
硫酸铝溶液中,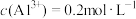 ,则
,则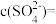
 ;将该溶液稀释至
;将该溶液稀释至 ,稀释后溶液中的
,稀释后溶液中的 的物质的量为
的物质的量为 。
。(3)
 某金属硝酸盐
某金属硝酸盐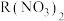 中含有
中含有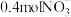 ,则
,则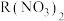 的摩尔质量为
的摩尔质量为 的相对原子质量为
的相对原子质量为(4)现有标准状况下
 和
和 混合气体为
混合气体为 ,其质量为
,其质量为 ,则此混合气体中,
,则此混合气体中, 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
名校
6 . 回答下列问题:
(1)某同学将标准状况下44.8 L的HCl气体溶于水,配成500 mL的溶液。所配成的盐酸溶液的物质的量浓度为___________ ,稀释到2 L,此时盐酸溶液物质的量浓度为___________ 。
(2)在400mL 2 的
的 溶液中,溶质的质量是
溶液中,溶质的质量是___________ ,此溶液中的 的物质的量浓度为
的物质的量浓度为___________ 。
(3)在氨水溶液中,有多种微粒, 的摩尔质量为
的摩尔质量为___________ ,1mol  含有的电子数目为
含有的电子数目为___________ ,1mol  含有的质子数目为
含有的质子数目为___________ 。
(1)某同学将标准状况下44.8 L的HCl气体溶于水,配成500 mL的溶液。所配成的盐酸溶液的物质的量浓度为
(2)在400mL 2
 的
的 溶液中,溶质的质量是
溶液中,溶质的质量是 的物质的量浓度为
的物质的量浓度为(3)在氨水溶液中,有多种微粒,
 的摩尔质量为
的摩尔质量为 含有的电子数目为
含有的电子数目为 含有的质子数目为
含有的质子数目为
您最近一年使用:0次
名校
7 . 根据所学知识填空:
(1)___________ mol H2O中含有的氧原子数与1.5 mol CO2中含有的氧原子数相等。
(2)标准状况下,4.48L NH3中N原子质量为___________ g,H原子数目为___________ 。
(3)已知a g A和b g B恰好完全反应生成0.2 mol C和d g D,则C的摩尔质量为___________ (用含a、b、d的表达式表示)。
(4)NA为阿伏加德罗常数,标准状况下,m g某气体中含有b个分子,则n g该气体在相同状态下的体积为___________ L(用含m、n、b、NA的表达式表示)
(5)将80.0 g无水硫酸铁溶于水配制成500 mL溶液,若从中取出50 mL,用水稀释到100 mL,所得溶液中Fe3+的物质的量浓度为___________ 。
(1)
(2)标准状况下,4.48L NH3中N原子质量为
(3)已知a g A和b g B恰好完全反应生成0.2 mol C和d g D,则C的摩尔质量为
(4)NA为阿伏加德罗常数,标准状况下,m g某气体中含有b个分子,则n g该气体在相同状态下的体积为
(5)将80.0 g无水硫酸铁溶于水配制成500 mL溶液,若从中取出50 mL,用水稀释到100 mL,所得溶液中Fe3+的物质的量浓度为
您最近一年使用:0次
名校
解题方法
8 . 下列说法正确的是
| A.某气体X相对氢气的密度是16,则该气体的摩尔质量为32 |
B.V L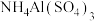 溶液中含a g 溶液中含a g  ,取此溶液 ,取此溶液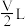 用水稀释为5V L,则稀释后溶液中 用水稀释为5V L,则稀释后溶液中 为 为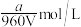 (不考虑水解) (不考虑水解) |
C.常温常压下,同质量的气体X和气体Y,体积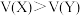 ,则摩尔质量 ,则摩尔质量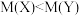 |
D.m g气体Y含分子数为b,则n g该气体在标准状况下体积为( 为阿伏加德罗常数的值) 为阿伏加德罗常数的值)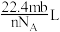 |
您最近一年使用:0次
2021-10-17更新
|
173次组卷
|
2卷引用:江西省抚州市临川区第十中学2022届高三月考化学试卷
名校
9 . 某同学用溶质质量分数为15%的稀盐酸和大理石反应来制取二氧化碳气体:
(1)用20.3g溶质质量分数为37%的浓盐酸能配制上述稀盐酸___ g(结果精确到1g)。
(2)若需收集10瓶(每瓶以125mL计算)二氧化碳气体,问至少需要多少克上述稀盐酸与足量的大理石反应才能制得___ (实验条件下二氧化碳的密度为2g/L)?(写出计算过程,结果精确到0.01g)
(1)用20.3g溶质质量分数为37%的浓盐酸能配制上述稀盐酸
(2)若需收集10瓶(每瓶以125mL计算)二氧化碳气体,问至少需要多少克上述稀盐酸与足量的大理石反应才能制得
您最近一年使用:0次
2021-09-27更新
|
75次组卷
|
2卷引用:四川省绵阳南山中学2021-2022学年高一上学期入学考试化学试题
名校
解题方法
10 . 硫酸和氢氟酸(HF)的溶液可作为矿物中稀有元素的萃取液。实验室模拟生产该萃取液,要求萃取液中硫酸的浓度为2mol·L-1,氢氟酸的浓度为4mol·L-1。现有一批回收酸液共40mL,经测定其中氢氟酸浓度25mol·L-1,硫酸的浓度为1mol·L-1。
(1)现要用此回收酸配制上述萃取液,40mL回收酸液经稀释可以得到4mol·L-1的氢氟酸的体积为___________ mL。
(2)在40mL回收酸中加入___________ mL密度为1.84g·cm-3、浓度为98%的浓硫酸,然后再稀释得到符合要求的萃取液。在此过程中,配制该萃取液所需玻璃仪器有烧杯、玻璃棒、试剂瓶、胶头滴管、量筒和___________ 。若加入浓硫酸后,立刻定容至相应体积,则所得浓度会___________ (填“偏大”或“偏小”或“不变”)
(1)现要用此回收酸配制上述萃取液,40mL回收酸液经稀释可以得到4mol·L-1的氢氟酸的体积为
(2)在40mL回收酸中加入
您最近一年使用:0次



