1 . 类比是研究物质性质的常用方法之一、下列类比正确的是
①Cu与 能化合生成
能化合生成 ,则Fe与
,则Fe与 能化合生成
能化合生成
②Mg在空气中燃烧生成MgO,则Na在空气中燃烧生成
③ 可以治疗胃酸过多,则NaOH也可以治疗胃酸过多
可以治疗胃酸过多,则NaOH也可以治疗胃酸过多
④Fe可以置换出 溶液中的铜,则Al也可以置换出
溶液中的铜,则Al也可以置换出 溶液中的铜
溶液中的铜
①Cu与
 能化合生成
能化合生成 ,则Fe与
,则Fe与 能化合生成
能化合生成
②Mg在空气中燃烧生成MgO,则Na在空气中燃烧生成

③
 可以治疗胃酸过多,则NaOH也可以治疗胃酸过多
可以治疗胃酸过多,则NaOH也可以治疗胃酸过多④Fe可以置换出
 溶液中的铜,则Al也可以置换出
溶液中的铜,则Al也可以置换出 溶液中的铜
溶液中的铜| A.①④ | B.②③ | C.①③ | D.②④ |
您最近半年使用:0次
解题方法
2 . 甲,乙两份等质量的NaHCO3固体,将甲充分加热后,再加入足量盐酸,乙不加热也加入足量盐酸,反应完全后,甲,乙两份中实际参加反应的盐酸的质量比为
| A.1∶1.5 | B.2∶1 | C.1∶2 | D.1∶1 |
您最近半年使用:0次
3 . 化学与生活、生产息息相关。请回答下列问题:
(1)以下为中学化学中常见的几种物质:①二氧化碳;②熔融KCl;③NaHSO4固体;④铜;⑤H2SO4溶液;⑥澄清石灰水,其中属于电解质的有_______ (填序号,下同),属于非电解质的有_______ 。
(2)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。用小苏打片治疗胃酸过多的离子方程式为_______ 。
(3)工业上制备漂白粉常将氯气通入冷的石灰乳中,发生反应的化学方程式为_______ 。
(4)储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,发生的化学反应如下:
①配平化学方程式_______ :
_______C+_______K2Cr2O7+_______H2SO4=_______K2SO4+_______CO2↑+_______Cr2(SO4)3+_______H2O。
②在上述反应中生成标准状况下的11.2LCO2,转移电子数为_______ 。
(1)以下为中学化学中常见的几种物质:①二氧化碳;②熔融KCl;③NaHSO4固体;④铜;⑤H2SO4溶液;⑥澄清石灰水,其中属于电解质的有
(2)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。用小苏打片治疗胃酸过多的离子方程式为
(3)工业上制备漂白粉常将氯气通入冷的石灰乳中,发生反应的化学方程式为
(4)储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,发生的化学反应如下:
①配平化学方程式
_______C+_______K2Cr2O7+_______H2SO4=_______K2SO4+_______CO2↑+_______Cr2(SO4)3+_______H2O。
②在上述反应中生成标准状况下的11.2LCO2,转移电子数为
您最近半年使用:0次
解题方法
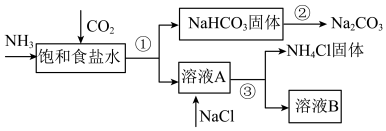
4 . 我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。
联合制碱法的主要流程如下(部分物质已略去):___________ (填序号)。
(2)纯碱属于___________ (填“酸”“碱”或“盐”)。
(3)根据上述流程图,将化学方程式补充完整:___________ 。
 +___________+___________=___________↓+
+___________+___________=___________↓+
(4)向饱和食盐水中应先通___________ (填“ ”或“
”或“ ”)。
”)。
(5)煅烧 固体的化学方程式是
固体的化学方程式是___________ 。
(6)下列联合制碱法流程说法正确的是___________ (填字母)。
a.副产物 可用作肥料
可用作肥料
b.溶液B中一定含有 、
、 、
、
c.①中 析出是因为
析出是因为 不溶于水
不溶于水
(7)②这个步骤生成的产物可以循环使用的是___________ (填化学式)。
联合制碱法的主要流程如下(部分物质已略去):
(2)纯碱属于
(3)根据上述流程图,将化学方程式补充完整:
 +___________+___________=___________↓+
+___________+___________=___________↓+
(4)向饱和食盐水中应先通
 ”或“
”或“ ”)。
”)。(5)煅烧
 固体的化学方程式是
固体的化学方程式是(6)下列联合制碱法流程说法正确的是
a.副产物
 可用作肥料
可用作肥料b.溶液B中一定含有
 、
、 、
、
c.①中
 析出是因为
析出是因为 不溶于水
不溶于水(7)②这个步骤生成的产物可以循环使用的是
您最近半年使用:0次
解题方法
5 . A、B、C、D四种化合物均由前三周期元素组成,其中A含有四种元素,A、B、C的焰色反应均为黄色,C为强碱,D为产生温室气体效应的气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。
(1)反应①的化学方程式为___________ 。
(2)反应②的离子方程式为___________ 。
(3)向B溶液中加入熟石灰可制烧碱,该反应的化学方程式为___________ 。
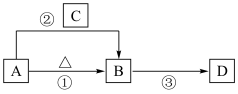
(1)反应①的化学方程式为
(2)反应②的离子方程式为
(3)向B溶液中加入熟石灰可制烧碱,该反应的化学方程式为
您最近半年使用:0次
解题方法
6 . 化学与生产生活息息相关,下列生产生活实例与所述化学知识没有关联的是
| 选项 | 生产生活实例 | 化学知识 |
| A | 补铁剂与维生素C同时服用效果更佳 | 维生素C具有还原性 |
| B | 用小苏打作发泡剂烘焙面包 | NaHCO3可与酸反应产生气体 |
| C | 用Na2S标准液检测污水中Cu2+含量 | CuS属于难溶电解质 |
| D | 用聚乙烯塑料制作食品保鲜膜 | 聚乙烯燃烧能生成CO2和H2O |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
7 . 下列对应离子方程式正确的是
| A | 向饱和 溶液中通入过量 溶液中通入过量 | 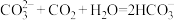 |
| B |  溶液中加入过量的 溶液中加入过量的 溶液 溶液 | 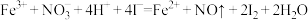 |
| C |  溶液与过量石灰水反应 溶液与过量石灰水反应 |  |
| D |  溶液中通入少量 溶液中通入少量 气体 气体 | 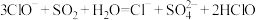 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-04-29更新
|
673次组卷
|
2卷引用:2024届陕西省榆林市高三下学期第二次模拟检测理科综合试题-高中化学
解题方法
8 . 生活离不开化学,生活中有许多中学化学常见的物质,它们的主要成分如下表:
回答下列问题:
(1) 中所含化学键类型为
中所含化学键类型为___________ (填“离子键”或“共价键”)。
(2)明矾可用来制备氢氧化铝,请选择与之反应的最佳试剂:___________ (填“氨水”或“氢氧化钠溶液”)。
(3) 的电离方程式为
的电离方程式为___________ 。
(4) 溶液中混有少量
溶液中混有少量 ,可加适量的
,可加适量的 溶液除杂,离子方程式为
溶液除杂,离子方程式为___________ , 固体中若含有少量
固体中若含有少量 固体,可采取的除杂方法为
固体,可采取的除杂方法为___________ 。
(5)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:___________ 。
(6) 属于
属于___________ 电解质(填“强”、“弱”或“非”)。
| 商品 | 食盐 | 明矾 | 84消毒液 |
| 主要成分 | ① | ② | ③ |
| 商品 | 发酵粉 | 白醋 | 洁厕灵 |
| 主要成分 | ④ | ⑤ | ⑥ |
(1)
 中所含化学键类型为
中所含化学键类型为(2)明矾可用来制备氢氧化铝,请选择与之反应的最佳试剂:
(3)
 的电离方程式为
的电离方程式为(4)
 溶液中混有少量
溶液中混有少量 ,可加适量的
,可加适量的 溶液除杂,离子方程式为
溶液除杂,离子方程式为 固体中若含有少量
固体中若含有少量 固体,可采取的除杂方法为
固体,可采取的除杂方法为(5)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:
(6)
 属于
属于
您最近半年使用:0次
解题方法
9 . 质量为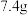 的
的 、
、 、
、 组成的固体混合物溶于水配成
组成的固体混合物溶于水配成 溶液,其中
溶液,其中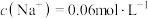 。若把等质量的固体混合物加热至恒重,残留固体的质量是
。若把等质量的固体混合物加热至恒重,残留固体的质量是
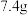 的
的 、
、 、
、 组成的固体混合物溶于水配成
组成的固体混合物溶于水配成 溶液,其中
溶液,其中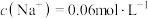 。若把等质量的固体混合物加热至恒重,残留固体的质量是
。若把等质量的固体混合物加热至恒重,残留固体的质量是A.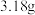 | B.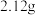 | C.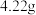 | D. |
您最近半年使用:0次
10 . 下列有关Na2CO3和NaHCO3的性质,叙述错误的是
A.鉴别Na2CO3和NaHCO3可以用BaCl2溶液,不可用 溶液 溶液 |
| B.Na2CO3比NaHCO3更稳定 |
| C.NaHCO3可以用于泡沫灭火器的反应物质 |
| D.除去NaHCO3溶液中混有的少量Na2CO3,用加热法 |
您最近半年使用:0次



