名校
解题方法
1 . (1)汽车尾气中的CO、NO、NO2等有毒气体会危害人体健康,可在汽车尾部加催化转化器,将有毒气体转化为无毒气体。
已知:①2NO(g)+O2(g)=2NO2(g) △H1=-112.3kJ·mol-1
②NO2(g)+CO(g)=NO(g)+CO2(g) △H2=-234kJ·mol-1
③N2(g)+O2(g)=2NO(g) △H3=+179.5kJ·mol-1
请写出CO和NO2生成无污染气体的热化学方程式___ 。
(2)若将CO和NO按不同比例投入一密闭容器中发生反应:2CO(g)+2NO(g) N2(g)+2CO2(g) △H=-759.8kJ·mol-1,反应达到平衡时,N2的体积分数随n(CO)/n(NO)的变化曲线如图1。
N2(g)+2CO2(g) △H=-759.8kJ·mol-1,反应达到平衡时,N2的体积分数随n(CO)/n(NO)的变化曲线如图1。

①b点时,平衡体系中C、N原子个数之比接近___ ;
②a、b、c三点CO的转化率从大到小的顺序为___ ;a、c、d三点的平衡常数从大到小的顺序为___ 。
③若n(CO)/n(NO)=0.8,反应达平衡时,N2的体积分数为20%,则CO的转化率为__ 。
(3)若将NO2与O2通入甲中设计成如图2所示装置,D电极上有红色物质析出,则A电极处通入的气体为____ (填化学式);A电极的电极反应式为____ ;一段时间后,若乙中需加0.2molCu(OH)2使溶液复原,则转移的电子数为___ 。
(4)已知:25℃时,H2C2O4的电离常数Ka1=5.9×10—2,Ka2=6.4×10-5,则25℃时,0.1mol·L-1NaHC2O4溶液中各离子浓度由大到小的顺序为____ ,若向该溶液中加入一定量NaOH固体,使c(HC2O4-)=c(C2O42-),则此时溶液呈___ (填“酸性”“碱性”或“中性”)。
已知:①2NO(g)+O2(g)=2NO2(g) △H1=-112.3kJ·mol-1
②NO2(g)+CO(g)=NO(g)+CO2(g) △H2=-234kJ·mol-1
③N2(g)+O2(g)=2NO(g) △H3=+179.5kJ·mol-1
请写出CO和NO2生成无污染气体的热化学方程式
(2)若将CO和NO按不同比例投入一密闭容器中发生反应:2CO(g)+2NO(g)
 N2(g)+2CO2(g) △H=-759.8kJ·mol-1,反应达到平衡时,N2的体积分数随n(CO)/n(NO)的变化曲线如图1。
N2(g)+2CO2(g) △H=-759.8kJ·mol-1,反应达到平衡时,N2的体积分数随n(CO)/n(NO)的变化曲线如图1。
①b点时,平衡体系中C、N原子个数之比接近
②a、b、c三点CO的转化率从大到小的顺序为
③若n(CO)/n(NO)=0.8,反应达平衡时,N2的体积分数为20%,则CO的转化率为
(3)若将NO2与O2通入甲中设计成如图2所示装置,D电极上有红色物质析出,则A电极处通入的气体为
(4)已知:25℃时,H2C2O4的电离常数Ka1=5.9×10—2,Ka2=6.4×10-5,则25℃时,0.1mol·L-1NaHC2O4溶液中各离子浓度由大到小的顺序为
您最近一年使用:0次
2019-10-31更新
|
229次组卷
|
2卷引用:吉林省吉林市2020届高三第三次调研测试(4月) 理综化学试题
解题方法
2 . 近期发现,H2S是继NO、CO之后的第三个生命体系气体信号分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
(1)下列事实中,不能比较硫与氯元素非金属性强弱的是____________ (填标号)。
A.将Cl2通入Na2S溶液中,有黄色浑浊出现 B.比较次氯酸和硫酸的酸性强弱
C.氯气与铁反应生成氯化铁,硫和铁反应生成硫化亚铁 D.还原性:H2S>HCl
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

通过计算,可知系统(Ⅰ)和系统(Ⅱ)制备氢气的热化学方程式分别为___________ 、_______ ,制得等量H2所需能量较少的是_______ 。
(3)H2S与CO2在高温下发生反应:H2S(g)+CO2(g) COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
①H2S的平衡转化率α1=______ %,反应平衡常数K=_____ 。(可用分数表示)
②在620 K重复试验,平衡后水的物质的量分数为0.03,H2S的转化率α2_________ α1,该反应的△H___ 0。(填“>”“<”或“=”)
③向反应器中再分别充入下列气体,能使H2S转化率增大的是____________ (填标号)
A.H2S B.CO2 C.COS D.N2
(1)下列事实中,不能比较硫与氯元素非金属性强弱的是
A.将Cl2通入Na2S溶液中,有黄色浑浊出现 B.比较次氯酸和硫酸的酸性强弱
C.氯气与铁反应生成氯化铁,硫和铁反应生成硫化亚铁 D.还原性:H2S>HCl
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

通过计算,可知系统(Ⅰ)和系统(Ⅱ)制备氢气的热化学方程式分别为
(3)H2S与CO2在高温下发生反应:H2S(g)+CO2(g)
 COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。①H2S的平衡转化率α1=
②在620 K重复试验,平衡后水的物质的量分数为0.03,H2S的转化率α2
③向反应器中再分别充入下列气体,能使H2S转化率增大的是
A.H2S B.CO2 C.COS D.N2
您最近一年使用:0次
名校
解题方法
3 . 碳、氮、硫的化合物在生产生活中广泛存在。请回答:
(1)以CO2与NH3为原料可合成化肥尿素[CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-l59.5kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l) ΔH=-160.5kJ·mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式__ 。
(2)T温度时在容积为2L的恒容密闭容器中只充入1.00molNO2气体发生反应:2NO(g)+O2(g) 2NO2(g) ∆H<0。不同时刻测得容器中n(NO2)如下表:
2NO2(g) ∆H<0。不同时刻测得容器中n(NO2)如下表:
①升高温度K值___ (增大、减小),T温度时化学平衡常数K=___ mol-1·L
②从0~2s该反应的平均速率v(NO2)=___ 。
③对可逆反应2NO(g)+O2(g) 2NO2(g) ∆H<0。恒温,恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是
2NO2(g) ∆H<0。恒温,恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是___ 。
A.混合气体的密度不再变化
B.混合气体的压强不再变化
C.氧气的转化率不再变化
D.N2、O2、NO的物质的量之比为1:1:2
(3)常温下,用SO2与NaOH溶液反应可得到NaHSO3、Na2SO3等。
①已知Na2SO3水溶液显碱性,原因是___ (写出主要反应的离子方程式),该溶液中,c(Na+)___ 2c(SO32-)+c(HSO3-)(填“>”“<”或“=”)。
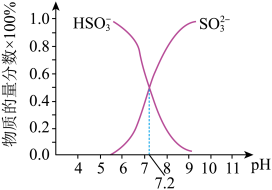
②在某NaHSO3、Na2SO3混合溶液中HSO3-、SO32-物质的量分数随pH变化曲线如图所示(部分),根据图示,则SO32-的第一步水解平衡常数=____ 。
(1)以CO2与NH3为原料可合成化肥尿素[CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-l59.5kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l) ΔH=-160.5kJ·mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式
(2)T温度时在容积为2L的恒容密闭容器中只充入1.00molNO2气体发生反应:2NO(g)+O2(g)
 2NO2(g) ∆H<0。不同时刻测得容器中n(NO2)如下表:
2NO2(g) ∆H<0。不同时刻测得容器中n(NO2)如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO2)/mol | 1.00 | 0.80 | 0.65 | 0.55 | 0.50 | 0.50 |
①升高温度K值
②从0~2s该反应的平均速率v(NO2)=
③对可逆反应2NO(g)+O2(g)
 2NO2(g) ∆H<0。恒温,恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是
2NO2(g) ∆H<0。恒温,恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是A.混合气体的密度不再变化
B.混合气体的压强不再变化
C.氧气的转化率不再变化
D.N2、O2、NO的物质的量之比为1:1:2
(3)常温下,用SO2与NaOH溶液反应可得到NaHSO3、Na2SO3等。
①已知Na2SO3水溶液显碱性,原因是
②在某NaHSO3、Na2SO3混合溶液中HSO3-、SO32-物质的量分数随pH变化曲线如图所示(部分),根据图示,则SO32-的第一步水解平衡常数=

您最近一年使用:0次
2020-04-30更新
|
73次组卷
|
2卷引用:吉林省长春市第二十九中学2020届高三上学期期末考试化学试题
4 . 氨和肼(N2H4)都是氮元素的重要氢化物,在工农业生产、生活中有广泛应用。
(1)工业中常用以下反应合成氨:N2+3H2 2NH3△H<0。某实验室在三个不同条件的密闭容器中,分别加入浓度均为c(N2)=0.100mol/L,c(H2)=0.300mol/L进行反应时,N2的浓度随时间的变化如下图①、②、③曲线所示:
2NH3△H<0。某实验室在三个不同条件的密闭容器中,分别加入浓度均为c(N2)=0.100mol/L,c(H2)=0.300mol/L进行反应时,N2的浓度随时间的变化如下图①、②、③曲线所示:

装置③仅有一个反应条件与①不同,该条件为_______________ ,实验②平衡时H2的转化率为_____________ ;
(2)肼是一种具有强还原性的无色油状液体,可用作燃料。
①在火箭推进器中装有胼(N2H4)和液态H2O2,已知0.4mol液态N2H4和足量液态H2O2反应,生成气态N2和气态H2O,放出256.6kJ的热量。该反应的热化学方程式为_____________________________________________________ 。
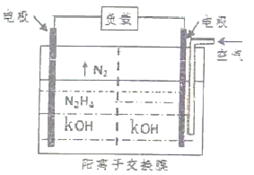
②肼(N2H4)-空气燃料电池是一种环保型碱性燃料电池,电解质溶液是20%-30%的KOH溶液。已知肼在101kPa、25℃条件下的燃烧热为624kJ·mol-1,如果此燃料电池的能量转化率为50%,当消耗空气2.24L(已折算为标准状况下体积)时,则此电池产生的电能约为_________ kJ。(假设空气中氧气的体积含量为20%,产物为液态水)
(3)肼又称“联氨”,为二元弱碱,在水中的电离方程式与氨相似,肼第一步电离反应的平衡常数值为____________ .(已知:N2H4+H+ N2H5+的K=8.7×107;KW=1.0×10-14)
N2H5+的K=8.7×107;KW=1.0×10-14)
(1)工业中常用以下反应合成氨:N2+3H2
 2NH3△H<0。某实验室在三个不同条件的密闭容器中,分别加入浓度均为c(N2)=0.100mol/L,c(H2)=0.300mol/L进行反应时,N2的浓度随时间的变化如下图①、②、③曲线所示:
2NH3△H<0。某实验室在三个不同条件的密闭容器中,分别加入浓度均为c(N2)=0.100mol/L,c(H2)=0.300mol/L进行反应时,N2的浓度随时间的变化如下图①、②、③曲线所示:
装置③仅有一个反应条件与①不同,该条件为
(2)肼是一种具有强还原性的无色油状液体,可用作燃料。
①在火箭推进器中装有胼(N2H4)和液态H2O2,已知0.4mol液态N2H4和足量液态H2O2反应,生成气态N2和气态H2O,放出256.6kJ的热量。该反应的热化学方程式为
②肼(N2H4)-空气燃料电池是一种环保型碱性燃料电池,电解质溶液是20%-30%的KOH溶液。已知肼在101kPa、25℃条件下的燃烧热为624kJ·mol-1,如果此燃料电池的能量转化率为50%,当消耗空气2.24L(已折算为标准状况下体积)时,则此电池产生的电能约为

(3)肼又称“联氨”,为二元弱碱,在水中的电离方程式与氨相似,肼第一步电离反应的平衡常数值为
 N2H5+的K=8.7×107;KW=1.0×10-14)
N2H5+的K=8.7×107;KW=1.0×10-14)
您最近一年使用:0次
解题方法
5 . H2S是存在于燃气中的一种有害气体,脱除H2S的方法有很多。
(1)国内有学者设计了“Cu2+一沉淀氧化”法脱除H2S。该法包括生成CuS沉淀,氧化CuS(Cu2++CuS+4Cl—=S+2CuCl2—)及空气氧化CuCl2—再生Cu2+。
①反应H2S(aq)+Cu2+(aq)⇌CuS(s)+2H+(aq)的K=__________
②再生Cu2+反应的离子方程式为____________ 。
(2)采用生物脱硫技术时,H2S与碱反应转化为HS-,在脱氮硫杆菌参与下,HS-被NO3-氧化为SO42—、NO3—被还原为N2。当33.6 m3(标准状况)某燃气(H2S的含量为0.2%)脱硫时,消耗NO3—的物质的量为___ mol。
(3)已知下列热化学方程式:
Ⅰ.H2(g)+ O2(g)=H2O(l) ∆H1=-285.8kJ∙mol-1
O2(g)=H2O(l) ∆H1=-285.8kJ∙mol-1
Ⅱ. H2(g)+S(s)=H2S(g) ∆H2=-20.6kJ∙mol-1
Ⅲ.S(s)+O2(g)=SO2(g) ∆H3=-296.8kJ∙mol-1
则以Claus法脱除H2S的反应:2H2S(g)+SO2 (g)=3S(s)+2H2O(1) △H=________ kJ/mol。
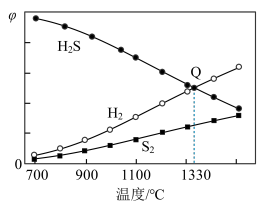
(4)101 kPa下,H2S分解:2H2S(g) ⇌ 2H2(g)+S2(g)。保持压强不变,反应达到平衡时,气体的体积分数(φ)随温度的变化曲线如图:
①在密闭容器中,关于反应2H2S(g) ⇌ 2H2(g)+S2 (g)的说法正确的是____ (填字母)。
A.Kp随温度的升高而增大
B.低压有利于提高HpS的平衡分解率
C.维持温度、气体总压强不变时,向平衡体系中通入氩气,则v(正)<v(逆)
D.在恒容密闭容器中进行反应,当气体密度不再变化时,反应达到平衡状态
②图中Q点:H2S的平衡转化率为____ ;S2(g)的分压为____ kPa;1330℃时,反应2H2S(g) ⇌ 2H2(g)+S2(g)的Kp=_____ (Kp为以分压表示的平衡常数)。
(1)国内有学者设计了“Cu2+一沉淀氧化”法脱除H2S。该法包括生成CuS沉淀,氧化CuS(Cu2++CuS+4Cl—=S+2CuCl2—)及空气氧化CuCl2—再生Cu2+。
①反应H2S(aq)+Cu2+(aq)⇌CuS(s)+2H+(aq)的K=
②再生Cu2+反应的离子方程式为
(2)采用生物脱硫技术时,H2S与碱反应转化为HS-,在脱氮硫杆菌参与下,HS-被NO3-氧化为SO42—、NO3—被还原为N2。当33.6 m3(标准状况)某燃气(H2S的含量为0.2%)脱硫时,消耗NO3—的物质的量为
(3)已知下列热化学方程式:
Ⅰ.H2(g)+
 O2(g)=H2O(l) ∆H1=-285.8kJ∙mol-1
O2(g)=H2O(l) ∆H1=-285.8kJ∙mol-1Ⅱ. H2(g)+S(s)=H2S(g) ∆H2=-20.6kJ∙mol-1
Ⅲ.S(s)+O2(g)=SO2(g) ∆H3=-296.8kJ∙mol-1
则以Claus法脱除H2S的反应:2H2S(g)+SO2 (g)=3S(s)+2H2O(1) △H=
(4)101 kPa下,H2S分解:2H2S(g) ⇌ 2H2(g)+S2(g)。保持压强不变,反应达到平衡时,气体的体积分数(φ)随温度的变化曲线如图:

①在密闭容器中,关于反应2H2S(g) ⇌ 2H2(g)+S2 (g)的说法正确的是
A.Kp随温度的升高而增大
B.低压有利于提高HpS的平衡分解率
C.维持温度、气体总压强不变时,向平衡体系中通入氩气,则v(正)<v(逆)
D.在恒容密闭容器中进行反应,当气体密度不再变化时,反应达到平衡状态
②图中Q点:H2S的平衡转化率为
您最近一年使用:0次
2020-01-31更新
|
336次组卷
|
3卷引用:吉林省白山市2020届高三上学期期末联考化学试题
6 . 雾霾严重危害人类健康和生态环境,开发稳定高效的脱硫脱硝工艺是当前国内外研究的热点。
(1)天然气中含有的微量H2S会腐蚀管道和设备,在1200℃下进行脱硫处理,H2S会被氧气氧化为SO2,并产生水蒸气。
请写出该反应的热化学方程式:__________________ 。
(2)利用 NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝,将NO、SO2氧化为硝酸和硫酸而除去。在温度一定时, 、溶液pH对脱硫脱硝的影响如下图所示:
、溶液pH对脱硫脱硝的影响如下图所示:
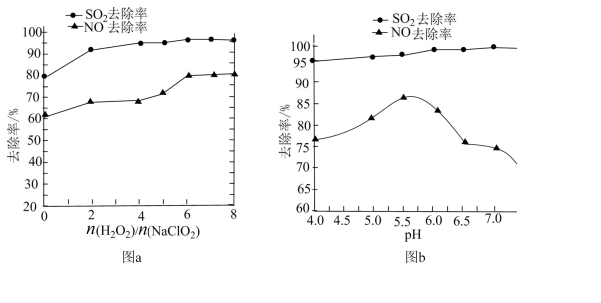
①从图a和图b中可知脱硫脱硝最佳 是
是_______ 、最佳pH是________ 。
②图b中SO2的去除率随pH的增大而增大,而NO的去除率在pH>5.5时反而减小,请解释NO去除率减小的可能原因___________________ 。
(3)臭氧也是理想的烟气脱硝剂,其脱硝的反应之一为 2NO2(g)+O3(g) N2O5(g)+O2(g),不同温度下,在体积为1 L的甲、乙两个恒容密闭容器中均充入l mol O3和2 mol NO2,相关信息如下图所示,请回答下列问题:
N2O5(g)+O2(g),不同温度下,在体积为1 L的甲、乙两个恒容密闭容器中均充入l mol O3和2 mol NO2,相关信息如下图所示,请回答下列问题:
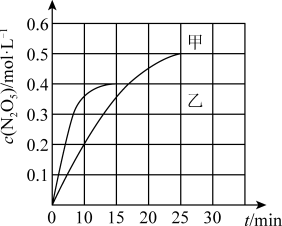
①0~15 min内乙容器中反应的平均速率:v(NO2)=__________ 。(保留2位有效数字)
②下列措施能提高容器乙中 NO2转化率的是________ (填字母标号)
A.向容器中充入氦气,增大容器的压强
B.升高容器的温度
C.向容器中再充人一定量的 NO2
D.向容器中再充入l mol O3和2 mol NO2
(1)天然气中含有的微量H2S会腐蚀管道和设备,在1200℃下进行脱硫处理,H2S会被氧气氧化为SO2,并产生水蒸气。
| 化学键 | H-S | O=O | H-O | SO2中共价键 |
| 键能/(kJ▪mol-1) | 339 | 498 | 464 | 1083 |
请写出该反应的热化学方程式:
(2)利用 NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝,将NO、SO2氧化为硝酸和硫酸而除去。在温度一定时,
 、溶液pH对脱硫脱硝的影响如下图所示:
、溶液pH对脱硫脱硝的影响如下图所示:
①从图a和图b中可知脱硫脱硝最佳
 是
是②图b中SO2的去除率随pH的增大而增大,而NO的去除率在pH>5.5时反而减小,请解释NO去除率减小的可能原因
(3)臭氧也是理想的烟气脱硝剂,其脱硝的反应之一为 2NO2(g)+O3(g)
 N2O5(g)+O2(g),不同温度下,在体积为1 L的甲、乙两个恒容密闭容器中均充入l mol O3和2 mol NO2,相关信息如下图所示,请回答下列问题:
N2O5(g)+O2(g),不同温度下,在体积为1 L的甲、乙两个恒容密闭容器中均充入l mol O3和2 mol NO2,相关信息如下图所示,请回答下列问题:
①0~15 min内乙容器中反应的平均速率:v(NO2)=
②下列措施能提高容器乙中 NO2转化率的是
A.向容器中充入氦气,增大容器的压强
B.升高容器的温度
C.向容器中再充人一定量的 NO2
D.向容器中再充入l mol O3和2 mol NO2
您最近一年使用:0次
2020-10-10更新
|
397次组卷
|
4卷引用:江西省南昌市第二中学2020-2021学年高二上学期第一次月考化学试题



