1 . 砷及其化合物有着广泛的用途。砷有两种常见的弱酸,砷酸(H3AsO4)和亚砷酸(H3AsO3)。已知砷酸(H3AsO4)的pKa1、pKa2、pKa3依次为2.25、6.77、11.40(pKa=-lgKa)。回答下列问题:
(1)已知:As(s)+ H2(g)+2O2(g)=H3AsO4(s) ΔHl
H2(g)+2O2(g)=H3AsO4(s) ΔHl
H2(g)+ O2(g)=H2O(1) ΔH2
O2(g)=H2O(1) ΔH2
As(s)+ O2(g)=
O2(g)= As2O5(s)ΔH3
As2O5(s)ΔH3
则反应As2O5(g)+3H2O(1)=2H3AsO4(s) ΔH=_________ 。
(2)写出砷酸(H3AsO4)的第二步电离方程式___________________________________ 。
(3)NaH2AsO4溶液呈______ (填“酸性”、“中性”或“碱性”),试通过计算说明________________________ 。
(4)亚砷酸(H3AsO3)水溶液中存在多种微粒形态,各种微粒分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与溶液的pH关系如下图所示。

以酚酞为指示剂(变色范围pH:8.2~10.0),将NaOH溶液逐滴加入H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为__________________________ 。
(5)某化学兴趣小组同学欲探究可逆反应AsO +I2+2OH-
+I2+2OH- AsO
AsO +2I-+ H2O。设计如下图Ⅰ所示装置。实验操作及现象:按图Ⅰ装置加入试剂并连接装置,电流由C2流入C1。 当电流变为零时,向图Ⅰ装置左边烧杯中逐滴加入一定量2mol/L盐酸,发现又产生电流,实验中电流与时间的关系如图Ⅱ所示。
+2I-+ H2O。设计如下图Ⅰ所示装置。实验操作及现象:按图Ⅰ装置加入试剂并连接装置,电流由C2流入C1。 当电流变为零时,向图Ⅰ装置左边烧杯中逐滴加入一定量2mol/L盐酸,发现又产生电流,实验中电流与时间的关系如图Ⅱ所示。
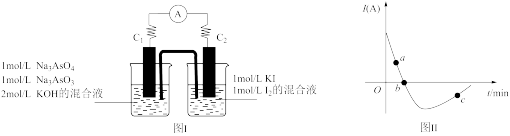
①图Ⅱ中AsO 的逆反应速率:a
的逆反应速率:a____ b( 填“ >”、” <”或“ =” )。
②写出图Ⅱ中c点对应图Ⅰ装置的正极反应式__________________________ 。
③能判断该反应达到平衡状态的是________________ 。
a.2v(I-)正=v(AsO )逆 b.溶液的pH不再变化
)逆 b.溶液的pH不再变化
c.电流表示数变为零 d.溶液颜色不再变化
(1)已知:As(s)+
 H2(g)+2O2(g)=H3AsO4(s) ΔHl
H2(g)+2O2(g)=H3AsO4(s) ΔHlH2(g)+
 O2(g)=H2O(1) ΔH2
O2(g)=H2O(1) ΔH2As(s)+
 O2(g)=
O2(g)= As2O5(s)ΔH3
As2O5(s)ΔH3则反应As2O5(g)+3H2O(1)=2H3AsO4(s) ΔH=
(2)写出砷酸(H3AsO4)的第二步电离方程式
(3)NaH2AsO4溶液呈
(4)亚砷酸(H3AsO3)水溶液中存在多种微粒形态,各种微粒分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与溶液的pH关系如下图所示。

以酚酞为指示剂(变色范围pH:8.2~10.0),将NaOH溶液逐滴加入H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为
(5)某化学兴趣小组同学欲探究可逆反应AsO
 +I2+2OH-
+I2+2OH- AsO
AsO +2I-+ H2O。设计如下图Ⅰ所示装置。实验操作及现象:按图Ⅰ装置加入试剂并连接装置,电流由C2流入C1。 当电流变为零时,向图Ⅰ装置左边烧杯中逐滴加入一定量2mol/L盐酸,发现又产生电流,实验中电流与时间的关系如图Ⅱ所示。
+2I-+ H2O。设计如下图Ⅰ所示装置。实验操作及现象:按图Ⅰ装置加入试剂并连接装置,电流由C2流入C1。 当电流变为零时,向图Ⅰ装置左边烧杯中逐滴加入一定量2mol/L盐酸,发现又产生电流,实验中电流与时间的关系如图Ⅱ所示。
①图Ⅱ中AsO
 的逆反应速率:a
的逆反应速率:a②写出图Ⅱ中c点对应图Ⅰ装置的正极反应式
③能判断该反应达到平衡状态的是
a.2v(I-)正=v(AsO
 )逆 b.溶液的pH不再变化
)逆 b.溶液的pH不再变化c.电流表示数变为零 d.溶液颜色不再变化
您最近一年使用:0次
名校
2 . 氨气是重要的化工原料。
(1)已知: N2(g)+O2(g)=2NO(g) △H= +180.5kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H= -905kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H= -483.6kJ·mol-1
写出氨气在高温高压催化剂条件下生成氮气和氢气的热化学方程式:_____________________ ;如果在1 L密闭容器中,3mol NH3 在等温条件下充分反应,2min后达到平衡,平衡时吸收的热量为92.4 kJ ,则在这段时间内v(H2)=___________________ ;保持温度不变,将起始NH3的物质的量调整为8 mol,平衡时NH3的转化率为_________________ 。
(2)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式:___________________ ,科学家利用此原理,设计成氨气一氧气燃料电池,则通入氨气的电极是 _____________ (填“正极”或“负极”);碱性条件下,该电极发生反应的电极反应式为______________________________________ 。
(3)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H<0。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是
4NO(g)+6H2O(g) △H<0。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是____________ (填字母代号)。
a.增大压强 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
(4)如果某氨水的电离程度为1%,向浓度为0.01 mol/L MgCl2溶液中滴加氨水,则开始产生沉淀时(忽略溶液体积变化)溶液中的NH3·H2O的浓度为______________ (已知Ksp[Mg(OH)2]=4.010-12])。
(1)已知: N2(g)+O2(g)=2NO(g) △H= +180.5kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H= -905kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H= -483.6kJ·mol-1
写出氨气在高温高压催化剂条件下生成氮气和氢气的热化学方程式:
(2)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式:
(3)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) △H<0。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是
4NO(g)+6H2O(g) △H<0。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是a.增大压强 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
(4)如果某氨水的电离程度为1%,向浓度为0.01 mol/L MgCl2溶液中滴加氨水,则开始产生沉淀时(忽略溶液体积变化)溶液中的NH3·H2O的浓度为
您最近一年使用:0次
名校
解题方法
3 . 氢气是一种高能燃料,也广泛应用在工业合成中。
(1)标准摩尔生成焓是指在25℃和101kPa,最稳定的单质生成1mol化合物的焓变。已知25℃和101kPa
时下列反应:
①2C2H6(g)+7O2(g)=4CO2(g) +6H2O(l) △H=-3116 kJ·mol-1
②C(石墨,s)+O2(g) =CO2(g) △H=-393.5 kJ·mol-1
③2H2(g)+O2(g) =2H2O(l) △H=-571.6 kJ·mol-1
写出乙烷标准生成焓的热化学方程式:___________________________________________ 。
(2)已知合成氨的反应为:N2+3H2 2NH3 △H<0。某温度下,若将1mol N2和2.8mol H2分别投入到初始体积为2L的恒温恒容、恒温恒压和恒容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请回答下列问题:
2NH3 △H<0。某温度下,若将1mol N2和2.8mol H2分别投入到初始体积为2L的恒温恒容、恒温恒压和恒容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请回答下列问题:

①图中代表反应在恒容绝热容器中进行的曲线是______ (用a、b、c表示)
②曲线a条件下该反应的平衡常数K=_________ 。
③b容器中M点,v(正)____ v(逆)(填“大于”、“小于”或“等于”)
(3)利用氨气可以设计成高能环保燃料电池,用该电池电解含有NO2-的碱性工业废水,在阴极产生N2。阴极电极反应式为______ ;标准状况下,当阴极收集到11.2 LN2时,理论上消耗NH3的体积为_____ 。
(4)氨水是制备铜氨溶液的常用试剂,通过以下反应及数据来探究配制铜氨溶液的最佳途径。
已知:Cu(OH)2(s) ⇌Cu2++2OH- Ksp=2.2×10-20
Cu2++4NH3·H2O ⇌[Cu (NH3) 4]2+(深蓝色)+4H2O Kβ=7.24×1012
①请用数据说明利用该反应:Cu(OH)2(s) +4NH3·H2O ⇌[Cu (NH3) 4]2++4H2O+2OH-配制铜氨溶液是否可行:_________________________________________ 。
②已知反应Cu(OH)2(S) +2NH3·H2O+2NH 4+⇌[Cu (NH3) 4]2++4H2O K=5.16×102。向盛有少量Cu(OH)2固体的试管中加入14 mol·L-1的氨水,得到悬浊液;此时若加入适量的硫酸铵固体,出现的现象为_______________ ;解释出现该现象的原因是_____________________ 。
(1)标准摩尔生成焓是指在25℃和101kPa,最稳定的单质生成1mol化合物的焓变。已知25℃和101kPa
时下列反应:
①2C2H6(g)+7O2(g)=4CO2(g) +6H2O(l) △H=-3116 kJ·mol-1
②C(石墨,s)+O2(g) =CO2(g) △H=-393.5 kJ·mol-1
③2H2(g)+O2(g) =2H2O(l) △H=-571.6 kJ·mol-1
写出乙烷标准生成焓的热化学方程式:
(2)已知合成氨的反应为:N2+3H2
 2NH3 △H<0。某温度下,若将1mol N2和2.8mol H2分别投入到初始体积为2L的恒温恒容、恒温恒压和恒容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请回答下列问题:
2NH3 △H<0。某温度下,若将1mol N2和2.8mol H2分别投入到初始体积为2L的恒温恒容、恒温恒压和恒容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请回答下列问题:
①图中代表反应在恒容绝热容器中进行的曲线是
②曲线a条件下该反应的平衡常数K=
③b容器中M点,v(正)
(3)利用氨气可以设计成高能环保燃料电池,用该电池电解含有NO2-的碱性工业废水,在阴极产生N2。阴极电极反应式为
(4)氨水是制备铜氨溶液的常用试剂,通过以下反应及数据来探究配制铜氨溶液的最佳途径。
已知:Cu(OH)2(s) ⇌Cu2++2OH- Ksp=2.2×10-20
Cu2++4NH3·H2O ⇌[Cu (NH3) 4]2+(深蓝色)+4H2O Kβ=7.24×1012
①请用数据说明利用该反应:Cu(OH)2(s) +4NH3·H2O ⇌[Cu (NH3) 4]2++4H2O+2OH-配制铜氨溶液是否可行:
②已知反应Cu(OH)2(S) +2NH3·H2O+2NH 4+⇌[Cu (NH3) 4]2++4H2O K=5.16×102。向盛有少量Cu(OH)2固体的试管中加入14 mol·L-1的氨水,得到悬浊液;此时若加入适量的硫酸铵固体,出现的现象为
您最近一年使用:0次
2017-03-15更新
|
631次组卷
|
4卷引用:湖北省黄冈中学2020届高三2月月考理综化学试题
解题方法
4 . 纯过氧化氢(H2O2)是淡蓝色的黏稠液体,可任意比例与水混溶,广泛应用于医疗消毒、绿色化学合成等领域。回答下列问题:
(1)已知:H2(g)+ O2(g)=H2O(l)∆H1=-286kJ·mol-1
O2(g)=H2O(l)∆H1=-286kJ·mol-1
H2(g)+O2(g)=H2O2(l)∆H2=-188kJ·mol-1
过氧化氢分解反应2H2O2(l)=2H2O(l)+O2(g)的∆H=_____ kJ·mol-1。
(2)100℃时,在不同金属离子存在下,纯过氧化氢24h的分解率见下表:
①由上表数据可知,能使过氧化氢分解反应活化能降低最多的离子是____ 。贮运过氧化氢时,可选用的容器材质为____ (填标号)。
A.不锈钢 B.纯铝 C.黄铜 D.铸铁
②已知反应:H2O2(l)=H2O(1)+ O2(g)K=2.88×1020。纯H2O2相对稳定,原因是H2O2分解反应的
O2(g)K=2.88×1020。纯H2O2相对稳定,原因是H2O2分解反应的___ (填编号)。
A.ΔH比较小 B.K不够大 C.速率比较小 D.活化能比较大
(3)H2O2的强氧化性使其对大多数致病菌和病毒具有消杀功能。用3%医用H2O2对传染病房喷洒消毒时,地板上有气泡冒出,该气体是___ 。
(4)过氧化氢的制备方法很多,早期制备方法如下:
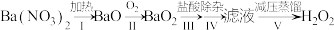
①Ⅰ为分解反应,产物除BaO、O2外,还有一种红棕色气体。该反应的化学方程式是___ 。
②Ⅱ为可逆反应,促进该反应正向进行的措施是___ (答一条即可)。
(1)已知:H2(g)+
 O2(g)=H2O(l)∆H1=-286kJ·mol-1
O2(g)=H2O(l)∆H1=-286kJ·mol-1H2(g)+O2(g)=H2O2(l)∆H2=-188kJ·mol-1
过氧化氢分解反应2H2O2(l)=2H2O(l)+O2(g)的∆H=
(2)100℃时,在不同金属离子存在下,纯过氧化氢24h的分解率见下表:
| 离子 | 加入量(mg·L-1) | 分解率% | 离子 | 加入量(mg·L-1) | 分解率% |
| 无 | 0 | 2 | Fe3+ | 1.0 | 15 |
| Al3+ | 10 | 2 | Cu2+ | 0.1 | 86 |
| Zn2+ | 10 | 10 | Cr3+ | 0.1 | 96 |
①由上表数据可知,能使过氧化氢分解反应活化能降低最多的离子是
A.不锈钢 B.纯铝 C.黄铜 D.铸铁
②已知反应:H2O2(l)=H2O(1)+
 O2(g)K=2.88×1020。纯H2O2相对稳定,原因是H2O2分解反应的
O2(g)K=2.88×1020。纯H2O2相对稳定,原因是H2O2分解反应的A.ΔH比较小 B.K不够大 C.速率比较小 D.活化能比较大
(3)H2O2的强氧化性使其对大多数致病菌和病毒具有消杀功能。用3%医用H2O2对传染病房喷洒消毒时,地板上有气泡冒出,该气体是
(4)过氧化氢的制备方法很多,早期制备方法如下:
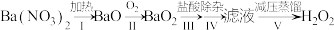
①Ⅰ为分解反应,产物除BaO、O2外,还有一种红棕色气体。该反应的化学方程式是
②Ⅱ为可逆反应,促进该反应正向进行的措施是
您最近一年使用:0次
解题方法
5 . 氮氧化物(NOx)是严重的大气污染物,能引起雾霾、光化学烟雾、酸雨等环境问题。回答下列问题:
(1)氧化还原法消除NOx的转化如下:
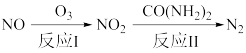
已知:NO(g)+O3(g)=NO2(g)+O2(g)△H=-201kJ·mol-1
2NO(g)+O2(g)=2NO2(g)△H=-116kJ·mol-1
反应I只有一种生成物,则反应I的热化学方程式为_______________ 。
(2)柴油机氮氧化物(NOx)处理技术是一种系统简单,占用空间较小的柴油车尾气处理技术,氮氧化物主要在催化转化装置中被处理。柴油发动机工作时在稀燃(O2充足、柴油较少)和富燃(O2不足、柴油较多)条件下交替进行,催化转化装置中的物质变化如图所示。
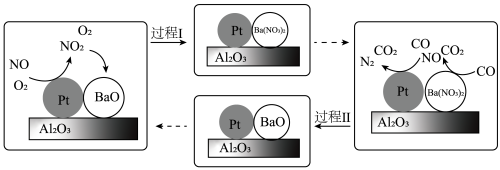
①BaO吸收NO2的化学方程式是______________ 。
②研究CO2对BaO吸收氮氧化物的影响,一定温度下,测得气体中CO2的体积分数与氮氧化物吸收率的关系如图所示。

下列相关分析中正确的是_______________ 。
A.一定范围内,氮氧化物吸收率随CO2体积分数的增大而下降,原因可能是BaO与CO2反应生成BaCO3,覆盖在BaO表面
B.当CO2体积分数达到10%~20%时,氮氧化物吸收率依然较高,其原因可能是BaCO3在一定程度上也能吸收NOx
C.若柴油中硫含量较高,在稀燃过程中,柴油中的硫氧化为SO2,2BaO+2SO2+O2=2BaSO4,BaO吸收氮氧化物的能力会下降至较低水平
D.以上分析均不对
(3)用食盐水作电解液电解烟气脱氮的原理如图所示,NO被阳极产生的氧化性物质氧化为 ,尾气经氢氧化钠溶液吸收后排入空气。电流密度和溶液pH对烟气脱氮的影响如图所示。
,尾气经氢氧化钠溶液吸收后排入空气。电流密度和溶液pH对烟气脱氮的影响如图所示。
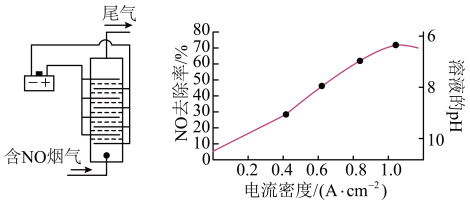
①NO被阳极产生的氧化性物质氧化为 反应的离子方程式为
反应的离子方程式为_______________ 。
②溶液的pH对NO去除率影响的原因是_______________ 。
(1)氧化还原法消除NOx的转化如下:
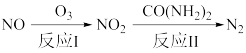
已知:NO(g)+O3(g)=NO2(g)+O2(g)△H=-201kJ·mol-1
2NO(g)+O2(g)=2NO2(g)△H=-116kJ·mol-1
反应I只有一种生成物,则反应I的热化学方程式为
(2)柴油机氮氧化物(NOx)处理技术是一种系统简单,占用空间较小的柴油车尾气处理技术,氮氧化物主要在催化转化装置中被处理。柴油发动机工作时在稀燃(O2充足、柴油较少)和富燃(O2不足、柴油较多)条件下交替进行,催化转化装置中的物质变化如图所示。

①BaO吸收NO2的化学方程式是
②研究CO2对BaO吸收氮氧化物的影响,一定温度下,测得气体中CO2的体积分数与氮氧化物吸收率的关系如图所示。

下列相关分析中正确的是
A.一定范围内,氮氧化物吸收率随CO2体积分数的增大而下降,原因可能是BaO与CO2反应生成BaCO3,覆盖在BaO表面
B.当CO2体积分数达到10%~20%时,氮氧化物吸收率依然较高,其原因可能是BaCO3在一定程度上也能吸收NOx
C.若柴油中硫含量较高,在稀燃过程中,柴油中的硫氧化为SO2,2BaO+2SO2+O2=2BaSO4,BaO吸收氮氧化物的能力会下降至较低水平
D.以上分析均不对
(3)用食盐水作电解液电解烟气脱氮的原理如图所示,NO被阳极产生的氧化性物质氧化为
 ,尾气经氢氧化钠溶液吸收后排入空气。电流密度和溶液pH对烟气脱氮的影响如图所示。
,尾气经氢氧化钠溶液吸收后排入空气。电流密度和溶液pH对烟气脱氮的影响如图所示。
①NO被阳极产生的氧化性物质氧化为
 反应的离子方程式为
反应的离子方程式为②溶液的pH对NO去除率影响的原因是
您最近一年使用:0次
2020-09-25更新
|
442次组卷
|
2卷引用:湖北省黄冈市2021届高三9月质量检测化学试题
解题方法
6 . H2S是存在于燃气中的一种有害气体,脱除H2S的方法有很多。
(1)国内有学者设计了“Cu2+一沉淀氧化”法脱除H2S。该法包括生成CuS沉淀,氧化CuS(Cu2++CuS+4Cl—=S+2CuCl2—)及空气氧化CuCl2—再生Cu2+。
①反应H2S(aq)+Cu2+(aq)⇌CuS(s)+2H+(aq)的K=__________
②再生Cu2+反应的离子方程式为____________ 。
(2)采用生物脱硫技术时,H2S与碱反应转化为HS-,在脱氮硫杆菌参与下,HS-被NO3-氧化为SO42—、NO3—被还原为N2。当33.6 m3(标准状况)某燃气(H2S的含量为0.2%)脱硫时,消耗NO3—的物质的量为___ mol。
(3)已知下列热化学方程式:
Ⅰ.H2(g)+ O2(g)=H2O(l) ∆H1=-285.8kJ∙mol-1
O2(g)=H2O(l) ∆H1=-285.8kJ∙mol-1
Ⅱ. H2(g)+S(s)=H2S(g) ∆H2=-20.6kJ∙mol-1
Ⅲ.S(s)+O2(g)=SO2(g) ∆H3=-296.8kJ∙mol-1
则以Claus法脱除H2S的反应:2H2S(g)+SO2 (g)=3S(s)+2H2O(1) △H=________ kJ/mol。
(4)101 kPa下,H2S分解:2H2S(g) ⇌ 2H2(g)+S2(g)。保持压强不变,反应达到平衡时,气体的体积分数(φ)随温度的变化曲线如图:
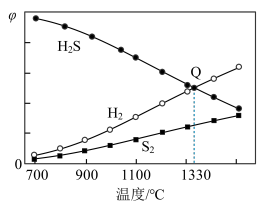
①在密闭容器中,关于反应2H2S(g) ⇌ 2H2(g)+S2 (g)的说法正确的是____ (填字母)。
A.Kp随温度的升高而增大
B.低压有利于提高HpS的平衡分解率
C.维持温度、气体总压强不变时,向平衡体系中通入氩气,则v(正)<v(逆)
D.在恒容密闭容器中进行反应,当气体密度不再变化时,反应达到平衡状态
②图中Q点:H2S的平衡转化率为____ ;S2(g)的分压为____ kPa;1330℃时,反应2H2S(g) ⇌ 2H2(g)+S2(g)的Kp=_____ (Kp为以分压表示的平衡常数)。
(1)国内有学者设计了“Cu2+一沉淀氧化”法脱除H2S。该法包括生成CuS沉淀,氧化CuS(Cu2++CuS+4Cl—=S+2CuCl2—)及空气氧化CuCl2—再生Cu2+。
①反应H2S(aq)+Cu2+(aq)⇌CuS(s)+2H+(aq)的K=
②再生Cu2+反应的离子方程式为
(2)采用生物脱硫技术时,H2S与碱反应转化为HS-,在脱氮硫杆菌参与下,HS-被NO3-氧化为SO42—、NO3—被还原为N2。当33.6 m3(标准状况)某燃气(H2S的含量为0.2%)脱硫时,消耗NO3—的物质的量为
(3)已知下列热化学方程式:
Ⅰ.H2(g)+
 O2(g)=H2O(l) ∆H1=-285.8kJ∙mol-1
O2(g)=H2O(l) ∆H1=-285.8kJ∙mol-1Ⅱ. H2(g)+S(s)=H2S(g) ∆H2=-20.6kJ∙mol-1
Ⅲ.S(s)+O2(g)=SO2(g) ∆H3=-296.8kJ∙mol-1
则以Claus法脱除H2S的反应:2H2S(g)+SO2 (g)=3S(s)+2H2O(1) △H=
(4)101 kPa下,H2S分解:2H2S(g) ⇌ 2H2(g)+S2(g)。保持压强不变,反应达到平衡时,气体的体积分数(φ)随温度的变化曲线如图:

①在密闭容器中,关于反应2H2S(g) ⇌ 2H2(g)+S2 (g)的说法正确的是
A.Kp随温度的升高而增大
B.低压有利于提高HpS的平衡分解率
C.维持温度、气体总压强不变时,向平衡体系中通入氩气,则v(正)<v(逆)
D.在恒容密闭容器中进行反应,当气体密度不再变化时,反应达到平衡状态
②图中Q点:H2S的平衡转化率为
您最近一年使用:0次
2020-01-31更新
|
336次组卷
|
3卷引用:2019年湖北省十堰市高三元月调研考试理综化学试题
7 . 研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:
Fe2O3(s)+3CO(s,石墨)═2Fe(s)+3CO2(g)△H1=+489.0kJ•mol﹣1
C(s,石墨)+CO2(g)═2CO(g)△H2=+172.5kJ•mol﹣1
则CO还原Fe2O3(s)的热化学方程式为_____ 。
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H
CH3OH(g)+H2O(g)△H
①取一定体积CO2和H2的混合气体(物质的量之比为1:3),加入恒容密闭容器中,发生上述反应反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图1所示,则该反应的△H____ 0(填“>”、“<”或“=”,下同)。
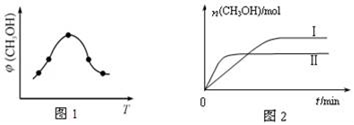
②在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图2所示,曲线I、Ⅱ对应的平衡常数关系为KⅠ_____ KⅡ。
(3)以CO2为原料还可以合成多种物质。
①工业上尿素[CO(NH2)2]由CO2和NH3在一定条件下合成.开始以氨碳比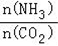 =3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为
=3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为_____ 。
②将足量CO2通入饱和氨水中可得氮肥NH4HCO3,已知常温下一水合氨Kb=1.8×10﹣5,碳酸一级电离常数Ka=4.3×10﹣7,则NH4HCO3溶液呈_____ (填“酸性”、“中性”或“碱性”)。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:
Fe2O3(s)+3CO(s,石墨)═2Fe(s)+3CO2(g)△H1=+489.0kJ•mol﹣1
C(s,石墨)+CO2(g)═2CO(g)△H2=+172.5kJ•mol﹣1
则CO还原Fe2O3(s)的热化学方程式为
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H
CH3OH(g)+H2O(g)△H①取一定体积CO2和H2的混合气体(物质的量之比为1:3),加入恒容密闭容器中,发生上述反应反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图1所示,则该反应的△H

②在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图2所示,曲线I、Ⅱ对应的平衡常数关系为KⅠ
(3)以CO2为原料还可以合成多种物质。
①工业上尿素[CO(NH2)2]由CO2和NH3在一定条件下合成.开始以氨碳比
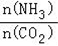 =3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为
=3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为②将足量CO2通入饱和氨水中可得氮肥NH4HCO3,已知常温下一水合氨Kb=1.8×10﹣5,碳酸一级电离常数Ka=4.3×10﹣7,则NH4HCO3溶液呈
您最近一年使用:0次
2017-03-06更新
|
293次组卷
|
2卷引用:2016-2017学年湖北省宜昌市部分重点中学高二上学期期末考试化学试卷
解题方法
8 . 请完成下列小题:
(1)工业上可利用CO2和H2生成甲醇,热化学方程式如下:
CO2(g)+3H2(g) CH3OH(l)+H2O(g) △H=Q1 kJ·mol-1
CH3OH(l)+H2O(g) △H=Q1 kJ·mol-1
又查资料得知:①CH3OH(l)+ O2(g)
O2(g)  CO2(g)+H2(g) △H=Q2 kJ·mol-1
CO2(g)+H2(g) △H=Q2 kJ·mol-1
②H2O(g)= H2O(l) △H=Q3 kJ·mol-1
则表示甲醇的燃烧热的热化学方程式为________________ 。
某同学设计了一个甲醇燃料电池,并用该电池电解200mL一定浓度的NaCl与CuSO4混合溶液,其装置如图:
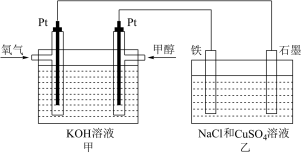
(2)写出甲中通入甲醇这一极的电极反应式_______________________ 。
(3)理论上乙中两极所得气体的体积随时间变化的关系如图所示(已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式___________ ,原混合溶液中NaCl的物质的量浓度为_______ mol/L。(设溶液体积不变)

(4)当向上述甲装置中通入标况下的氧气336mL时,理论上在铁电极上可析出铜的质量为_________ g。
(5)已知草酸H2C2O4为弱酸。
①常温下,下列事实能说明草酸是弱电解质的是____________ 。
A.向草酸钠溶液加酚酞,溶液变红
B.取一定量草酸溶液加水稀释至10倍,pH变化小于1
C.草酸能使酸性KMnO4溶液褪色
D.取相同pH的草酸溶液和盐酸,分别加入足量的大小、形状相同的镁条,草酸溶液反应速度快
②常温下,0.1mol·L-1的草酸溶液与pH=13的NaOH溶液等体积混合,所得溶液的pH为6,则c(HC2O4-)+2c(C2O42-)=________________ 。(用准确的数学表达式表示)
(1)工业上可利用CO2和H2生成甲醇,热化学方程式如下:
CO2(g)+3H2(g)
 CH3OH(l)+H2O(g) △H=Q1 kJ·mol-1
CH3OH(l)+H2O(g) △H=Q1 kJ·mol-1又查资料得知:①CH3OH(l)+
 O2(g)
O2(g)  CO2(g)+H2(g) △H=Q2 kJ·mol-1
CO2(g)+H2(g) △H=Q2 kJ·mol-1②H2O(g)= H2O(l) △H=Q3 kJ·mol-1
则表示甲醇的燃烧热的热化学方程式为
某同学设计了一个甲醇燃料电池,并用该电池电解200mL一定浓度的NaCl与CuSO4混合溶液,其装置如图:

(2)写出甲中通入甲醇这一极的电极反应式
(3)理论上乙中两极所得气体的体积随时间变化的关系如图所示(已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式

(4)当向上述甲装置中通入标况下的氧气336mL时,理论上在铁电极上可析出铜的质量为
(5)已知草酸H2C2O4为弱酸。
①常温下,下列事实能说明草酸是弱电解质的是
A.向草酸钠溶液加酚酞,溶液变红
B.取一定量草酸溶液加水稀释至10倍,pH变化小于1
C.草酸能使酸性KMnO4溶液褪色
D.取相同pH的草酸溶液和盐酸,分别加入足量的大小、形状相同的镁条,草酸溶液反应速度快
②常温下,0.1mol·L-1的草酸溶液与pH=13的NaOH溶液等体积混合,所得溶液的pH为6,则c(HC2O4-)+2c(C2O42-)=
您最近一年使用:0次
2010·湖北武汉·一模
9 . 丙烯是一种重要的化工原料。2000年以来,我国丙烯的使用量已超过乙烯,且一直保持增长趋势。
(1)2010年12月18日位于浙江平湖市独山港区石化工业发展区内一个丙烯储罐突然爆炸起火,大火产生的高温使消防队员难以靠近火场。已知丙烯的燃烧热为2049 kJ/mol,则其燃烧反应的热化学方程式为:___________________ 。
(2)丙烯在酸性催化剂存在下,聚合生成二聚体、三聚体的混合物,将其加入汽油中,可提高汽油的__________ 。在催化剂存在下,丙烯聚合生成聚丙烯树脂,其反应的化学方程式为________________ 。
(3)制取丙烯腈的方法常有如下两种:
方法①CH≡CH+H-CN CH2=CH-CN
CH2=CH-CN
方法②2CH2=CH-CH3+2NH3+3O2 2CH2=CH-CN+6H2O
2CH2=CH-CN+6H2O
相比较而言,方法②的优点是___________________________ 。
(4)现以丙烯为原料,合成环酯J。已知:烯烃复分解反应是指在催化剂作用下,实现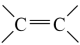 两边基团换位的反应。如两个丙烯分子进行烯烃换位,生成丁烯和乙烯。
两边基团换位的反应。如两个丙烯分子进行烯烃换位,生成丁烯和乙烯。
2CH2=CHCH3 CH3CH=CHCH3+CH2=CH2
CH3CH=CHCH3+CH2=CH2
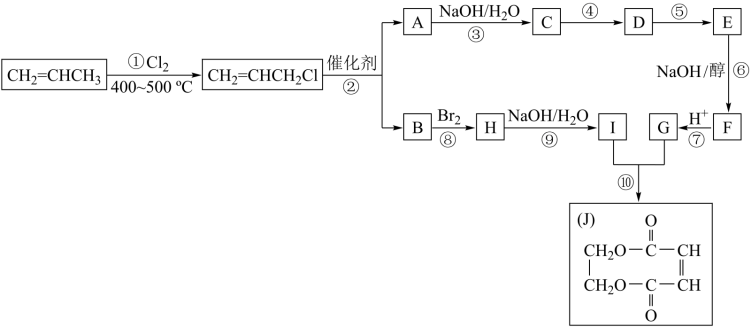
请按要求填空:
(i)写出下列反应的反应类型:①______________ ,⑥_________________ 。
(ii)反应④是与HCl加成,设计这一步反应的目的是_____________ ,物质E的结构简式是____________ 。
(iii)有机化合物C有多种同分异构体,请写出其中属于酯类且能发生银镜反应的所有同分异构体的结构简式_________________ 。
(1)2010年12月18日位于浙江平湖市独山港区石化工业发展区内一个丙烯储罐突然爆炸起火,大火产生的高温使消防队员难以靠近火场。已知丙烯的燃烧热为2049 kJ/mol,则其燃烧反应的热化学方程式为:
(2)丙烯在酸性催化剂存在下,聚合生成二聚体、三聚体的混合物,将其加入汽油中,可提高汽油的
(3)制取丙烯腈的方法常有如下两种:
方法①CH≡CH+H-CN
 CH2=CH-CN
CH2=CH-CN方法②2CH2=CH-CH3+2NH3+3O2
 2CH2=CH-CN+6H2O
2CH2=CH-CN+6H2O相比较而言,方法②的优点是
(4)现以丙烯为原料,合成环酯J。已知:烯烃复分解反应是指在催化剂作用下,实现
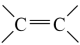 两边基团换位的反应。如两个丙烯分子进行烯烃换位,生成丁烯和乙烯。
两边基团换位的反应。如两个丙烯分子进行烯烃换位,生成丁烯和乙烯。2CH2=CHCH3
 CH3CH=CHCH3+CH2=CH2
CH3CH=CHCH3+CH2=CH2
请按要求填空:
(i)写出下列反应的反应类型:①
(ii)反应④是与HCl加成,设计这一步反应的目的是
(iii)有机化合物C有多种同分异构体,请写出其中属于酯类且能发生银镜反应的所有同分异构体的结构简式
您最近一年使用:0次



