解题方法
1 . 砷及其化合物有着广泛的用途。砷有两种常见的弱酸,砷酸(H3AsO4)和亚砷酸(H3AsO3)。已知砷酸(H3AsO4)的pKa1、pKa2、pKa3依次为2.25、6.77、11.40(pKa=-lgKa)。回答下列问题:
(1)已知:As(s)+ H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+ O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
As(s)+ O2(g)=
O2(g)= As2O5(s) ΔH3
As2O5(s) ΔH3
则反应As2O5(s)+3H2O(l)=2H3AsO4(s) ΔH=______ 。
(2)写出砷酸(H3AsO4)的第二步电离方程式_______ 。
(3)NaH2AsO4溶液呈___ (填“酸性”“中性”或“碱性”),试通过计算说明_______ 。
(4)亚砷酸(H3AsO3)水溶液中存在多种微粒形态,各种微粒分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与溶液的pH关系如图所示。

以酚酞为指示剂(变色范围pH 8.2~10.0),将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为_______ 。
(5)某化学兴趣小组同学欲探究可逆反应:AsO33-+I2+2OH- AsO43-+2I-+H2O。设计图Ⅱ所示装置。实验操作及现象:按图Ⅱ装置加入试剂并连接装置,电流由C2流入C1。当电流变为零时,向图Ⅱ装置左边烧杯中逐滴加入一定量2 mol·L-1盐酸,发现又产生电流,实验中电流与时间的关系如图Ⅲ所示。
AsO43-+2I-+H2O。设计图Ⅱ所示装置。实验操作及现象:按图Ⅱ装置加入试剂并连接装置,电流由C2流入C1。当电流变为零时,向图Ⅱ装置左边烧杯中逐滴加入一定量2 mol·L-1盐酸,发现又产生电流,实验中电流与时间的关系如图Ⅲ所示。

①图Ⅲ中AsO43-的逆反应速率:a__ (填“>”“<”或“=”)b。
②写出图Ⅲ中c点对应图Ⅱ装置的正极反应式______ 。
③能判断该反应达到平衡状态的是__ 。
a 2v(I-)正=v(AsO33-)逆b 溶液的pH不再变化
c 电流表示数变为零 d 溶液颜色不再变化
(1)已知:As(s)+
 H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1H2(g)+
 O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2As(s)+
 O2(g)=
O2(g)= As2O5(s) ΔH3
As2O5(s) ΔH3则反应As2O5(s)+3H2O(l)=2H3AsO4(s) ΔH=
(2)写出砷酸(H3AsO4)的第二步电离方程式
(3)NaH2AsO4溶液呈
(4)亚砷酸(H3AsO3)水溶液中存在多种微粒形态,各种微粒分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与溶液的pH关系如图所示。

以酚酞为指示剂(变色范围pH 8.2~10.0),将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为
(5)某化学兴趣小组同学欲探究可逆反应:AsO33-+I2+2OH-
 AsO43-+2I-+H2O。设计图Ⅱ所示装置。实验操作及现象:按图Ⅱ装置加入试剂并连接装置,电流由C2流入C1。当电流变为零时,向图Ⅱ装置左边烧杯中逐滴加入一定量2 mol·L-1盐酸,发现又产生电流,实验中电流与时间的关系如图Ⅲ所示。
AsO43-+2I-+H2O。设计图Ⅱ所示装置。实验操作及现象:按图Ⅱ装置加入试剂并连接装置,电流由C2流入C1。当电流变为零时,向图Ⅱ装置左边烧杯中逐滴加入一定量2 mol·L-1盐酸,发现又产生电流,实验中电流与时间的关系如图Ⅲ所示。
①图Ⅲ中AsO43-的逆反应速率:a
②写出图Ⅲ中c点对应图Ⅱ装置的正极反应式
③能判断该反应达到平衡状态的是
a 2v(I-)正=v(AsO33-)逆b 溶液的pH不再变化
c 电流表示数变为零 d 溶液颜色不再变化
您最近一年使用:0次
2 . [2017·新课标I]近期发现,H2S是继NO、CO之后的第三个生命体系气体信号分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
(1)下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是_________ (填标号)。
A.氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以
B.氢硫酸的导电能力低于相同浓度的亚硫酸
C.0.10 mol·L−1的氢硫酸和亚硫酸的pH分别为4.5和2.1
D.氢硫酸的还原性强于亚硫酸
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。______________ 、______________ ,制得等量H2所需能量较少的是_____________ 。 =
=_______ %,反应平衡常数K=________ 。
②在620 K重复试验,平衡后水的物质的量分数为0.03,H2S的转化率
_____  ,该反应的
,该反应的 H
H_____ 0。(填“>”“<”或“=”)
③向反应器中再分别充入下列气体,能使H2S转化率增大的是________ (填标号)
A.H2S B.CO2 C.COS D.N2
(1)下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是
A.氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以
B.氢硫酸的导电能力低于相同浓度的亚硫酸
C.0.10 mol·L−1的氢硫酸和亚硫酸的pH分别为4.5和2.1
D.氢硫酸的还原性强于亚硫酸
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

(3)H2S与CO2在高温下发生反应:H2S(g)+CO2(g) COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
 =
=②在620 K重复试验,平衡后水的物质的量分数为0.03,H2S的转化率

 ,该反应的
,该反应的 H
H③向反应器中再分别充入下列气体,能使H2S转化率增大的是
A.H2S B.CO2 C.COS D.N2
您最近一年使用:0次
2017-08-09更新
|
10917次组卷
|
10卷引用:云南省大理白族自治州祥云县第一中学2020届高三下学期4月月考理综化学试题
云南省大理白族自治州祥云县第一中学2020届高三下学期4月月考理综化学试题2017年全国普通高等学校招生统一考试理综化学(新课标Ⅰ卷精编版)河北省唐山市第一中学2017-2018学年高二上学期第一次月考化学试题2018届广东省揭阳市高三上学期第一次月考化学试题重庆市第二中学2018届高三3月测试化学试题(已下线)《考前20天终极攻略》-5月29日 化学反应原理综合(已下线)解密20 原理综合题(教师版)——备战2018年高考化学之高频考点解密【市级联考】广东省化州市2019年高三上学期第二次模拟考试理科综合化学试题广东省江门市新会区陈经纶中学2022-2023学年高二上学期第5段月考化学试题重庆十八中两江实验中学校2022-2023学年高二上学期第一次月考化学试题
名校
解题方法
3 . 燃煤烟气中含有大量SO2和NO,某科研小组研究SO2和NO的吸收方法。
回答下列问题:
(1)已知SO2(g)+O3(g) SO3(g)+O2(g) △H1=-241.6 kJ· mol-1
SO3(g)+O2(g) △H1=-241.6 kJ· mol-1
NO(g)+O3(g) NO2(g)+O2(g) △H2=-199.8kJ· mol-1
NO2(g)+O2(g) △H2=-199.8kJ· mol-1
则反应SO3(g)+NO(g) SO2(g)+NO2(g)的△H=
SO2(g)+NO2(g)的△H=________ kJ· mol-1
(2)在恒温条件下,向2L恒容密闭容器中加入1 molNO和1molO3发生反应NO(g)+O3(g) NO2(g)+O2(g),2min时达到平衡状态。
NO2(g)+O2(g),2min时达到平衡状态。
①若测得2min内v(NO)=0.21 mol· L-1· min-1,则平衡时NO的转化率α1=________ ;若其它条件保持不变,在恒压条件下进行,则平衡时NO的转化率α2________ α1(填“>”“<”或“=”)
②保持温度不变,向2min后的平衡体系中再加入0.3 moNO2和0.04 molNO,此时平衡将向________ (填“正”或“逆”)方向移动
③该反应的逆反应速率与时间的关系如下图所示,反应在t1、t3、t5时刻均达到平衡状态。t2、t6时刻都只改变了某一个条件,则t2时刻改变的条件是________ ,t6时刻改变的条件是________ ,t4时刻改变条件后v(正) ________ v(逆)(填“>”“<”或“=”)

(3)处理烟气中SO2也可采用碱液吸收法。已知25℃时,K(NH3·H2O)=1.8×10-5;H2SO3的Ka1=1.5×10-2,Ka2=1.0×10-7;Ksp(CaSO4)=7.1×10-5。
第1步:用过量的浓氨水吸收SO2,并在空气中氧化;
第2步:加入石灰水,发生反应Ca2++2OH-+2NH4++SO42- CaSO4↓+2NH3·H2O。
CaSO4↓+2NH3·H2O。
①25℃时,0.1mol·L-1(NH4)2SO3溶液呈________ (填“酸性”“碱性”或“中性”)。
②计算第2步反应的平衡常数K=________ (列出计算式即可)。
回答下列问题:
(1)已知SO2(g)+O3(g)
 SO3(g)+O2(g) △H1=-241.6 kJ· mol-1
SO3(g)+O2(g) △H1=-241.6 kJ· mol-1NO(g)+O3(g)
 NO2(g)+O2(g) △H2=-199.8kJ· mol-1
NO2(g)+O2(g) △H2=-199.8kJ· mol-1 则反应SO3(g)+NO(g)
 SO2(g)+NO2(g)的△H=
SO2(g)+NO2(g)的△H=(2)在恒温条件下,向2L恒容密闭容器中加入1 molNO和1molO3发生反应NO(g)+O3(g)
 NO2(g)+O2(g),2min时达到平衡状态。
NO2(g)+O2(g),2min时达到平衡状态。①若测得2min内v(NO)=0.21 mol· L-1· min-1,则平衡时NO的转化率α1=
②保持温度不变,向2min后的平衡体系中再加入0.3 moNO2和0.04 molNO,此时平衡将向
③该反应的逆反应速率与时间的关系如下图所示,反应在t1、t3、t5时刻均达到平衡状态。t2、t6时刻都只改变了某一个条件,则t2时刻改变的条件是

(3)处理烟气中SO2也可采用碱液吸收法。已知25℃时,K(NH3·H2O)=1.8×10-5;H2SO3的Ka1=1.5×10-2,Ka2=1.0×10-7;Ksp(CaSO4)=7.1×10-5。
第1步:用过量的浓氨水吸收SO2,并在空气中氧化;
第2步:加入石灰水,发生反应Ca2++2OH-+2NH4++SO42-
 CaSO4↓+2NH3·H2O。
CaSO4↓+2NH3·H2O。①25℃时,0.1mol·L-1(NH4)2SO3溶液呈
②计算第2步反应的平衡常数K=
您最近一年使用:0次
2019-01-12更新
|
457次组卷
|
3卷引用:【市级联考】云南省昆明市2019届高三上学期1月复习诊断测试理科综合化学试题
名校
解题方法
4 . 实现“低碳经济”的一项重要课题就是研究如何将CO2转化为可利用的资源。因此,研究CO2 的综合利用对“低碳社会”的构述构建具有重要意义。
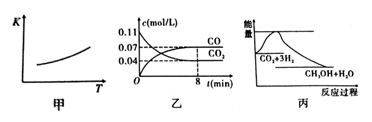
(1)一定条件下CO2可以和铁反应:Fe(s)+CO2(g) FeO(s)+CO(g),该反应的平衡常数(K)与温度(T)的关系如图甲所示:
FeO(s)+CO(g),该反应的平衡常数(K)与温度(T)的关系如图甲所示:
①该反应的△H______ 0(填“<”、“=”或“>”)。
②下列措施,能使平衡时 增大的是
增大的是______ (填序号)。
A.充入一定量的CO B.升高温度 C.使用催化剂
③一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2,反应过程中CO2和CO的物质的量浓度与时间的关系如图乙所示。该反应的平衡常数K=_____________ 。
(2)目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),图丙表示该反应过程中能量的变化。
CH3OH(g)+H2O(g),图丙表示该反应过程中能量的变化。
①下列关于该反应的说法,正确的是______ (填序号)。
A.△H<0,△S<0 B.△H>0,△S<0 C.△H>0,△S>0 D.△H<0,△S>0
②已知:CO2(g)+3H2(g) CH3OH(l)+H2O(l) △H=-143.0kJ•mol-1;
CH3OH(l)+H2O(l) △H=-143.0kJ•mol-1;
H2(g)+ O2(g)=H2O(l) △H=-285.8kJ•mol-1。
O2(g)=H2O(l) △H=-285.8kJ•mol-1。
写出表示CH3OH燃烧热的热化学方程式:________________________________ 。
③一种以甲醇为原料的燃料电池,使用合适的合金为电极,以氢氧化钠溶液、甲醇、氧气为原料,该电池负极的电极反应式为_______________________________ 。
(3)以CO2为原料还可以合成多种氮肥。
①工业上由CO2和NH3在一定条件下合成尿素的化学方程式为CO2(g)+2NH3(g) CO(NH2)2(l)+H2O(g)。起始以
CO(NH2)2(l)+H2O(g)。起始以 =5投料进行反应,达到化学平衡时CO2的转化率为60%,则NH3的平衡转化率为
=5投料进行反应,达到化学平衡时CO2的转化率为60%,则NH3的平衡转化率为______________ 。
②将足量CO2通入饱和氨水中可制得碳铵(NH4HCO3)。已知室温下Kb(NH3·H2O)=1.8×10-5,Kal(H2CO3)=4.3×10-7,则 0.lmol/LNH4HCO3 溶液呈_________ (填“酸性”“中性”或“碱性”)。
(1)一定条件下CO2可以和铁反应:Fe(s)+CO2(g)
 FeO(s)+CO(g),该反应的平衡常数(K)与温度(T)的关系如图甲所示:
FeO(s)+CO(g),该反应的平衡常数(K)与温度(T)的关系如图甲所示:
①该反应的△H
②下列措施,能使平衡时
 增大的是
增大的是A.充入一定量的CO B.升高温度 C.使用催化剂
③一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2,反应过程中CO2和CO的物质的量浓度与时间的关系如图乙所示。该反应的平衡常数K=
(2)目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),图丙表示该反应过程中能量的变化。
CH3OH(g)+H2O(g),图丙表示该反应过程中能量的变化。①下列关于该反应的说法,正确的是
A.△H<0,△S<0 B.△H>0,△S<0 C.△H>0,△S>0 D.△H<0,△S>0
②已知:CO2(g)+3H2(g)
 CH3OH(l)+H2O(l) △H=-143.0kJ•mol-1;
CH3OH(l)+H2O(l) △H=-143.0kJ•mol-1;H2(g)+
 O2(g)=H2O(l) △H=-285.8kJ•mol-1。
O2(g)=H2O(l) △H=-285.8kJ•mol-1。写出表示CH3OH燃烧热的热化学方程式:
③一种以甲醇为原料的燃料电池,使用合适的合金为电极,以氢氧化钠溶液、甲醇、氧气为原料,该电池负极的电极反应式为
(3)以CO2为原料还可以合成多种氮肥。
①工业上由CO2和NH3在一定条件下合成尿素的化学方程式为CO2(g)+2NH3(g)
 CO(NH2)2(l)+H2O(g)。起始以
CO(NH2)2(l)+H2O(g)。起始以 =5投料进行反应,达到化学平衡时CO2的转化率为60%,则NH3的平衡转化率为
=5投料进行反应,达到化学平衡时CO2的转化率为60%,则NH3的平衡转化率为②将足量CO2通入饱和氨水中可制得碳铵(NH4HCO3)。已知室温下Kb(NH3·H2O)=1.8×10-5,Kal(H2CO3)=4.3×10-7,则 0.lmol/LNH4HCO3 溶液呈
您最近一年使用:0次
名校
5 . 某废水中含有的NH 在一定条件下可被O2氧化,反应过程如下:
在一定条件下可被O2氧化,反应过程如下:
①NH4+(aq)+3/2O2(g)=NO2-(aq)+2H+(aq)+H2O(l) ΔH = -273kJ/mol
②NO2-(aq)+1/2O2(g)=NO3-(aq) ΔH = -73kJ/mol
下列叙述不正确 的是
 在一定条件下可被O2氧化,反应过程如下:
在一定条件下可被O2氧化,反应过程如下:①NH4+(aq)+3/2O2(g)=NO2-(aq)+2H+(aq)+H2O(l) ΔH = -273kJ/mol
②NO2-(aq)+1/2O2(g)=NO3-(aq) ΔH = -73kJ/mol
下列叙述
| A.1mol的NH3和1mol 的NH4+都有10×6.02×1023个电子 |
| B.室温下,0.1 mol/L HNO2溶液pH>1,则NaNO2溶液显碱性 |
| C.NH4+(aq)+2O2(g)=NO3-(aq)+2H+(aq)+H2O(l) ΔH= -346kJ/mol |
| D.在上述两次转化过程中,废水的酸性先增大然后逐渐减弱 |
您最近一年使用:0次
2017-06-02更新
|
628次组卷
|
3卷引用:云南省临沧市第一中学2018届高三下学期第一次月考化学试题
解答题-原理综合题
|
适中(0.65)
|
名校
6 . 空气中含有吸入颗粒物PM2.5,严重影响人的生理和健康,因此改善发质结构、机动车辆措施能有效减少PM2.5、SO2、NO3等的污染。请回答下列问题:
(1)将一定量的某PM2.5样品用蒸馏水溶解制成待测试样(忽略OH-)。常温下,测得该试样的组成及其浓度如下表:
根据表中数据判断,该试样的pH =________ 。
(2)汽车尾气中NOx和CO的生成。已知:气缸中生成NO的反应为N2(g)+O2(g) 2NO(g) △H>0。恒温,恒容密闭容器中,下列叙述,能说明该反应达到化学平衡状态的是
2NO(g) △H>0。恒温,恒容密闭容器中,下列叙述,能说明该反应达到化学平衡状态的是________ (填序号)。
A.混合气体的密度不再变化 B.混合气体的平均分子质量不再变化
C.N2、O2、NO的物质的量之比为1:1:2 D.氧气的转化率不再变化
E.生成lmol N2的间时有lmol O2被消耗
(3)为减少CO2、SO2的排放,常采取的措施如下:
①将煤转化为清洁气体燃料。已知:H2(g)+1/2O2(g)= H2O(g) △H =-241.8kJ • mol-1; C(s)+1/2O2(g)=CO(g)△H =-110.5kJ • mol-1。写出焦炭与水蒸气反应的热化学方程式:_____________________________________ 。
②洗涤含SO2的烟气。下列物质,可作为洗涤含SO2烟气的洗涤剂的是______ (填序号)。
A.浓氨水 B.碳酸氢钠饱和溶液 C.FeCl3饱和溶液 D.酸性CaCl2饱和溶液
(4)某湿度下,反应2NO(g)+O2(g) 2NO2(g)中,在保证O2浓度不变的情况下,增大容器的体积, 平衡将
2NO2(g)中,在保证O2浓度不变的情况下,增大容器的体积, 平衡将_____ (填“正反应方向” “逆反应方向”或“不”)移动。
判断的依据是__________________________________ 。
(5)甲醇燃料电池可能成为未来便携电子产品应用的主流。某种甲醇燃料电池的工作原理如图14所示,则通入a气体的电极,电极反应式为_________________ 。

(6)—定条件下,甲醇与一氧化碳反应可以合成乙酸。常温条件下,将a mol/L的CH3COOH溶液与bmol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO-),用含a和b的代数式表示,该混合溶液中醋酸的电离常数为___________________ 。
(1)将一定量的某PM2.5样品用蒸馏水溶解制成待测试样(忽略OH-)。常温下,测得该试样的组成及其浓度如下表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3﹣ | Cl﹣ |
| 浓度/mol·L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据判断,该试样的pH =
(2)汽车尾气中NOx和CO的生成。已知:气缸中生成NO的反应为N2(g)+O2(g)
 2NO(g) △H>0。恒温,恒容密闭容器中,下列叙述,能说明该反应达到化学平衡状态的是
2NO(g) △H>0。恒温,恒容密闭容器中,下列叙述,能说明该反应达到化学平衡状态的是A.混合气体的密度不再变化 B.混合气体的平均分子质量不再变化
C.N2、O2、NO的物质的量之比为1:1:2 D.氧气的转化率不再变化
E.生成lmol N2的间时有lmol O2被消耗
(3)为减少CO2、SO2的排放,常采取的措施如下:
①将煤转化为清洁气体燃料。已知:H2(g)+1/2O2(g)= H2O(g) △H =-241.8kJ • mol-1; C(s)+1/2O2(g)=CO(g)△H =-110.5kJ • mol-1。写出焦炭与水蒸气反应的热化学方程式:
②洗涤含SO2的烟气。下列物质,可作为洗涤含SO2烟气的洗涤剂的是
A.浓氨水 B.碳酸氢钠饱和溶液 C.FeCl3饱和溶液 D.酸性CaCl2饱和溶液
(4)某湿度下,反应2NO(g)+O2(g)
 2NO2(g)中,在保证O2浓度不变的情况下,增大容器的体积, 平衡将
2NO2(g)中,在保证O2浓度不变的情况下,增大容器的体积, 平衡将判断的依据是
(5)甲醇燃料电池可能成为未来便携电子产品应用的主流。某种甲醇燃料电池的工作原理如图14所示,则通入a气体的电极,电极反应式为

(6)—定条件下,甲醇与一氧化碳反应可以合成乙酸。常温条件下,将a mol/L的CH3COOH溶液与bmol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO-),用含a和b的代数式表示,该混合溶液中醋酸的电离常数为
您最近一年使用:0次
2017-06-10更新
|
213次组卷
|
2卷引用:云南省曲靖市第一中学2017届高三高考复习质量监测考试(八)理综化学试题



