名校
解题方法
1 . 下列说法正确的是
A.反应N2(g)+3H2(g) 2NH3(g)的△H<0,△S>0 2NH3(g)的△H<0,△S>0 |
| B.反应2CO+2NO=N2+2CO2在常温下能自发进行,则反应的△H>0,△S<0 |
| C.反应4Fe(s)+3O2(g)=2Fe2O3(s)常温下可自发进行,该反应为吸热反应 |
| D.反应TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) △H>0能自发进行,其原因是△S>0 |
您最近一年使用:0次
2022-11-16更新
|
141次组卷
|
2卷引用:湖北省十堰市县区普通高中联合体2022-2023学年高二上学期11月期中联考化学试题
解题方法
2 . 二氧化碳甲烷化助力我国2060年前实现“碳中和”,其中涉及的主要反应如下:
反应Ⅰ:CO₂(g)+4H₂(g) CH₄(g)+2H₂O(g) △H=-164.7kJ·mol⁻¹
CH₄(g)+2H₂O(g) △H=-164.7kJ·mol⁻¹
反应Ⅱ:CO₂(g)+H₂(g) CO(g)+H₂O(g) △H=+41.2kJ·mol⁻¹
CO(g)+H₂O(g) △H=+41.2kJ·mol⁻¹
回答下列问题:
(1)由热化学方程式可知,反应Ⅰ属于反应_______(填写序号)
(2)动力学研究:在多个1L恒容密闭装置中,分别充入1molCO₂和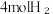 发生上述反应Ⅰ,在不同温度下反应到10分钟时,测得H₂转化率与温度关系如图1所示。已知该反应的速率方程为
发生上述反应Ⅰ,在不同温度下反应到10分钟时,测得H₂转化率与温度关系如图1所示。已知该反应的速率方程为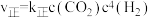 ,
,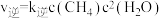 ,其中
,其中 、
、 为速率常数,只受温度影响。
为速率常数,只受温度影响。

①图1中,至a点的H₂平均反应速率为_______  。
。
②图1中,v(a)逆_______ v(c)逆(填“>”、“=”或“<”)。
③图1中c点的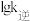 对应的是图2中的
对应的是图2中的_______ 点。
④图1中a点的v正,v逆与a点的K(平衡常数)、Q(浓度商)的关系是
______ 。
(3)热动力学研究:向10L的恒压密闭装置中充入5mol CO₂和20mol H₂,在不同温度下同时发生上述反应Ⅰ和反应Ⅱ,得到平衡时各含碳物质的物质的量n(X)与温度T的关系如下图所示。

①当反应Ⅰ和反应Ⅱ均达到化学平衡状态时,维持温度不变,压缩装置体积,则反应Ⅱ的平衡移动方向是_______ (填序号)。
A.正向移动 B.逆向移动 C.不移动 D.无法确定
②曲线Z表示的是_______ (填写含碳元素物质的化学式)的物质的量与温度的关系,简述其在温度段500K~800K物质的量增大的原因_______ 。
③800K时,反应Ⅱ的平衡常数为_______ (计算结果保留两位有效数字)。
反应Ⅰ:CO₂(g)+4H₂(g)
 CH₄(g)+2H₂O(g) △H=-164.7kJ·mol⁻¹
CH₄(g)+2H₂O(g) △H=-164.7kJ·mol⁻¹反应Ⅱ:CO₂(g)+H₂(g)
 CO(g)+H₂O(g) △H=+41.2kJ·mol⁻¹
CO(g)+H₂O(g) △H=+41.2kJ·mol⁻¹回答下列问题:
(1)由热化学方程式可知,反应Ⅰ属于反应_______(填写序号)
| A.高温自发 | B.低温自发 | C.恒自发 | D.恒不自发 |
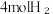 发生上述反应Ⅰ,在不同温度下反应到10分钟时,测得H₂转化率与温度关系如图1所示。已知该反应的速率方程为
发生上述反应Ⅰ,在不同温度下反应到10分钟时,测得H₂转化率与温度关系如图1所示。已知该反应的速率方程为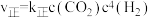 ,
,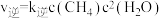 ,其中
,其中 、
、 为速率常数,只受温度影响。
为速率常数,只受温度影响。
①图1中,至a点的H₂平均反应速率为
 。
。②图1中,v(a)逆
③图1中c点的
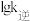 对应的是图2中的
对应的是图2中的④图1中a点的v正,v逆与a点的K(平衡常数)、Q(浓度商)的关系是

(3)热动力学研究:向10L的恒压密闭装置中充入5mol CO₂和20mol H₂,在不同温度下同时发生上述反应Ⅰ和反应Ⅱ,得到平衡时各含碳物质的物质的量n(X)与温度T的关系如下图所示。

①当反应Ⅰ和反应Ⅱ均达到化学平衡状态时,维持温度不变,压缩装置体积,则反应Ⅱ的平衡移动方向是
A.正向移动 B.逆向移动 C.不移动 D.无法确定
②曲线Z表示的是
③800K时,反应Ⅱ的平衡常数为
您最近一年使用:0次
名校
3 . 已知反应: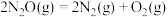
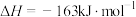 ,下列说法正确的是
,下列说法正确的是
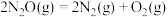
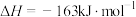 ,下列说法正确的是
,下列说法正确的是| A.高温下自发 | B.低温下自发 | C.任何温度均自发 | D.任何温度不自发 |
您最近一年使用:0次
2022-11-13更新
|
71次组卷
|
2卷引用:湖北省鄂州市部分高中教科研协作体2022-2023学年高二上学期期中考试化学试题
解题方法
4 . 下列关于反应方向、速率和平衡的说法正确的是
| A.凡是放热反应均是自发进行的反应,吸热反应都是非自发的 |
| B.化学平衡状态指的是反应物和生成物浓度相等时的状态 |
| C.一般使用催化剂可以降低反应的活化能,增大活化分子百分数,从而提高反应物的转化率 |
| D.反应NH3(g)+HCl(g)=NH4Cl(s)在常温下能自发进行,说明该反应的ΔH<0 |
您最近一年使用:0次
5 .  可通过下列方法回收处理,并加以利用:
可通过下列方法回收处理,并加以利用:
反应①:

反应②: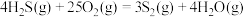
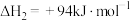
反应③: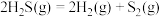

下列说法正确的是
 可通过下列方法回收处理,并加以利用:
可通过下列方法回收处理,并加以利用:反应①:


反应②:
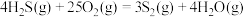
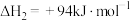
反应③:
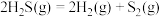

下列说法正确的是
| A.反应①可在任意温度下自发进行 |
B.反应②使用催化剂时 减小 减小 |
C.反应③的化学平衡常数表达式为 |
D.由上述反应可得 的 的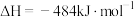 |
您最近一年使用:0次
6 .  在常温下为固体,结构和白磷类似,呈正四面体形,与
在常温下为固体,结构和白磷类似,呈正四面体形,与 互为同素异形体。已知:断裂
互为同素异形体。已知:断裂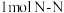 和
和 所需要的能量分别为
所需要的能量分别为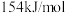 和
和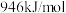 ,下列说法错误的是
,下列说法错误的是
 在常温下为固体,结构和白磷类似,呈正四面体形,与
在常温下为固体,结构和白磷类似,呈正四面体形,与 互为同素异形体。已知:断裂
互为同素异形体。已知:断裂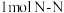 和
和 所需要的能量分别为
所需要的能量分别为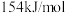 和
和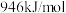 ,下列说法错误的是
,下列说法错误的是A. 含有 含有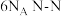 ,而且 ,而且 分子的熔沸点比 分子的熔沸点比 高 高 |
B.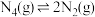 反应放热,故 反应放热,故 比 比 稳定 稳定 |
C.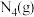 分解生成 分解生成 在任何温度下均能自发进行 在任何温度下均能自发进行 |
D. 和 和 的相互转化为氧化还原反应 的相互转化为氧化还原反应 |
您最近一年使用:0次
7 . 在一定温度下,氯气溶于水的过程为:
①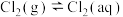 ;
;
②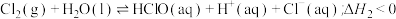 ,下列说法错误的是
,下列说法错误的是
①
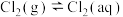 ;
;
②
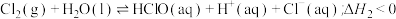 ,下列说法错误的是
,下列说法错误的是A. |
B.②的平衡常数表达式为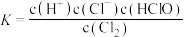 |
C.升高温度,氯水中的 减小 减小 |
D.取氯水稀释,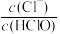 增大 增大 |
您最近一年使用:0次
8 . 已知: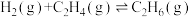
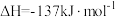 。请回答下列问题:
。请回答下列问题:
(1)该反应在_______ (填“低温”、“高温”或“任何温度”下能自发进行。
(2)若上述反应在恒温恒容密闭容器中进行,则下列条件能判断该反应达到平衡状态的是_______(填标号)。
(3)若在10 L的密闭容器内2 mol H2(g)与a molC2H4(g)进行上述反应,测得 的平衡转化率与投料比X,
的平衡转化率与投料比X,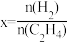 以及温度的关系如图所示。
以及温度的关系如图所示。
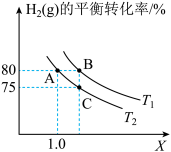
①反应从开始分别进行到A、B、C点时,_______ (填“吸收”或“放出”)的热量QA、QB、QC由大到小的顺序为_______ 。
②T1_______ (填“>”、“<”或“=”)T2。
③B点对应的体系中a=_______ 。A、B、C点对应体系的气体总压强pA、pB、pC由小到大的顺序为_______ 。
(4)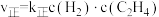 ,
,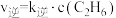 ,其中k正和k逆为速率常数,只与温度有关。若其他条件不变,则温度从T1变化到T2的过程中,下列推断合理的是_______(填标号)。
,其中k正和k逆为速率常数,只与温度有关。若其他条件不变,则温度从T1变化到T2的过程中,下列推断合理的是_______(填标号)。
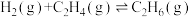
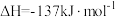 。请回答下列问题:
。请回答下列问题:(1)该反应在
(2)若上述反应在恒温恒容密闭容器中进行,则下列条件能判断该反应达到平衡状态的是_______(填标号)。
| A.容器内混合气体的平均相对分子质量不变 | B.c正(H2)=c逆(C2H6) |
| C.容器内混合气体的压强不变 | D.容器内混合气体的密度不变 |
 的平衡转化率与投料比X,
的平衡转化率与投料比X,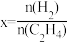 以及温度的关系如图所示。
以及温度的关系如图所示。
①反应从开始分别进行到A、B、C点时,
②T1
③B点对应的体系中a=
(4)
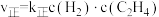 ,
,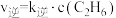 ,其中k正和k逆为速率常数,只与温度有关。若其他条件不变,则温度从T1变化到T2的过程中,下列推断合理的是_______(填标号)。
,其中k正和k逆为速率常数,只与温度有关。若其他条件不变,则温度从T1变化到T2的过程中,下列推断合理的是_______(填标号)。| A.k正增大的倍数大于k逆 | B.k正增大的倍数小于k逆 |
C.k正减小的倍数大于 | D.k正减小的倍数小于k逆 |
您最近一年使用:0次
2022-11-07更新
|
112次组卷
|
3卷引用:湖北省恩施州高中教育联盟2022-2023学年高二上学期期中考试化学试题
名校
9 . 2022北京冬奥会采用氢气作为火炬燃料,选择氢能汽车作为赛事交通服务用车,充分体现了绿色奥运的理念。已知:
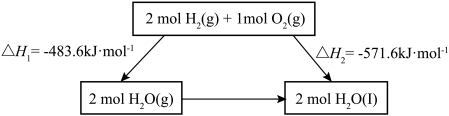
下列说法不正确 的是

下列说法
| A.氢气既可以通过燃烧反应提供热能,也可以设计成燃料电池提供电能 |
B. 的过程中, 的过程中, , , |
C.断裂2mol 和1mol 和1mol 中化学键所需能量大于断裂2mol 中化学键所需能量大于断裂2mol 中化学键所需能量 中化学键所需能量 |
D.化学反应的 ,只与反应体系的始态和终态有关,与反应途径无关 ,只与反应体系的始态和终态有关,与反应途径无关 |
您最近一年使用:0次
2022-11-04更新
|
620次组卷
|
9卷引用: 湖北省恩施市第一中学2022-2023学年高二下学期期中考试化学试题
名校
10 . 下列有关化学反应原理的说法中正确的是
| A.需要加热的反应都是非自发反应,不需要加热的反应都是自发反应 |
B.反应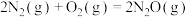  ,则该反应能自发进行 ,则该反应能自发进行 |
| C.100mL2mol/L的盐酸与锌片反应,加入少量NaCl固体,反应速率不变 |
| D.若反应可以自发,则该反应的速率一定较快 |
您最近一年使用:0次
2022-11-04更新
|
325次组卷
|
2卷引用:湖北省荆州市沙市中学2022-2023学年高二上学期11月期中考试化学试题



