1 . 汽车尾气未经处理直接排放,会严重污染环境。某反应可有效降低汽车尾气污染物的排放,一定条件下该反应经历三个基元反应,反应历程如图所示(TS表示过渡态)。下列说法错误的是
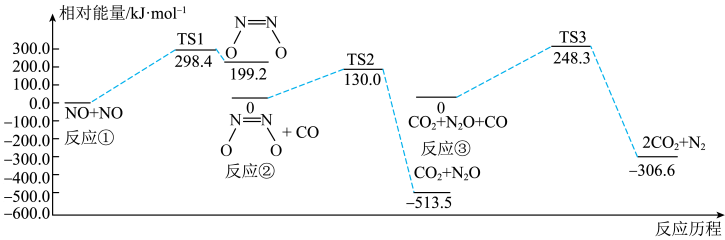
| A.反应达平衡后提高反应温度,反应物转化率减小 |
| B.使用催化剂可以降低反应的活化能,提高活化分子百分数,但不改变反应物的平衡转化率 |
| C.该化学反应的速率主要由反应③决定 |
D.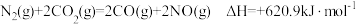 |
您最近一年使用:0次
2 . 除少数卤化物外,大部分非金属卤化物都易水解,且反应不可逆。卤化物的水解机理分亲核水解和亲电水解。发生亲核水解的结构条件:中心原子具有 和有空的价轨道;发生亲电水解的结构条件:中心原子有孤对电子,可作Lewis碱,接受H2O的H+进攻。其中SiCl4的亲核水解机理如图。下列说法错误的是
和有空的价轨道;发生亲电水解的结构条件:中心原子有孤对电子,可作Lewis碱,接受H2O的H+进攻。其中SiCl4的亲核水解机理如图。下列说法错误的是
 和有空的价轨道;发生亲电水解的结构条件:中心原子有孤对电子,可作Lewis碱,接受H2O的H+进攻。其中SiCl4的亲核水解机理如图。下列说法错误的是
和有空的价轨道;发生亲电水解的结构条件:中心原子有孤对电子,可作Lewis碱,接受H2O的H+进攻。其中SiCl4的亲核水解机理如图。下列说法错误的是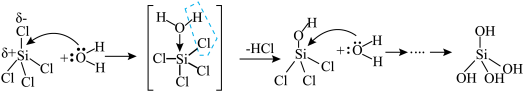
| A.上述过程Si的杂化方式发生了改变 | B.根据上述机理,NF3不能发生水解 |
| C.预测NCl3能发生亲电水解 | D.CCl4的水解机理与上述过程类似 |
您最近一年使用:0次
名校
3 . 下列说法正确的是
| A.在同一化合物中,金属元素显正价,则非金属元素一定显负价 |
| B.化学变化常伴随着发光,则有发光现象的变化一定是化学变化 |
| C.化合物是由不同种元素组成的纯净物,则由不同种元素组成的纯净物一定是化合物 |
| D.催化剂的质量在反应前后不变,则在反应前后质量不变的物质一定是该反应的催化剂 |
您最近一年使用:0次
4 . 工业上以乙苯为原料制备苯乙烯。主要有以下两种制备方法,T K时相应的热化学方程式及其平衡常数如下:
反应Ⅰ:直接脱氢
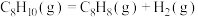
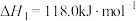 ,
,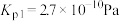
反应Ⅱ:氧化脱氢
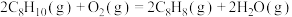
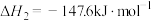 ,
,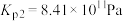
回答下列问题:
(1)①反应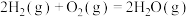 的平衡常数
的平衡常数
___________ (保留3位有效数字)。
②反应Ⅱ趋势远大于反应Ⅰ,从反应自发性角度分析其原因是___________ 。
(2)已知 ,忽略
,忽略 、
、 随温度的变化。当
随温度的变化。当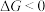 时,反应能自发进行。在100kPa下,直接脱氢反应的
时,反应能自发进行。在100kPa下,直接脱氢反应的 和
和 随温度变化的理论计算结果如图所示。
随温度变化的理论计算结果如图所示。 随温度的变化曲线为
随温度的变化曲线为___________ (选填“a”或“b”),判断的理由是___________ 。
②在某温度下,向恒容密闭容器中通入气态乙苯和氧气各1mol,初始压强为200kPa,只发生反应Ⅱ,达到平衡时,乙苯的转化率为99.8%,该反应的平衡常数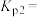
___________ kPa(保留小数点后一位;分压=总压×物质的量分数)。
(3)乙苯脱氢法制苯乙烯往往伴随副反应,一定条件下,为了提高反应速率和苯乙烯选择
性,应当___________ 。
反应Ⅰ:直接脱氢
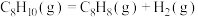
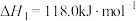 ,
,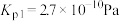
反应Ⅱ:氧化脱氢
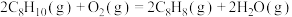
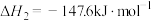 ,
,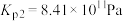
回答下列问题:
(1)①反应
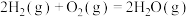 的平衡常数
的平衡常数
②反应Ⅱ趋势远大于反应Ⅰ,从反应自发性角度分析其原因是
(2)已知
 ,忽略
,忽略 、
、 随温度的变化。当
随温度的变化。当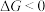 时,反应能自发进行。在100kPa下,直接脱氢反应的
时,反应能自发进行。在100kPa下,直接脱氢反应的 和
和 随温度变化的理论计算结果如图所示。
随温度变化的理论计算结果如图所示。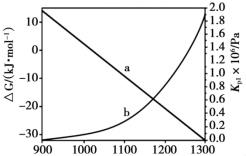
 随温度的变化曲线为
随温度的变化曲线为②在某温度下,向恒容密闭容器中通入气态乙苯和氧气各1mol,初始压强为200kPa,只发生反应Ⅱ,达到平衡时,乙苯的转化率为99.8%,该反应的平衡常数
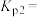
(3)乙苯脱氢法制苯乙烯往往伴随副反应,一定条件下,为了提高反应速率和苯乙烯选择
性,应当
您最近一年使用:0次
5 . 已知 催化反应
催化反应 历程如下图所示,催化历程中有
历程如下图所示,催化历程中有 参与。下列有关该反应的说法正确的是
参与。下列有关该反应的说法正确的是
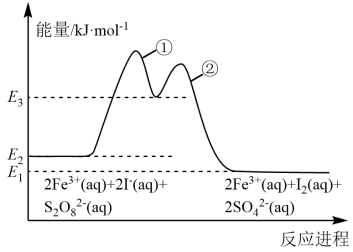
 催化反应
催化反应 历程如下图所示,催化历程中有
历程如下图所示,催化历程中有 参与。下列有关该反应的说法正确的是
参与。下列有关该反应的说法正确的是
| A.步骤①的速率常数大于步骤② |
| B.反应历程中存在非极性键的断裂和形成 |
| C.催化历程中,仅氧元素的化合价未发生变化 |
D.步骤②的热化学方程为:  |
您最近一年使用:0次
解题方法
6 . 利用计算机技术测得在甲、乙两种催化剂作用下由正丁烷(g)制备1-丁烯(g)的反应历程如下,其中标*的物质表示吸附在催化剂上的中间产物,过渡态均用TS表示,0.06eV表示1个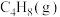 +1个
+1个 的能量,下列说法中正确的是
的能量,下列说法中正确的是
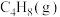 +1个
+1个 的能量,下列说法中正确的是
的能量,下列说法中正确的是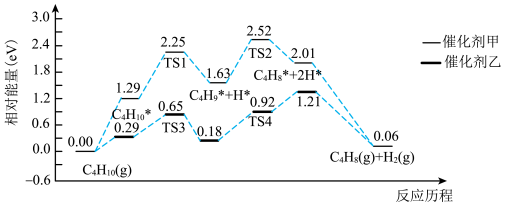
| A.催化剂甲比催化剂乙效果更好 |
| B.吸附在催化剂甲上的正丁烷(g)脱去第一个H比脱去第二个H更慢 |
| C.由正丁烷(g)制备1-丁烯(g)的反应在低温下更有利于自发进行 |
| D.该反应过程中,1 mol正丁烷(g)在催化剂乙表面吸附,吸收的热量为0.29 eV |
您最近一年使用:0次
2024-05-18更新
|
43次组卷
|
2卷引用:安徽省安庆市示范高中2024届高三下学期三模考试化学试题
解题方法
7 . 电催化偶联N2和CO2制备尿素 ,可实现室温下尿素的绿色合成。结合实验和计算机模拟在酸性介质中催化剂表面的反应历程如下图所示,吸附在催化剂表面的物种用*标注。下列有关该碳氮偶联过程的说法错误的是
,可实现室温下尿素的绿色合成。结合实验和计算机模拟在酸性介质中催化剂表面的反应历程如下图所示,吸附在催化剂表面的物种用*标注。下列有关该碳氮偶联过程的说法错误的是
 ,可实现室温下尿素的绿色合成。结合实验和计算机模拟在酸性介质中催化剂表面的反应历程如下图所示,吸附在催化剂表面的物种用*标注。下列有关该碳氮偶联过程的说法错误的是
,可实现室温下尿素的绿色合成。结合实验和计算机模拟在酸性介质中催化剂表面的反应历程如下图所示,吸附在催化剂表面的物种用*标注。下列有关该碳氮偶联过程的说法错误的是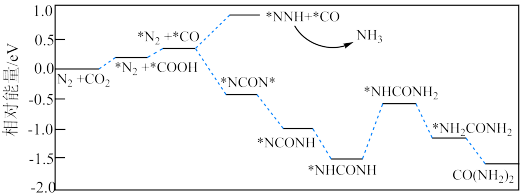
| A.化合价发生改变的元素有C和N |
| B.有O-N键的生成和断裂 |
| C.*NCON*的生成可减少副产物NH3的形成 |
D.该过程生成尿素的总反应式: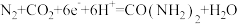 |
您最近一年使用:0次
名校
解题方法
8 . 氮氧化物( )都具有不同程度的毒性,是造成大气污染的主要物质,危害人体健康,其无害化处理成为研究热点,具有重要的意义。回答下列问题:
)都具有不同程度的毒性,是造成大气污染的主要物质,危害人体健康,其无害化处理成为研究热点,具有重要的意义。回答下列问题:
(1)NO在空气中发生氧化反应:
 ,该反应分两步完成,其反应历程如图所示。
,该反应分两步完成,其反应历程如图所示。_______ ;决定: 反应速率的是
反应速率的是_______ (填“反应I”或“反应Ⅱ”)。
(2)T℃,在密闭容器中尝试利用表面催化工艺分解NO,若用 分别表示
分别表示 ,NO,
,NO, 和固体催化剂,则在固体催化剂表面分解NO的反应过程可用下图表示:
和固体催化剂,则在固体催化剂表面分解NO的反应过程可用下图表示:
(3)厌氧氨化法(Anammox)是一种新型的氨氮去除技术,反应模型如图。 )是
)是_______ (填“极性”或“非极性”)分子。羟胺( )可看成氨分子内的一个氢原子被羟基取代的衍生物,则羟胺分子中N原子的杂化方式为
)可看成氨分子内的一个氢原子被羟基取代的衍生物,则羟胺分子中N原子的杂化方式为_______ ;
②该过程的总反应的方程式为_______ 。
(4)在恒温条件下,向初始压强为PMPa的恒容密闭容器中加入等物质的量CO和NO发生反应: ,反应达到平衡时,
,反应达到平衡时, 的体积分数为20%,则NO的转化率为
的体积分数为20%,则NO的转化率为_______ (保留一位小数)。该条件下反应平衡常数
_______ MPa-1(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 )都具有不同程度的毒性,是造成大气污染的主要物质,危害人体健康,其无害化处理成为研究热点,具有重要的意义。回答下列问题:
)都具有不同程度的毒性,是造成大气污染的主要物质,危害人体健康,其无害化处理成为研究热点,具有重要的意义。回答下列问题:(1)NO在空气中发生氧化反应:

 ,该反应分两步完成,其反应历程如图所示。
,该反应分两步完成,其反应历程如图所示。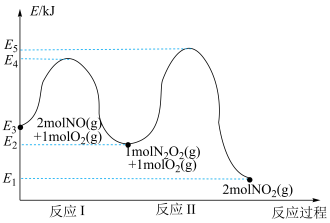
 反应速率的是
反应速率的是(2)T℃,在密闭容器中尝试利用表面催化工艺分解NO,若用
 分别表示
分别表示 ,NO,
,NO, 和固体催化剂,则在固体催化剂表面分解NO的反应过程可用下图表示:
和固体催化剂,则在固体催化剂表面分解NO的反应过程可用下图表示: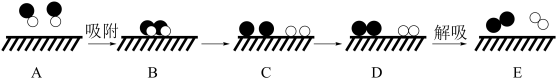
| A.b到c吸热,c到d放热 |
| B.当体系压强恒定时,反应达到平衡状态 |
C.除去体系中 可提高NO的平衡转化率 可提高NO的平衡转化率 |
| D.固体催化剂起到反应载体的作用,不改变反应的活化能和焓变 |
(3)厌氧氨化法(Anammox)是一种新型的氨氮去除技术,反应模型如图。
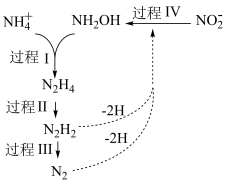
 )是
)是 )可看成氨分子内的一个氢原子被羟基取代的衍生物,则羟胺分子中N原子的杂化方式为
)可看成氨分子内的一个氢原子被羟基取代的衍生物,则羟胺分子中N原子的杂化方式为②该过程的总反应的方程式为
(4)在恒温条件下,向初始压强为PMPa的恒容密闭容器中加入等物质的量CO和NO发生反应:
 ,反应达到平衡时,
,反应达到平衡时, 的体积分数为20%,则NO的转化率为
的体积分数为20%,则NO的转化率为
您最近一年使用:0次
名校
9 . HCHO与O2可以在羟基磷灰石(HAP)表面催化氧化生成CO2、H2O,其反应历程如图所示(图中只画出了HAP的部分结构)。
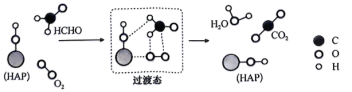
| A.HCHO分子中碳原子的杂化方式为sp2 |
B.若用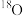 标记HAP中氧原子,则反应后 标记HAP中氧原子,则反应后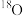 仍在HAP中 仍在HAP中 |
C.该反应可表示为 |
| D.CO2是由极性键形成的非极性分子 |
您最近一年使用:0次
解题方法
10 . 下列实验装置能达到实验目的的是
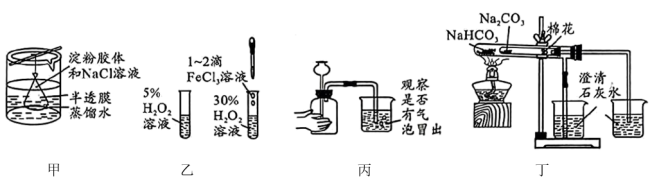
A.图甲装置可除去淀粉胶体中的 |
| B.图乙装置探究催化剂对化学反应速率的影响 |
| C.图丙装置检查装置的气密性 |
D.图丁装置可比较 和 和 的稳定性 的稳定性 |
您最近一年使用:0次



