名校
解题方法
1 . 下列有关合成氨条件选择的说法正确的是
| A.适当增加氢气的浓度可提高氮气的平衡转化率 | B.温度越高,速率越快,生产效益越好 |
| C.使用铁触媒能提高合成氨反应的平衡转化率 | D.将氨及时液化分离不利于提高氨的产率 |
您最近一年使用:0次
2023-12-03更新
|
128次组卷
|
3卷引用:天津市第十四中学2023-2024学年高二上学期第二次月考化学试卷
解题方法
2 . 常温下 是一种无色气体,能溶于浓硫酸、易水解,是有机合成和石油化工广泛应用的一种重要催化剂。工业上以铁硼矿(主要成分有
是一种无色气体,能溶于浓硫酸、易水解,是有机合成和石油化工广泛应用的一种重要催化剂。工业上以铁硼矿(主要成分有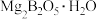 、
、 ,次要成分有
,次要成分有 、
、 、
、 、
、 )和萤石(主要成分为
)和萤石(主要成分为 ,含微量二氧化硅、硫单质)为原料制备
,含微量二氧化硅、硫单质)为原料制备 的流程如图所示:
的流程如图所示:

已知:① 溶液在“热溶浸”中,只能溶解
溶液在“热溶浸”中,只能溶解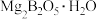 ;
;
②室温下,溶液 时,
时, 的溶解度为
的溶解度为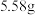 ;
;
③相关金属离子形成氢氧化物沉淀的 范围如下表所示:
范围如下表所示:
回答下列问题:
(1)产生的气体A是______ ;“热溶浸”时,下列措施能提高硼元素浸出率的有______ (填序号)。
a.粉碎矿石 b.适当升高“热溶浸”温度
c.适当缩短“热溶浸”时间 d.加快搅拌速度
(2)已知硼酸在水中的电离方程式为 。室温下,调节过滤1所得滤液的
。室温下,调节过滤1所得滤液的 值为4,析出硼酸固体,则滤液2中
值为4,析出硼酸固体,则滤液2中
_________  。
。
(3)补充完整反应釜中发生主要反应的化学方程式:①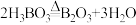 ;②
;②___________ ;过量浓硫酸的作用是___________ (答出2点)。
(4)根据下表,选择反应釜中的最佳反应条件:温度为________ ,硫酸质量分数为________ 。
不同反应条件对 产率的影响
产率的影响
(5)利用离子色谱法可以检测过滤3所得滤液中硫元素的含量,将样品通过检测液,进行色谱分析,得到如图所示结果,出现检测峰1的原因可能是___________ 。

(6)滤渣1通过下图所示操作可逐一分离硅、铝、铁三种元素,试剂①是___________ (填化学式),调节 的范围是
的范围是___________ 。

 是一种无色气体,能溶于浓硫酸、易水解,是有机合成和石油化工广泛应用的一种重要催化剂。工业上以铁硼矿(主要成分有
是一种无色气体,能溶于浓硫酸、易水解,是有机合成和石油化工广泛应用的一种重要催化剂。工业上以铁硼矿(主要成分有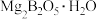 、
、 ,次要成分有
,次要成分有 、
、 、
、 、
、 )和萤石(主要成分为
)和萤石(主要成分为 ,含微量二氧化硅、硫单质)为原料制备
,含微量二氧化硅、硫单质)为原料制备 的流程如图所示:
的流程如图所示:
已知:①
 溶液在“热溶浸”中,只能溶解
溶液在“热溶浸”中,只能溶解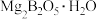 ;
;②室温下,溶液
 时,
时, 的溶解度为
的溶解度为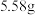 ;
;③相关金属离子形成氢氧化物沉淀的
 范围如下表所示:
范围如下表所示:| 金属离子 |  |  |  |
开始沉淀的 | 1.5 | 6.3 | 3.2 |
沉淀完全的 | 3.2 | 8.3 | 5.0 |
(1)产生的气体A是
a.粉碎矿石 b.适当升高“热溶浸”温度
c.适当缩短“热溶浸”时间 d.加快搅拌速度
(2)已知硼酸在水中的电离方程式为
 。室温下,调节过滤1所得滤液的
。室温下,调节过滤1所得滤液的 值为4,析出硼酸固体,则滤液2中
值为4,析出硼酸固体,则滤液2中
 。
。(3)补充完整反应釜中发生主要反应的化学方程式:①
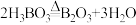 ;②
;②(4)根据下表,选择反应釜中的最佳反应条件:温度为
不同反应条件对
 产率的影响
产率的影响| 反应温度/℃ |  产率/% 产率/% | |
硫酸质量分数 | 硫酸质量分数 | |
| 60 | 9.5 | 54 |
| 70 | 11 | 62.5 |
| 80 | 37.4 | 78.8 |
| 90 | 47.7 | 82 |
| 100 | 47.1 | 81.4 |
| 110 | 46.5 | 80.5 |
| 120 | 46 | 79 |
(5)利用离子色谱法可以检测过滤3所得滤液中硫元素的含量,将样品通过检测液,进行色谱分析,得到如图所示结果,出现检测峰1的原因可能是

(6)滤渣1通过下图所示操作可逐一分离硅、铝、铁三种元素,试剂①是
 的范围是
的范围是
您最近一年使用:0次
名校
解题方法
3 . 某工厂采用如下工艺处理镍钴矿硫酸浸取液(含 、
、 、
、 、
、 、
、 和
和 )。实现镍、钴、镁元素的回收。
)。实现镍、钴、镁元素的回收。
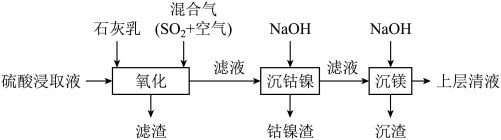
已知:
回答下列问题:
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为_______ (答出一条即可)。
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸(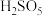 ),1mol
),1mol  中过氧键的数目为
中过氧键的数目为_______ 。
(3)“氧化”中,用石灰乳调节pH=4, 被
被 氧化为
氧化为 ,该反应的离子方程式为
,该反应的离子方程式为_______ ( 的电离第一步完全,第二步微弱);滤渣的成分为
的电离第一步完全,第二步微弱);滤渣的成分为 、
、 、
、_______ (填化学式)。
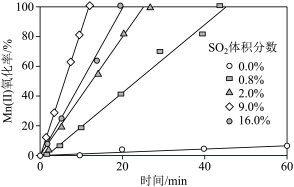
(4)“氧化”中保持空气通入速率不变,Mn(Ⅰ)氧化率与时间的关系如下。 体积分数为
体积分数为_______ 时,Mn(Ⅱ)氧化速率最大;继续增大 体积分数时,Mn(Ⅰ)氧化速率减小的原因是
体积分数时,Mn(Ⅰ)氧化速率减小的原因是_______ 。
(5)“沉钴镍”中得到的Co(Ⅱ)在空气中可被氧化成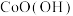 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(6)“沉镁”中为使 沉淀完全(25℃),需控制pH不低于
沉淀完全(25℃),需控制pH不低于_______ (精确至0.1)。
 、
、 、
、 、
、 、
、 和
和 )。实现镍、钴、镁元素的回收。
)。实现镍、钴、镁元素的回收。
已知:
| 物质 |  | 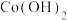 |  |  |
 |  |  |  | 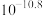 |
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸(
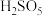 ),1mol
),1mol  中过氧键的数目为
中过氧键的数目为(3)“氧化”中,用石灰乳调节pH=4,
 被
被 氧化为
氧化为 ,该反应的离子方程式为
,该反应的离子方程式为 的电离第一步完全,第二步微弱);滤渣的成分为
的电离第一步完全,第二步微弱);滤渣的成分为 、
、 、
、(4)“氧化”中保持空气通入速率不变,Mn(Ⅰ)氧化率与时间的关系如下。
 体积分数为
体积分数为 体积分数时,Mn(Ⅰ)氧化速率减小的原因是
体积分数时,Mn(Ⅰ)氧化速率减小的原因是
(5)“沉钴镍”中得到的Co(Ⅱ)在空气中可被氧化成
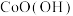 ,该反应的化学方程式为
,该反应的化学方程式为(6)“沉镁”中为使
 沉淀完全(25℃),需控制pH不低于
沉淀完全(25℃),需控制pH不低于
您最近一年使用:0次
名校
4 . 纯 遇热易发生分解,工业上通常制成
遇热易发生分解,工业上通常制成 固体以便运输和储存。制备
固体以便运输和储存。制备 的实验装置如图所示(夹持装置省略),其中A装置制备
的实验装置如图所示(夹持装置省略),其中A装置制备 ,C装置用于制备
,C装置用于制备 。回答下列问题:
。回答下列问题:
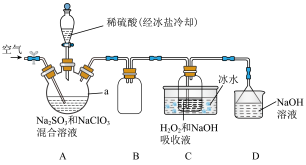
(1)仪器a的名称是___________ 。装置B的作用是___________ 。
(2)装置A中发生反应的离子方程式为___________ 。向装置A中通入空气的目的是___________ 。
(3)装置C中发生反应的化学方程式为___________ ;C装置采用“冰水浴”的目的是___________ 。
(4)研究测得C装置吸收液中的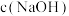 与
与 对粗产品中
对粗产品中 含量的影响如图所示。则最佳条件为
含量的影响如图所示。则最佳条件为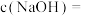
___________  ,
,
___________ 。

 遇热易发生分解,工业上通常制成
遇热易发生分解,工业上通常制成 固体以便运输和储存。制备
固体以便运输和储存。制备 的实验装置如图所示(夹持装置省略),其中A装置制备
的实验装置如图所示(夹持装置省略),其中A装置制备 ,C装置用于制备
,C装置用于制备 。回答下列问题:
。回答下列问题:
(1)仪器a的名称是
(2)装置A中发生反应的离子方程式为
(3)装置C中发生反应的化学方程式为
(4)研究测得C装置吸收液中的
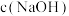 与
与 对粗产品中
对粗产品中 含量的影响如图所示。则最佳条件为
含量的影响如图所示。则最佳条件为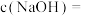
 ,
,

您最近一年使用:0次
名校
5 . I.在硫酸工业中,通过下列反应使SO2氧化成SO3:2SO2(g)+O2(g)  2SO3(g) ΔH=—196.6kJ•mol-1(已知:反应条件为催化剂、加热;催化剂是V2O5,在400~500℃时催化剂效果最好)。表中列出了在不同温度和压强下,反应达到平衡时SO2的转化率。
2SO3(g) ΔH=—196.6kJ•mol-1(已知:反应条件为催化剂、加热;催化剂是V2O5,在400~500℃时催化剂效果最好)。表中列出了在不同温度和压强下,反应达到平衡时SO2的转化率。
(1)从理论上分析,为了使二氧化硫尽可能多地转化为三氧化硫,应选择的条件是________ 。
(2)在实际生产中,选定的温度为400~500℃,原因是___________ 。
(3)在实际生产中,采用的压强为常压,原因是___________ 。
(4)在实际生产中,通入过量的空气,原因是___________ 。
(5)尾气中SO2必须回收,原因是___________ 。
II.Bodenstein研究了反应:2HI(g) H2(g)+I2(g) ΔH>0。在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表所示:
H2(g)+I2(g) ΔH>0。在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表所示:
(6)根据上述实验结果,该反应的平衡常数K的计算式为___________ 。
(7)上述反应中,正反应速率v正=k正x2(HI),逆反应速率v逆=k逆x(H2)•x(I2),其中k正、k逆为正、逆反应速率常数,则k逆为___________ (用含K和k正的代数式表示)。
III.在刚性容器压强为1.01MPa时,乙酸甲酯与氢气制备乙醇主要发生如下反应:CH3COOCH3(g)+2H2(g) CH3OH(g)+CH3CH2OH(g)。一定温度下,以n(CH3COOCH3):n(H2)=1:10的投料比进行反应,乙酸甲酯转化率与气体总压强的关系如图所示:
CH3OH(g)+CH3CH2OH(g)。一定温度下,以n(CH3COOCH3):n(H2)=1:10的投料比进行反应,乙酸甲酯转化率与气体总压强的关系如图所示:
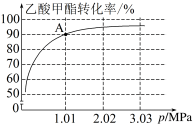
(8)A点时,CH3CH2OH(g)的体积分数为___________ %(保留一位小数)。
(9)此温度下,该反应的化学平衡常数Kp=___________ MPa-1(Kp为以分压表示的平衡常数,列出计算式,不要求计算结果)。
 2SO3(g) ΔH=—196.6kJ•mol-1(已知:反应条件为催化剂、加热;催化剂是V2O5,在400~500℃时催化剂效果最好)。表中列出了在不同温度和压强下,反应达到平衡时SO2的转化率。
2SO3(g) ΔH=—196.6kJ•mol-1(已知:反应条件为催化剂、加热;催化剂是V2O5,在400~500℃时催化剂效果最好)。表中列出了在不同温度和压强下,反应达到平衡时SO2的转化率。| 温度/℃ | 平衡时SO2的转化率/% | ||||
| 0.1MPa | 0.5MPa | 1MPa | 5MPa | 10MPa | |
| 450 | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 550 | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
(1)从理论上分析,为了使二氧化硫尽可能多地转化为三氧化硫,应选择的条件是
(2)在实际生产中,选定的温度为400~500℃,原因是
(3)在实际生产中,采用的压强为常压,原因是
(4)在实际生产中,通入过量的空气,原因是
(5)尾气中SO2必须回收,原因是
II.Bodenstein研究了反应:2HI(g)
 H2(g)+I2(g) ΔH>0。在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表所示:
H2(g)+I2(g) ΔH>0。在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表所示:| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.6 | 0.73 | 0.773 | 0.78 | 0.784 |
(6)根据上述实验结果,该反应的平衡常数K的计算式为
(7)上述反应中,正反应速率v正=k正x2(HI),逆反应速率v逆=k逆x(H2)•x(I2),其中k正、k逆为正、逆反应速率常数,则k逆为
III.在刚性容器压强为1.01MPa时,乙酸甲酯与氢气制备乙醇主要发生如下反应:CH3COOCH3(g)+2H2(g)
 CH3OH(g)+CH3CH2OH(g)。一定温度下,以n(CH3COOCH3):n(H2)=1:10的投料比进行反应,乙酸甲酯转化率与气体总压强的关系如图所示:
CH3OH(g)+CH3CH2OH(g)。一定温度下,以n(CH3COOCH3):n(H2)=1:10的投料比进行反应,乙酸甲酯转化率与气体总压强的关系如图所示:
(8)A点时,CH3CH2OH(g)的体积分数为
(9)此温度下,该反应的化学平衡常数Kp=
您最近一年使用:0次
名校
6 . 下列事实中,不能用勒夏特列原理解释的是
A. 溶液中加入 溶液中加入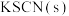 后颜色变深 后颜色变深 |
| B.用排饱和食盐水的方法收集氯气 |
C.棕红色 加压后颜色先变深后变浅 加压后颜色先变深后变浅 |
| D.500℃时比室温更有利于合成氨 |
您最近一年使用:0次
2023-11-23更新
|
133次组卷
|
2卷引用:陕西省 韩城市象山中学2023-2024学年高二上学期第三次月考化学试题
名校
解题方法
7 . 氨是制造化肥的重要原料,如图为工业合成氨的流程图,下列说法错误的是
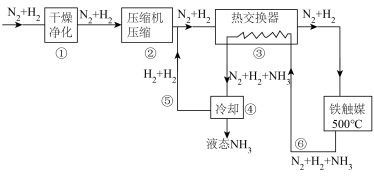

| A.工业上制氮气一般用分离液态空气法 |
| B.步骤③的作用是充分利用热量,减少能耗 |
C.步骤①中“净化”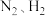 混合气体可以防止催化剂中毒 混合气体可以防止催化剂中毒 |
| D.步骤③中温度选择500℃,主要是考虑平衡时反应物的转化率 |
您最近一年使用:0次
2023-11-17更新
|
130次组卷
|
2卷引用:黑龙江省哈尔滨市第九中学校2023-2024学年高二上学期10月月考化学试题
名校
解题方法
8 . 通过对阳极泥的综合处理可以回收贵重金属,一种从铜阳极泥(主要成分为Se、Ag、Ag2Se、Cu、CuSO4和Cu2S等)中分离Ag、Se和Cu的新工艺流程如图所示:
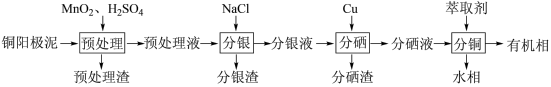
(1)已知预处理温度为80℃,此过程中S元素全部转化为最高价,则预处理时Cu2S发生反应的离子方程式为_______ 。
(2)比起传统工艺中采用浓硫酸作氧化剂,本工艺中采用稀H2SO4溶液添加MnO2作预处理剂的主要优点是_______ 。
(3)分银渣可用浓氨水溶液浸出并还原得到单质银,回收分银渣中的银,浸出过程温度不宜过高的原因是:_______ 。
(4)分硒渣(Cu2Se)经过氧化可得到H2SeO4.已知:H2SeO4=H++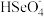 ,
,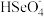
 H++
H++ ,若0.01 mol/LH2SeO4溶液的pH为x,则K(
,若0.01 mol/LH2SeO4溶液的pH为x,则K(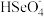 )=
)=_______ (写出含x的计算式)。
(5)分铜得到产品CuSO4·5H2O的具体操作如图:
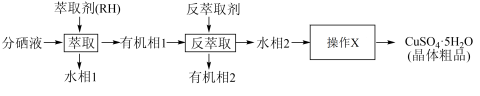
①萃取的原理为:2RH+Cu2+ R2Cu+2H+,则反萃取剂最好选用
R2Cu+2H+,则反萃取剂最好选用_______ (填化学式)溶液。
②操作X为_______ ,过滤;
③为了减少CuSO4·5H2O的损失,最好选用_______ 进行洗涤。
A.冷水 B.热水 C.无水乙醇
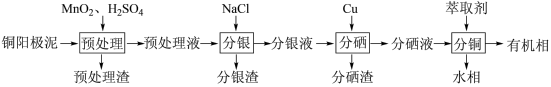
(1)已知预处理温度为80℃,此过程中S元素全部转化为最高价,则预处理时Cu2S发生反应的离子方程式为
(2)比起传统工艺中采用浓硫酸作氧化剂,本工艺中采用稀H2SO4溶液添加MnO2作预处理剂的主要优点是
(3)分银渣可用浓氨水溶液浸出并还原得到单质银,回收分银渣中的银,浸出过程温度不宜过高的原因是:
(4)分硒渣(Cu2Se)经过氧化可得到H2SeO4.已知:H2SeO4=H++
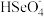 ,
,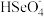
 H++
H++ ,若0.01 mol/LH2SeO4溶液的pH为x,则K(
,若0.01 mol/LH2SeO4溶液的pH为x,则K(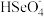 )=
)=(5)分铜得到产品CuSO4·5H2O的具体操作如图:

①萃取的原理为:2RH+Cu2+
 R2Cu+2H+,则反萃取剂最好选用
R2Cu+2H+,则反萃取剂最好选用②操作X为
③为了减少CuSO4·5H2O的损失,最好选用
A.冷水 B.热水 C.无水乙醇
您最近一年使用:0次
9 . 下列有关工业合成氨反应:
 的说法
的说法不正确 的是

 的说法
的说法| A.合成氨采取循环操作目的是提高氮气和氢气的利用率 |
B.除原料气中CO反应: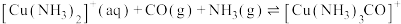  ,适宜低温高压环境 ,适宜低温高压环境 |
| C.合成塔压强调控在10MPa~30MPa之间,是对生产设备条件和经济成本的综合考虑结果 |
| D.合成塔使用热交换控制体系温度400~500℃左右,主要目的是有利于平衡正向移动 |
您最近一年使用:0次
2023-11-10更新
|
254次组卷
|
5卷引用:新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高二上学期第二次月考试化学试卷
新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高二上学期第二次月考试化学试卷浙江省钱塘联盟2023-2024学年高二上学期11月期中联考化学试题【定心卷】2.4 化学反应的调控随堂练习-人教版2023-2024学年选择性必修1(已下线)寒假作业04 化学反应的方向及调控-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)宁夏回族自治区石嘴山市平罗县平罗中学2023-2024学年高二下学期5月期中化学试题
名校
解题方法
10 . 工业上用生物法处理 的原理如下:
的原理如下:
反应1:
反应2: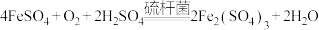
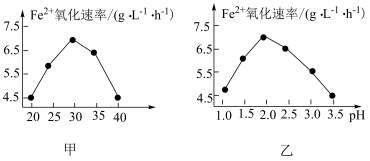
以硫杆菌作催化剂时,反应温度及溶液 对
对 氧化速率的影响分别如图甲、图乙所示。下列有关说法错误的是
氧化速率的影响分别如图甲、图乙所示。下列有关说法错误的是
 的原理如下:
的原理如下:反应1:

反应2:
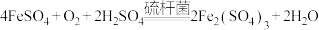
以硫杆菌作催化剂时,反应温度及溶液
 对
对 氧化速率的影响分别如图甲、图乙所示。下列有关说法错误的是
氧化速率的影响分别如图甲、图乙所示。下列有关说法错误的是
A.反应1的条件下,还原性: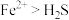 |
B.当反应温度过高时, 氧化速率下降的原因可能是硫杆菌失去活性 氧化速率下降的原因可能是硫杆菌失去活性 |
C.由图甲和图乙可得出结论:使用硫杆菌作催化剂的最佳条件为 、 、 |
D.当反应1中转移 电子时,反应1中消耗的 电子时,反应1中消耗的 在标准状况下的体积为 在标准状况下的体积为 |
您最近一年使用:0次
2023-11-09更新
|
118次组卷
|
2卷引用:河南省南阳市第一中学校2023-2024学年高二上学期第三次月考化学试题



