1 . 只要善于观察和发现,化学之美随处可见。下列说法错误的是
| A.“日照香炉生紫烟”涉及胶体的丁达尔效应 |
| B.石蕊遇到碱性溶液变为蓝色与平衡移动有关 |
| C.五彩缤纷的烟花,是电子由基态跃迁到激发态时,能量以光的形式释放出来 |
| D.晶莹剔透的大块水晶是由熔融态的二氧化硅缓慢冷却得到的 |
您最近一年使用:0次
2 . 根据下列实验操作及现象所得出的结论或解释正确的是
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | FeCl3+3KSCN⇌Fe(SCN)3+3KCl在平衡体系中加入KCl晶体 | 溶液颜色不变 | 加入少量KCl晶体,不会影响该化学平衡 |
| B | 取相同大小、形状和质量的Cu粒分别投入稀硝酸和浓硝酸中 | Cu粒与浓硝酸反应更剧烈 | 实验目的是探究浓度对化学反应速率的影响 |
| C | 相同的铝片分别与同温同体积且c(H+)=1 mol·L-1的盐酸、硫酸反应 | 铝与盐酸反应产生气泡较快 | 可能是Cl-对该反应起到促进作用 |
| D | 等体积pH=2的两种酸HX和HY分别与足量的锌反应 | HX溶液放出的氢气较多 | HX的酸性比HY强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 我国在第75届联合国大会上正式提出了2030年实现碳达峰、2060年实现碳中和的目标,所以研发利用二氧化碳技术,降低空气中二氧化碳含量成为重要的任务。
Ⅰ.化石燃料的燃烧产生大量的二氧化碳。已知25℃时,相关物质的燃烧热数据如表:
(1)则25℃时H2(g)和C(石墨,s)生成C2H2(l)的热化学方程式为___________ 。
Ⅱ.二氧化碳甲烷化反应合成替代天然气,是利用二氧化碳的技术之一
甲烷化主反应:CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH =-165 kJ∙mol-1
CH4(g)+2H2O(g) ΔH =-165 kJ∙mol-1
副反应:ⅰ.CO(g)+3H2(g) CH4(g)+H2O(g) ΔH1 =___________;
CH4(g)+H2O(g) ΔH1 =___________;
ⅱ.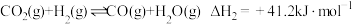 ;
;
ⅲ. =-90kJ∙mol-1;
=-90kJ∙mol-1;
ⅳ. C(s)+H2O(g) CO(g)+H2(g) ΔH4 = +131.3kJ∙mol-1。
CO(g)+H2(g) ΔH4 = +131.3kJ∙mol-1。
(2)反应ⅰ的ΔH1=___________ 。
(3)在恒温恒容的密闭容器中,关于反应ⅲ叙述正确的是___________。
(4)某容器中加入一定量的CO2和H2,保持温度和压强不变的情况下,达平衡后再向该容器中注入Ar稀释,反应ⅲ的化学平衡将___________ (填“正向移动”“逆向移动”或“不移动”),平衡时,CO2的分压P(CO2)___________ (填“增大”、“减小”或“不变”,下同)。
(5)以4molH2和1molCO2为初始原料,在催化剂(Ni/xMg)作用下保持总压为P0时,若只发生反应 ,不同温度下在相同时间测得CO2的转化率如图所示。
,不同温度下在相同时间测得CO2的转化率如图所示。
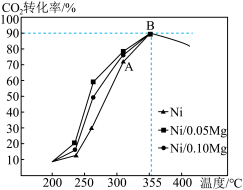
①B点的平衡常数KP___________ 。
②由图像可知,影响该催化剂活性的因素有___________ 。
Ⅰ.化石燃料的燃烧产生大量的二氧化碳。已知25℃时,相关物质的燃烧热数据如表:
| 物质 | H2(g) | C(石墨,s) | C2H2(l) |
| 燃烧热ΔH(kJ∙mol-1) | -285.8 | -393.5 | -1299.5 |
Ⅱ.二氧化碳甲烷化反应合成替代天然气,是利用二氧化碳的技术之一
甲烷化主反应:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ΔH =-165 kJ∙mol-1
CH4(g)+2H2O(g) ΔH =-165 kJ∙mol-1副反应:ⅰ.CO(g)+3H2(g)
 CH4(g)+H2O(g) ΔH1 =___________;
CH4(g)+H2O(g) ΔH1 =___________;ⅱ.
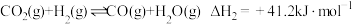 ;
;ⅲ.
 =-90kJ∙mol-1;
=-90kJ∙mol-1;ⅳ. C(s)+H2O(g)
 CO(g)+H2(g) ΔH4 = +131.3kJ∙mol-1。
CO(g)+H2(g) ΔH4 = +131.3kJ∙mol-1。(2)反应ⅰ的ΔH1=
(3)在恒温恒容的密闭容器中,关于反应ⅲ叙述正确的是___________。
| A.用CO2、H2、H2O表示的速率之比为1:2:2,可以作为判断化学平衡的依据。 |
| B.容器中气体的压强不变,不能作为平衡的判断依据。 |
| C.容器内的气体密度不变时,可以作为平衡的判断依据。 |
| D.使用催化剂不能改变平衡转化率。 |
(5)以4molH2和1molCO2为初始原料,在催化剂(Ni/xMg)作用下保持总压为P0时,若只发生反应
 ,不同温度下在相同时间测得CO2的转化率如图所示。
,不同温度下在相同时间测得CO2的转化率如图所示。
①B点的平衡常数KP
②由图像可知,影响该催化剂活性的因素有
您最近一年使用:0次
名校
4 . 5mL0.1mol·L-1FeCl3溶液与1mL0.1mol·L-1KI溶液发生反应: ,达到平衡。下列说法正确的是
,达到平衡。下列说法正确的是
 ,达到平衡。下列说法正确的是
,达到平衡。下列说法正确的是| A.加入四氯化碳,振荡,静置分层,下层为紫红色,表明该化学反应存在限度 |
| B.在溶液中加入KSCN,溶液呈血红色,表明该化学反应存在限度 |
| C.加入苯,振荡,平衡不移动 |
| D.向该平衡体系中加水,平衡逆向移动 |
您最近一年使用:0次
2023-10-17更新
|
31次组卷
|
3卷引用:山东学情2023-2024学年高二上学期10月质量检测(人教版)化学试题
名校
5 . 下列事实不能用勒夏特列原理解释的是
A.对于反应2NO2(g) N2O4(g),增大压强(缩小体积),混合气体颜色先变深后变浅 N2O4(g),增大压强(缩小体积),混合气体颜色先变深后变浅 |
| B.H2、I2、HI三者的平衡,混合气体加压(缩小体积),平衡后颜色变深 |
| C.开启汽水瓶后,瓶中马上泛起大量泡沫 |
D.利用反应Na(l)+KCl(l) NaCl(l)+K(g)制取金属钾,选取适宜的温度 NaCl(l)+K(g)制取金属钾,选取适宜的温度 |
您最近一年使用:0次
2023-10-17更新
|
255次组卷
|
3卷引用:山东学情2023-2024学年高二上学期10月质量检测(人教版)化学试题
解题方法
6 . 工业上以铬铁矿[主要成分为 ,含少量
,含少量 、
、 杂质]为主要原料制备红矾钾
杂质]为主要原料制备红矾钾 的工艺流程如图所示:
的工艺流程如图所示:
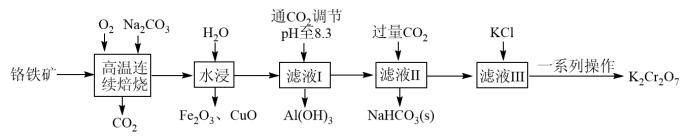
请回答下列问题:
(1)已知“高温连续焙烧”阶段 元素转化为
元素转化为 。
。
①焙烧时采取“多层逆流焙烧”,即将固体粉末从炉顶投料,氧气从炉底鼓入,这样做的优点为_______ 。
② 与纯碱反应的化学方程式为
与纯碱反应的化学方程式为_______ 。
(2)滤液Ⅱ中发生反应的离子方程式为_______ 。
(3)一系列操作包括: 蒸发溶剂至
蒸发溶剂至_______ ,停止加热、_______ 抽滤、重结晶。
(4)生产过程中产生的 酸性废液可通过钡盐沉淀法处理,其过程为:先将
酸性废液可通过钡盐沉淀法处理,其过程为:先将 酸性废液碱化处理,再加入
酸性废液碱化处理,再加入 。废液需进行碱化处理的目的是
。废液需进行碱化处理的目的是_______ [已知:
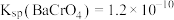 ]。
]。
(5)除了“一系列操作”中所得母液可循环利用外,上述流程中可循环利用的物质还有 、
、_______ (填化学式)。
 ,含少量
,含少量 、
、 杂质]为主要原料制备红矾钾
杂质]为主要原料制备红矾钾 的工艺流程如图所示:
的工艺流程如图所示:
请回答下列问题:
(1)已知“高温连续焙烧”阶段
 元素转化为
元素转化为 。
。①焙烧时采取“多层逆流焙烧”,即将固体粉末从炉顶投料,氧气从炉底鼓入,这样做的优点为
②
 与纯碱反应的化学方程式为
与纯碱反应的化学方程式为(2)滤液Ⅱ中发生反应的离子方程式为
(3)一系列操作包括:
 蒸发溶剂至
蒸发溶剂至(4)生产过程中产生的
 酸性废液可通过钡盐沉淀法处理,其过程为:先将
酸性废液可通过钡盐沉淀法处理,其过程为:先将 酸性废液碱化处理,再加入
酸性废液碱化处理,再加入 。废液需进行碱化处理的目的是
。废液需进行碱化处理的目的是
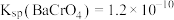 ]。
]。(5)除了“一系列操作”中所得母液可循环利用外,上述流程中可循环利用的物质还有
 、
、
您最近一年使用:0次
解题方法
7 . 向碘水、淀粉的混合液中加入 溶液,蓝色褪去(已知碘水中存在平衡:
溶液,蓝色褪去(已知碘水中存在平衡:
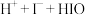 )。为探究褪色原因,设计的实验过程如图所示:
)。为探究褪色原因,设计的实验过程如图所示:
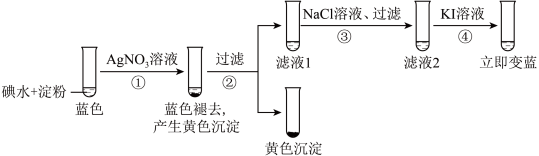
下列叙述正确的是
 溶液,蓝色褪去(已知碘水中存在平衡:
溶液,蓝色褪去(已知碘水中存在平衡:
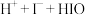 )。为探究褪色原因,设计的实验过程如图所示:
)。为探究褪色原因,设计的实验过程如图所示:
下列叙述正确的是
A.过程①中平衡 正向移动,所得溶液中 正向移动,所得溶液中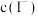 增大 增大 |
| B.过程②中为提高过滤的效率,应用玻璃棒引流并搅拌 |
C.过程③中若用 溶液代替 溶液代替 ,过程④中的现象仍为立即变蓝 ,过程④中的现象仍为立即变蓝 |
D.过程④中氧化 的微粒可能是 的微粒可能是 |
您最近一年使用:0次
解题方法
8 .  时,将足量某碳酸氢盐
时,将足量某碳酸氢盐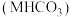 固体置于真空恒容密闭容器中发生反应:
固体置于真空恒容密闭容器中发生反应:
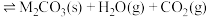 ,该反应达到平衡时体系中气体的总浓度为
,该反应达到平衡时体系中气体的总浓度为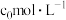 。下列说法正确的是
。下列说法正确的是
 时,将足量某碳酸氢盐
时,将足量某碳酸氢盐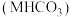 固体置于真空恒容密闭容器中发生反应:
固体置于真空恒容密闭容器中发生反应:
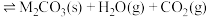 ,该反应达到平衡时体系中气体的总浓度为
,该反应达到平衡时体系中气体的总浓度为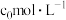 。下列说法正确的是
。下列说法正确的是A.当混合气体中 的体积分数不变时,说明该反应达到平衡 的体积分数不变时,说明该反应达到平衡 |
B.向平衡体系中加入适量 增大 增大 |
C.向平衡体系中充入适量 ,逆反应速率增大 ,逆反应速率增大 |
D. 时,该反应的化学平衡常数为 时,该反应的化学平衡常数为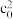 |
您最近一年使用:0次
2023-05-10更新
|
763次组卷
|
6卷引用:山东省聊城市齐鲁名校大联盟2023届高三第三次联考化学试题
山东省聊城市齐鲁名校大联盟2023届高三第三次联考化学试题(已下线)【知识图鉴】单元讲练测选择性必修1第2单元02基础练(已下线)专题08 反应速率与化学平衡-2023年高考化学真题题源解密(新高考专用)(已下线)考点22 化学平衡状态与化学平衡(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点2 化学平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)选择题16-20
名校
9 . 下列实验操作、实验现象及解释或结论都正确且有因果关系的是
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A |  在平衡体系中加入KCl晶体 在平衡体系中加入KCl晶体 | 溶液颜色变浅 | 加入生成物该化学平衡向逆反应方向移动 |
| B | 常温下,用pH计测定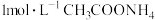 溶液 溶液 | 测得pH=7 |  溶液对水的电离程度无影响 溶液对水的电离程度无影响 |
| C | 将硫酸铝溶液加入到天然淡水中,搅拌,静置 | 水变澄清,絮状沉淀下沉到底部 |  的水解与天然水中 的水解与天然水中 的水解互相促进,生成 的水解互相促进,生成 胶体 胶体 |
| D | 用pH试纸测得相同浓度的pH NaClO溶液、 溶液的pH 溶液的pH | NaClO溶液的pH约为9, 溶液的pH约为8 溶液的pH约为8 |  的酸性比HClO强 的酸性比HClO强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-18更新
|
268次组卷
|
6卷引用:山东省聊城第三中学2021-2022学年高二上学期第三次质量检测化学试题
10 . 在恒温恒容条件下,能使A(g)+B(g)  C(g)+D(g)逆反应速率增大且平衡向右移动的措施是
C(g)+D(g)逆反应速率增大且平衡向右移动的措施是
 C(g)+D(g)逆反应速率增大且平衡向右移动的措施是
C(g)+D(g)逆反应速率增大且平衡向右移动的措施是| A.减小C的浓度 | B.增大D的浓度 | C.减小B的浓度 | D.增大A的浓度 |
您最近一年使用:0次
2021-05-21更新
|
155次组卷
|
3卷引用:山东省聊城市第二中学2022-2023学年高二上学期开学考试化学试题
山东省聊城市第二中学2022-2023学年高二上学期开学考试化学试题辽宁省大连市普兰店区第一中学2020-2021学年高二上学期第二阶段考试化学试题(已下线)2.3.2 影响化学平衡状态的因素-2021-2022学年高二化学课后培优练(人教版选修4)



